面食制品是一种传统主食。我国早在公元前2700年就有了磨粉的记载,到了汉唐时代,我国以蒸煮加工为主的面食得到广泛发展[1]。由于地域的差异,面食制品的种类不尽相同,例如国外的面包,披萨及各种糕点以及我国的馒头、花卷、饼类等。面食制品有着深厚的消费基础,深受人们的喜爱,更是有层出不穷的创新面食,不断刺激人们的味蕾,使面食始终稳居居民主食首选的位置[2]。
面食制品之所以在世界范围内受到人们的喜爱,除了其可以提供人们生存的基本能量外,不同的加工过程使其具有特定风味也是重要的原因之一。现阶段面食制品的加工过程一般经过酵母发酵作为预处理,然后再经过不同的热加工过程使其熟化,如蒸煮,焙烤等,而面食制品风味主要来源则是其熟化过程(热加工过程)。在此过程中,面食制品形成其独特的风味。其中,非酶促的美拉德反应(包括Strecker降解)、焦糖化反应以及脂质氧化过程被认为是面食制品风味形成的主要途径[3-8]。HWANG等[9]以小麦粉为原料,分别在160、185 ℃下进行加热挤出,对其挥发性物质的产生规律进行了探讨,结果发现,在低温及高水分含量的环境下,挥发性物质的来源以油脂氧化为主,多为醛、酮、醇类物质;随着温度的升高及水分含量的降低,美拉德反应所产生的挥发性物质对整体挥发性物质的构成具有更多的贡献,代表物质为吡嗪、呋喃、吡咯以及含硫化合物。另外,BIRCH等[10-11]讨论了酵母种类、浓度和发酵温度对于面包产品最终风味的影响,通过对烤制面包的挥发性物质进行动态顶空收集并鉴定,发现酵母浓度的增加,促进了与酵母发酵相关的挥发性物质的产生,如丁二酮和苯乙醛。而高发酵温度(15、35 ℃)增加了与油脂氧化相关的挥发性物质,如己醛和庚醛。
顶空固相微萃取技术(headspace-solid phase micro-extraction,HS-SPME)主要用于气体、液体或者固体样本中挥发性组分的检测。不仅方便快捷,对挥发性物质检测十分灵敏,并且可以有效对含量较低、挥发性低的物质起到富集作用,因此对挥发性物质的检测研究中运用最多。例如REGA等[12]就利用此技术对橙汁的挥发物质顶空聚集吸附后进行了气相色谱-质谱联用(gas chromatography-mass spectrometer,GC-MS)分析。
综上,现阶段面食制品的风味研究主要集中于寻找其特征风味和某些特征风味化合物的前体物质及其与加工条件的关系,对热加工过程中发酵面食制品风味的生成规律仍然缺乏整体性的认识。因此,本文以发酵小麦粉为研究对象,探究在加热过程中不同温度点,发酵小麦粉挥发性物质的构成及特点,确定热加工过程中各挥发性物质形成的温度以及不同工艺温度点挥发性风味物质的构成特点,其目的在于揭示发酵面食制品在热加工过程中基础风味的形成规律,为提高和改善相关面食制品的风味提供理论基础。
1 材料与方法
1.1 材料与试剂
去皮小麦(水分、灰分、湿面筋质量分数分别为6.8%、 0.62%、 30.8%;稳定时间9.5 min),购于当地超市;C7~C30饱和烷烃及各挥发性物质标椎品,Sigma-Aldrich公司;二甲基硅油,天津市大茂化学试剂厂;安琪高活性干酵母,安琪酵母股份有限公司。
1.2 仪器与设备
Buhler制粉机,瑞士布勒公司;Supelco 50/30 μm DVB/CAR/PDMS手动固相微萃取(SPME)萃取头,美国Supelco公司;Agilent 7890A/5975C气相色谱质谱联用仪,安捷伦科技有限公司;BS224S电子分析天平,赛多利斯科学仪器;HH-4型数显恒温水浴锅,常州智博瑞仪器制造有限公司;Scientz-10ND型冷冻干燥机,宁波新芝生物科技有限公司。
1.3 实验方法
1.3.1 样品处理
应用制粉机采用AACC26—21A方法获得小麦粉[3]。发酵小麦粉制作工艺:首先取100 g小麦粉,按1%的质量分数加入1 g酵母粉,再加入60 mL水一起搅拌至表面光滑,于32 ℃,75%的湿度下醒发至2倍体积;然后取出面团于-80 ℃下迅速降温,并立即冻干,得到冻干后的发酵小麦粉于-30 ℃保藏,用于实验。
1.3.2 加热过程及挥发性物质的萃取
取发酵小麦粉和水以5∶4(g∶mL)混合为光滑面团,并称取3.6 g面团于20 mL顶空进样瓶1中均匀涂壁,以获得最大接触面积,且能够迅速传热,减少面团结构对挥发性物质挥发的阻碍。加热过程采用真空辅助加热系统,把装有面团的样品瓶1于60 ℃的油浴锅中加热30 min,使挥发性物质在瓶内达到饱和;与此同时,准备一个空的20 mL顶空进样瓶2于60 ℃水浴锅中维持温度恒定,并使用真空泵对进样瓶2做抽真空利用进样瓶1、2之间的压力差,通过聚四氟乙烯管连接3 min,使进样瓶1中的气体导入进样瓶2中;然后用SPME萃取头对进样瓶2中挥发物质进行吸附30 min,同时对进样瓶1进行升温,当达到下一温度点(70、80、90、100、110、120、130 ℃)后(温度选择参考发酵面食制品的热加工工艺,大多数面食制品的热加工温度在100~200 ℃。同时,本文在加热至130 ℃后,面团已出现明显的碳化现象,故最终的温度定为130 ℃),进样瓶1连接真空泵和外界,利用真空泵抽气3 min至-0.1 MPa,使进样瓶1中残留气体去除,随后往复以上操作。实验示意图如图1所示。

图1 挥发性成分萃取实验示意图
Fig.1 Schematic diagram of volatile matter extraction
1.3.3 挥发性物质的分离与检测
采用GC-MS对所吸附的挥发性物质进行分离与检测。进样方式为将萃取头插入气相色谱进样口解析5 min后拔出。
色谱条件:色谱柱为Agilent HP-5MS(30 m×0.25 mm, 0.25 μm);柱温:初始温度35 ℃,保持3 min,随后以5 ℃/min的速率程序升温至280 ℃;载气为He,载气流速1 mL/min,进样口温度为260 ℃。质谱条件:EI电离源,电离能量70 eV;离子源温度230 ℃,四极杆温度150 ℃;采集方式为全扫描模式,离子扫描范围m/z 40~400。
以相同的分离检测条件对C7~C30饱和烷烃进行进样检测,用于计算各未知物的保留指数。通过保留指数筛选,并与NIST/EPA/NIH标准质谱库(版本2.2)以及各挥发物标准化合物比对,对未知化合物进行定性分析。
2 结果与分析
2.1 加热过程中发酵小麦粉挥发性物质的组成
基于色谱峰质谱图与NIST标准质谱库中质谱图的比照,以及未知物与标准品保留指数的对比,发酵小麦粉的加热过程中共发现88种挥发性化合物,分别为醛类19种、醇类15种、酮类11种、含苯衍生物15种、呋喃类11种、酸酯类10种和杂环类化合物7种。
如表1所示,挥发性醛类占所有鉴定化合物比例最大,并且含碳数6~10个的醛是加热早期的主要产物,包括己醛,庚醛,壬醛,反-2-庚烯醛和辛醛,这些醛被认为是小麦面包香气的主要成分[10],原材料中不饱和脂肪酸(如油酸,亚油酸和亚麻酸)是以上化合物形成的主要前体物质[13]。碳主链在C10~C12的醛类,如反,反-2,4-癸二烯醛,反-2-癸烯醛,2,4-癸二烯醛,十一醛,在低温下未被检测到,当温度逐渐升高时才被检出。
挥发性醇、酮类同样是加热过程中被检出的2种主要的挥发性化合物,并且许多醇类在整个加热过程中都可以被检测到,如3-甲基-1-丁醇、1-戊醇、1-己醇、1-庚醇、1-辛烯-3-醇等。研究发现,面包芯的主要风味物质1-己醇、1-辛烯-3-醇和1-辛醇均来自亚油酸的氧化反应[10, 14],同时,这几种挥发性醇相对含量的变化在整个加热过程中也是较大的。如表1所示,挥发性酮类中2-甲基-环戊酮和3-辛烯-2-酮在70 ℃加热后被检测到。其中,具有玫瑰香的3-辛烯-2-酮可在全麦面包的面包芯中检测到[15]。
在加热过程中共检测到了11种呋喃和15种含苯衍生物。特别是一些对面食制品整体风味有贡献的含苯类物质存在于整个加热过程中,如糠醛、苯甲醛、苯乙醛和苯乙酮等[16-17]。另外,几种具有更复杂的结构呋喃衍生物,如2-呋喃甲醇、1-(2-呋喃基)-乙酮、3-苯基-呋喃等,在高于120 ℃加热后被检测出来,这些挥发物多被认为是美拉德反应的产物,对面制品的整体风味轮廓有较大贡献。
酸酯类化合物的形成在加热过程中具有明显的规律性。整个加热过程中只存在少量低分子量的酯类,而大多数酸脂类化合物都是在温度较高时才被检测到,如丁酸丁酯、乙酸己酯和苯甲酸甲酯。虽然酸脂类化合物的相对含量较少,但它们在小麦面包芯香气中的贡献非常重要,因为它们具有较小的阈值和令人愉快的、甜的,果味味道[18]。
2.2 加热过程中发酵小麦粉挥发性物质构成的特点
为了直观地展示出加热过程中不同挥发物的形成温度,本文将各挥发性化合物的生成温度由温度轮廓图的形式展示出来(图2)。同时,通过对实验数据进行主成分分析以及作出含量变化的热度图(图3),探讨不同加热温度下发酵小麦粉挥发性物质的构成特点和变化规律。
表1 发酵小麦粉加热时产生的挥发性物质成分
Table 1 Volatile compounds from the fermented wheat flour in the heating process
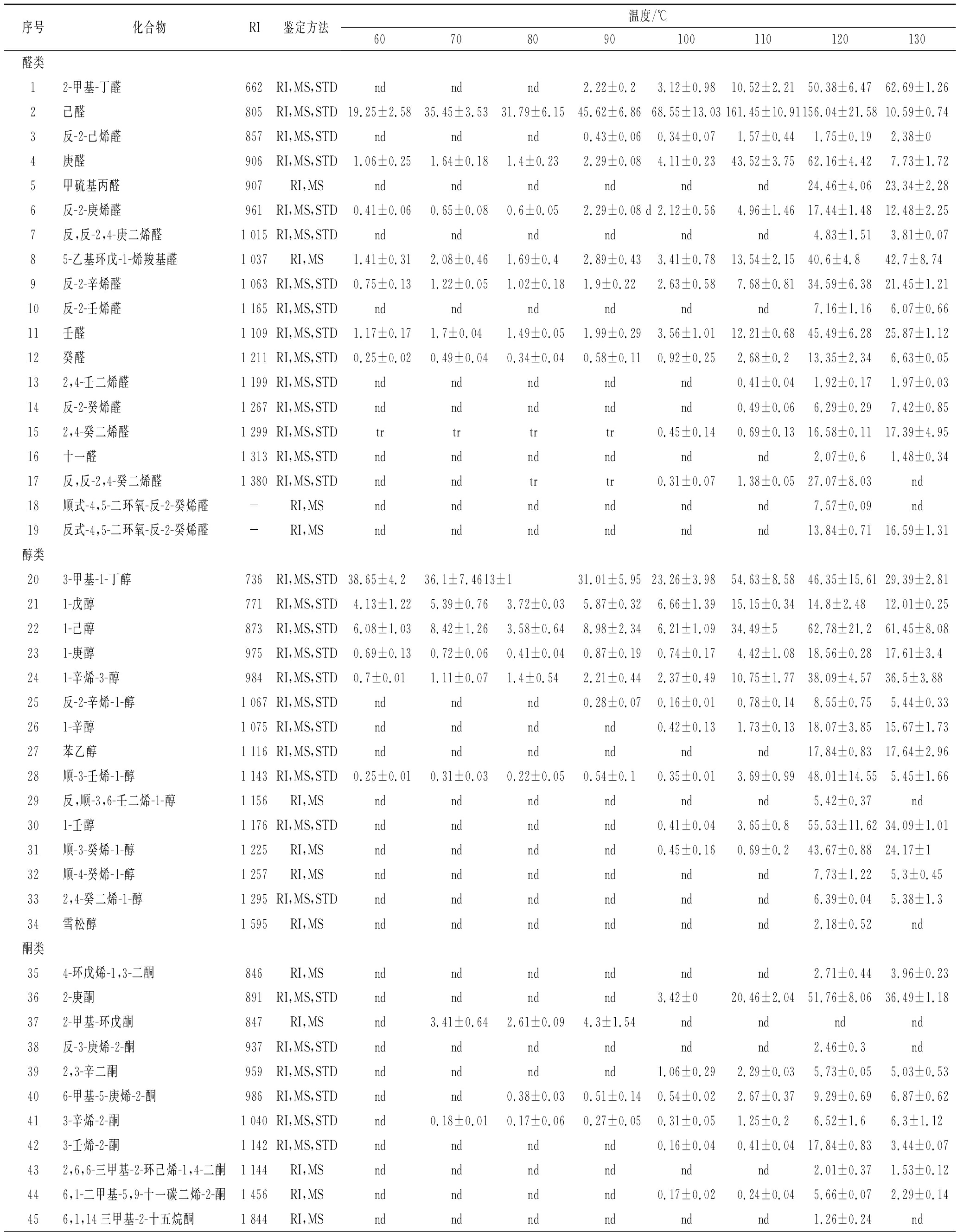
序号化合物RI鉴定方法温度/℃60708090100110120130醛类12-甲基-丁醛662RI,MS,STDndndnd2.22±0.23.12±0.9810.52±2.2150.38±6.4762.69±1.262己醛805RI,MS,STD19.25±2.5835.45±3.5331.79±6.1545.62±6.8668.55±13.03161.45±10.91156.04±21.5810.59±0.743反-2-己烯醛857RI,MS,STDndndnd0.43±0.060.34±0.071.57±0.441.75±0.192.38±04庚醛906RI,MS,STD1.06±0.251.64±0.181.4±0.232.29±0.084.11±0.2343.52±3.7562.16±4.427.73±1.725甲硫基丙醛907RI,MSndndndndndnd24.46±4.0623.34±2.286反-2-庚烯醛961RI,MS,STD0.41±0.060.65±0.080.6±0.052.29±0.08 d2.12±0.564.96±1.4617.44±1.4812.48±2.257反,反-2,4-庚二烯醛1 015RI,MS,STDndndndndndnd4.83±1.513.81±0.0785-乙基环戊-1-烯羧基醛1 037RI,MS1.41±0.312.08±0.461.69±0.42.89±0.433.41±0.7813.54±2.1540.6±4.842.7±8.749反-2-辛烯醛1 063RI,MS,STD0.75±0.131.22±0.051.02±0.181.9±0.222.63±0.587.68±0.8134.59±6.3821.45±1.2110反-2-壬烯醛1 165RI,MS,STDndndndndndnd7.16±1.166.07±0.6611壬醛1 109RI,MS,STD1.17±0.171.7±0.041.49±0.051.99±0.293.56±1.0112.21±0.6845.49±6.2825.87±1.1212癸醛1 211RI,MS,STD0.25±0.020.49±0.040.34±0.040.58±0.110.92±0.252.68±0.213.35±2.346.63±0.05132,4-壬二烯醛1 199RI,MS,STDndndndndnd0.41±0.041.92±0.171.97±0.0314反-2-癸烯醛1 267RI,MS,STDndndndndnd0.49±0.066.29±0.297.42±0.85152,4-癸二烯醛1 299RI,MS,STDtrtrtrtr0.45±0.140.69±0.1316.58±0.1117.39±4.9516十一醛1 313RI,MS,STDndndndndndnd2.07±0.61.48±0.3417反,反-2,4-癸二烯醛1 380RI,MS,STDndndtrtr0.31±0.071.38±0.0527.07±8.03nd18顺式-4,5-二环氧-反-2-癸烯醛-RI,MSndndndndndnd7.57±0.09nd19反式-4,5-二环氧-反-2-癸烯醛-RI,MSndndndndndnd13.84±0.7116.59±1.31醇类203-甲基-1-丁醇736RI,MS,STD38.65±4.236.1±7.4613±131.01±5.9523.26±3.9854.63±8.5846.35±15.6129.39±2.81211-戊醇771RI,MS,STD4.13±1.225.39±0.763.72±0.035.87±0.326.66±1.3915.15±0.3414.8±2.4812.01±0.25221-己醇873RI,MS,STD6.08±1.038.42±1.263.58±0.648.98±2.346.21±1.0934.49±562.78±21.261.45±8.08231-庚醇975RI,MS,STD0.69±0.130.72±0.060.41±0.040.87±0.190.74±0.174.42±1.0818.56±0.2817.61±3.4241-辛烯-3-醇984RI,MS,STD0.7±0.011.11±0.071.4±0.542.21±0.442.37±0.4910.75±1.7738.09±4.5736.5±3.8825反-2-辛烯-1-醇1 067RI,MS,STDndndnd0.28±0.070.16±0.010.78±0.148.55±0.755.44±0.33261-辛醇1 075RI,MS,STDndndndnd0.42±0.131.73±0.1318.07±3.8515.67±1.7327苯乙醇1 116RI,MS,STDndndndndndnd17.84±0.8317.64±2.9628顺-3-壬烯-1-醇1 143RI,MS,STD0.25±0.010.31±0.030.22±0.050.54±0.10.35±0.013.69±0.9948.01±14.555.45±1.6629反,顺-3,6-壬二烯-1-醇1 156RI,MSndndndndndnd5.42±0.37nd301-壬醇1 176RI,MS,STDndndndnd0.41±0.043.65±0.855.53±11.6234.09±1.0131顺-3-癸烯-1-醇1 225RI,MSndndndnd0.45±0.160.69±0.243.67±0.8824.17±132顺-4-癸烯-1-醇1 257RI,MSndndndndndnd7.73±1.225.3±0.45332,4-癸二烯-1-醇1 295RI,MS,STDndndndndndnd6.39±0.045.38±1.334雪松醇1 595RI,MSndndndndndnd2.18±0.52nd酮类354-环戊烯-1,3-二酮846RI,MSndndndndndnd2.71±0.443.96±0.23362-庚酮891RI,MS,STDndndndnd3.42±020.46±2.0451.76±8.0636.49±1.18372-甲基-环戊酮847RI,MSnd3.41±0.642.61±0.094.3±1.54ndndndnd38反-3-庚烯-2-酮937RI,MS,STDndndndndndnd2.46±0.3nd392,3-辛二酮959RI,MS,STDndndndnd1.06±0.292.29±0.035.73±0.055.03±0.53406-甲基-5-庚烯-2-酮986RI,MS,STDndnd0.38±0.030.51±0.140.54±0.022.67±0.379.29±0.696.87±0.62413-辛烯-2-酮1 040RI,MS,STDnd0.18±0.010.17±0.060.27±0.050.31±0.051.25±0.26.52±1.66.3±1.12423-壬烯-2-酮1 142RI,MS,STDndndndnd0.16±0.040.41±0.0417.84±0.833.44±0.07432,6,6-三甲基-2-环己烯-1,4-二酮1 144RI,MSndndndndndnd2.01±0.371.53±0.12446,1-二甲基-5,9-十一碳二烯-2-酮1 456RI,MSndndndnd0.17±0.020.24±0.045.66±0.072.29±0.14456,1,14三甲基-2-十五烷酮1 844RI,MSndndndndndnd1.26±0.24nd
续表1
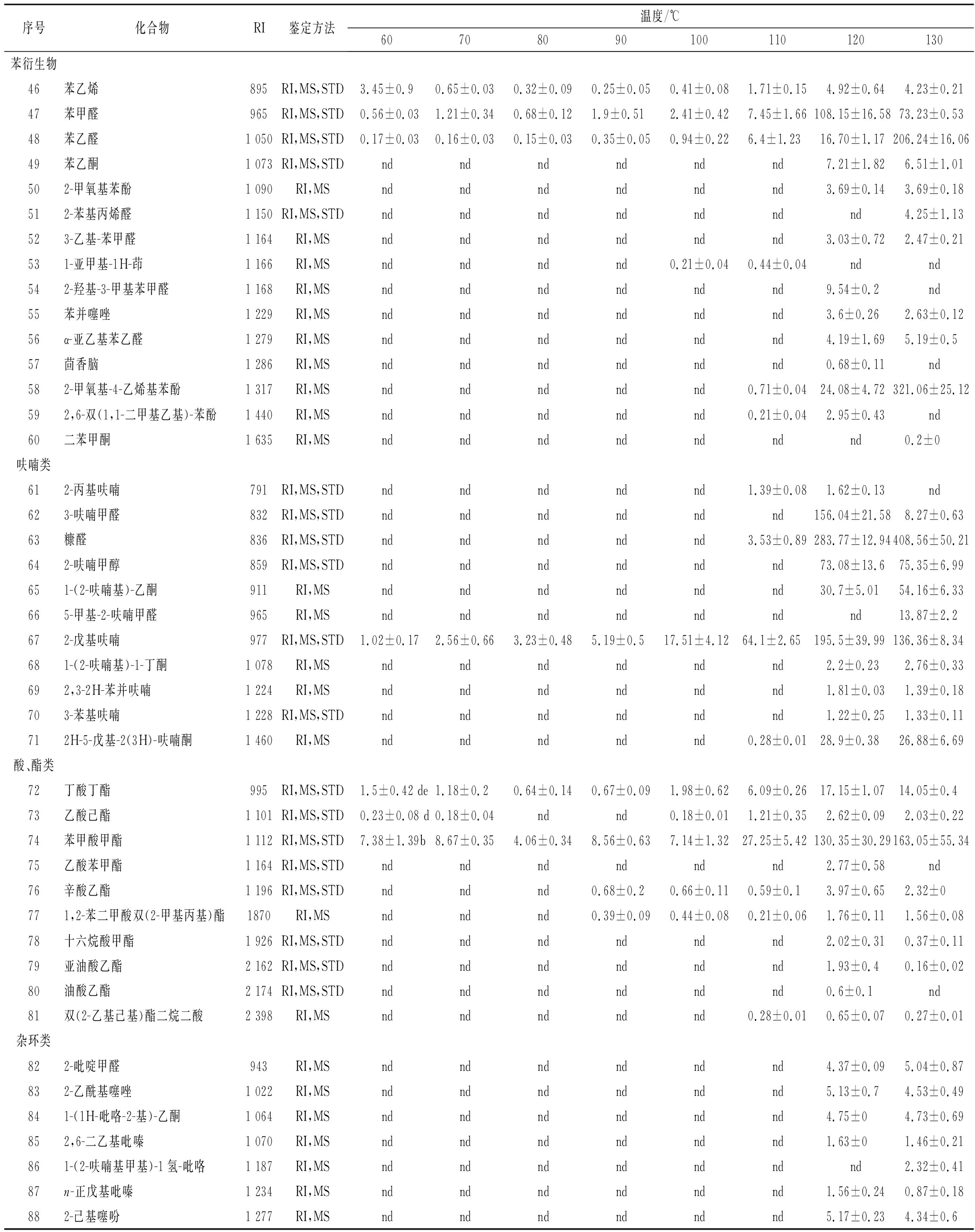
序号化合物RI鉴定方法温度/℃60708090100110120130苯衍生物46苯乙烯895RI,MS,STD3.45±0.90.65±0.030.32±0.090.25±0.050.41±0.081.71±0.154.92±0.644.23±0.2147苯甲醛965RI,MS,STD0.56±0.031.21±0.340.68±0.121.9±0.512.41±0.427.45±1.66108.15±16.5873.23±0.5348苯乙醛1 050RI,MS,STD0.17±0.030.16±0.030.15±0.030.35±0.050.94±0.226.4±1.2316.70±1.17206.24±16.0649苯乙酮1 073RI,MS,STDndndndndndnd7.21±1.826.51±1.01502-甲氧基苯酚1 090RI,MSndndndndndnd3.69±0.143.69±0.18512-苯基丙烯醛1 150RI,MS,STDndndndndndndnd4.25±1.13523-乙基-苯甲醛1 164RI,MSndndndndndnd3.03±0.722.47±0.21531-亚甲基-1H-茚1 166RI,MSndndndnd0.21±0.040.44±0.04ndnd542-羟基-3-甲基苯甲醛1 168RI,MSndndndndndnd9.54±0.2nd55苯并噻唑1 229RI,MSndndndndndnd3.6±0.262.63±0.1256α-亚乙基苯乙醛1 279RI,MSndndndndndnd4.19±1.695.19±0.557茴香脑1 286RI,MSndndndndndnd0.68±0.11nd582-甲氧基-4-乙烯基苯酚1 317RI,MSndndndndnd0.71±0.0424.08±4.72321.06±25.12592,6-双(1,1-二甲基乙基)-苯酚1 440RI,MSndndndndnd0.21±0.042.95±0.43nd60二苯甲酮1 635RI,MSndndndndndndnd0.2±0呋喃类612-丙基呋喃791RI,MS,STDndndndndnd1.39±0.081.62±0.13nd623-呋喃甲醛832RI,MS,STDndndndndndnd156.04±21.588.27±0.6363糠醛836RI,MS,STDndndndndnd3.53±0.89283.77±12.94408.56±50.21642-呋喃甲醇859RI,MS,STDndndndndndnd73.08±13.675.35±6.99651-(2-呋喃基)-乙酮911RI,MSndndndndndnd30.7±5.0154.16±6.33665-甲基-2-呋喃甲醛965RI,MSndndndndndndnd13.87±2.2672-戊基呋喃977RI,MS,STD1.02±0.172.56±0.663.23±0.485.19±0.517.51±4.1264.1±2.65195.5±39.99136.36±8.34681-(2-呋喃基)-1-丁酮1 078RI,MSndndndndndnd2.2±0.232.76±0.33692,3-2H-苯并呋喃1 224RI,MSndndndndndnd1.81±0.031.39±0.18703-苯基呋喃1 228RI,MS,STDndndndndndnd1.22±0.251.33±0.11712H-5-戊基-2(3H)-呋喃酮1 460RI,MSndndndndnd0.28±0.0128.9±0.3826.88±6.69酸、酯类72丁酸丁酯995RI,MS,STD1.5±0.42 de1.18±0.20.64±0.140.67±0.091.98±0.626.09±0.2617.15±1.0714.05±0.473乙酸己酯1 101RI,MS,STD0.23±0.08 d0.18±0.04ndnd0.18±0.011.21±0.352.62±0.092.03±0.2274苯甲酸甲酯1 112RI,MS,STD7.38±1.39b8.67±0.354.06±0.348.56±0.637.14±1.3227.25±5.42130.35±30.29163.05±55.3475乙酸苯甲酯1 164RI,MS,STDndndndndndnd2.77±0.58nd76辛酸乙酯1 196RI,MS,STDndndnd0.68±0.20.66±0.110.59±0.13.97±0.652.32±0771,2-苯二甲酸双(2-甲基丙基)酯1870RI,MSndndnd0.39±0.090.44±0.080.21±0.061.76±0.111.56±0.0878十六烷酸甲酯1 926RI,MS,STDndndndndndnd2.02±0.310.37±0.1179亚油酸乙酯2 162RI,MS,STDndndndndndnd1.93±0.40.16±0.0280油酸乙酯2 174RI,MS,STDndndndndndnd0.6±0.1nd81双(2-乙基己基)酯二烷二酸2 398RI,MSndndndndnd0.28±0.010.65±0.070.27±0.01杂环类822-吡啶甲醛943RI,MSndndndndndnd4.37±0.095.04±0.87832-乙酰基噻唑1 022RI,MSndndndndndnd5.13±0.74.53±0.49841-(1H-吡咯-2-基)-乙酮1 064RI,MSndndndndndnd4.75±04.73±0.69852,6-二乙基吡嗪1 070RI,MSndndndndndnd1.63±01.46±0.21861-(2-呋喃基甲基)-1氢-吡咯1 187RI,MSndndndndndndnd2.32±0.4187n-正戊基吡嗪1 234RI,MSndndndndndnd1.56±0.240.87±0.18882-己基噻吩1 277RI,MSndndndndndnd5.17±0.234.34±0.6
注:表中数据为峰面积(×106),为3次重复的平均值±标准误;“nd”,样品中未检测到该化合物;“tr”,痕量检测;“MS”,通过与质谱比对鉴定;“RI”,通过与保留指数比对鉴定;“STD”,通过与标准化合物比对鉴定
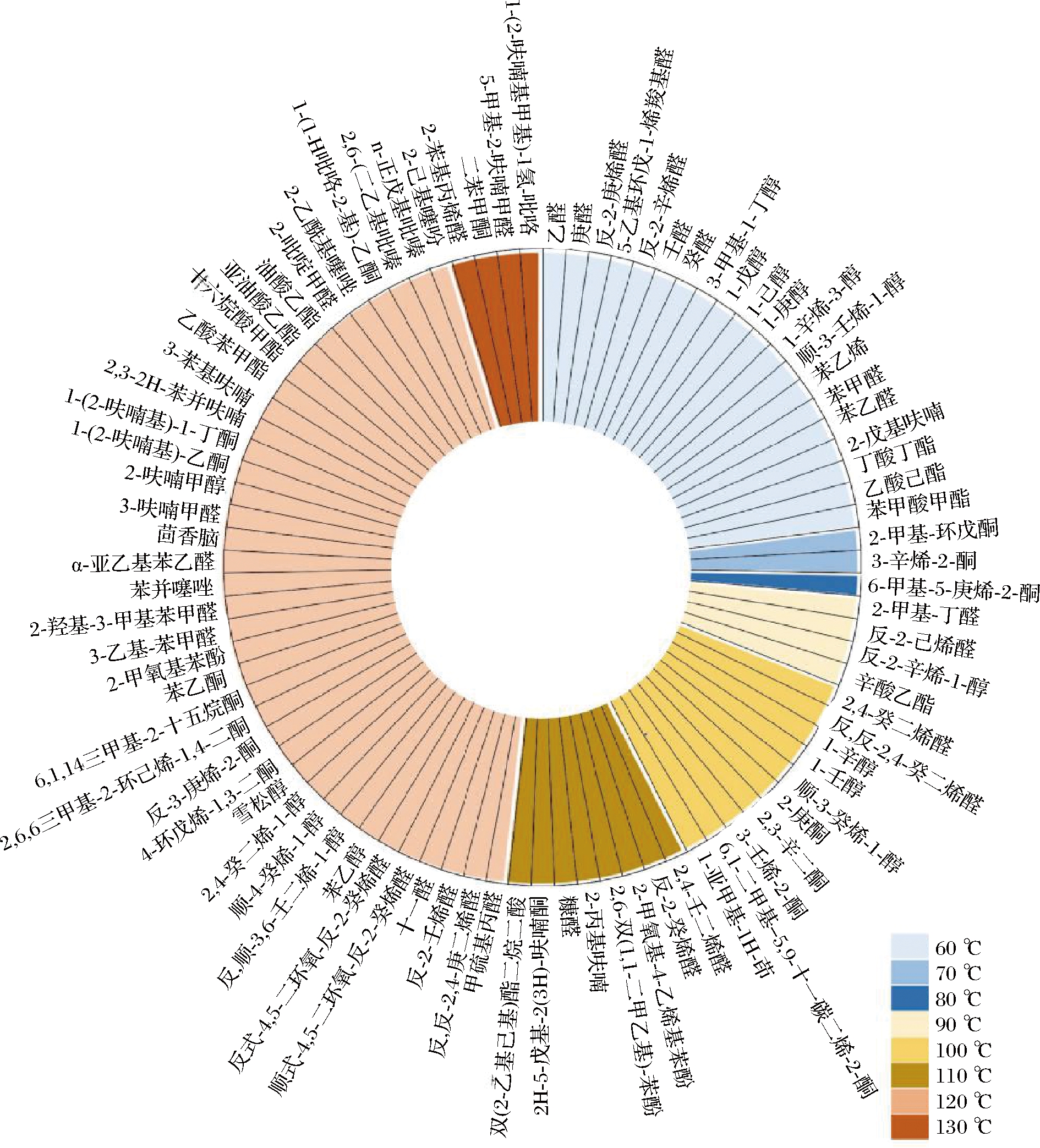
图2 加热过程中发酵小麦粉各挥发性物质的形成温度
Fig.2 The forming temperature of different volatile
compounds from fermented wheat flour during heating
由图2可知,不同温度下发酵小麦粉挥发性组分的构成有显著差异。在60 ℃时共鉴定出20种挥发物,包括醛(7种)、醇(6种)、芳烃(3种)、酸和酯(3种)以及呋喃类(1种)。通过与30 ℃(数据未给出)下发酵小麦粉挥发物的构成比较发现,这2个温度点的挥发物构成基本一致,说明这些化合物并不是在60 ℃产生的,它们是发酵小麦粉的基本挥发性成分。同时,从该温度下挥发性物质的构成来看,短链醛类和醇类是构成发酵小麦粉基本风味的主要物质。随着温度的升高,在70、80、90 ℃时分别检测出了2种、1种和4种新的挥发物。这些挥发物都是醛、酮和酯类化合物,且碳链数都低于10个。由图3可知,在低于90 ℃时,这些挥发物都具有相类似的变化趋势,除2-甲基-丁醛在110 ℃会大量产生外,其余挥发性化合物的含量均随温度的升高有略微的升高,说明在温度较低时(<100 ℃)挥发物的生成反应并不剧烈。当温度>100 ℃时,开始形成大量的长链醇、醛类化合物,具体为在100、110、120和130 ℃下分别新产生了10、8、38和4种挥发性物质,包括大量的油脂氧化的产物,如2,4-壬二烯醛、1-壬醇等醛、醇类化合物,同时还包括一定量的美拉德反应产物,如甲硫基丙醛等一些含氮、硫化合物。这种现象是由于温度升高和水分活度降低增加了美拉德反应和脂质的氧化,同时高温也增加了挥发性物质的挥发程度[19]。特别是温度达到120 ℃时,新产生的挥发性物质数目最多,共产生新挥发性产物38种,包括醛(6种)、醇(5种)、酮(4种)、苯衍生物(7种)、呋喃类(6种)、酸和酯(4种)和杂环类(6种)。因此,可以推断120 ℃ 是发酵小麦粉在热加工过程中风味形成的关键温度点,在此温度下,发酵小麦粉整体的挥发性物质轮廓变得更加丰富。
由图3中色调的冷暖变化可知,在加热过程中温度较低时(<100 ℃),绝大多数挥发物的相对含量变化较小。当温度超过100 ℃尤其是当温度接近于120 ℃时,大多数化合物的颜色开始加深,表明120 ℃不仅是新挥发物生成最多的一个温度点,同时也是已有挥发物相对含量大幅度增加的一个关键温度点。但并不是所有挥发性化合物的含量都随着温度的升高而提高,如己醛、庚醛、反-2-辛烯醛、壬醛、癸醛、3-甲基-1-丁醇、1-辛烯-3-醇、顺-3-壬烯-1-醇、1-壬醇、顺-3-癸烯-1-醇和3-呋喃甲醛等醇、醛类物质在加热后期的含量有下降的趋势,研究发现造成这种现象的原因在于发酵过程对面团加热过程中的油脂氧化反应有一定的抑制作用[14]。同时,由主成分分析结果可知,加热过程中不同温度点的挥发物构成具有明显的差异,由图4可知,不同温度点在得分图中可以明确地被分开,其中主成分1对总差异有58.0%的贡献,主成分2对总差异有16.3%的贡献。加热过程中发酵小麦粉在60~100 ℃的样品均位于第1主成分的负载荷区域且有重合,这表明在这些温度点发酵小麦粉挥发性物质的构成区别不大。而高温点发酵小麦粉挥发性物质的构成有较大差异,特别是当温度>110 ℃时,各温度点在得分图中可以被明显区分开来,分别位于坐标轴1、2、4象限,这表明当温度高于110 ℃时发酵小麦粉产生的挥发性物质开始有显著差异。通过比较与得分图相对应的载荷图(图5)可知,庚醛、1-戊醇、顺-3-壬烯-1-醇、3-壬烯-2-酮和双(2-乙基己基)酯二烷二酸是120 ℃样品区别于其他温度点主要的差异来源物质;在130 ℃时,2-甲氧基-4-乙烯基苯酚、糠醛和苯乙醛对差异的贡献则较大。研究发现,苯乙醛和糠醛的形成多是美拉德反应产生的[19],1-戊醇、庚醛则分别来自于亚油酸和油酸的自动氧化[14]。

图3 不同加热温度下发酵小麦粉挥发性物质热图
Fig.3 Heatmaps of whole volatile compounds in the
course ofduring heating
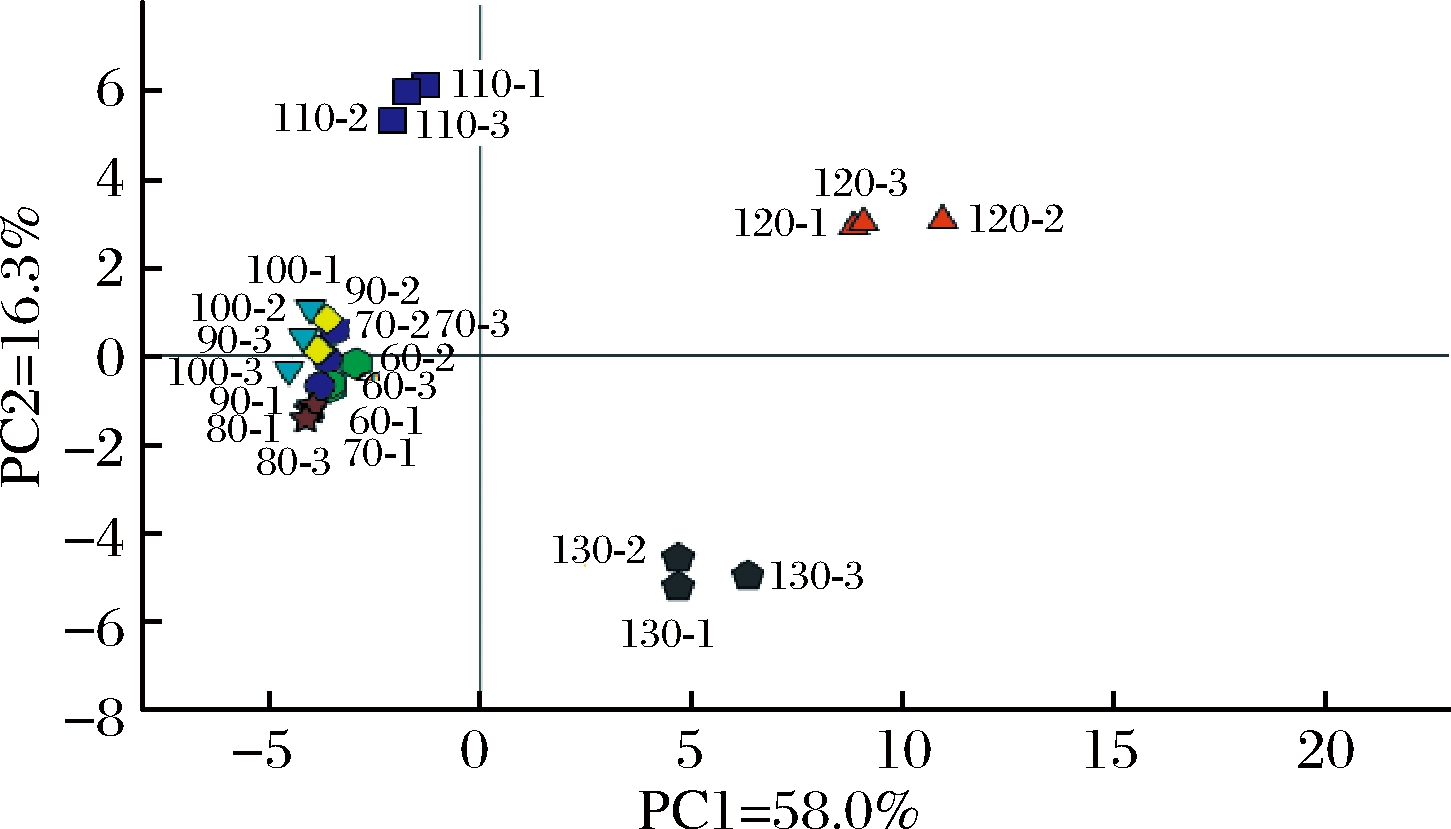
图4 加热过程中发酵小麦粉挥发性物质
主成分分析得分图
Fig.4 Score scatter plot of volatiles from fermented
wheat flour during heating

图5 加热过程中发酵小麦粉挥发性物质
主成分分析载荷图
Fig.5 Loading plot of volatiles from fermented
wheat flour during heating
加热过程中的脂质氧化是发酵小麦粉风味的重要来源之一,在所有挥发性产物中,如己醛、庚醛、壬醛、反-2-庚烯醛和辛醛等醛类,1-己醇、1-辛烯-3-醇和1-辛醇等醇类及苯甲醛、3-辛烯-2-酮和苯乙酮等醛酮均是发酵小麦粉相关制品风味和香气的主要来源,这些物质大多数源于脂质的氧化反应。在整个加热过程中,上述物质均随着加热温度升高含量不断增加,在120 ℃达到峰值,而后随着温度的升高含量开始下降。高温下生成的挥发性物质大部分都具有特殊香气,如反,反-2,4-癸二烯醛具有清香气味,浓度低时类似葡萄柚和柑橘的香味;反-2-癸烯醛有橙子及鸡、家禽肉香味;苯乙醇具有清甜的玫瑰样花香等,这些挥发性物质均于120 ℃开始生成,它们使相关面食制品拥有更加丰富和饱满的风味。美拉德反应是面食制品风味的另一个重要来源,其反应速度随加工温度的升高而增加,如1-(2-呋喃基)-乙酮、3-苯基-呋喃等被认为是美拉德反应产物的物质,均于120 ℃下生成。同时,这些物质随着温度继续升高含量呈上升趋势,然而若温度过高可能致使美拉德反应产生致癌物质,对食品安全造成影响。
综上,120 ℃是加热过程中发酵小麦粉制品风味形成的一个关键温度控制节点,大部分基础风味物质在该温度下达到峰值,同时该温度下也因美拉德反应、脂质氧化等反应而生成了许多特征风味物质。因此,通过调节和控制加热过程中的温度和相应温度下的保留时间,对于改善和调控发酵小麦粉制品的风味品质在理论层面是完全可行的。
3 结论
真空辅助固相微萃取气质联用技术可以有效检测热加工过程中发酵小麦粉的挥发性物质。120 ℃是整个热加工过程中的重要关键温度点,大多数挥发性物质在这个温度下生成,其他挥发性物质的相对含量也开始大幅度提高。基本明晰了加热过程中各温度下挥发性物质生成规律及变化的趋势,通过调节和控制加热过程中的温度和相应温度下的保留时间,对于实现发酵小麦粉热加工过程中的人工调节在理论层面是可行的。
[1] 李里特,薛佳.论传统小麦面食的现代化与工业化[J]. 粮食与食品工业, 2010,17(5): 12-15.
[2] 李里特.中国传统发酵面制品创新与面食现代化[J]. 粮食与食品工业, 2009,16(5):6-8.
[3] HANSEN A S,SCHIEBERLE P.Generation of aroma compounds during sourdough fermentation: Applied and fundamental aspects[J].Trends in Food Science & Technology,2005,16(1):85-94.
[4] WANG C,CHIN C K,HO C T,et al.Changes of fatty acids and fatty acid-derived flavor compounds by expressing the yeast Δ-9 desaturase gene in tomato[J].Journal of Agricultural and Food Chemistry,1996,44(10):3 399-3 402.
[5] CREMER D R,EICHNER K.The reaction kinetics for the formation of Strecker aldehydes in low moisture model systems and in plant powders[J].Food Chemistry,2000,71(1):37-43.
[6] YAHYA H,LINFOREH R S,COOK D J.Flavour generation during commercial barley and malt roasting operations:A time course study[J].Food Chem,2014,145:378-387.
[7] HELOU C,GADONNA W P,ROBERT N,et al.The impact of raw materials and baking conditions on Maillard reaction products, thiamine,folate,phytic acid and minerals in white bread[J].Food Funct,2016,7(6):2 498-2 507.
[8] PURLIS E.Browning development in bakery products:A review[J].Journal of Food Engineering,2010,99(3):239-249.
[9] HWANG H I,HARTMAN T G,KARWE M V,et al.Aroma generation in extruded and heated wheat flour[J]. Lipds in Food Flavors,1994, 558:144-157.
[10] BIRCH A N,PETERSEN M A,HANSEN Å S.The aroma profile of wheat bread crumb influenced by yeast concentration and fermentation temperature[J].LWT - Food Science and Technology,2013,50(2):480-488.
[11] BIRCH A N,PETERSEN M A,ARNEBORG N,et al. Influence of commercial baker′s yeasts on bread aroma profiles[J].Food Research International,2013, 52(1):160-166.
[12] REGA B,FOURNIER N,GUICHARD E.Solid phase microextraction (SPME) of orange juice flavor:Odor representativeness by direct gas chromatography olfactometry (D-GC-O)[J].Journal of Agricultural and Food Chemistry,2003,51(24):7 092-7 099.
[13] CORSETTI A,SETTANNI L.Lactobacilli in sourdough fermentation[J].Food Research International,2007,40(5):539-558.
[14] MAIRE M,REGA B,CUVELIER M E,et al.Lipid oxidation in baked products: Impact of formula and process on the generation of volatile compounds[J].Food Chem,2013,141(4):3 510-3 518.
[15] NOR QHAIRUL IZZREEN M N,PETERSEN M A,HANSEN Å S.Volatile compounds in crumb of whole-meal wheat bread fermented with different yeast levels and fermentation temperatures[J].Cereal Chemistry Journal,2016,93(2):209-216.
[16] MATTIOLO E,LICCIARDELLO F,LOMBARDO G M,et al.Volatile profiling of durum wheat kernels by HS-SPME/GC-MS [J].European Food Research and Technology,2016,243(1):147-155.
[17] RENMAN S U,PATERSON A,PIGGOTT J R.Flavour in sourdough breads:A review[J].Trends in Food Science &Technology,2006,17(10):557-566.
[18] PICO J,BERNAL J,GOMEZ M.Wheat bread aroma compounds in crumb and crust: A review[J].Food Res Int,2015,75:200-215.
[19] HOFMANN T,MÜNCH P,SCHIEBERLE P.Quantitative model studies on the formation of aroma-active aldehydes and acids by Strecker-type reactions[J].Journal of Agricultural and Food Chemistry,2000,48(2):434-440.