地参为唇形科地笋属植物硬毛地笋Lycopus lucidus var. hirtus Regel的干燥根茎,其性平、味甘,有化瘀止血、益气利水之功效[1],是我国名贵的中草药,曾收载于2009版《湖南省中药材标准》[2],晚秋以后采挖出饱满脆嫩的根茎可作蔬菜食用,营养丰富、味道鲜美,享有“蔬菜珍品”之美誉,是一种传统的药食兼用佳品[3]。前期研究表明地参主要含有酚酸类[4]、多糖类[5]、挥发油[6]、三萜类、黄酮类[7-8]等资源性化学成分,具有抗氧化、抗炎、增强免疫、降血糖血脂、抗肿瘤等多种生物活性[9-11],极具药用价值,同时地参还含有丰富的氨基酸、粗蛋白、矿物元素等物质[12-14],营养价值高。
矿物元素是促进植物光合作用和有机物合成必不可少的成分[15],是评价食材营养价值和安全性的重要因素[16]。近年来兴起的“元素医学”研究发现,矿物元素对中药的疗效有促进和协同作用[17-18]。矿物元素的种类和含量不仅与植物的种类、年份等自身因素有关,还与种植的环境因素(土壤、气候、水源等)以及肥料施用情况有关,可以表征不同产地的品质差异,用于药材产地判别[19],同时药材中重金属超标问题也日益突出,成为影响其安全性和进出口的重要因素[20]。因此,研究地参中元素的种类和含量,分析其分布规律,可对地参品质评价和栽培引种提供参考。
目前,元素测定的方法主要集中在原子吸收光谱法[21]、原子荧光光谱法[22]、电感耦合原子发射光谱法(inductively coupled plasma optical emission spectrometer,ICP-OES)[14,16]、电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,ICP-MS)[18,20,23]等。原子吸收光谱法效率低、耗时长,且存在较强的基体效应[24];原子荧光光谱法灵敏度高,被广泛应用于食品中砷、汞的测定,是食品安全国家标准强制使用方法[25-26];ICP-OES法可同时进行多元素测定,但灵敏度较低,不利于痕量元素的检测;而ICP-MS法具有灵敏度高、干扰少、线性动态范围宽且样品引入方便等优点,适用于不同含量级别的多元素同时测定[27-28],是目前较为常用的元素测定方法。微波消解前处理技术相较于干法和湿法消解具有消解更彻底、速度快且损失小等优点[28],应用较广。
地参在我国大部分地区都有分布和栽培,其中以云南、广西、江苏、山东、四川、重庆等地为主产区[29],目前,针对不同产地地参元素的系统研究未见报道。因此,本研究利用凯氏定氮法,微波消解前处理技术结合ICP-MS和氢化物原子荧光光谱法首次对我国地参主产区栽培品种中22种元素进行测定,并利用相关性、主成分和聚类分析对其进行分析和评价,基本代表了我国主产区地参中元素的总体情况,以期为地参药食兼用的药用价值、营养价值以及安全性提供基础数据,也为地参资源的栽培引种、产地判别和开发利用提供参考依据。
1 材料与方法
1.1 材料与试剂
地参自采或委托采集于我国地参主要栽培基地,详见表1,鉴定为唇形科地笋属植物硬毛地笋的干燥根茎。将地参洗净泥沙,晾干水分,置于恒温干燥箱45 ℃烘干至恒重,将其粉碎过35目筛,备用。
表1 地参产地信息
Table 1 The habitats of Lycopus lucidus var. hirtus Regel
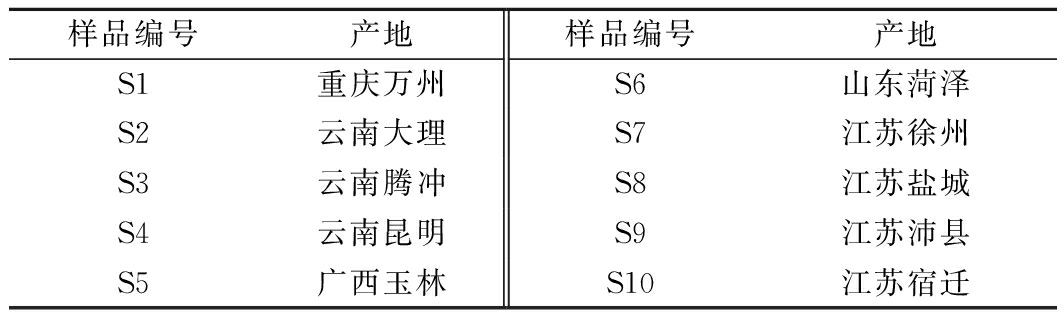
样品编号产地样品编号产地S1重庆万州S6山东菏泽S2云南大理S7江苏徐州S3云南腾冲S8江苏盐城S4云南昆明S9江苏沛县S5广西玉林S10江苏宿迁
单元素标准溶液(1 000 μg/mL):K(GSB04-1733-2004)、Na(GSB04-1738-2004)、Ca(GSB04-1720-2004)、Mg(GSB04-1735-2004)、Al(GSB04-1713-2004)、P(GSB04-1741-2004)、Fe(GSB04-1726-2004)、Zn(GSB04-1761-2004)、Se(GSB04-1751-2004)、Cu(GSB04-1725-2004)、Co(GSB04-1722-2004)、Ba(GSB04-1717-2004)、Mo(GSB04-1737-2004)、B(GSB04-1716-2004)、Ni(GSB04-1740-2004)、Mn(GSB04-1736-2004)、Cd(GSB04-1721-2004)、Cr(GSB04-1723-2004)、Pb(GSB04-1742-2004)、As(GSB04-1714-2004)、Hg(GSB04-1729-2004),国家有色金属及电子材料分析测试中心;MOS级浓HNO3,北京化学试剂研究所;实验用水为去离子超纯水;其他试剂均为优级纯,成都科龙试剂厂。实验所用容量瓶、移液管、烧杯等玻璃器皿均采用10%(体积分数)HNO3溶液浸泡24 h,然后用去离子超纯水冲洗干净,备用。
1.2 主要仪器
EXPEC 7000型电感耦合等离子体质谱仪,聚光科技(杭州)股份有限公司;AFS-8510型原子荧光光度计,北京海光仪器有限公司;MARS6型高压微波消解仪,美国CEM公司;Kjeltec 8400型全自动凯氏定氮仪,丹麦FOSS分析仪器公司;Milli-Q Advantage A10型超纯水机,美国Millipore公司;SQP Sartorius型万分之一电子天平,德国Sartorius公司。
1.3 分析方法
1.3.1 样品前处理
(1)称取地参样品粉末0.35 g(精确至0.000 1 g)于消化管中,参照标准[30]制备样品消化液,全自动凯氏定氮仪蒸馏滴定测定N元素含量。
(2)取地参样品粉末0.25 g(精确至0.000 1 g)于聚四氟乙烯消解罐内,加入8 mL浓HNO3,密封,浸泡过夜,置于微波消解仪中,按设定的消解程序处理:先经12 min由室温升温至150 ℃,保持10 min,然后以8 ℃/min的速率升温至190 ℃,保持20 min。消解完全后,取出消解罐,在通风橱中以120 ℃将酸挥尽,转移并用去离子超纯水定容至50 mL容量瓶中。取8 mL浓HNO3同法制备空白溶液。Hg测定时,无需挥酸,直接转移定容至25 mL测定;As测定时,加入5%硫脲和5%抗坏血酸2.5 mL,50%(体积分数) HCl 2.5 mL,定容至25 mL反应30 min后测定。
1.3.2 标准工作溶液的制备
分别精密移取21种元素标准溶液适量,用0.5%(体积分数)HNO3溶液逐级稀释,配制成K、Na、Ca、Mg、Al、P、Fe质量浓度为0、40、200、400、1 200、2 000 μg/L的混合标准工作液1;B、Mn、Zn、Cu、Ba质量浓度为0、10、50、100、300、500 μg/L,Se、Co、Ni、Cd、Cr、Pb质量浓度为0、1、5、10、30、50 μg/L、Mo质量浓度为0、0.1、0.5、1、3、5 μg/L的混合标准工作液2,供ICP-MS分析。As质量浓度为0、2、4、8、12、16 μg/L,Hg质量浓度为0、0.4、0.8、1.6、2.4、3.2 μg/L,供氢化物原子荧光光谱法分析。
1.3.3 元素测定
调节各仪器条件,优化其工作参数,采用全自动凯氏定氮仪测定N,氢化物发生原子荧光光谱法测定As、Hg ICP-MS测定K、Na、Ca、Mg、Al、P、Fe、B、Mn、Zn、Cu、Ba、Se、Co、Ni、Cd、Cr、Pb、Mo。
1.4 数据处理
采用Microsoft Excel 2007软件对测定数据进行处理,计算各元素含量平均值,以![]() 表示。采用SPSS 20软件对数据进行相关性分析、主成分分析和聚类分析。
表示。采用SPSS 20软件对数据进行相关性分析、主成分分析和聚类分析。
2 结果与分析
2.1 方法学考察
2.1.1 方法的线性关系
将1.3.2的系列标准工作液按照优化后的仪器参数进样测定,仪器工作站自动得出各元素的线性回归方程及线性关系。线性回归方程、线性范围、相关系数如表2所示,结果显示各元素标准曲线线性相关系数为0.998 1~0.999 9,表明所用方法线性关系均良好。
2.1.2 精密度试验
取同一标准溶液按1.3.3平行测定6次,计算各元素浓度的相对标准偏差(relative standard deviation,RSD)值。结果显示各元素RSD值为0.58%~2.79%,表明仪器精密度良好,符合分析方法要求。
2.1.3 重复性试验
精密称取地参样品(S1)0.25 g,平行6份,按1.3.1进行样品溶液制备,1.3.3测定并计算各元素质量分数的RSD值为1.09%~2.49%,表明方法的重复性良好。
2.1.4 稳定性试验
取同一样品溶液(S1),按1.3.3每隔0.5 h测定1次,持续6次,测定各元素质量分数,计算RSD值为0.67%~2.85%,表明样品溶液在3 h内稳定性良好。
表2 21种元素的线性回归方程、线性范围、相关系数
Table 2 Linear equation, linear range and correlation
coefficient of 21 kinds elements

元素标准曲线相关系数线性范围/(μg·L-1)KY=1.999×10-5X-107.30.999 740~2 000NaY=1.593×10-5X-4320.999 940~2 000CaY=1.987×10-2X-1220.999 940~2 000MgY=2.381×10-5X-14.020.999 940~2 000AlY=1.913×10-5X-5.8080.999 940~2 000PY=4.106×10-4X+20.730.999 440~2 000FeY=1.078×10-5X-13.990.999 940~2 000ZnY=4.794×10-5X-9.360.998 910~500CuY=5.952×10-5X+10.920.998 710~500BaY=8.867×10-6X-0.1010.999 810~500MnY=9.999×10-6X+1.4690.999 910~500BY=9.746×10-5X+4.7030.998 110~500MoY=6.905×10-5X-0.0330.999 90.1~5CoY=1.396×10-5X+0.9740.998 31~50NiY=4.064×10-5X-0.2220.999 91~50SeY=6.136×10-3X-14.890.999 91~50CdY=9.304×10-5X-0.0020.999 91~50CrY=1.516×10-5X+1.3880.998 71~50PbY=3.109×10-5X-0.051 20.999 81~50AsY=126.808X+19.4500.999 92~16HgY=437.631X-16.9770.999 50.4~3.2
2.1.5 加样回收率试验
精密称取已测定含量的地参样品(S1)0.25 g各6份,分别加入各元素标准溶液适量,按1.3.1项下进行样品溶液制备,1.3.3项下测定并计算回收率和RSD值,结果表明各元素的平均回收率为94.36%~108.05%,RSD值为0.97%~2.68%,符合分析方法要求。
2.2 地参样品中22种元素测定结果
取10个不同产地地参样品按1.3.1进行样品溶液制备,平行3份,并测定,结果见表3,地参中含有丰富的营养元素和无机元素,不同产地元素种类大致相同,但含量存在一定差异。
营养元素N是构成蛋白质的基础元素,含量较高,不同产地平均含量为20.01 mg/g。其中南方产区(S1、S2、S3、S4、S5)的含量极为接近,平均含量为13.12 mg/g;北方产区(S6、S7、S8、S9)的结果更为接近,平均值为23.81 mg/g,约为南方的2倍;产自江苏宿迁(S10)的地参样品中含量最高,为39.26 mg/g。地参中P平均含量为3.10 mg/g,不同产地的含量规律同N元素。
在20种无机元素中,K、Ca、Mg这3种元素的平均含量远远高于其他元素,其中含量最高的是K,平均值为21.98 mg/g,其次是Ca(1.81 mg/g)和Mg(1.24 mg/g)。K含量在样品S1~S6中基本一致,但在同为江苏产地的S10样品中达到最高值(26.47 mg/g),S8中最低(17.63 mg/g);Ca、Mg在不同产区含量无明显规律,江苏徐州(S7)样品中Ca、Mg含量均为最高。
微量元素中Na含量最高,平均含量为315.58 μg/g,但样品中Na的含量相差较大,江苏盐城(S8)样品中Na含量最高(929.80 μg/g),约为江苏沛县(S9)样品的13倍。其次是Al(246.50 μg/g)、Fe(156.14 μg/g)、Zn(37.01 μg/g)、Mn(29.23 μg/g)、Cu(25.94 μg/g)、Ba(9.90 μg/g)、Ni(6.26 μg/g)、B(3.98 μg/g)、Cr(1.12 μg/g)、Mo(0.76 μg/g)、Co(0.52 μg/g),Se具有较低的含量(0.132 μg/g)。重庆万州(S1)样品中Fe、Al、Mn、Ba、Co含量最高,江苏徐州(S7)样品中Zn、Cu、Cr、Se、B含量最高,广西玉林(S5)样品中Ni含量最高,江苏沛县(S9)样品中Mo含量最高。
重金属元素中,Cu的含量范围在17.50~52.84 μg/g,平均含量25.94 μg/g;Cd含量范围为0.009~0.177 μg/g,平均含量0.054 μg/g;Pb含量为0.069~2.141 μg/g,平均含量0.517 μg/g;As含量为0.040~0.730 μg/g,平均含量0.233 μg/g;Hg的含量最低(0.010 μg/g)。Cd、Hg在各产区中的含量相差不大,Pb、As存在较大差异,江苏徐州(S7)样品中Pb、As含量均为各产区中最高,但均未超过《药用植物及制剂外经贸绿色行业标准》[31]的相关规定(Pb≤5.0 μg/g,As≤2.0 μg/g),而样品S1、S4、S6~S10中的Cu及重金属总量均超标(Cu≤20.0 μg/g,总量≤20.0 μg/g)。
2.3 地参样品中22种元素含量的相关性分析
相关性分析采用文献[17-18]报道的方法,利用SPSS 20软件对各元素进行分析,结果详见表4,地参中有31对元素呈极显著正相关(P<0.01):Ca-Mg、N-P、Fe-Ba、P-Se、Fe-Co、Ba-Co、N-Mo、K-As、Mg-Se、Mg-Cu、Fe-Mn、Fe-Al等,地参中还有15对元素呈正相关(P<0.05):K-Mg、K-P、Ca-Fe、Mg-P、Zn-Se、P-Mo、N-As、Ca-Al、Zn-Cu等,表明上述46对元素在吸收积累过程中具有较好的协同作用,例如元素Mg能促进植物对Ca、Se、Cu、K、P的吸收富集,元素Fe能促进植物对Ba、Co、Mn、Al、Se、Ca的吸收富集。样品中N-Co、Co-B、Ba-Mo、N-Cd这4对元素呈负相关(P<0.05),Co-Mo、Mo-Cd这2对元素呈极显著负相关(P<0.01),表明这6对元素在吸收累积过程中存在拮抗作用,例如Co元素会抑制植物对N、B、Mo的吸收富集,Cd元素会抑制植物对N、Mo的吸收富集。
表3 不同产地地参中22种元素测定结果(n=3)
Table 3 Determination of 22 kinds of elements in samples from different habitats(n=3)
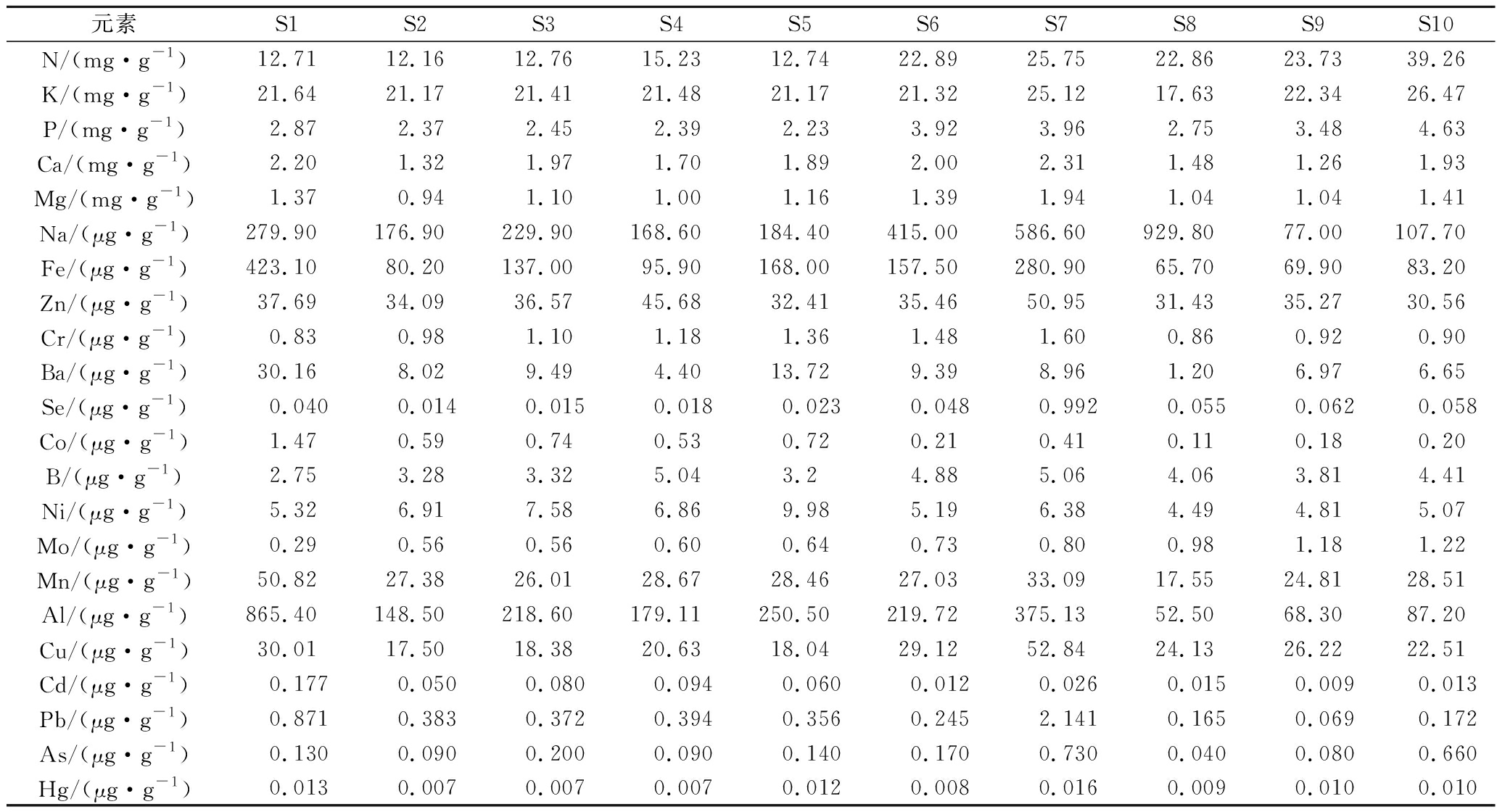
元素S1S2S3S4S5S6S7S8S9S10N/(mg·g-1)12.7112.1612.7615.2312.7422.8925.7522.8623.7339.26K/(mg·g-1)21.6421.1721.4121.4821.1721.3225.1217.6322.3426.47P/(mg·g-1)2.872.372.452.392.233.923.962.753.484.63Ca/(mg·g-1)2.201.321.971.701.892.002.311.481.261.93Mg/(mg·g-1)1.370.941.101.001.161.391.941.041.041.41Na/(μg·g-1)279.90176.90229.90168.60184.40415.00586.60929.8077.00107.70Fe/(μg·g-1)423.1080.20137.0095.90168.00157.50280.9065.7069.9083.20Zn/(μg·g-1)37.6934.0936.5745.6832.4135.4650.9531.4335.2730.56Cr/(μg·g-1)0.830.981.101.181.361.481.600.860.920.90Ba/(μg·g-1)30.168.029.494.4013.729.398.961.206.976.65Se/(μg·g-1)0.0400.0140.0150.0180.0230.0480.9920.0550.0620.058Co/(μg·g-1)1.470.590.740.530.720.210.410.110.180.20B/(μg·g-1)2.753.283.325.043.24.885.064.063.814.41Ni/(μg·g-1)5.326.917.586.869.985.196.384.494.815.07Mo/(μg·g-1)0.290.560.560.600.640.730.800.981.181.22Mn/(μg·g-1)50.8227.3826.0128.6728.4627.0333.0917.5524.8128.51 Al/(μg·g-1)865.40148.50218.60179.11250.50219.72375.1352.5068.3087.20 Cu/(μg·g-1)30.0117.5018.3820.6318.0429.1252.8424.1326.2222.51 Cd/(μg·g-1)0.1770.0500.0800.0940.0600.0120.0260.0150.0090.013 Pb/(μg·g-1)0.8710.3830.3720.3940.3560.2452.1410.1650.0690.172 As/(μg·g-1)0.1300.0900.2000.0900.1400.1700.7300.0400.0800.660 Hg/(μg·g-1)0.0130.0070.0070.0070.0120.0080.0160.0090.0100.010
表4 不同产地地参中22种元素间的相关性分析
Table 4 Correlation analysis of 22 elements in Lycopus lucidus var. hirtus Regel from different habitats

元素NKNaCaMgPFeZnCrBaSeCoBNiMoMnAlCuCdPbAsHgN1.000K0.6041.000Na0.113-0.4491.000Ca0.0930.4410.1251.000Mg0.4480.639*0.2630.800**1.000P0.904**0.711*0.0380.3180.663*1.000Fe-0.2540.1740.0890.751*0.5980.0421.000Zn-0.1140.2950.1100.4340.5250.0480.4051.000Cr-0.0190.2340.1360.5020.5650.1620.1750.5581.000Ba-0.3860.084-0.2360.5180.253-0.1130.878**0.036-0.1091.000Se0.2800.4760.3720.4970.836**0.4070.3800.739*0.598-0.0471.000Co-0.652*-0.067-0.2640.4230.028-0.4620.768**0.143-0.1630.890**-0.1191.000B0.5570.3200.2630.1530.4060.534-0.2590.5110.533-0.5930.468-0.655*1.000Ni-0.564-0.038-0.3310.158-0.125-0.5810.0390.0860.4260.119-0.0220.345-0.2911.000Mo0.842**0.3150.072-0.3600.0540.634*-0.605-0.290-0.145-0.638*0.0890.840**0.416-0.4611.000Mn-0.2390.307-0.2560.5980.4130.0380.905**0.311-0.0490.922**0.1540.840**-0.3310.014-0.5971.000Al-0.3700.079-0.0140.643*0.411-0.0900.971**0.3150.0060.936**0.1820.872**-0.3820.036-0.698*0.950**1.000Cu0.3280.4160.4280.5520.884**0.5350.5440.693*0.5090.1350.921**-0.0580.463-0.2880.0750.3180.3621.000Cd-0.642*-0.165-0.1930.359-0.069-0.5060.701*0.211-0.2540.795**-0.1840.955**-0.5350.2230.823**0.794**0.832**-0.0951.000Pb0.0110.4080.2970.645*0.818**0.2070.655*0.796**0.5390.2720.923**0.2570.2510.098-0.2680.4640.5070.872**0.1901.000As0.683*0.864**0.0290.5890.830**0.735*0.2070.3570.370-0.0610.718*-0.1930.450-0.0780.3470.1560.0430.622-0.2830.6101.000Hg0.2330.4610.3610.4980.820**0.3610.3830.756*0.612-0.0420.998**-0.0920.4520.0250.0450.1590.1900.904**-0.1590.934**0.703*1.000
注:“**”表示P<0.01,“*”表示P<0.05
2.4 地参样品中22种元素的主成分分析
2.4.1 主成分筛选及贡献率
由于地参中各元素含量在量纲上存在较大差异,为了保障分析结果的客观准确,利用SPSS 20对原始数据进行标准化处理后,再进行主成分分析,得到主成分特征值及贡献率。如表5所示,提取到4个主成分因子(特征值>1),前2个主成分累积贡献率达70.144%,主成分1主要反映了元素Mg、Pb、Cu的贡献,主成分2主要反映了Co、Cd、Ba的特征贡献,表明这2个因子在反映产地和地参中各元素的相互关系中起主导作用,能够客观反映两者间的内在联系。
表5 主成分的特征值及方差贡献率
Table 5 Eigenvalues and variance contribution of
principle components

主成分特征值方差贡献/%累积方差贡献率/%18.25637.52837.52827.17632.61670.14432.62011.90782.05141.7477.94289.993
2.4.2 主成分得分、综合评分及产地排序
利用每个主成分所对应的特征值占所提取主成分总特征值之和的比例作为权重得到综合主成分表达式为F综=0.417F1+0.362F2+0.132F3+0.088F4,并根据综合得分情况对不同产地进行排序,如表6所示,重庆万州(S1)、江苏徐州(S7)、广西玉林(S5)的样品综合得分排名前3,但由于S1和S7中Cu和重金属总量均超标,故从元素角度考虑,广西玉林(S5)地参品质较优。
表6 样品主成分得分、综合得分及其排序
Table 6 Principal component scores, comprehensive
scores and ranking
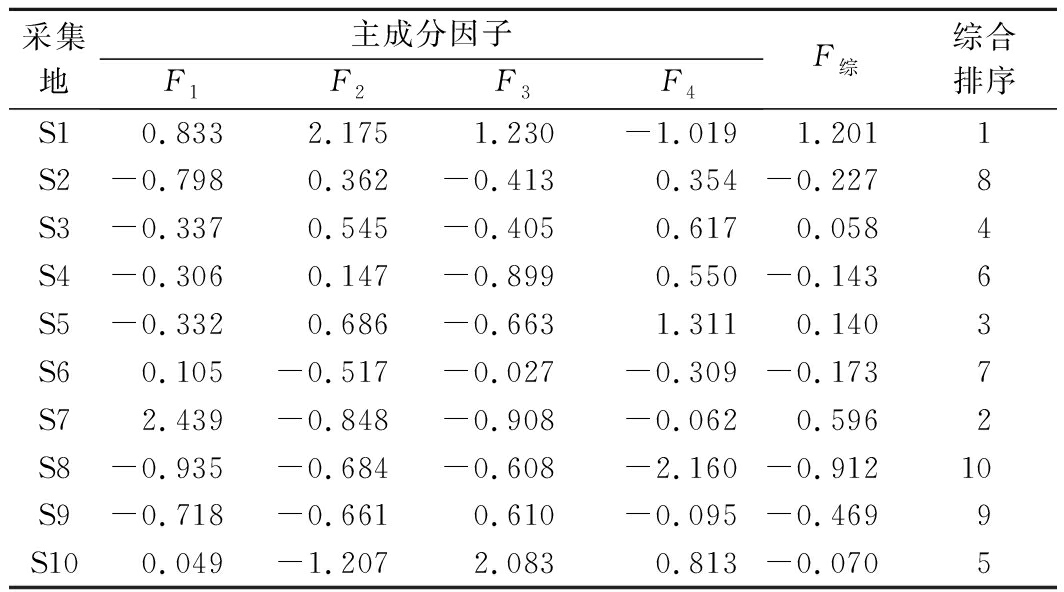
采集地主成分因子F1F2F3F4F综综合排序S10.8332.1751.230-1.0191.2011S2-0.7980.362-0.4130.354-0.2278S3-0.3370.545-0.4050.6170.0584S4-0.3060.147-0.8990.550-0.1436S5-0.3320.686-0.6631.3110.1403S60.105-0.517-0.027-0.309-0.1737S72.439-0.848-0.908-0.0620.5962S8-0.935-0.684-0.608-2.160-0.91210S9-0.718-0.6610.610-0.095-0.4699S100.049-1.2072.0830.813-0.0705
2.5 地参样品中22种元素聚类分析
采用SPSS 20对10批不同产地地参样品进行聚类分析,以22种元素作为变量可以分为三大类,样品S1为第Ⅰ类,S7为第Ⅱ类,这与主成分分析中综合排序结果一致;其余8组样品归为第Ⅲ类,其中在第Ⅲ类中,S2、S3、S4、S5(南方)和S6、S8、S9、S10(北方)又可独立成2个小类,该结果表明地域接近的产地能够很好的聚为一类,说明样品中元素的含量差异跟产地密切相关,存在地域性特征,可为地参的产地判别提供参考。
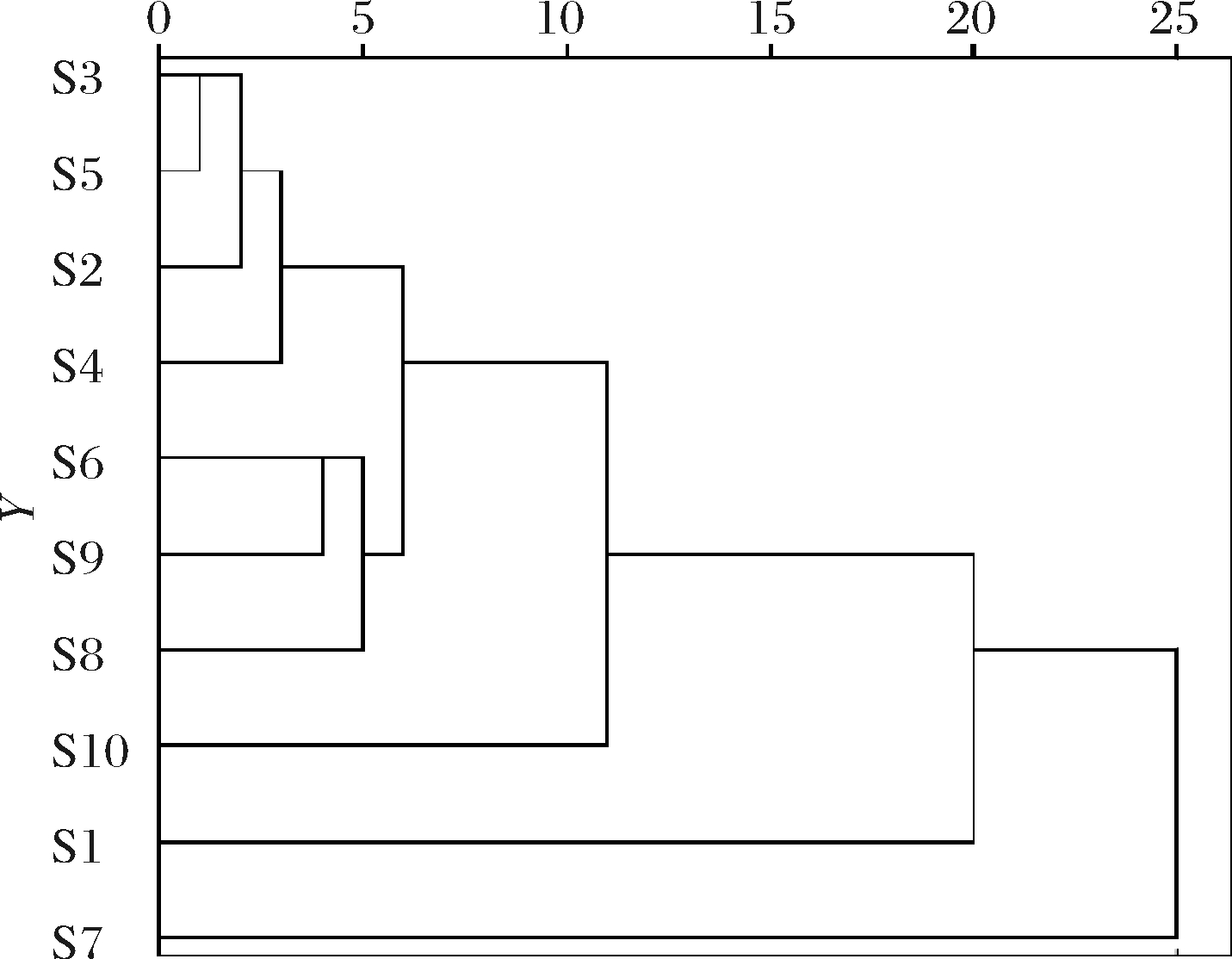
图1 样品的聚类分析
Fig.1 Cluster analysis of samples
3 结论与讨论
植物中元素含量多与生态因子土壤、气候以及施肥状况有关,且植物不同部位对元素的吸收富集存在差异[20]。植物在生长发育过程中,根茎作为营养成分等物质的直接吸收者,直接与土壤、肥料接触,其元素含量需监测评估。地参作为以根茎为药用和食用部位的植物,测定其营养元素、微量元素和重金属元素对其品质评价具有重要意义。
研究结果显示,10批不同产地地参中所含元素的种类基本一致,含量高低顺序为K>N>P>Ca>Mg>Na>Al>Fe>Zn>Mn>Cu>Ba>Ni>B>Cr>Mo>Pb>Co>As>Se>Cd>Hg。植物细胞中高浓度的K+可调节生长素和细胞分裂素的分泌从而影响其根茎的形成与生长,N、P元素作为构成蛋白质的必需元素,含量高低直接影响其新陈代谢速率与根茎的生长[32],所以在地参的生长过程中,应施予足够的钾肥和氮肥,以供正常生长所需,提高产量。Ca、Mg作为地参的无机特征元素,是地参生长发育、有效成分积累过程中的重要参与者。Ca是人体必需的矿物质元素,是生物体许多生理生化过程的触发器,是构成人体骨骼和牙齿的主要成分,地参中平均Ca含量高达1.81 mg/g,可用于开发为Ca补充剂。Mg参与人体中几乎所有的新陈代谢过程,特别是对心脏活动、心血管系统有很好的调节和保护作用。地参中还有其他有利的微量元素,如Fe是人体必需的微量元素,组成血红蛋白的重要成分,参与氧的运输和储存;Zn作为人体中多种酶的组成成分参与酶活动,能促进人体新陈代谢,提高免疫功能;Mn与人体中蛋白质、脂肪和碳水化合物的代谢密切相关,且是多种中药生物酶的活性中心。
Cu是人体的必需微量元素,但同时也是有害金属元素,人体中蓄积过多会引起中毒。本研究对不同产地地参中重金属进行分析发现,所有产地Cu含量普遍较高,来自山东菏泽、江苏一带的北方产地Cu含量均超标,特别是S7(江苏徐州)超过限量值近2倍,且其Pb和As含量在10个产地中含量同样最高。因此,在地参的规范化栽培过程中,应对其土壤和肥料的重金属进行监控,提高地参质量及安全性。
本研究采用凯氏定氮法、氢化物原子荧光光谱法及ICP-MS测定了不同产地地参中的营养元素、微量元素及重金属元素含量,基本涵盖了我国地参主产区,可大致反映地参中元素基本情况,并通过相关性分析、主成分分析和聚类分析进行综合评价,为地参的栽培引种、质量控制、安全性评价、产地判别和开发利用提供科学依据。
[1] 赵国平,戴慎. 中药大辞典[M]. 上海: 上海科学技术出版社, 2006.
[2] 湖南省食品药品监督管理局. 湖南省中药材标准(2009年版)[M]. 长沙:湖南科学技术出版社, 2010:57.
[3] 王文净, 高春燕. 地参的研究发展现状[J]. 农产品加工, 2017(7): 60-62.
[4] LU Y H, TIAN C R, GAO C Y, et al. Nutritional profiles, phenolics, and DNA damage protective effect of Lycopus lucidus Turcz. root at different harvest times[J]. International Journal of Food Properties, 2017, 20(S3): 3 062-3 077.
[5] YANG X B, LV Y, TIAN L M, et al. Composition and systemic immune activity of the polysaccharides from an herbal tea(Lycopus lucidus Turcz)[J]. Agriculture and Food Chemistry, 2010, 58(10): 6 075-6 080.
[6] 彭涛, 王金梅, 张前军, 等. 硬毛地笋挥发性成分研究[J]. 天然产物研究与开发, 2012, 24(3): 342-344.
[7] REN Q, DING L, SUN S S, et al. Chemical identification and quality evaluation of Lycopus lucidus Turcz by UHPLC-Q-TOF-MS and HPLC-MS/MS and hierarchical clustering analysis[J]. Biomedical Chromatography Bmc, 2017,31(5): 3 867-3 869.
[8] 彭涛, 王微, 张前军, 等. 硬毛地笋化学成分研究[J]. 天然产物研究与开发, 2013, 25(6): 782-784;806.
[9] YU J Q, LEI J C, ZHANG X Q, et al. Anticancer, antioxidant and antimicrobial activities of the essential oil of Lycopus lucidus Turcz. var. hirtus Regel[J]. Food Chemistry, 2011, 126(4): 1 593-1 598.
[10] 熊伟, 谭德勇, 陈贵元, 等. 地参多糖对小鼠免疫功能影响的实验研究[J]. 时珍国医国药, 2011, 22(1): 11-13.
[11] 朱苗, 李刚凤, 谢勇, 等. 地参研究进展[J]. 广州化工, 2016, 44(17): 20-21;46.
[12] 许泳吉, 钟惠民, 杨波, 等. 野生植物地参中营养成分的测定[J]. 光谱实验室, 2003, 20(4): 528-529.
[13] 张荣平, 周宁娜, 罗天诰. 地参中氨基酸、粗蛋白和元素分析[J]. 中医药研究, 1998, 14(5): 54-55.
[14] 刘红, 陈燕芹, 张宇, 等. 微波辅助消解ICP-AES法测定地笋中18种元素[J]. 食品科技, 2014, 39(2): 270-273.
[15] 毕坤. 论矿物元素在农作物中的综合平衡效应[J]. 贵州地质, 1998(1): 61-70.
[16] 魏永生, 侯雅慧, 郭妮, 等. 微波消解-ICP-OES法测定4种常见绿叶蔬菜中的22种矿物元素[J]. 化学工程师, 2018, 32(10): 21-24.
[17] 谢敏, 汪洁, 张启立, 等. 甘肃不同产地黄管秦艽中无机元素的相关性和主成分分析[J]. 天然产物研究与开发, 2016, 28(9): 1 402-1 408.
[18] 严宝飞, 富莹雪, 宿树兰, 等. 不同产地黄芩茎叶无机元素的ICP-MS分析与评价[J]. 中草药, 2018, 49(22): 5 418-5 425.
[19] 袁建民, 何璐, 杨晓琼, 等. 香叶天竺葵不同部位中19种无机元素分布规律研究[J]. 江西农业学报, 2019, 31(11): 98-104.
[20] 陈宏降, 罗益远, 刘佳楠, 等. ICP-MS分析鱼腥草不同部位中无机元素差异[J]. 中国新药杂志, 2019, 28(22): 2 769-2 775.
[21] 王迁. 原子吸收光谱法测定洛川苹果中的微量元素[J]. 食品工业, 2019, 40(12): 308-310.
[22] 林海兰, 朱日龙, 于磊, 等. 水浴消解-原子荧光光谱法测定土壤和沉积物中砷、汞、硒、锑和铋[J]. 光谱学与光谱分析, 2020, 40(5): 1 528-1 533.
[23] 杨春花, 毕健梁, 周美丽, 等. 快速石墨消解-电感耦合等离子体质谱法测定海菜中13种无机元素[J]. 食品与发酵工业, 2019, 45(16): 281-285.
[24] 胡曙光, 苏祖俭, 蔡文华, 等. 石墨炉原子吸收法测定高盐食品中的铅及其干扰消除的研究[J]. 中国食品卫生杂志,2015, 27(4): 394-398.
[25] 中华人民共和国国家卫生和计划生育委员会. GB 5009.11—2014 食品安全国家标准 食品中总砷和无机砷的测定[S]. 北京:中国标准出版社, 2014.
[26] 中华人民共和国国家卫生和计划生育委员会. GB 5009.17—2014 食品安全国家标准 食品中总汞和有机汞的测定[S]. 北京:中国标准出版社, 2014.
[27] 李冰, 周剑雄, 詹秀春. 无机多元素现代仪器分析技术[J]. 地质学报, 2011, 85(11): 1 878-1 916.
[28] 熊冬华, 李刚凤, 杨天友, 等. 梵净山茶中18种矿物质元素的主成分、相关性和聚类分析[J]. 天然产物研究与开发, 2017, 29(11): 1 888-1 894.
[29] 姜峰, 倪穗, 岑冲锋, 等. 不同种源地参在宁波地区的适应性及多糖含量比较研究[J]. 中国野生植物资源, 2019, 38(5): 20-24.
[30] 中华人民共和国国家卫生和计划生育委员会, 国家食品药品监督管理总局. GB 5009.5—2016 食品安全国家标准 食品中蛋白质的测定[S]. 北京:中国标准出版社, 2016.
[31] 中华人民共和国商务部. WM/T 2—2004药用植物及制剂外经贸绿色行业标准[S]. 北京: 中国标准出版社, 2004.
[32] 曾波, 何忠俊, 毛昆明, 等. 药用植物施肥研究进展[J]. 云南农业大学学报, 2007(4): 587-592.