桑叶是桑科(Moraceae)桑属(Moris)多年生木本植物桑树的主要产出物。早在1993年我国国家卫生部公布桑叶为药食两用植物,桑叶营养物质丰富且具有多重药理作用[1-3]。桑叶生长快,繁殖期短,年产量可达2 kg/m2,然而只有1%~3%的桑叶资源被利用。因此,开发利用桑叶资源具有重要意义[4]。
近十几年来,国内外许多学者在桑叶与健康、桑叶与食品开发等方面进行了大量的研究。已开发出桑叶茶、桑叶咀嚼片、桑叶干粉、桑叶营养素等食品和保健品[5]。但是在开发桑叶食品的过程中,发现一个普遍的问题,桑叶挥发性成分复杂, 存在较重的草腥味,导致部分人群对其难以接受,阻碍了其在食品领域的发展。
近年来,益生菌发酵技术得到了长足的发展。有研究表明,果蔬经过乳酸菌发酵之后,不仅能使果蔬功能性成分较好保留且能对果蔬挥发性风味物质的种类和含量造成较大改变[6]。徐慧钰[7]利用植物乳酸菌发酵将柚子汁中的苦味物质柚皮苷转化为没有苦味的柚皮素。从而达到对柚子汁的脱苦效果,使得柚子汁的风味得到改善;刘莹等[8]研究发现,通过乳酸菌发酵不仅能去除胡萝卜原浆中令人不愉快的药腥味且会产生许多芳香物质和营养物质。SHANG等[9]利用乳酸菌发酵去除木瓜涩味,为解决水果的涩味问题提供了一种自然的方法。李彤等[10]利用乳酸菌发酵复合豆乳发现,发酵后豆乳中醇、酸、酯类等香气成分显著增加,有利于降低豆乳豆腥味。
目前尚未有文章研究引起桑叶草腥味的具体物质,也未见利用乳酸菌发酵的方式去除桑叶草腥味的报道,因此,本研究利用气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS), 气相色谱嗅闻法(gas chromatography olfactometry,GC-O)等手段跟踪发酵过程中挥发性风味物质变化,分析乳酸菌发酵对桑叶草腥味的影响,并初步鉴定出新鲜桑叶中产生草腥味的物质。利用主成分分析法研究桑叶不同发酵阶段风味物质的差异性,找出对风味贡献最大的物质。
1 材料与方法
1.1 材料与试剂
桑叶,品种为金强,选取健康无虫蛀病变10月份的叶片;NaCl(分析纯),重庆川东化工集团有限公司;短乳杆菌(Lactobacillus brevis)、肠膜明串珠菌(Leuconostoc mesenteroides),中国微生物菌种保藏中心;2-辛醇(内标),德国Dr.Ehrenstorfer GmbH公司。
1.2 仪器与设备
VD-650超净工作台,苏州净化设备有限公司;HH.BLL.600-S电热恒温培养箱,上海跃进医疗器械厂;SYQ-DSX-280B高压灭菌锅,上海申安医疗器械厂;GC-MS2010气相质谱联用仪,日本岛津公司;固相微萃取,美国 Supelo 公司;Sniffer 9000 嗅味检测仪,瑞士 Brechbühler 公司;DK-8D 三孔电热恒温水槽,上海齐欣科学仪器有限公司。
1.3 试验方法
1.3.1 桑叶发酵
将新鲜桑叶[水分、蛋白质(以干物质计)、多糖、粗纤维质量分数分别为77.25%、18.29%、208.72 mg/g、13.25%]清洗干净,剪切成2 cm宽条状后放入100 mL锥形瓶中(投叶量为10 g),加入5%(湿基)葡萄糖和60 mL纯水,新鲜桑叶经灭菌处理(102 ℃ 20 min)后,得到未发酵桑叶样品,放至室温,接种5%(湿基)短乳杆菌∶肠膜明串珠菌=1∶1混合菌液,在30 ℃恒温培养箱中培养48 h[11]。
1.3.2 挥发性物质的提取
分别称取 5.0 g 发酵0、24、36、48 h桑叶样品置于20 mL螺口顶空样品瓶中,加入2 mL饱和NaCl溶液以加速挥发性成分的扩散。再向瓶内加入10 μL 2-辛醇(0.5 g/L)标准品作为内标物,用聚四氟乙烯隔垫密封,将100 μm PDMS萃取头插入萃取瓶中,于60 ℃水浴中平衡10 min后开始萃取,顶空吸附40 min。然后在GC-MS进样口250 ℃解吸5 min,同时启动仪器采集数据。
1.3.3 GC-MS分析条件
色谱条件:色谱柱为DB-5MS毛细管柱(30 m×0.25 mm×0.25 μm);升温程序为柱温箱起始温度为40 ℃,保持2 min,先以5 ℃/min升温到120 ℃,保持2 min,4 ℃/min升温到180 ℃,保持2 min,再以6 ℃/min升温到250 ℃,保持5 min;载气为高纯He,流速1 mL /min,压力49.5 kPa;进样口温度250 ℃; 柱流量1 mL/min;不分流进样。
质谱条件:电子轰击离子源;离子源温度230 ℃;接口温度250 ℃;溶剂延迟时间3 min; ACQ方式为Scan;质量扫描范围m/z 40~400。
1.3.4 挥发性成分的定性与定量分析
标准谱库NIST08、NIST08s和NIST14、NIST14s对化合物进行检索匹配,选择匹配度>80的物质并参考相关文献定性,以内标法定量。
1.3.5 GC-O分析
本试验采用强度法[12]对新鲜桑叶挥发性风味物质进行GC-O分析。嗅辨仪器条件:嗅味检测仪的传输线温度220 ℃,用 16 mL/min的湿润空气作为嗅闻载气。固定3名闻香员,平均每人嗅闻2次。每次运行分析程序时,闻香员需全程嗅闻,并记录气味成分的保留时间、气味特征与气味强度。根据 0 表示无气味、 1表示气味微弱、 2表示气味中等、 3表示气味较强、 4表示气味非常强来打分。将6次嗅闻中重复出现4次的嗅闻记录作为最终结果,气味活度值计算[13]如公式(1)所示:
气味活度值![]()
(1)
1.3.6 风味感官评价
确定7个主要风味指标,分别是腐臭味、酸味、青草味、蘑菇味、花香、果香、豆腥味,进行了风味剖面分析[14]。感官鉴评人员由10位食品专业学生组成,他们都熟悉桑叶的风味。感官评价员严格按照表1感官评价标准依次对各气味特征进行打分[15];将待测样品放置于小样品杯中,样品温度保持在30 ℃左右。总分采用5分制原则,0分代表没有该气味;3分代表该气味强度中等;5分代表该气味极强,综合取平均值,将其结果绘制成雷达图。
表1 感官评价参照标准
Table 1 Reference standard of sensory evaluation

气味特征气味定义参照物质参考值/分腐臭味腐烂叶菜气味常温放置1周后腐烂的青菜5酸味泡菜酸味新鲜切碎的泡菜5青草味新鲜割碎的青草香气新鲜割碎的青草5蘑菇味新鲜蘑菇香气新鲜切碎的蘑菇5花香切碎的混合花瓣的淡淡香气切碎的玫瑰、月季混合花瓣5果香新鲜成熟水果相关联的混合香气混合水果黄桃、菠萝等5豆腥味大豆豆腥味未煮沸的鲜榨豆浆5
1.4 数据处理
利用Excel 2013进行数据整理及计算,SPSS 19.0进行数据统计分析,Origin 8.1进行作图。
2 结果与分析
2.1 桑叶发酵时间的确定
OD600 是追踪液体培养物中微生物生长的标准方法,其可以评价乳酸菌在该条件下的成长情况[16]。由图1可知,发酵液中OD600值在48 h达到峰值,随发酵的不断进行,总酸不断积累,pH值也会随之降低,高浓度总酸具有反馈抑制作用,抑制了乳酸菌的生长繁殖。发酵液中总酸含量在36 h后趋于平缓,可能是由于发酵36 h后高浓度总酸抑制了乳酸菌的生长,导致其产酸量下降。综合考虑,本实验将分析桑叶0~48 h桑叶发酵样品中的挥发性风味成分。

图1 发酵时间对OD600值与总酸含量的影响
Fig.1 Effect of fermentation time on OD600
value and total acid content
2.2 发酵过程中桑叶的感官评价分析
如图2所示,桑叶乳酸菌发酵的各个阶段感官品质存在较大差异。发酵0 h桑叶的青草味、蘑菇味占主导地位,并伴有豆腥味。发酵24 h青草味、蘑菇味、豆腥味有所减弱,并增加了轻微花香和果香。发酵36 h花香和果香味占主导地位并伴随轻微的酸味,而青草味、豆腥味消失,蘑菇味大幅度下降。发酵48 h花香和果香占主导地位,并产生微弱的腐臭味和酸味,青草味、豆腥味和蘑菇味消失。这表明,乳酸菌发酵使得桑叶中青草味、腥味物质向花果香、甜香等物质转化。但发酵时间不应过长,否则会产生大量的带有汗臭味和腐臭味的物质。有研究表明不同发酵时间段的不同香型强度变化与挥发性化合物的组成和含量存在一定相关性[17]。

图2 不同发酵阶段桑叶感官评价雷达图
Fig.2 Radar charts for sensory evaluation of mulberry
leaves at different fermentation stages
2.3 发酵过程中桑叶挥发性风味物质的比较分析
由不同发酵阶段桑叶的总离子流程图(图3)可知,不同发酵阶段桑叶中挥发性物质存在明显差异,表明桑叶在发酵过程中其挥发性成分发生了动态变化。由挥发性组分的鉴定结果(表2)可知,从发酵0、24、36、48 h桑叶中共鉴定出116种挥发性物质,主要包括烃类26种,醇类23种,醛类17种,酮类10种,酯类26种,酚类4种,酸类6种和其他类化合物4种。0、24、36、48 h分别检测出49、42、53、61种挥发性物质。
发酵前桑叶中的酯类化合物总量为5.29%,共6种。发酵过程中酯类化合物含量和种类随着发酵时间的延长逐渐增加,在36 h达到峰值,分别为28.93%和17种。这表明乳酸菌发酵过程中产生酸类化合物与醇类化合物发生某种酯化反应生成大量酯类化合物[18]。酯类物质一般呈果香味[19]。发酵桑叶中新增含量最多的酯类为水杨酸甲酯,其天然存在于冬青油、樱桃、苹果等水果的果汁中,具有冬青叶香味与果香味。其次是具有白兰地酒香气的辛酸乙酯,以及己酸乙酯、癸酸乙酯、乙酸苄酯等具有花香和果香的酯类,其中短碳链的脂肪酸酯类在常温中易挥发,因而具有较大的风味贡献潜力。
醇类物质含量在发酵过程中呈现先上升后下降的趋势,并在36 h达到峰值,为20.2%,与0 h相比增加了32.43%,且种类差异较大。通过微生物发酵可以利用氨基酸代谢产生醇类物质[18]。不饱和醇阈值较低,气味明显[20]。C6醇是果蔬中青味主要来源[21]。其中顺式-3-己烯醇、3-辛醇在0 h含量较高,但在之后的发酵过程中未检测到,顺式-3-己烯醇具有强烈的青草味、3-辛醇具有油脂味和草药味。1-辛烯-3-醇、2-乙基己醇在整个阶段均有检出且随着发酵时间的延长逐渐降低。1-辛烯-3-醇具有土腥味和蘑菇味。与0 h相比,发酵36 h时,新增加且含量较高的挥发性物质为具有苹果白兰地香气的异戊醇、芳香气味的苯甲醇、玫瑰样花香的苯乙醇以及铃兰香气的芳樟醇。说明通过乳酸菌发酵可降低桑叶中的青草味和腥味,并产生花香果香等令人愉悦的香气成分,与感官评定结果一致。
与0 h相比,发酵过程中醛类、烷烃类化合物整体呈现下降趋势,且种类差异较大。整个发酵过程均有检出的化合物为壬醛和癸醛。醛类化合物呈现的气味特征与浓度有关,具有很强的气味叠加效应[22],高浓度的醛类物质会带来异味[23],而且醛类物质是不稳定的化合物,特别是在微生物作用下,在食品基质中会被还原为醇或被氧化为酸[24]。这可以解释发酵后的桑叶中醛类物质相对含量低而醇类和酸类物质相对含量高。烷烃类化合物的阈值一般较高,所以对风味的贡献较小。
酚类、酸类及酮类化合物含量在发酵过程中持续增加,其中丁香酚是主要的酚类物质,在整个发酵过程均有检出且随着发酵的进行含量持续增加,其具有浓郁的丁香花香,是发酵桑叶主要的呈味物质。少量的酸类物质对桑叶青草味具有掩盖作用[25],但发酵时间过长会产生大量的辛酸、己酸等具有汗臭味和辣味的酸类化合物。所以适度发酵会改善桑叶的感官品质而过度发酵反而会使桑叶的感官品质降低,这与感官评价结果一致。酮类来源于醛类物质的进一步氧化、氨基酸分解或微生物氧化[26],这也是发酵过后酮类化合物显著性增加的原因(P<0.05)。发酵36 h时,甲基庚烯酮是主要的酮类化合物,其含量占同时期酮类化合物的58.96%,具有浓郁的水果香味,这也是桑叶发酵后重要的呈味物质,对发酵后桑叶风味的形成具有重要作用。
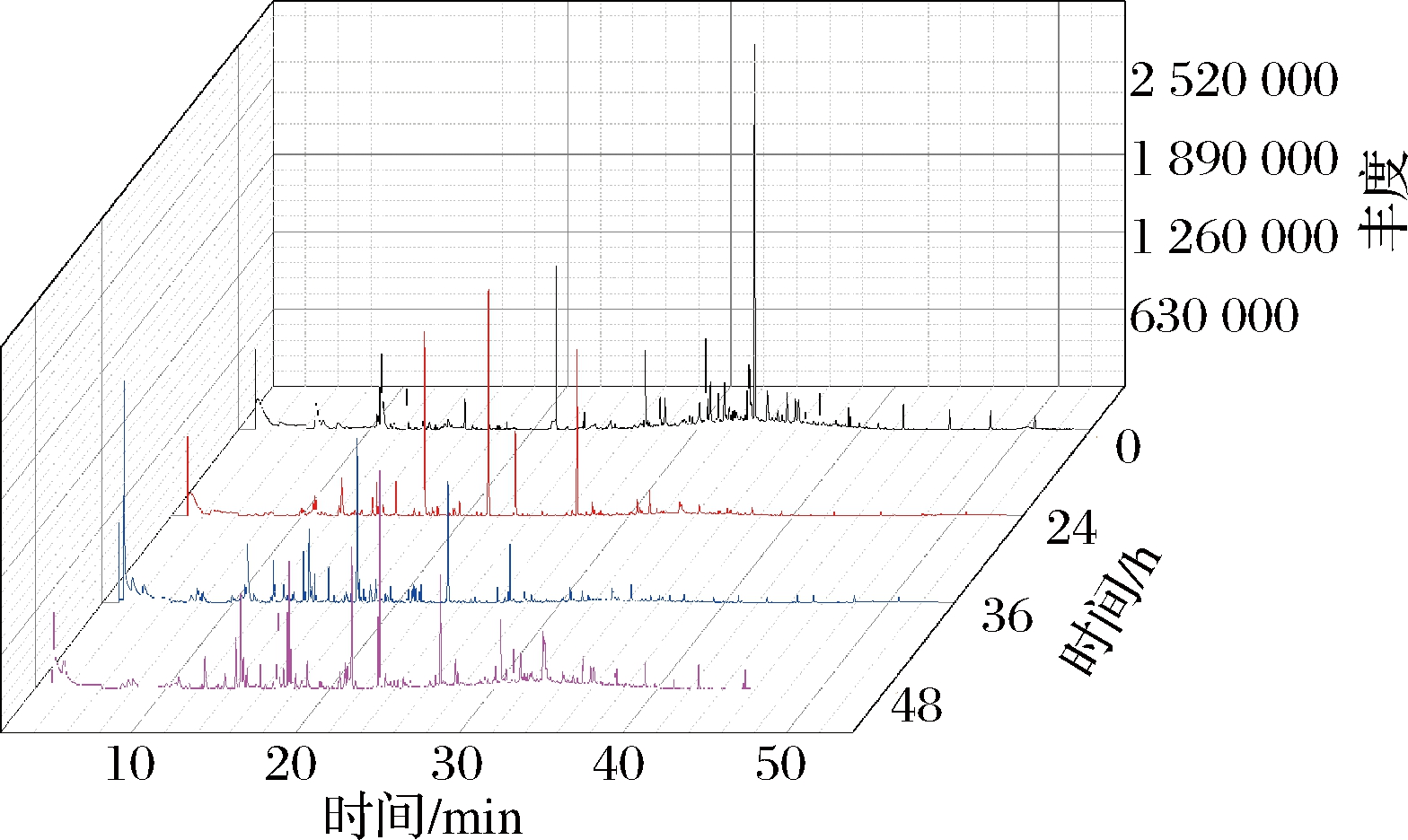
图3 桑叶不同发酵阶段的总离子流图
Fig.3 Total ion chromatograms of mulberry leaves during
different fermentation periods
2.4 桑叶中特征性风味物质分析
食物会产生许多挥发性化合物,但并不是所有成分都对香味有贡献。大多数情况下,色谱图中最强的峰对食品香味贡献反而不大,而小峰物质对香味影响大,因此色谱峰的强度并不能反映各组分对香味贡献的实际情况。所以需要引入香气活度值(odor activity value,OAV)的概念,将物质浓度和感觉阈值结合起来,对物质气味作出评价。当物质的OAV>1时,该物质可能对食品总体气味有直接影响,且在一定范围内,OAV越大说明该组分对总体气味贡献越大[30]。由表3可知,未发酵桑叶中OAV>1的风味化合物按OAV值从大到小依次为1-辛烯-3-醇>肉豆蔻醛>丁香酚>辛醇>壬醛>反-2-辛烯醛>癸醛>β-环柠檬醛>顺式-3-己烯醇。这些物质多呈青草味和腥味,所以未发酵桑叶具有强烈令人不愉快的草腥味。通过乳酸菌发酵之后,呈现青草味和腥味的物质含量显著性降低(P<0.05),转而增加了呈现浓郁花香、果香的芳樟醇、壬醇等醇类和己酸乙酯、癸酸乙酯等酯类化合物,且具有强烈丁香花气味的丁香酚含量显著性增加(P<0.05),成为发酵桑叶中OAV最高的化合物,直接影响了发酵桑叶的挥发性风味。
表2 桑叶挥发性风味物质在发酵中的变化 单位/%
Table 2 Changes of volatile flavor substances in mulberry leaves during fermentation
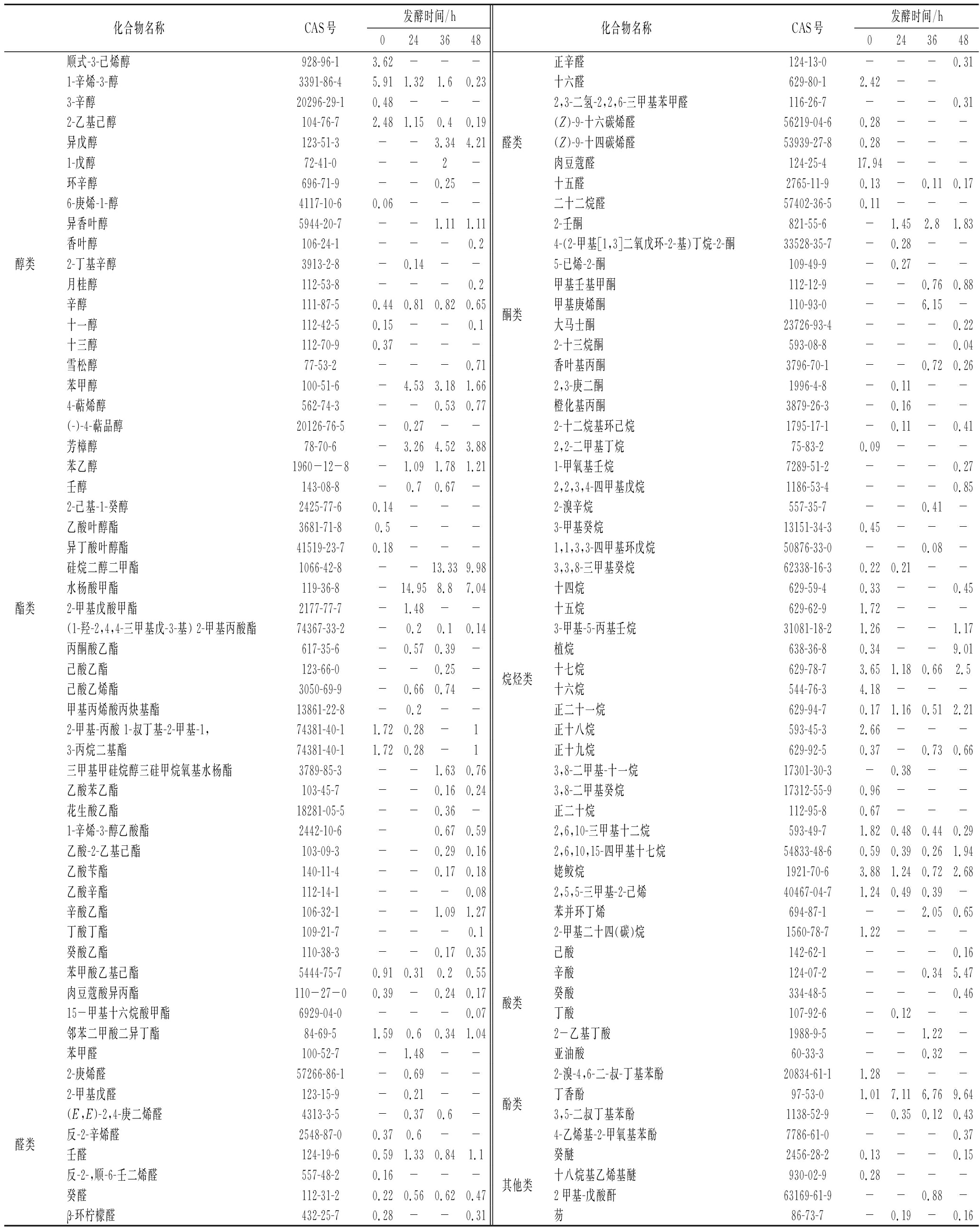
化合物名称CAS号发酵时间/h化合物名称CAS号发酵时间/h02436480243648顺式-3-己烯醇928-96-13.62---正辛醛124-13-0---0.311-辛烯-3-醇3391-86-45.911.321.60.23十六醛629-80-12.42--3-辛醇20296-29-10.48---2,3-二氢-2,2,6-三甲基苯甲醛116-26-7---0.312-乙基己醇104-76-72.481.150.40.19(Z)-9-十六碳烯醛56219-04-60.28---异戊醇123-51-3--3.344.21醛类(Z)-9-十四碳烯醛53939-27-80.28---1-戊醇72-41-0--2-肉豆蔻醛124-25-417.94---环辛醇696-71-9--0.25-十五醛2765-11-90.13-0.110.176-庚烯-1-醇4117-10-60.06---二十二烷醛57402-36-50.11---异香叶醇5944-20-7--1.111.112-壬酮821-55-6-1.452.81.83香叶醇106-24-1---0.24-(2-甲基[1,3]二氧戊环-2-基)丁烷-2-酮33528-35-7-0.28--醇类2-丁基辛醇3913-2-8-0.14--5-已烯-2-酮109-49-9-0.27--月桂醇112-53-8---0.2甲基壬基甲酮112-12-9--0.760.88辛醇111-87-50.440.810.820.65酮类甲基庚烯酮110-93-0--6.15-十一醇112-42-50.15--0.1大马士酮23726-93-4---0.22十三醇112-70-90.37---2-十三烷酮593-08-8---0.04雪松醇77-53-2---0.71香叶基丙酮3796-70-1--0.720.26苯甲醇100-51-6-4.533.181.662,3-庚二酮1996-4-8-0.11--4-萜烯醇562-74-3--0.530.77橙化基丙酮3879-26-3-0.16--(-)-4-萜品醇20126-76-5-0.27--2-十二烷基环己烷1795-17-1-0.11-0.41芳樟醇78-70-6-3.264.523.882,2-二甲基丁烷75-83-20.09---苯乙醇1960-12-8-1.091.781.211-甲氧基壬烷7289-51-2---0.27壬醇143-08-8-0.70.67-2,2,3,4-四甲基戊烷1186-53-4---0.852-己基-1-癸醇2425-77-60.14---2-溴辛烷557-35-7--0.41-乙酸叶醇酯3681-71-80.5---3-甲基癸烷13151-34-30.45---异丁酸叶醇酯41519-23-70.18---1,1,3,3-四甲基环戊烷50876-33-0--0.08-硅烷二醇二甲酯1066-42-8--13.339.983,3,8-三甲基癸烷62338-16-30.220.21--水杨酸甲酯119-36-8-14.958.87.04十四烷629-59-40.33--0.45酯类2-甲基戊酸甲酯2177-77-7-1.48--十五烷629-62-91.72---(1-羟-2,4,4-三甲基戊-3-基) 2-甲基丙酸酯74367-33-2-0.20.10.143-甲基-5-丙基壬烷31081-18-21.26--1.17丙酮酸乙酯617-35-6-0.570.39-植烷638-36-80.34--9.01己酸乙酯123-66-0--0.25-烷烃类十七烷629-78-73.651.180.662.5己酸乙烯酯3050-69-9-0.660.74-十六烷544-76-34.18---甲基丙烯酸丙炔基酯13861-22-8-0.2--正二十一烷629-94-70.171.160.512.212-甲基-丙酸 1-叔丁基-2-甲基-1,74381-40-11.720.28-1正十八烷593-45-32.66---3-丙烷二基酯74381-40-11.720.28-1正十九烷629-92-50.37-0.730.66三甲基甲硅烷醇三硅甲烷氧基水杨酯3789-85-3--1.630.763,8-二甲基-十一烷17301-30-3-0.38--乙酸苯乙酯103-45-7--0.160.243,8-二甲基癸烷 17312-55-90.96---花生酸乙酯18281-05-5--0.36-正二十烷112-95-80.67---1-辛烯-3-醇乙酸酯2442-10-6-0.670.592,6,10-三甲基十二烷593-49-71.820.480.440.29乙酸-2-乙基己酯103-09-3--0.290.162,6,10,15-四甲基十七烷54833-48-60.590.390.261.94乙酸苄酯140-11-4--0.170.18姥鲛烷1921-70-63.881.240.722.68乙酸辛酯112-14-1---0.082,5,5-三甲基-2-己烯40467-04-71.240.490.39-辛酸乙酯106-32-1--1.091.27苯并环丁烯694-87-1--2.050.65丁酸丁酯109-21-7---0.12-甲基二十四(碳)烷1560-78-71.22---癸酸乙酯110-38-3--0.170.35己酸142-62-1---0.16苯甲酸乙基己酯5444-75-70.910.310.20.55辛酸124-07-2--0.345.47肉豆蔻酸异丙酯110-27-00.39-0.240.17酸类癸酸334-48-5---0.4615-甲基十六烷酸甲酯6929-04-0---0.07丁酸107-92-6-0.12--邻苯二甲酸二异丁酯84-69-51.590.60.341.042-乙基丁酸1988-9-5--1.22-苯甲醛100-52-7-1.48--亚油酸60-33-3- -0.32-2-庚烯醛57266-86-1-0.69--2-溴-4,6-二-叔-丁基苯酚20834-61-11.28---2-甲基戊醛123-15-9-0.21--酚类丁香酚97-53-01.017.116.769.64(E,E)-2,4-庚二烯醛4313-3-5-0.370.6-3,5-二叔丁基苯酚1138-52-9-0.350.120.43醛类反-2-辛烯醛2548-87-00.370.6--4-乙烯基-2-甲氧基苯酚7786-61-0---0.37壬醛124-19-60.591.330.841.1癸醚2456-28-20.13--0.15反-2-,顺-6-壬二烯醛557-48-20.16---其他类十八烷基乙烯基醚930-02-90.28---癸醛112-31-20.220.560.620.472甲基-戊酸酐63169-61-9--0.88-β-环柠檬醛432-25-70.28--0.31芴86-73-7-0.19-0.16
注:-表示未检出(下同)
表3 主体风味物质的OAV 单位:μg/kg
Table 3 OAV of main flavor substance
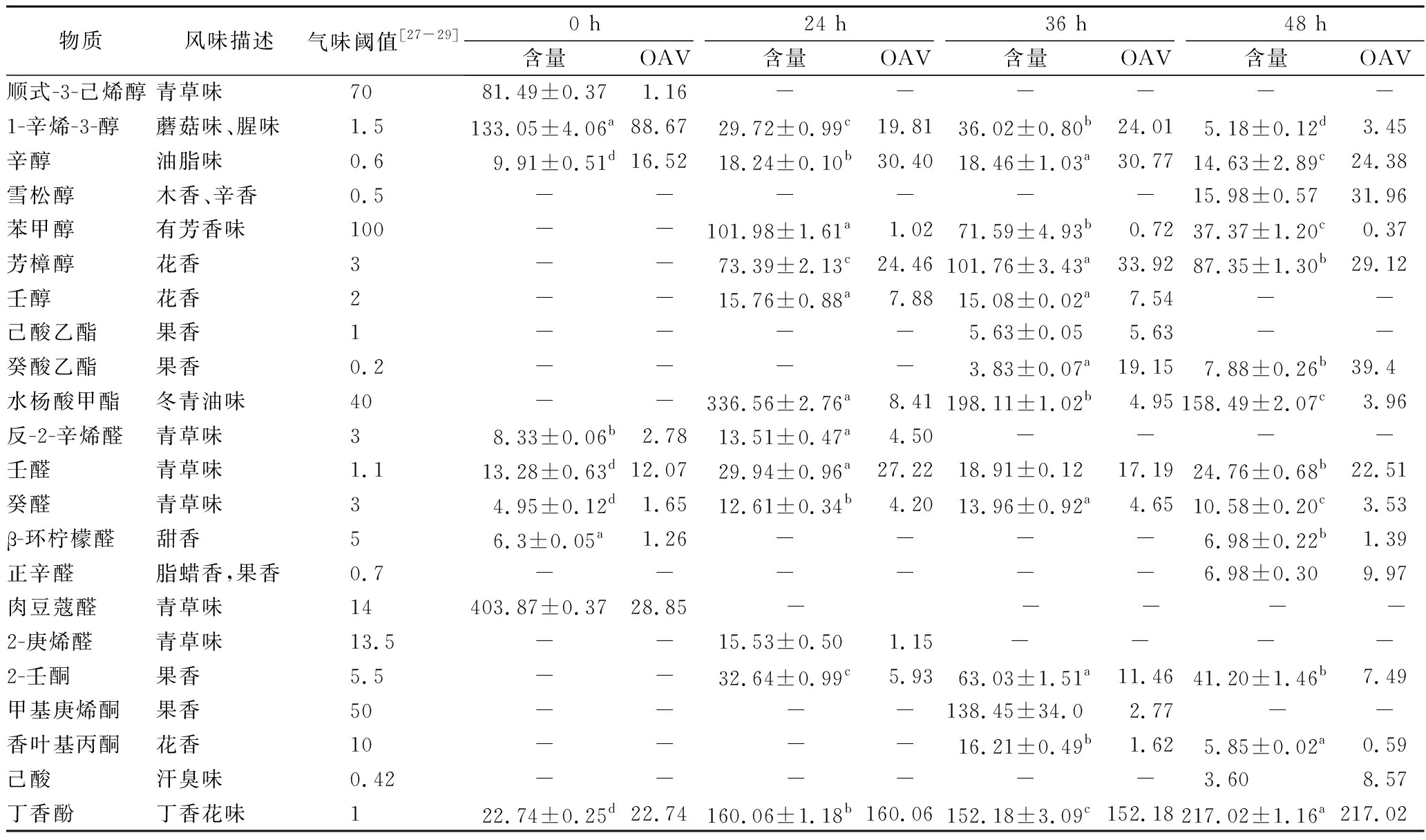
物质风味描述气味阈值[27-29]0 h24 h36 h48 h含量OAV含量OAV含量OAV含量OAV顺式-3-己烯醇青草味7081.49±0.371.16------1-辛烯-3-醇蘑菇味、腥味1.5133.05±4.06a88.6729.72±0.99c19.8136.02±0.80b24.015.18±0.12d3.45辛醇油脂味0.69.91±0.51d16.5218.24±0.10b30.4018.46±1.03a30.7714.63±2.89c24.38雪松醇木香、辛香0.5------15.98±0.5731.96苯甲醇有芳香味100--101.98±1.61a1.0271.59±4.93b0.7237.37±1.20c0.37芳樟醇花香3--73.39±2.13c24.46101.76±3.43a33.9287.35±1.30b29.12壬醇花香2--15.76±0.88a7.8815.08±0.02a7.54--己酸乙酯果香1----5.63±0.055.63--癸酸乙酯果香0.2----3.83±0.07a19.157.88±0.26b39.4水杨酸甲酯冬青油味40--336.56±2.76a8.41198.11±1.02b4.95158.49±2.07c3.96反-2-辛烯醛青草味38.33±0.06b2.7813.51±0.47a4.50----壬醛青草味1.113.28±0.63d12.0729.94±0.96a27.2218.91±0.1217.1924.76±0.68b22.51癸醛青草味34.95±0.12d1.6512.61±0.34b4.2013.96±0.92a4.6510.58±0.20c3.53β-环柠檬醛甜香56.3±0.05a1.26----6.98±0.22b1.39正辛醛脂蜡香,果香0.7------6.98±0.309.97肉豆蔻醛青草味14403.87±0.3728.85 - - - - -2-庚烯醛青草味13.5--15.53±0.501.15- - --2-壬酮果香5.5--32.64±0.99c5.9363.03±1.51a11.4641.20±1.46b7.49甲基庚烯酮果香50-- --138.45±34.02.77 --香叶基丙酮花香10-- --16.21±0.49b1.625.85±0.02a0.59己酸汗臭味0.42-- ----3.608.57丁香酚丁香花味122.74±0.25d22.74160.06±1.18b160.06152.18±3.09c152.18217.02±1.16a217.02
注:不同小写字母表示在P<0.05水平上存在显著性差异
2.5 未发酵桑叶的GC-O结果分析
通过 GC-O 嗅辨实验,在未发酵桑叶中共鉴定出11种带有明显气味且能与GC-MS结果匹配的物质和1种未知、被感官评定员嗅闻到但却无法与仪器检测结果相对应的物质。可能因为这种物质含量极低,但它的阈值也很低,所以仪器无法对其进行检测,但能被感官鉴评员所感受到[31],其中包含醇类物质4种、醛类物质5种、酚类物质1种和酯类物质1种,醇类和醛类化合物相对含量占所有气味活性成分的91.12%,其对未发酵桑叶风味起主导作用。如表4所示,通过GC-O嗅辨出的带有青草味和腥味的物质有顺式-3-己烯醇、1-辛烯-3-醇、反-2-辛烯醛、壬醛、癸醛、肉豆蔻醛。其中具有青草味的顺式-3-己烯醇、肉豆蔻醛在发酵后消失,而壬醛、癸醛含量呈先上升后下降的趋势。1-辛烯-3-醇在整个发酵过程中均有检出并且随着发酵的进行含量逐渐降低,与未发酵桑叶相比,发酵48 h桑叶中1-辛烯-3-醇含量减少96.11%。反-2-辛烯醛在发酵24 h略有增加,之后未检测到。因此可以认为桑叶中的青草味和腥味是顺式-3-己烯醇、1-辛烯-3-醇、反-2-辛烯醛、壬醛、癸醛、肉豆蔻醛共同作用的结果。结合OAV可知,这几种物质对风味的影响程度从大到小依次是1-辛烯-3-醇>肉豆蔻醛>壬醛>反-2-辛烯醛>癸醛>顺式-3-己烯醇。
表4 未发酵桑叶挥发性成分GC-O嗅辨结果
Table 4 GC-O smelling results of volatile components in
unfermented mulberry leaves
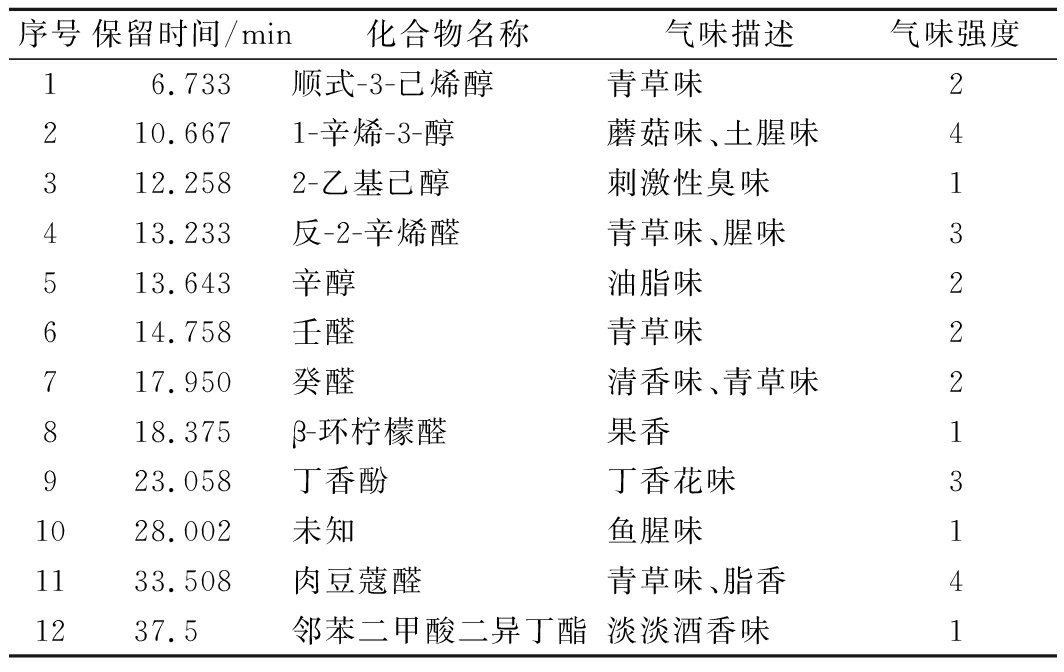
序号保留时间/min化合物名称气味描述气味强度16.733顺式-3-己烯醇青草味2210.6671-辛烯-3-醇蘑菇味、土腥味4312.2582-乙基己醇刺激性臭味1413.233反-2-辛烯醛青草味、腥味3513.643辛醇油脂味2614.758壬醛青草味2717.950癸醛清香味、青草味2818.375β-环柠檬醛果香1923.058丁香酚丁香花味31028.002未知鱼腥味11133.508肉豆蔻醛青草味、脂香41237.5邻苯二甲酸二异丁酯淡淡酒香味1
2.6 桑叶发酵过程中挥发性物质主成分分析
以桑叶不同发酵阶段7 类挥发性物质的相对含量为指标,用SPSS 进行主成分分析(principal component analysis,PCA),得到各主成分的特征值、方差贡献率、累计方差贡献率。结果如表5 所示,提取到特征值>1的2个主成分,且这2个主成分的方差累计贡献率达到87.285%,表示能够解释桑叶不同发酵阶段香气大部分的成分信息,因此,选择这2个主成分进行风味品质分析。
桑叶不同发酵阶段样品中7类挥发性物质的载荷分析如图4所示,酯类和醛酮类作为主要挥发性物质与PC1 高度正相关(载荷系数分别为0.995、0.814),酚类与PC1呈高度负相关(载荷系数为-0.982);PC2中载荷最高的正相关挥发性物质为醇类(载荷系数为0.982)。上述结果说明醛类、酯类、醇类以及酚类物质是不同发酵阶段样品中含量发生显著变化的挥发性物质。
不同发酵阶段样品的得分如图5所示,第一主成分得分较高的为36 h发酵样品和48 h发酵样品,影响它们的主要挥发性成分为醛类、酯类和酚类物质,它们可能决定了36 h发酵样品和48 h发酵样品的风味特征;0 h发酵样品在第一主成分上得分最低,其单独位于第二象限,PC1可以将它与其他3种样品完全区分开。根据距离的远近,发酵各个时间段挥发性物质存在较大差异。即PCA可以对桑叶不同发酵阶段样品进行有效区分。
表5 主成分的特征值及方差贡献率
Table 5 Eigenvalues of principal components and
variance contribution rate

成分合计方差/%累计/%13.96756.67156.67122.14330.61587.285
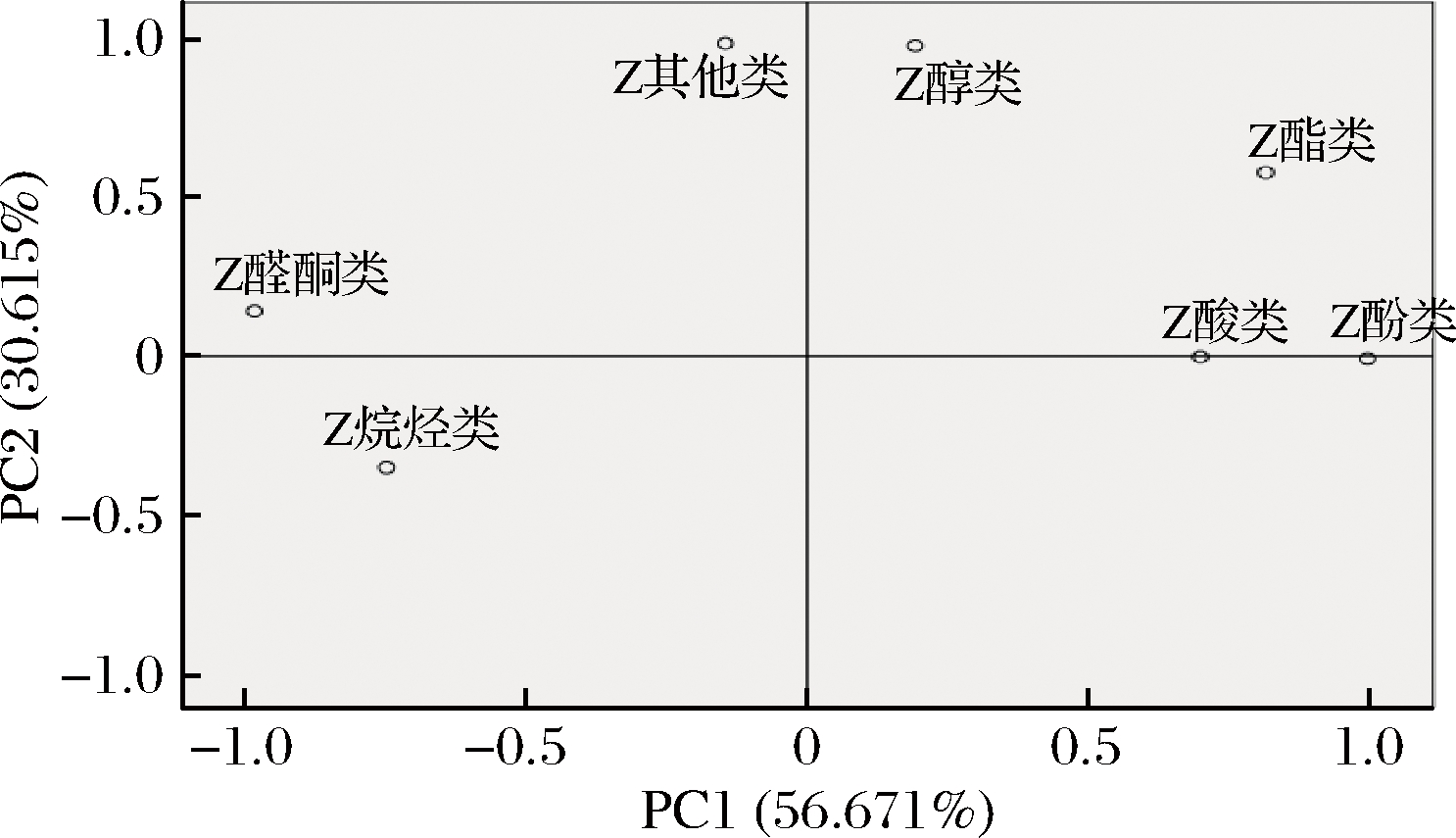
图4 不同发酵时间样品中7类挥发性物质的
载荷分布图
Fig.4 Load distribution of 7 types of volatile substances in
samples at different fermentation times
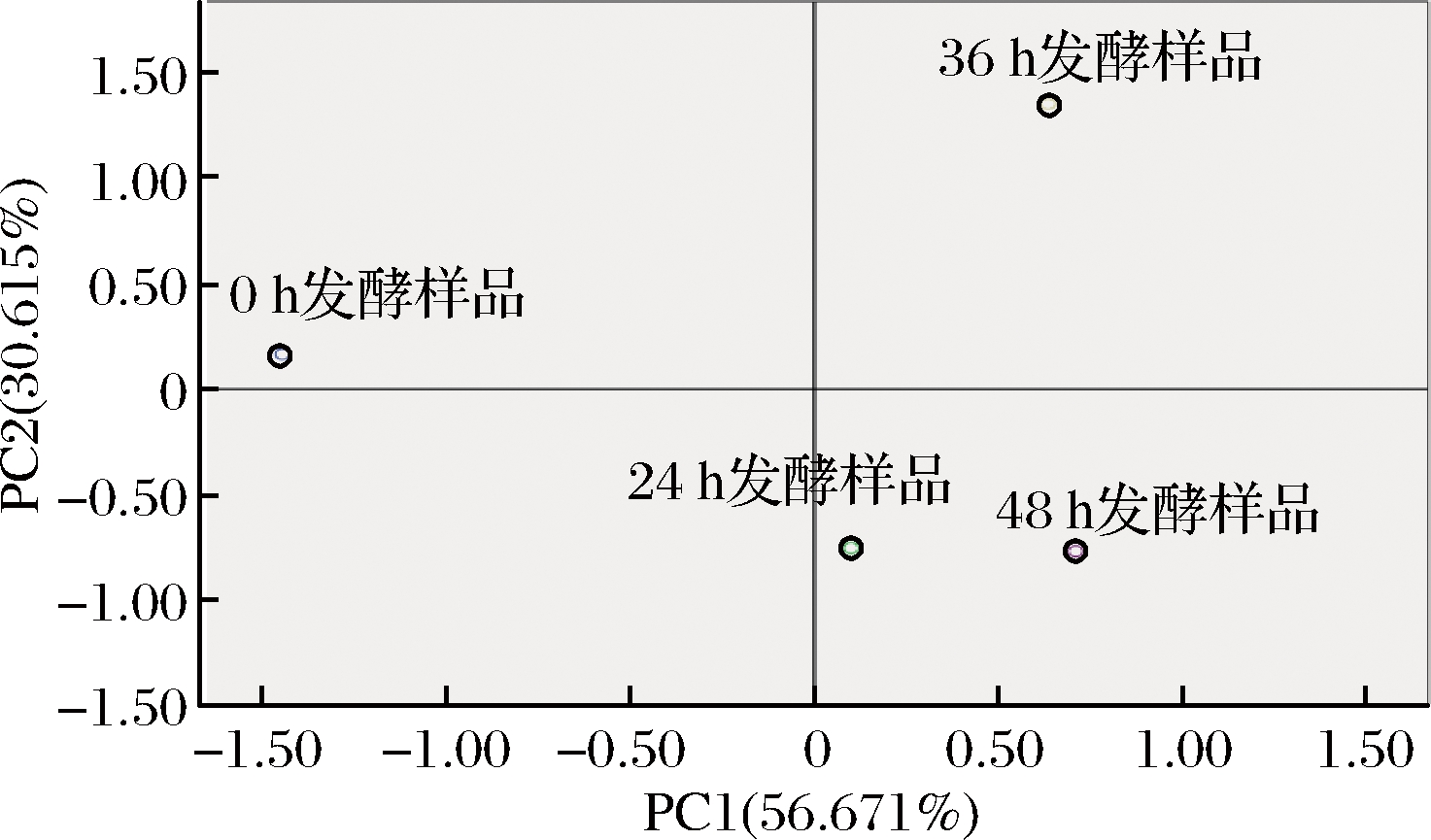
图5 不同发酵时间样品的得分图
Fig.5 Score graphs of samples with different
fermentation times
3 结论
通过GC-O实验结合香气活度值可以鉴定出桑叶中呈现草腥味的物质为顺式-3-己烯醇、1-辛烯-3-醇、反-2-辛烯醛、壬醛、癸醛、肉豆蔻醛。并且通过对不同发酵阶段桑叶的挥发性成分进行分析可知,桑叶在不同发酵时段的挥发性风味物质种类和含量均处于动态变化中,且整体风味是由青草味、蘑菇味、腥味向花香、果香等香味转化而来。通过主成分分析可知,桑叶不同发酵样品中含量发生显著变化的挥发性物质是醛类、酯类、醇类以及酚类物质。得分较高的是36 h发酵样品。说明通过主成分分析法研究桑叶不同阶段发酵风味物质的差异性,找出对风味贡献最大的物质是可行的。该研究结果可为提高桑叶的食用价值和定向加工技术等提供重要科学依据。
[1] BUTT M S, NAZIR A, SULTAN M T, et al. Morus alba L. nature′s functional tonic[J]. Trends in Food Science & Technology, 2008,19(10):505-512.
[2] GRYN-RYNKO A, BAZYLAK G, OLSZEWSKA-SLONINA D. New potential phytotherapeutics obtained from white mulberry (Morus alba L.) leaves[J]. Biomedicine & Pharmacotherapy, 2016,84:628-636.
[3] CHAN E W C, LYE P Y, WONG S K. Phytochemistry, pharmacology, and clinical trials of Morus alba[J]. Chin J Nat Med, 2016,14(1):17-30.
[4] GUO N, ZHU Y, JIANG Y, et al. Improvement of flavonoid aglycone and biological activity of mulberry leaves by solid-state fermentation[J]. Industrial Crops & Products, 2020,148:112 287.
[5] 刘青茹,王彬,周春江,等. 桑叶理化成分及其加工技术研究进展[J]. 农产品加工, 2017(12):48-51;53.
[6] YANG J, JI Y, PARK H, et al. Selection of functional lactic acid bacteria as starter cultures for the fermentation of Korean leek (Allium tuberosum Rottler ex Sprengel.)[J]. International Journal of Food Microbiology, 2014,191:164-171.
[7] 徐慧珏.两株乳酸菌对沙田柚汁的脱苦研究[D]. 广州:华南理工大学, 2014.
[8] 刘莹,焦梦悦,王丽霞,等. 响应面法优化乳酸菌发酵胡萝卜原浆工艺及香气成分变化分析[J]. 食品工业科技, 2017,38(15):85-92;116.
[9] SHANG Y H, CAO H, MA Y L, et al. Effect of lactic acid bacteria fermentation on tannins removal in Xuan Mugua fruits[J]. Food Chemistry, 2019,274:118-122.
[10] 李彤,彭珍,熊涛. 乳酸菌发酵对复合豆乳饮料营养成分、香气成分及抗氧化活性的影响[J]. 食品与发酵工业, 2018,44(4):111-118.
[11] 高鹤.植物乳杆菌发酵对苦瓜及其多糖组分的理化性质与降血糖功能的影响[D]. 南昌:南昌大学, 2019.
[12] GUEN S L, PROST C, DEMAIMAY M. Evaluation of the representativeness of the odor of cooked mussel extracts and the relationship between sensory descriptors and potent odorants[J]. Journal of Agricultural and Food Chemistry, 2001,49(3):1 321-1 327.
[13] 田怀香,吴譞,秦蓝,等. 基于GC-MS和GC-O的调味品鸡精特征风味物质研究[J]. 现代食品科技,2016,32(9):287-294;185.
[14] 夏克胜.珍珠贝固体发酵—酶解制备呈味基料的研究[D]. 广州:华南理工大学, 2012.
[15] 杨潇,刘野,胡蝶,等. 热加工西瓜汁关键异味成分的初步鉴定[J]. 食品工业科技, 2019,40(5):219-224.
[16] 董自艳,戴翚,马仕洪,等. 紫外-可见分光光度法快速确定细菌菌液的浓度[J]. 中国药品标准, 2014,15(2):120-121.
[17] HEMPFLING K, FASTOWSKI O, KOPP M, et al. Analysis and sensory evaluation of gooseberry (Ribes uva crispa L.) volatiles[J]. Journal of Agricultural and Food Chemistry, 2013,61(26):6 240-6 249.
[18] 阮文权,陈坚,孙胜利,等.酯类风味物质微生物代谢机理研究[J].生物技术,1996,6(6):31-34.
[19] MART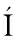 M P, MESTRES M, SALA C, et al. Solid-phase microextraction and gas chromatography olfactometry analysis of successively diluted samples:A new approach of the aroma extract dilution analysis applied to the characterization of wine aroma[J]. Journal of Agricultural and Food Chemistry, 2003,51(27):7 861-7 865.
M P, MESTRES M, SALA C, et al. Solid-phase microextraction and gas chromatography olfactometry analysis of successively diluted samples:A new approach of the aroma extract dilution analysis applied to the characterization of wine aroma[J]. Journal of Agricultural and Food Chemistry, 2003,51(27):7 861-7 865.
[20] 潘冰燕, 鲁晓翔, 张鹏, 等. GC-MS结合电子鼻分析1-MCP处理对线椒低温贮藏期挥发性物质的影响[J]. 食品科学, 2016,37(2):238-243.
[21] KOBAYASHI A,KUBOTA K,JOKI Y,et al.(Z)-3-hexenyl-β-d-glucopyranoside in fresh tea leaves as a precursor of green odor[J].Bioscience,Biotechnology and Biochemisty,1994,58(3):592-593.
[22] 王毅, 徐艳群, 徐坤, 等. HS-SPME-GC-MS技术分析不同加工阶段的甲鱼腥味成分变化[J]. 食品与发酵工业, 2016,42(12):189-193.
[23] CAGNO R D, FILANNINO P, GOBBETTI M. Lactic acid fermentation drives the optimal volatile flavor-aroma profile of pomegranate juice[J]. International Journal of Food Microbiology, 2017,248:56-62.
[24] CAGNO R D, SURICO R F, PARADISO A, et al. Effect of autochthonous lactic acid bacteria starters on health-promoting and sensory properties of tomato juices[J]. International Journal of Food Microbiology, 2009,128(3):473-483.
[25] 张菊华,单杨,李高阳. 乳酸菌发酵蔬菜汁的研究进展[J]. 饮料工业, 2003(6):27-31.
[26] 张娜.中华绒螯蟹风味物质的研究[D].无锡:江苏大学,2008.
[27] 吴静, 黄卉, 李来好, 等. HS-SPME-GC-MS分析大蒜水提取物对罗非鱼肉腥味的影响[J]. 食品与发酵工业, 2019,45(14):133-142.
[28] 邓娜娜,马永昆,张龙, 等. 不同杀菌处理桑椹果醋香气质量的主成分分析[J]. 食品与发酵工业, 2014,40(4):172-177.
[29] 吴林, 张强, 臧慧明,等.气味活度值法评价蓝莓果皮、果肉、果汁挥发性香气成分[J].食品工业科技,2020,41(1):195-200.
[30] 刘登勇, 周光宏, 徐幸莲. 确定食品关键风味化合物的一种新方法:“ROAV”法[J]. 食品科学, 2008(7):370-374.
[31] 陈光静,郑炯,丁涌波,等. 顶空-固相微萃取-气相色谱-质谱联用结合嗅闻法分析异味薏米的异味成分[J]. 食品与发酵工业, 2018,44(1):230-237.