拟穴青蟹(Scylla paramamosain)简称青蟹,属甲壳纲梭子蟹科,广泛分布于印度-西太平洋热带地区,我国主要分布在东南沿海区域[1],是我国重要的经济蟹类。青蟹体型较大,成长速度快,一年便可成熟食用,且肉质鲜美、营养丰富,具有良好的滋补作用,被视为珍贵的海洋产品,素有“海上人参”的美称[2]。青蟹繁殖期主要集中在6~10月份,雌性青蟹的性腺会产生红色或黄色样物质,通常与肝胰腺交融在一起,俗称“膏蟹”。其中,黄油蟹属非正常发育的雌性青蟹,是一种极其稀有和名贵的蟹类珍品,仅在雌性青蟹繁殖期间的特殊情况下才会产生,数百只野生青蟹才会产生一只黄油蟹,且产出时间和捕获后存活时间较短,被称为“蟹中贵族”,其每50 g的售价可达数十元甚至上百元不等。虽然一些沿海水产养殖企业通过改善雌性青蟹的生长条件,可在一定程度上提高黄油蟹产生的几率,但目前市场上养殖黄油蟹的供应量仍然较少,且其品质和价格均不如野生黄油蟹。
青蟹在生殖发育后期会进一步增肥和脱壳,但极少部分雌性青蟹会由于摄入过多的营养或者其他因素,在性腺周围积聚大量脂肪,导致其过肥而无法顺利脱壳,不能最终转变为正常发育成熟的青蟹。而这种无法顺利脱壳的雌性青蟹,在每年夏天的繁殖季节,会和正常发育成熟的雌性青蟹一起暂时生活在海边浅滩。当海潮退去时,剧烈的阳光会使浅滩水温升高,这种雌性青蟹受到环境等因素刺激,其体内积聚的脂肪分解成金黄色油状脂滴,并渗透到蟹体各个部位,在脂滴的浸润下,会使蟹体全身呈现出黄油色,故称之为“黄油蟹”。在积聚的脂肪分解过程中,性腺也会伴随着脂肪分解,待性腺完全消失后,黄油蟹便完全成熟。在黄油蟹完全成熟的前期,性腺会保留一段时间,该特殊生命形式下的雌性青蟹十分罕见,被称之为“黄油蟹前体”。
食物感官特性代表可被接受的程度,由嗅觉带来的气味感和味觉带来的味感是食物感官特性主要的2个方面[3]。气味感主要由体内脂肪酸、蛋白质和氨基酸等物质在分解过程中产生的挥发性物质构成,主要包括烃类、醛类、酮类、醇类和酯类等,构成了食物的主体气味[4-5]。构成味感的主要成分包括游离氨基酸、有机酸、可溶性糖和核酸等物质(主要是游离氨基酸和核酸)[6]。核酸主要呈现出鲜味口感,游离氨基酸味感层次较复杂,可呈现出苦味、鲜味和甘味等味感[7]。含量较高的K、Na等无机盐对食物的味感也有一定的影响[8]。
近些年来,青蟹的研究主要集中在正常青蟹的繁育、养殖及其对营养品质和风味物质等影响[9-11],黄油蟹作为一种极其稀有和名贵的水珍品,其相关研究亟需开展,尤其是对另一种非正常发育的生命形式—黄油蟹前体营养品质及风味方面的研究,在国内外均未见有报道。鉴于此,本研究以正常青蟹和黄油蟹前体的性腺为原料,对其相关营养成分和感官特性进行分析,旨在初步分析黄油蟹前体的营养品质和风味,并进一步了解正常青蟹性腺的营养品质和风味。通过比较黄油蟹前体和正常青蟹,为合理评价黄油蟹前体的营养品质和风味差异提供数据参考,同时也为后续进一步研发生产商品化的高品质黄油蟹提供理论依据。
正常雌性青蟹、黄油蟹前体样品,深圳市蟹之王水产有限公司提供。分别对2种青蟹进行前处理,刷去体表污垢并用毛巾擦拭干净,称取质量并记录;将头胸甲打开后,用经消毒处理的镊子(在火焰上灼烧10 s)分别将肌肉、性腺和肝胰腺剥离至干净的表面皿,充分混匀,分别称取质量并记录,并置于-18 ℃冰箱保存备用。
主要试剂:乙酸镁、NaOH、浓H2SO4、CuSO4、无水乙醚、盐酸、KOH、甲醇、磺基水杨酸、NaCl、无水Na2SO4等均为分析纯,正己烷为色谱纯,HNO3、HClO4均为优级纯,均购自安徽国药集团有限公司。
DHG-9123 J精密恒温鼓风干燥箱,上海三发科学仪器有限公司;DRZ-4马弗炉,上海试验电炉厂;FA104 N电子分析天平,上海民桥精密科学仪器有限公司;CT15RT 台式高速冷冻离心机,上海天美生化仪器设备工程有限公司;L-8900氨基酸全自动分析仪,日本HITACHI公司;5975C-7890A气相色谱-质谱联用仪、DB-5MS色谱柱(60 m×0.32 mm,0.25 μm),美国Agilent公司;HH-2数显水浴锅,江苏金坛市环宇科学仪器厂;IRIS IntrepidⅡ电感耦合等离子体发射光谱仪,美国Thermo Electron公司;AFS-3100原子荧光分光光度计,北京科创海光仪器有限公司。
1.3.1 营养品质的测定
1.3.1.1 性腺指数(gonadosomatic index,GSI)的测定
GSI按照公式(1)计算[12]:
(1)
1.3.1.2 基本营养成分的测定
水分测定参考GB 5009.3—2016《食品安全国家标准 食品中水分的测定》;灰分测定参考GB 5009.4—2016《食品安全国家标准 食品中灰分的测定》;粗蛋白测定参考GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》;粗脂肪测定参考 GB 5009.6—2016《食品安全国家标准 食品中脂肪的测定》。
1.3.1.3 氨基酸含量的测定与评价
精确称量样品0.10 g移至10 mL安瓿瓶中,加入5 mL 6 mol/L HCl溶液,将安瓿瓶用N2充满,在酒精喷灯下,快速将安瓿瓶密封,放到130 ℃的烘箱水解3~4 h,水解结束后将水解液进行冷却,并转移到100 mL容量瓶中定容。取1 mL定容后的水解液冷冻干燥,加1 mL 0.02 mol/L HCl溶液溶解,用孔径0.22 μm微孔滤膜对溶液进行过滤,滤液备用,采用氨基酸全自动分析仪对水解液进行测定[13]。
根据 FAO/WHO 1973年建议的每克氮中氨基酸评分标准模式和全鸡蛋蛋白质的氨基酸模式,对性腺的营养价值进行氨基酸评分(amino acid score,AAS)和化学评分(chemical score,CS),分别按公式(2)(3)(4)计算[14]:
标准模式氨基酸含量/(mg·g-1N)=
(2)
AAS/%=
(3)
(4)
1.3.1.4 矿物质含量的测定
称取0.50 g性腺样品,置于200 mL带有表面皿的烧杯中,加入12 mL浓HNO3和6 mL HClO4溶液,盖上表面皿,在可控温电热板上进行加热消解,至溶液大约剩2~3 mL,观察溶液,若为澄清则停止加热,反之取下烧杯待冷却后再加入3 mL HClO4溶液进行加热,直至完全澄清,冷却后转至25 mL容量瓶进行定容,摇匀后备用。最后采用电感耦合等离子体发射光谱仪测定各种矿物质含量[15]。
1.3.2 风味物质含量测定
1.3.2.1 游离氨基酸的测定
准确称取冷冻干燥后的性腺样品1.00 g,将其研磨后加入4%的磺基水杨酸10 mL,进行混匀振荡,静置1 h,使其进行酸解和萃取。以12 000 r/min离心30 min,离心结束后吸取1 mL上清液,用孔径为0.22 μm水相滤膜对上清液进行抽滤,滤液备用。采用氨基酸全自动分析仪对上清液进行测定[16]。味觉活度值(taste acti ity alue,TA )的计算参考CHEN等[17]的方法,TA >1认为对味觉贡献较大。
1.3.2.2 挥发性风味物质测定
采用顶空固相微萃取分离挥发性物质。准确称取(5.00±0.01) g性腺样品于20 mL顶空瓶中,将老化的萃取头通过隔膜插入,并暴露于顶空瓶的顶部空间,经60 ℃水浴加热萃取40 min,将吸附完成的萃取针由GC-MS注射口250 ℃解析5 min后进样,启动仪器进行数据收集[18]。
色谱条件:挥发性风味物质的分析通过 GC-MS 进行。以流速1.3 mL/min的He为载体,不分流进样,色谱柱为DB-5MS柱(60 m×0.32 mm,0.25 μm);进样口温度250 ℃。升温程序:初始温度40 ℃,无保留;以5 ℃/min的升温速度升至100 ℃,无保留;以5 ℃/min升温至180 ℃,无保留;再以5 ℃/min的升温速度升至240 ℃,保持5 min;汽化室温度240 ℃。
质谱条件:电子轰击(EI)离子源;电子能量70 e ,离子源温度230 ℃,接口温度250 ℃;电子倍增器电压1576 ;质量扫描范围40~450 amu/s。
本实验结果除挥发性风味物质测定的数据外,其余数据均表示为平均值±标准差,且通过软件SPSS 20.0进行显著性检验,同行(列)字母不同(P<0.05)表示差异显著。
2.1.1 GSI比较
正常雌性青蟹的GSI为(14.21±1.59),显著高于黄油蟹前体(5.89±0.63)(P<0.05)。其原因主要是在黄油蟹形成的过程中,其性腺组织会逐渐分解成油状物质,导致其性腺慢慢萎缩,直至消失。因此,黄油蟹前体的性腺指数小于正常青蟹,但也正是由于部分性腺分解产生的物质才使得黄油蟹前体更加鲜美,食用价值更高。
2.1.2 基本成分组成
由表1可知,2种生命形式青蟹的性腺水分含量无显著差别,黄油蟹前体性腺中的灰分含量显著高于正常青蟹(P<0.05),但其粗蛋白和粗脂肪均显著低于正常青蟹(P<0.05),原因可能是由于在黄油蟹完全成熟的前期过渡阶段,随着性腺的逐渐分解,不仅性腺中的脂肪会被分解成黄油状物质而被排出性腺组织外,且性腺中的蛋白质也同时被分解,导致其粗蛋白和粗脂肪含量均显著降低。
表1 不同生长形态的雌性青蟹性腺的基本成分 单位:%
Table 1 Nutrients compositions in the gonads from female mud crab in different growth-forms

生命形式水分含量粗蛋白含量粗脂肪含量灰分含量正常青蟹48.03±0.00a38.39±0.25a14.21±0.12a1.97±0.02b黄油蟹前体49.17±0.00a33.18±0.46b8.29±0.14b2.05±0.00a
2.1.3 氨基酸组成及评价
2.1.3.1 水解氨基酸组成及含量
蛋白质构成机体组织并维持组织的生长更新和修补,参与机体重要的生理功能和氧化功能,是机体中极为重要的营养素,也是各种生命活动极为重要的物质基础[19]。蛋白质由不同氨基酸组成,蛋白质中氨基酸的比例和种类决定了青蟹性腺的营养价值[20]。由表2可知,2种不同生命形式的雌性青蟹水解氨基酸,除实验方法(酸水解)导致色氨酸无法检测外,共检测出17种氨基酸。包括7种必需氨基酸:蛋氨酸(Met)、亮氨酸(Leu)、异亮氨酸(Ile)、缬氨酸( al)、赖氨酸(Lys)、苏氨酸(Thr)和苯丙氨酸(Phe);10种非必需氨基酸:组氨酸(His)、精氨酸(Arg)、天冬氨酸(Asp)、谷氨酸(Glu)、甘氨酸(Gly)、丙氨酸(Ala)、酪氨酸(Tyr)、丝氨酸(Ser)、半胱氨酸(Cys)和脯氨酸(Pro)。
由表2可知,黄油蟹前体和正常青蟹性腺中所检测出的氨基酸种类及含量高低顺序一致,含量最高的均为Glu、Asp和Leu,同时黄油蟹前体中检测出的水解氨基酸含量均显著低于正常青蟹(P<0.05),但均高于中华绒螯蟹性腺[21],原因可能是由于其性腺蛋白质分解,导致总蛋白质含量降低,水解氨基酸含量也随之降低,但其EAA/TAA及EAA/NEAA均高于正常青蟹,更符合FAO/WHO(EAA/TAA在0.4左右,EAA/NEAA在0.6以上)的推荐标准[22],因此黄油蟹前体的性腺蛋白质质量优于正常青蟹。
表2 不同生长形态的雌性青蟹性腺水解氨基酸含量 单位:g/100 g
Table 2 Hydrolyzed amino acid contents in the gonads from female mud crab in different growth-forms

氨基酸种类正常青蟹黄油蟹前体蛋氨酸Met0.90±0.06a0.67±0.09b异亮氨酸Ile1.53±0.09a1.20±0.15b亮氨酸Leu2.42±0.15a1.90±0.25b缬氨酸 al1.96±0.12a1.54±0.18b苏氨酸Thr1.35±0.08a1.04±0.13b赖氨酸Lys1.77±0.09a1.39±0.18b苯丙氨酸Phe1.19±0.07a0.92±0.12bEAA11.12±0.73a8.66±1.05b组氨酸His0.95±0.05a0.75±0.09b精氨酸Arg1.76±0.11a1.41±0.20b半必需氨基酸2.71±0.16a2.16±0.27b谷氨酸Glu4.18±0.25a3.33±0.44b天冬氨酸Asp2.36±0.13a1.86±0.25b丙氨酸Ala1.34±0.06a1.08±0.13b甘氨酸Gly1.20±0.05a0.97±0.11b酪氨酸Tyr1.14±0.09a0.83±0.12b半胱氨酸Cys0.24±0.03a0.17±0.03b丝氨酸Ser1.31±0.09a1.02±0.12b脯氨酸Pro1.51±0.10a1.18±0.17bNEAA18.70±0.80a10.44±1.36bTAA32.53±2.08a21.26±2.76bEAA/TAA0.330.41EAA/NEAA0.590.83
注:EAA,必需氨基酸总量;NEAA,非必需氨基酸总量;TAA,氨基酸总量(下同)
2.1.3.2 必需氨基酸组成评价
蛋白质的营养价值主要取决于必需氨基酸的种类及含量和氨基酸的组成比例,所含氨基酸的种类齐全、含量丰富及比例适宜的氨基酸更容易被人体吸收,营养价值也更高[23]。利用AAS和CS对正常青蟹和黄油蟹前体性腺中必需氨基酸进行评价,结果见表3。
表3 不同生长形态雌性青蟹性腺必需氨基酸组成评价
Table 3 E aluation of essential amino acid compositions of the gonads from female mud crab in different growth-forms

必需氨基酸正常青蟹黄油蟹前体mg/g NAASCSmg/g NAASCSFAO评分模式标准值鸡蛋蛋白质标准异亮氨酸Ile2491.000.752260.900.68250331亮氨酸Leu3940.900.743580.810.67440534赖氨酸Lys2880.850.702620.770.59340441缬氨酸 al3191.000.792900.910.71318410苏氨酸Thr2200.880.751960.780.67250292蛋氨酸+半胱氨酸Met+Cys1860.850.481580.720.41220386苯丙氨酸+酪氨酸Phe+Tyr3791.000.673300.870.58380565
以AAS作为评价标准时,正常青蟹和黄油蟹前体性腺的2种限制氨基酸均为Lys和Met+Cys,这与以CS作为评价标准的结果相一致。在性腺组织中,黄油蟹前体的AAS数值均低于正常青蟹,CS数值也均低于正常青蟹,这可能与黄油蟹前体性腺中蛋白质被分解,导致其蛋白质和氨基酸含量较低有关。
2.1.4 矿物质组成及含量
矿物质元素是人体生长发育所需的六大营养素之一,在维持人体健康和生长发育的过程中起重要作用,是构成机体组织的重要物质,参与人体各项重要的生命活动[24],众所周知,矿物质在机体中无法自己合成,必须从外界摄入,所以人们在日常饮食中摄入丰富的矿物质就显得尤为重要。如表4所示,两者鲜样的矿物质含量均比较丰富。Na、K、P、Ca、Mg是人体重要的常量元素,是构成机体组织的基本成分,其中Na、K广泛分布于身体各个部位,参与神经传导,维持渗透压等许多重要生命活动,而Ca、Mg、P是构成骨骼和膜组织等的重要成分[25]。在性腺组织中,两者的K、Mg含量无显著差别,黄油蟹前体的Na、Ca含量显著低于正常青蟹,但其P含量显著高于正常青蟹(P<0.05),这种Ca和P含量的差异和失调也可能是导致黄油蟹前体在生殖发育期间无法完成正常脱壳的原因之一。
表4 不同生长形态雌性青蟹性腺矿物质含量 单位:mg/100 g
Table 4 Mineral contents in the gonads from female
mud crab in different growth-forms

种类正常青蟹黄油蟹前体Na64.37±1.88a48.79±3.93bK117.68±3.32a114.55±2.22aMg29.34±0.75a30.22±0.97aCa28.29±3.58a7.32±1.55bP601.92±9.47b680.62±20.63aFe*1.70±0.12b4.55±0.04aCu*0.39±0.01a0.35±0.01bZn*18.67±0.23b32.72±0.68aMn*0.82±0.02a0.57±0.04bSe*0.00±0.00b0.41±0.04a总含量863.19±19.37b920.09±30.11a
注:*表示微量元素。
矿物质尤其是一些微量元素对人体的生命活动起着极其重要的作用,微量元素的缺失可能会造成机体疾病的发生[26]。Fe与机体的能量代谢和造血功能关系密切,Zn是生长发育所需的重要元素之一,在协调免疫反应,生殖系统发育,味觉、视觉调节等方面均有重要作用[27],黄油蟹前体的性腺组织中Fe、Zn的含量显著高于正常青蟹(P<0.05),其含量分别为4.55和32.72 mg/100 g,远高于中华绒螯蟹[21]和中华鳖[28];Cu在体内起着维持神经系统的结构和功能、提高免疫力和预防相关疾病等作用,Mn是体内多种酶的组成成分[29],正常青蟹性腺组织中Cu、Mn的含量显著高于黄油蟹前体(P<0.05)。而Se在人体抗衰老和抗癌方面起着积极的作用[16],仅在黄油蟹前体性腺组织中检测出较高含量的Se(0.41 mg/100 g)。综合比较二者性腺组织中矿物质总含量,黄油蟹前体显著高于正常青蟹(P<0.05),但二者矿物质(尤其是微量元素)含量均比较丰富,可认为均是优良的矿物质补充来源。
2.2.1 游离氨基酸比较分析
TA 被广泛用于评价食物中味感物质对食物味感的影响及程度,通过比较同种物质在纯水中的味感阈值判断该物质对食物味感的影响程度[30]。构成食物味感的主要成分有游离氨基酸、核酸、有机酸等物质,Na、K的含量也会对味感有一定的影响[6-8]。由表4可知,K在正常青蟹和黄油蟹前体性腺组织鲜样中的含量分别为117.68和114.55 mg/100 g,换算成干样状态下其含量为226.44和225.36 mg/100 g,而K的味觉识别阈值为1.3 mg/mL,两者的TA 均大于1,可以推断出K与Na相似,也会对性腺组织的味感有一定的影响,赋予性腺组织略咸的口感,这可能是平时清蒸膏蟹时不放任何佐料吃起来也不寡淡的原因之一。
性腺组织中游离氨基酸的含量见表5,两者游离氨基酸和必需氨基酸总量均无显著差异。由表2和表5可看出,水解氨基酸的含量和游离氨基酸的含量之间并无关系。游离氨基酸中,Arg含量占总含量的50%左右,但在水解氨基酸中仅占5%左右,水解氨基酸中Glu和Asp含量较高,但在游离氨基酸中含量均较低,原因之一是在测量水解氨基酸的酸性水解过程中,谷氨酰胺和天冬酰胺会被氨基化为Glu和Asp[17],导致Glu和Asp的含量过高。
不同的氨基酸会呈现出不同的口味,主要包括鲜味、甘味和苦味[6-8]。Asp和Glu实际上呈现出酸味,但由于谷氨酸盐和天冬氨酸盐是味精的主要成分,是鲜味的主要来源,因此Asp和Glu被定义为鲜味氨基酸;Thr、Ser、Gly、Ala主要呈现出甘味,和可溶性糖一起构成食物甜味的主要来源;Ile、Leu、Tyr、Phe和His主要呈现出苦味;Lys、Met、 al、Cys、Arg和Pro味感层次较为复杂,其中Lys、Met、 al和Cys主要呈现负面影响,而Arg和Pro主要呈现出正面影响。
表5 不同生长形态雌性青蟹性腺游离氨基酸(FAA)
的含量、味感、味觉阈值及TA s
Table 5 The contents, taste attributes, taste thresholds,
and TA s of free amino acids in the gonads from
female mud crab in different growth-forms

氨基酸种类味感含量/(mg·g-1)正常青蟹黄油蟹前体味觉阈值/(mg·mL-1)TA 正常青蟹黄油蟹前体天冬氨酸Asp鲜(+)0.04±0.00a0.02±0.00b1.00.040.02苏氨酸Thr*甘(+)0.92±0.01a0.74±0.01b2.60.350.28丝氨酸Ser甘(+)0.55±0.01a0.29±0.00b1.50.370.19谷氨酸Glu鲜(+)1.55±0.00a1.48±0.01a0.35.174.93甘氨酸Gly甘(+)0.69±0.01a0.69±0.01a1.30.530.53丙氨酸Ala甘(+)2.05±0.01a1.84±0.03b0.63.423.07半胱氨酸Cys苦/甘/含S(-)0.02±0.03a0.00±0.00b---缬氨酸 al*甘/苦(-)0.52±0.01a0.46±0.05b0.41.301.15蛋氨酸Met*苦/甘/含S(-)0.43±0.01a0.41±0.04a0.31.431.37异亮氨酸Ile*苦(-)0.42±0.00a0.39±0.00a0.90.471.43亮氨酸Leu*苦(-)0.51±0.02a0.44±0.00b1.90.270.23酪氨酸Tyr苦(-)2.32±0.09b2.57±0.05a---苯丙氨酸Phe*苦(-)1.10±0.03a1.20±0.01a0.91.221.33赖氨酸Lys*甘/苦(-)2.91±0.06a2.18±0.06b0.55.824.36组氨酸His苦(-)0.68±0.02a0.60±0.01b0.23.403.00精氨酸Arg苦/苷(+)14.57±1.23a16.09±1.33a0.529.1432.18脯氨酸Pro甘/苦(+)2.22±0.05a2.20±0.04a3.00.740.73EAA6.00±0.24a5.82±0.13a总量30.69±1.12a31.60±0.99a
注:*必需氨基酸;(+)表示正面,(-)表示负面;-表示未有相关数据
海洋食品被人们喜爱的重要原因之一就是海产品鲜味和甘味氨基酸含量普遍较高,从而使食物滋味更鲜美[31]。2种不同生命形式的雌性青蟹性腺组织中的呈味氨基酸含量如图1所示,两者的鲜味、甘味和苦味氨基酸含量均无显著差别,但黄油蟹前体的甘味氨基酸含量略高于正常青蟹,苦味和鲜味氨基酸略低于正常青蟹,表明黄油蟹前体的性腺组织可能比正常青蟹的味感略好。
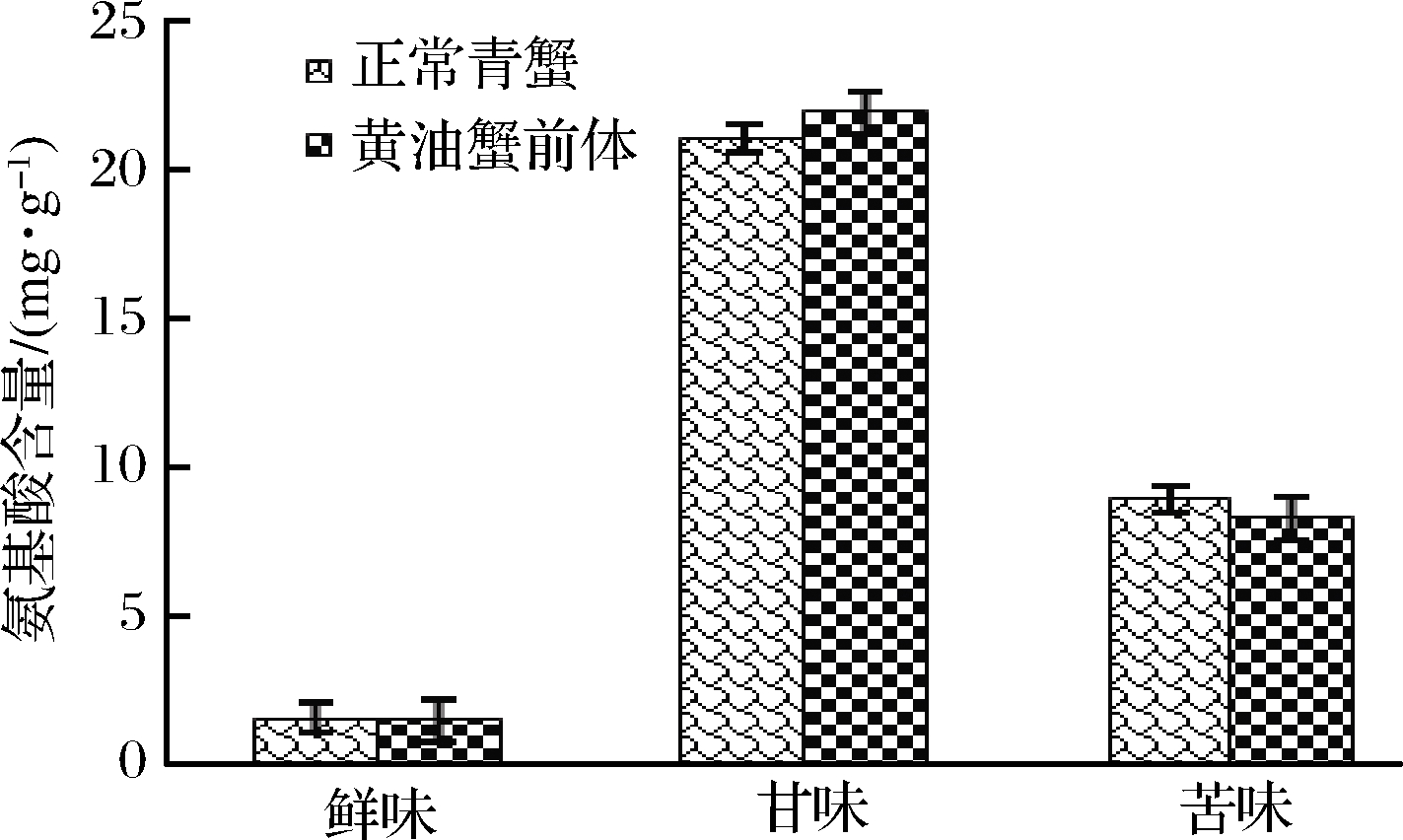
图1 不同生长形态雌性青蟹性腺的呈味氨基酸含量
Fig.1 Contents of taste amino acids in the gonads of female mud crab in different growth-forms
性腺组织的TA 见表5,虽然部分氨基酸含量较低,但由于其味觉阈值较低,TA 较高,对味感影响较大。TA >1的氨基酸主要包括Glu、Ala、 al、Met、Phe、Lys、His和Arg,这些氨基酸对性腺组织味感贡献较大。Glu、Ala和Arg对味感有正面影响,其中Arg对味感贡献最大,Arg和Ala构成了性腺组织的主要甘味感来源,Glu构成了性腺组织主要鲜味感来源。虽然黄油蟹前体的Glu和Ala的TA 略低于正常青蟹,但其Arg的TA 较高,且 al、Met、Lys和His的TA 均低于正常青蟹,综合比较,黄油蟹前体的性腺组织的味感更甘美。
2.2.2 挥发性风味物质相对含量
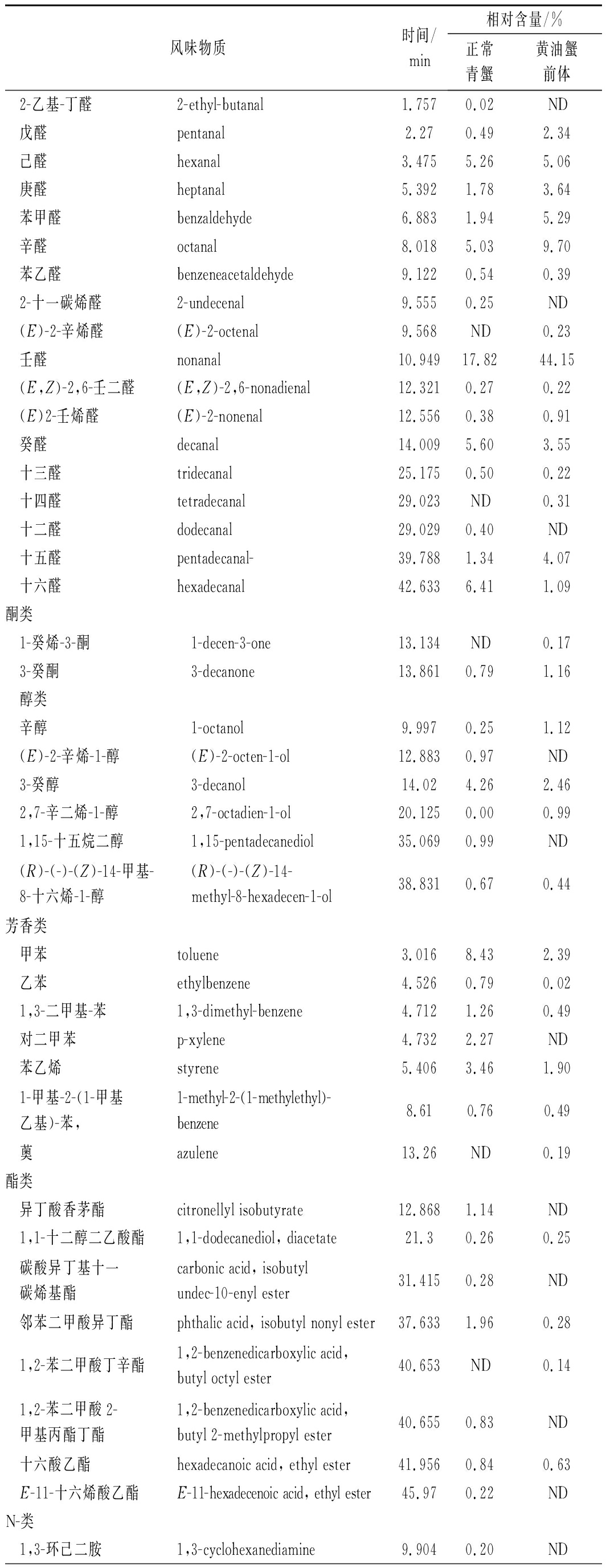
通过GC-MS对2种生命形式的雌性青蟹的挥发性风味物质进行检测,结果见表6所示,在性腺组织中共检出72种挥发性风味物质,其中正常青蟹55种,黄油蟹前体42种。所共有的物质有14种,这些物质构成性腺组织的主要风味。正常青蟹和黄油蟹前体含量最高的挥发性风味物质均为壬醛,分别占17.82%和44.15%。
表6 不同生长形态的雌性青蟹性腺中挥发性风味物质含量 单位:%
Table 6 The contents of olatile fla our compounds in the
gonads of female mud crab in different growth-forms

风味物质时间/min相对含量/%正常青蟹黄油蟹前体烃类1,3,5,7-环辛四烯1,3,5,7-cyclooctatetraene5.184.90NDD-柠檬烯D-limonene8.7392.291.084-甲基-2,7-辛二烯4-methyl-2,7-octadiene12.87ND0.621-(2-丙烯基)-环戊烯1-(2-propenyl)-cyclopentene13.675ND0.304-甲基-1,3-戊二烯4-methyl-1,3-pentadiene13.7940.38ND1-十八炔1-octadecyne16.441ND0.161-十六炔1-hexadecyne16.4430.25ND十二烷dodecane16.4540.22ND十三烷tridecane17.2880.220.165-乙基-1,3-环己二烯5-ethyl-1,3-cyclohexadiene19.7790.22ND2,6,10,15-四甲基-十七烷2,6,10,15-tetramethyl-heptadecane19.8710.39ND3-甲基-十三烷3-methyl-tridecane19.8790.32ND十四烷tetradecane21.0221.140.83(Z)-7-十四烯(Z)-7-tetradecene22.769ND0.2310甲基壬烷10-methylnonadecane23.2970.000.22十五烷pentadecane24.8360.470.29十六烷hexadecane28.6290.670.2116-十八烯16-octadecenal29.0220.47ND1,19-二十碳二烯1,19-eicosadiene38.5760.87ND醛类丁醛butanal1.7360.54ND
续表6
风味物质时间/min相对含量/%正常青蟹黄油蟹前体2-乙基-丁醛2-ethyl-butanal1.7570.02ND戊醛pentanal2.270.492.34己醛hexanal3.4755.265.06庚醛heptanal5.3921.783.64苯甲醛benzaldehyde6.8831.945.29辛醛octanal8.0185.039.70苯乙醛benzeneacetaldehyde9.1220.540.392-十一碳烯醛2-undecenal9.5550.25ND(E)-2-辛烯醛(E)-2-octenal9.568ND0.23壬醛nonanal10.94917.8244.15(E,Z)-2,6-壬二醛 (E,Z)-2,6-nonadienal12.3210.270.22(E)2-壬烯醛(E)-2-nonenal12.5560.380.91癸醛decanal14.0095.603.55十三醛tridecanal25.1750.500.22十四醛tetradecanal29.023ND0.31十二醛dodecanal29.0290.40ND十五醛pentadecanal-39.7881.344.07十六醛hexadecanal42.6336.411.09酮类1-癸烯-3-酮1-decen-3-one13.134ND0.173-癸酮3-decanone13.8610.791.16醇类辛醇1-octanol9.9970.251.12(E)-2-辛烯-1-醇(E)-2-octen-1-ol12.8830.97ND3-癸醇3-decanol14.024.262.462,7-辛二烯-1-醇2,7-octadien-1-ol20.1250.000.991,15-十五烷二醇1,15-pentadecanediol35.0690.99ND(R)-(-)-(Z)-14-甲基-8-十六烯-1-醇(R)-(-)-(Z)-14-methyl-8-hexadecen-1-ol38.8310.670.44芳香类甲苯toluene3.0168.432.39乙苯ethylbenzene4.5260.790.021,3-二甲基-苯1,3-dimethyl-benzene4.7121.260.49对二甲苯p-xylene4.7322.27ND苯乙烯styrene5.4063.461.901-甲基-2-(1-甲基乙基)-苯,1-methyl-2-(1-methylethyl)-benzene8.610.760.49薁azulene13.26ND0.19酯类异丁酸香茅酯citronellyl isobutyrate12.8681.14ND1,1-十二醇二乙酸酯1,1-dodecanediol, diacetate21.30.260.25碳酸异丁基十一碳烯基酯carbonic acid, isobutyl undec-10-enyl ester31.4150.28ND邻苯二甲酸异丁酯phthalic acid, isobutyl nonyl ester37.6331.960.281,2-苯二甲酸丁辛酯1,2-benzenedicarboxylic acid, butyl octyl ester40.653ND0.141,2-苯二甲酸2-甲基丙酯丁酯1,2-benzenedicarboxylic acid, butyl 2-methylpropyl ester40.6550.83ND十六酸乙酯hexadecanoic acid, ethyl ester41.9560.840.63E-11-十六烯酸乙酯E-11-hexadecenoic acid, ethyl ester45.970.22NDN-类1,3-环己二胺1,3-cyclohexanediamine9.9040.20ND
续表6
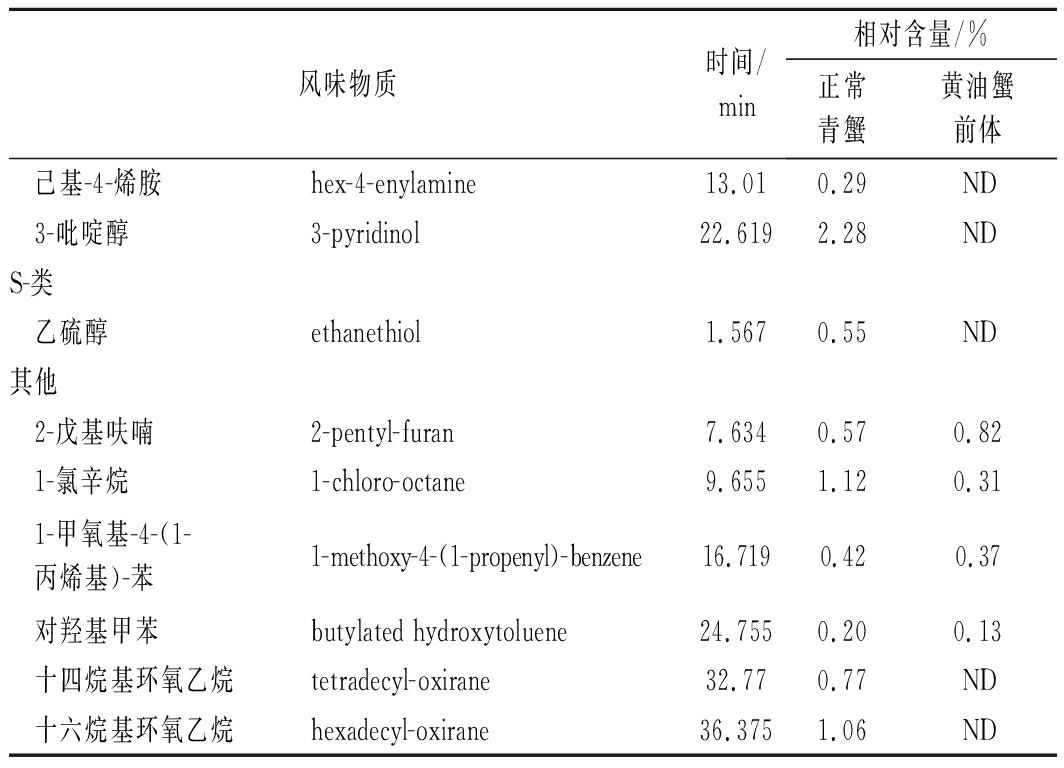
风味物质时间/min相对含量/%正常青蟹黄油蟹前体己基-4-烯胺hex-4-enylamine13.010.29ND3-吡啶醇3-pyridinol22.6192.28NDS-类乙硫醇ethanethiol1.5670.55ND其他2-戊基呋喃2-pentyl-furan7.6340.570.821-氯辛烷1-chloro-octane9.6551.120.311-甲氧基-4-(1-丙烯基)-苯1-methoxy-4-(1-propenyl)-benzene16.7190.420.37对羟基甲苯butylated hydroxytoluene24.7550.200.13十四烷基环氧乙烷 tetradecyl-oxirane32.770.77ND十六烷基环氧乙烷hexadecyl-oxirane36.3751.06ND
注:ND表示未检测到
各类挥发性风味化合物的含量如图2所示。在两者性腺组织中主要检测出的挥发性风味物质为醛类、醇类、芳香族类和烃类,其中正常青蟹,分别48.58%和81.17%和黄油蟹前体含量最高的均为醛类。由于烃类物质的阈值较高,只有在高浓度下才会引起嗅觉反应[32],虽然两者性腺组织烃类物质含量较高,但对整体风味贡献较小。同样,酮类、芳香烃类、酯类化合物的阈值也均较高,对风味贡献较小[33-34],但可能会有助于整体风味的提升。醇类大多数是脂质氧化分解的产物,醇类物质主要呈现出脂肪香气和酒香,长链饱和醇阈值较高,对风味影响较小,而不饱和醇阈值较低,对风味影响较大[35],两者性腺组织的醇类物质检出种类较少,且含量较低,对风味影响不大,但对整体风味可能存在一定影响。

图2 不同生长形态雌性青蟹性腺挥发性风味物质含量
Fig.2 The contents of olatile fla our compounds in the gonads of female mud crab in different growth-forms
醛类物质是由不饱和脂肪酸氧化以及氨基酸Strecker降解产生的,是一种低阈值的呈味物质,并且具有气味叠加效应,在种类和浓度较高的情况下,会呈现出复杂的嗅觉反应[36]。醛类由于其阈值较低,且普遍在肉类中含量较高,被认为是肉制品的主要呈香物质。在正常青蟹的性腺组织中检测出17种醛类物质,黄油蟹前体中检测出15种,正常青蟹含量最高的为壬醛、十六醛(6.41%)和己醛(5.26%),黄油蟹前体中含量最高的为壬醛、辛醛(9.70%)和苯甲醛(5.29%)。在性腺组织中,己醛、庚醛、苯甲醛、辛醛、壬醛、(E,Z)-2,6-壬二醛、(E)-2-壬烯醛等物质对主体风味贡献较大,己醛呈现出青草味,苯甲醛呈现出杏仁香、坚果香,辛醛呈现出青草味、油脂香气,壬醛呈现出脂肪和青草香味,而庚醛呈现出鱼腥味[32-34]。黄油蟹前体性腺组织中的庚醛、苯甲醛、辛醛、壬醛和(E)-2-壬烯醛均高于正常青蟹,且黄油蟹前体性腺中还含有少量的具有青草和脂肪香气的(E)-2-辛烯醛,两者主体呈香物质含量相差较大的主要原因之一可能是黄油蟹前体性腺组织在分解过程中,其脂肪和蛋白质的性质发生了变化(尤其是可分解为醛类物质的不饱和脂肪酸和氨基酸),转变或分解为挥发性风味物质。因此,综合判断黄油蟹前体的性腺组织的风味优于正常雌性青蟹。
2-戊基呋喃阈值较低,且具有泥土和蔬菜香气,其广泛存在于肉制品中,作为肉品脂质氧化的指示剂可能对肉品的整体风味作用巨大[36],黄油蟹前体性腺组织中2-戊基呋喃的含量(0.82%)高于正常青蟹(0.57%),进一步表明黄油蟹前体性腺的风味相对优于正常青蟹。
通过对正常发育雌性青蟹和黄油蟹前体性腺组织的营养品质和风味物质进行分析,结果表明,在营养品质方面,黄油蟹前体的GSI显著偏低(P<0.05);两者性腺组织的水分含量无显著差别,黄油蟹前体性腺中的灰分含量显著偏高(P<0.05),但粗蛋白和粗脂肪均显著偏低(P<0.05);黄油蟹前体的EAA和TAA均显著低于正常青蟹,但其蛋白质质量较好,更符合FAO/WHO标准;黄油蟹前体性腺的矿物质总量显著高于正常青蟹(P<0.05),且Zn的含量较高(32.72 mg/100 g)。风味物质方面,黄油蟹前体的甘味氨基酸含量略高,苦味和鲜味氨基酸含量略低,但二者之间均无显著差别;黄油蟹前体性腺组织中醛类物质及主要呈香物质相对含量较高。综上,黄油蟹前体性腺的营养品质并非完全优于正常雌性青蟹,但其风味相对优于正常雌性青蟹。
[1] 林琪,李少菁,黎中宝,等.中国东南沿海青蟹属(Scylla)的种类组成[J].水产学报,2007,31(2):211-219.
[2] 金燕, 杨荣华,周凌霄,等.蟹肉挥发性成分的研究[J].中国食品学报,2011,11(1):233-238.
[3] TURCHINI G M,MORETTI M,MENTASTI T,et al.Effects of dietary lipid source on fillet chemical composition,fla our olatile compounds and sensory characteristics in the freshwater fish tench (Tinca tinca L.)[J].Food Chemistry,2006,102(4):1 144-1 155.
[4] WANG S,HE Y,WANG Y,et al.Comparison of fla our qualities of three sourced Eriocheir Sinensis[J].Food Chemistry,2016,200:24-31.
[5] SARNOSKI P J,O’KEEFE S F,JAHNCKE M L,et al.Analysis of crab meat olatiles as possible spoilage indicators for blue crab (Callinectes sapidus) meat by gas chromatography-mass spectrometry[J].Food Chemistry,2017,122(3):930-935.
[6] GUO Y R,GU S Q,WANG X C,et al.Nutrients and non- olatile taste compounds in Chinese mitten crab by-products[J].Fisheries Science,2015,81(1):193-203.
[7] KONG L,CAI C,YE Y,et al.Comparison of non- olatile compounds and sensory characteristics of Chinese mitten crabs (Eriocheir sinensis) reared in lakes and ponds:Potential en ironmental factors[J].Aquaculture,2012,364-365:96-102.
[8] CHEN D W,ZHANG M,SHRESTHA S.Compositional characteristics and nutritional quality of Chinese mitten crab (Eriocheir sinensis)[J].Food Chemistry,2006,103(4):1 343-1 349.
[9] 王桂忠, 李少菁,陈志刚.青蟹(Scylla spp.)养殖现状及拟穴青蟹(S.paramamosain)种群生物学研究[J].厦门大学学报(自然科学版),2016,55(5):617-623.
[10] 李永亮, 赵欢欢,李荣华,等.拟穴青蟹(Scylla paramamosain)六个地理群体肌肉氨基酸和脂肪酸的比较分析[J].海洋与湖沼,2019,50(2):465-472.
[11] TANG L,WANG H,WANG C L,et al.Temperature potentially induced distincti e fla or of mud crab Scylla paramamosain mediated by gut microbiota[J].Scientific Reports,2020,10(1):3 720.
[12] CHANG G, WU X, CHENG Y, et al.Reproducti e performance,offspring quality,proximate and fatty acid composition of normal and precocious Chinese mitten crab Eriocheir sinensis[J].Aquaculture,2017,469:137-143.
[13] 陆剑锋, 焦道龙,张伟伟,等.速冻蟹黄粉的营养成分分析及品质评价[J].食品科学,2009,30(24):251-255.
[14] WHO/FAO/UNU.Protein and amino acid requirements in human nutrition:Report of a Joint FAO/WHO/UNU expert consultation[R].Gene a,WHO,2007.
[15] 邓宏玉, 刘芳芳,张秦蕾,等.5种禽肉中矿物质含量测定及营养评价[J].食品研究与开发,2017,38(6):21-24;103.
[16] 吴浩然, 林琳,程华峰,等.河蟹分割加工边角料的营养成分分析及品质评价[J].肉类工业,2019,(6):31-36;57.
[17] CHEN D W,ZHANG M.Non- olatile taste acti e compounds in the meat of Chinese mitten crab (Eriocheir sinensis)[J].Food Chemistry,2007,104(3):1 200-1 205.
[18] 陈舜胜, 蒋根栋.中华绒螯蟹蟹肉挥发性风味成分分析[J].食品科学,2009,30(20):308-311.
[19] 程汉良, 蒋飞,彭永兴,等.野生与养殖草鱼肌肉营养成分比较分析[J].食品科学,2013,34(13):266-270.
[20] WU X,ZHOU B,CHENG Y,et al.Comparison of gender differences in biochemical composition and nutritional alue of arious edible parts of the blue swimmer crab[J].Journal of Food Composition and Analysis,2009,23(2):154-159.
[21] WU H R,GE M T,ZHOU X H,et al.Nutritional qualities of normal and precocious adult male Chinese mitten crabs (Eriocheir sinensis)[J].Aquaculture Research,2019,50(8):2 267-2 275.
[22] FAO/WHO/UNU.Energy and protein requirements:Report of a Joint FAO/WHO/UNU expert consultation[R].Gene a,WHO,1985.
[23] 王广军, 陈鹏飞,余德光,等.佛罗里达鳖与中华鳖不同部位营养成分的比较分析[J].食品工业科技,2015,36(11):350-355.
[24] SHI X,LU J X,WU Q Y,et al.Comparati e analysis of growth performance between female and male mud crab Scylla paramamosain crablets:E idences from a four-month successi e growth experiment[J].Aquaculture,2019,505:351-362.
[25] 闫天龙, 古霞,邓维泽,等.通江花鸡蛋品质及营养成分分析[J].食品与发酵工业,2015,41(2):195-199.
[26] ANA L M,PATRICIA A,HELENA M L,et al.Nutritional quality and safety of cooked edible crab (Cancer pagurus)[J].Food Chemistry,2012,133(2):277-283.
[27] 夏剑秋, 张毅方.大豆中主要营养成分和微量元素的功能作用[J].中国油脂,2007,(1):71-73.
[28] 陈师师, 薛静,何中央,等.2种不同品系中华鳖的营养成分分析与比较[J].食品科学,2015,36(18):114-119.
[29] 孟学平, 郝珏,梁猛,等.西施舌可食部分微量元素分析与评价[J].食品科学,2012,33(4):167-172.
[30] DERMIKI M,PHANPHENSOPHON N,MOTTRAM D S,et al.Contributions of non- olatile and olatile compounds to the umami taste and o erall fla our of shiitake mushroom extracts and their application as fla our enhancers in cooked minced meat[J].Food Chemistry,2013,141(1):77-83.
[31] LIU C S,MENG F T,TANG X M,et al.Comparison of non olatile taste acti e compounds of wild and cultured mud crab Scylla paramamosain[J].Fisheries Science,2018,84(5):897-907.
[32] YU H Z,CHEN S S.Identification of characteristic aroma-acti e compounds in steamed mangro e crab (Scylla serrata)[J].Food Research International,2010,43(8):2 081-2 086.
[33] GU S Q,WANG X C,TAO N P,et al.Characterization of olatile compounds in different edible parts of steamed Chinese mitten crab (Eriocheir sinensis)[J].Food Research International,2013,54(1):81-92.
[34] ZHUANG K,WU N,WANG X,et al.Effects of 3 feeding modes on the olatile and non olatile compounds in the edible tissues of female Chinese mitten crab (Eriocheir sinensis)[J].Journal of Food Science,2016,81(4):968-981.
[35] GAO X C,GU S Q,WANG X C,et al.Comparison of olatile compounds in raw and cooked Chinese mitten crab hepatopancreas and gonads[J].Ad anced Materials Research,2014,941-944:1 040-1 044.
[36] ZHANG M,CHEN X,HAYAT K,et al.Characterization of odor-acti e compounds of chicken broth and impro ed fla or by thermal modulation in electrical stewpots[J].Food Research International,2018,109:72-81.