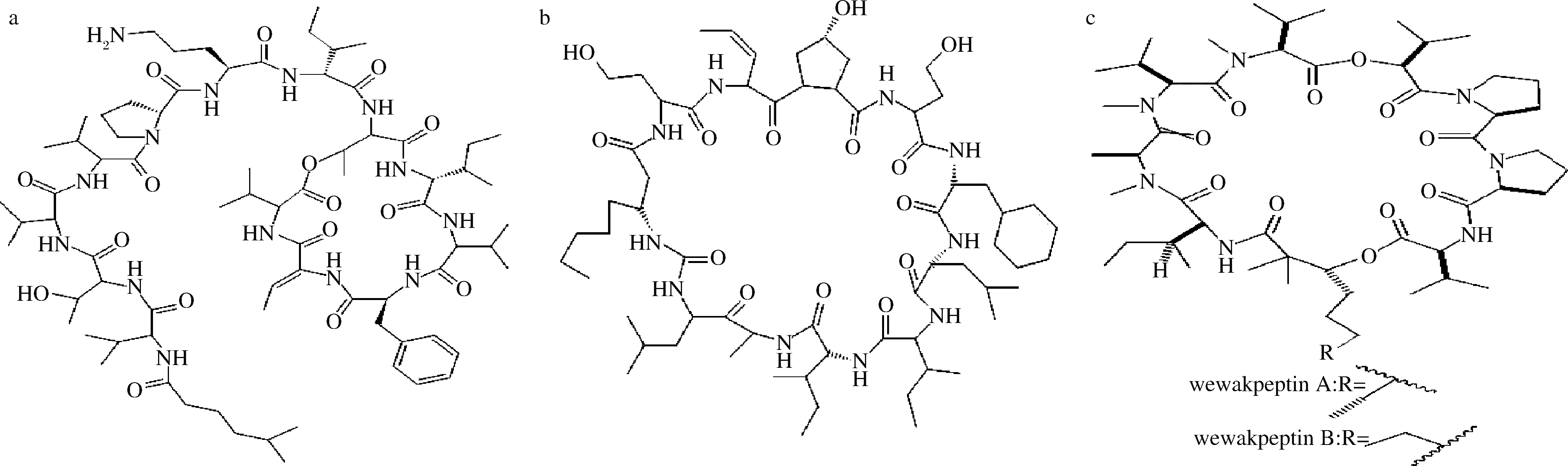
a-kahalalid F[8];b-hormothamnin A[9];c-wewakpeptin A和B[10]
图1 海藻环肽结构式
Fig.1 Structure of seaweed cyclic peptides
在肿瘤生物学、分子生物学、生物信息学等多学科的不断发展与交叉融合的背景下,研究人员已经在肿瘤的治疗方面取得显著成效。恶性肿瘤治疗方法一般是依据患者的肿瘤阶段分别采用手术、放射线、免疫和化学疗法等[1]来进行,但是这些治疗手段对人体仍然会造成一定的毒副作用,尤其是对中晚期患者所采取的放化疗法在将患者体内的恶性肿瘤细胞杀死的同时,对正常细胞也会有不可逆转的损伤,另外还伴随着人体不良反应。长期使用也会让癌细胞产生多重耐药性,使药物利用度降低[2]。据资料统计,估计2018年我国新增恶性肿瘤发病人数占据全球的1/5以上,死亡人数占据全球1/4以上[3]。恶性肿瘤已经成为人类健康安全的严重威胁,也给社会经济造成不可估量的损失。天然来源的低毒甚至无毒、高利用率的治疗肿瘤药物或辅助食品已成为药品行业和食品工业的研究热点。
海藻源活性肽是存在于海藻体内,经由直接提取法(物理提取和化学试剂提取)、蛋白酶酶解法、微生物发酵法或者通过化学合成法获取的介于蛋白质和氨基酸之间的生物活性肽,具有维持人体健康的生理调节功能[4]。我国海域辽阔,海藻资源极其丰富,微藻和浮游海藻因其独有的生活习性和生理结构成为海藻活性肽中被关注颇多的种类[5],研究人员对大型藻类的研究也在逐渐深入。海藻中存在的活性肽具有抗肿瘤增殖、破坏微丝网络、清除自由基等功能活性,对肿瘤细胞毒性较高但对正常细胞低毒(无毒),表明海藻不仅丰富了生物活性肽的来源而且具有用于恶性肿瘤化疗的潜力。本文依据近30年国内外相关文献,按照结构特征论述了海藻源活性肽的种类,并且重点总结海藻活性肽的基本制备方法、海藻抗肿瘤活性肽的活性评价方法及作用机制,以期为抗肿瘤药物和食品开发提供帮助。
海藻活性肽的分类多种多样,以海藻的大小可以分为微藻活性肽和大型藻海活性肽;以海藻的种类可以分为红藻活性肽、褐藻活性肽和绿藻活性肽;以活性肽的功能分类更广,有海藻抗氧化肽、抗癌肽、抗菌肽等等。生物活性肽的氨基酸组成、序列、长度、总电荷以及疏水性等结构特征均会对其活性产生影响[6]。本文按海藻活性肽的结构特征将其分为环肽、脂肽和线性肽。
环肽(cyclic peptides)是海藻肽中最常见的一类肽,是指一类由α-氨基酸和一些不常见的非蛋白氨基酸以肽键形成的环状天然小分子化合物[7]。藻类环肽通常比动物环肽要大,从软体动物中获得的环肽kahalalid A~E比同一家族的从羽藻中获取的kahalalid F要小得多。kahalalid F的分子式为C75H126N14O17,氨基酸序列为[D-aoIle-Thr- al-Z-Dhb-L-Phe- al-D-aoIle-L-Orn-L-Pro- al- al-Thr- al-5-MeHex],具有Thr-Ile-Orn-Pro- al- al-Thr- al和5-MB残基形成的侧链和Phe- al-Ile-Thr- al和DHAB的循环区的结构,对前列腺癌和乳腺癌细胞株具有强烈的毒性作用(IC50的范围从0.07~0.28 μmol/L),而且KF细胞毒性与多药耐药MDR1和酪氨酸激酶HER2/NEU的表达水平无关,仅与抗凋亡BCL-2蛋白的表达水平有关[8]。从蓝绿藻中发现具有溶细胞、细胞毒和神经毒等活性作用的环肽hormothamnin A,氨基酸序列为[D-Phe-D-Leu-L-Ile-D-allo-Ile-L-Leu-Gly-D-Baoa-L-Hser-Dhha-L-HyPro-L-Hser][9]。从鞘丝藻中分离出的2种环肽wewakpeptin A和B,研究发现此肽对NCI-H460人肺肿瘤和神经2A小鼠神经母细胞瘤细胞系细胞毒性较大(IC50约为0.4 μmol/L)[10],其氨基酸序列分别为MeAla-Me al-Me al-Hi a-Pro-Pro- al-Dhoya-Ile的异构体,结构式见图1。

a-kahalalid F[8];b-hormothamnin A[9];c-wewakpeptin A和B[10]
图1 海藻环肽结构式
Fig.1 Structure of seaweed cyclic peptides
脂肽(lipopeptidic)是一类由亲油的脂肪烃链和亲水的肽链两部分组成的具有两亲结构的化合物,由于其特殊的化学组成和两亲结构,使得脂肽具有抗菌活性外还具有多种特性[11]。从哈沙藻属蓝藻内得到具有抗真菌活性的脂肽hassallidin A,分子式为C62H99N11O24,氨基酸组成包括D-Tyr,D-Thr,L-Thr,D-allo-Thr,N-MeThr,D-Glu,L-Glu,Gly和脱氢氨基丁酸 (Dhb)[9]。jamaicamides A~C是从海洋蓝藻中分离出的3种具有抗肿瘤活性的高功能化脂肽,含有炔基溴化物、氯乙烯、甲氧基烯酮体系和吡咯烷酮环,分子式分别为C27H37N2O4ClBr、C27H37O4 N2Cl、C27H39O4 N2Cl。jamaicamides A~C对H-460人肺和神经-2A小鼠神经母细胞瘤细胞株均表现出细胞毒性。这3种脂肽对两个细胞系的IC50均约为15 μmol/L。而且这3种肽在5 μmol/L时都表现出钠通道阻断活性,对正常细胞产生的毒性效应较小,仅仅只有蛤蚌毒素在0.15 μmol/L时反应的一半[12]。从颤藻中新分离出2种均对HT-29和MDA-MB-435癌细胞株有抗增殖作用的环脂肽trichormamides C(IC50为1.7和1.0 μmol/L)和D(IC50为11.5和11.7 μmol/L)[13],trichormamides C是一种环十一肽,trichormamides D是一种环十二肽,两者均含有亲脂β-氨基癸酸残基,结构式见图2。
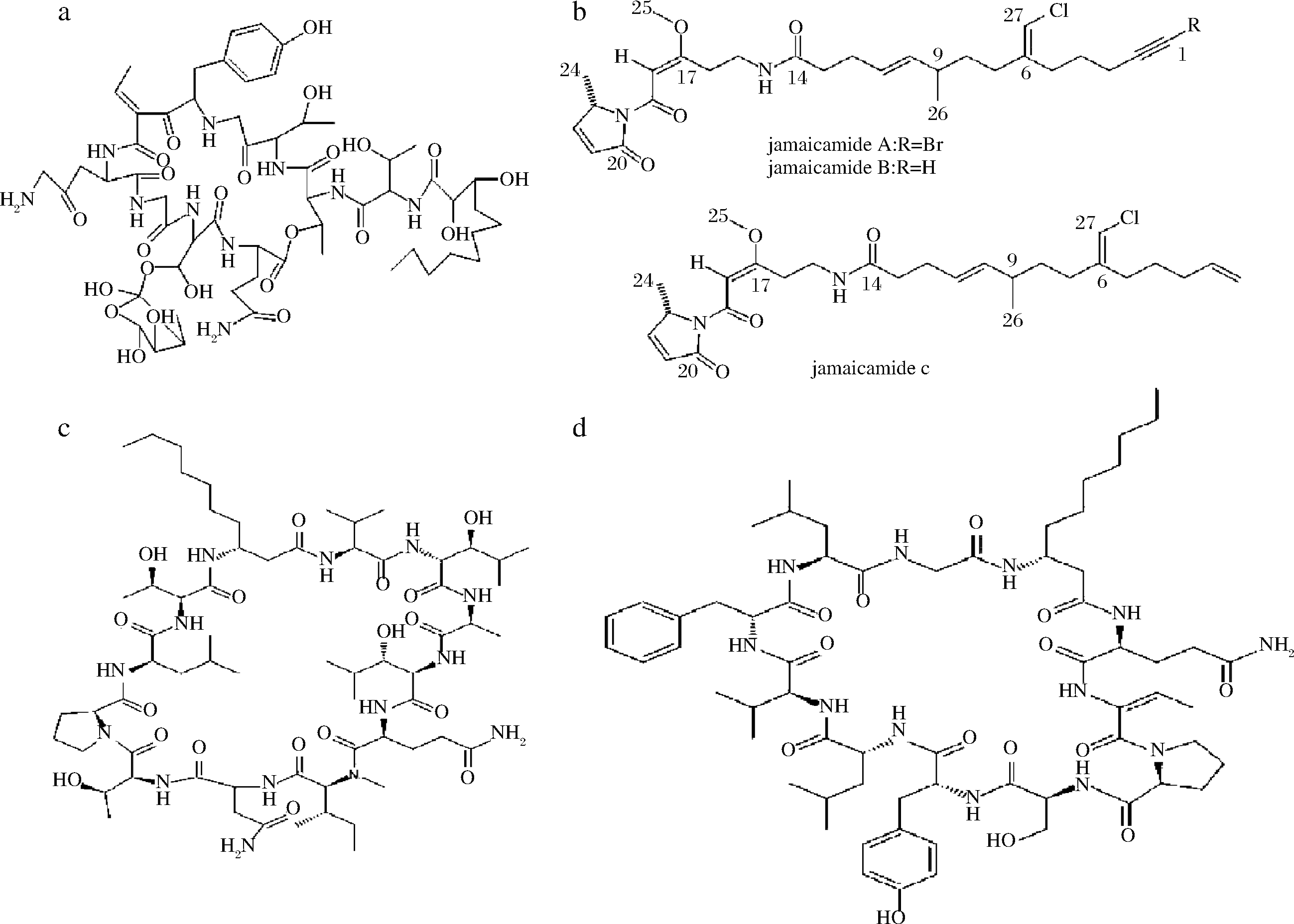
a-hassallidin A[9];b-jamaicamides A~C [12];c-trichormamides C;d-trichormamides D[13]
图2 海藻脂肽结构式
Fig.2 Structure of seaweed lipopeptidic
线性肽(linear peptides)是指由氨基酸经脱水缩合形成的线性结构的化合物。一般来说环肽比线性肽稳定性高,也具有更好的生物活性。从爱森藻中获得具有抗病毒和抗过敏活性的爱森藻肽,结构为L-吡咯啶酮-L-丙氨酸的线性肽[14]。另外从鹿角菜中提取出结构为L-吡咯烷酮基-α-L-谷酰胺基-L-谷酰胺的鹿角菜肽[15]。LUKE等[16]对巨大鞘丝藻进行分级提取发现线性肽desmethoxymajusculamide C (DMMC),含有氨基酸Ala、N-Me al、N-MePhe、N-MeIle、Gly(2)以及残基R-羟基酸2-羟基-3-甲基戊酸盐(Hmpa)、β-氨基酸3-氨基-2-甲基戊酸盐(Map)和4-氨基-2,2-二甲基-3-氧代戊酸(Dmop),并且证实此肽使细胞微丝网络破坏从而对HCT-116人结肠癌细胞系具有有效和选择性的抗实体肿瘤活性(IC50=20 nmol/L),结构式见图3。

a-爱森藻肽[14];b-鹿角菜肽[15];c-DMMC[16]
图3 海藻线性肽结构式
Fig.3 Structure of seaweed linear peptides
生物活性肽以其优越的生物功能特性赢得国内外专家学者广泛的研究。寻求高提取率同时不破坏活性肽活性的制备方法是进行活性肽研究的重要方面。目前关于海藻活性肽制备的方法主要有以下4种:直接提取法,酶解法、微生物发酵法和人工合成法。海藻活性肽的制备流程见图4。
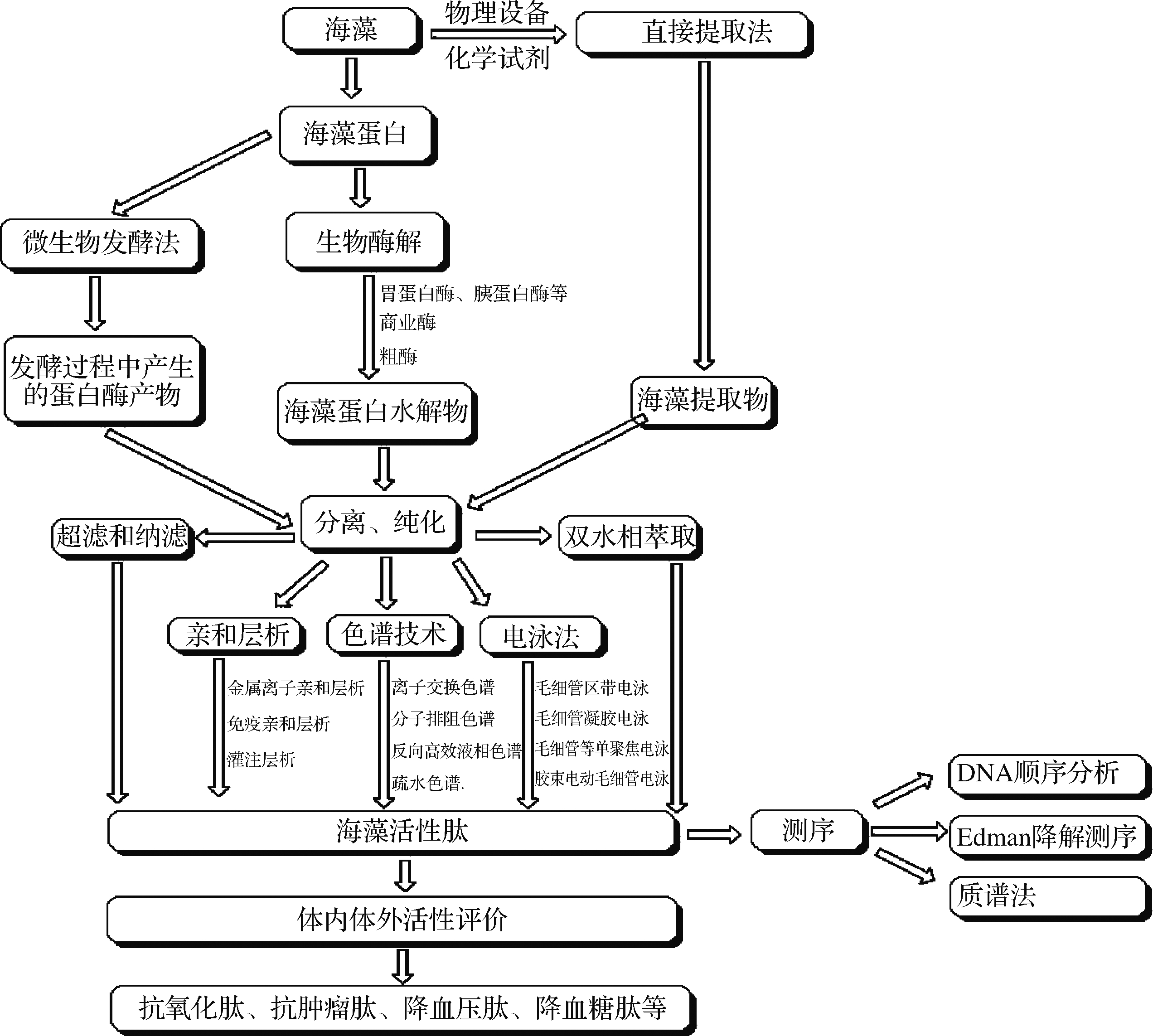
图4 海藻活性肽的制备流程
Fig.4 Preparation process of seaweed acti e peptide
直接提取法包括物理提取和化学提取。物理提取是在绿色环保的背景下逐渐发展起来的处理方法,在不使用化学试剂的条件下,直接将细胞破坏提取出细胞内的肽。低温超高压连续流法是物理提取的主要方法,该法可使藻细胞的细胞壁和细胞膜全部裂解,获取活性物质并保持肽的生物活性。另外反复冻融法与超声破坏结合也成为制备海藻活性肽的主要物理处理方法之一。
化学提取即使用化学试剂(强酸强碱、甲醇、乙醇、卤代烃等)提取后经分离纯化直接得到海藻活性肽。大多数微藻均用此法提取。MARK等[17]采用乙醇提取后,肽混合物经二氧化硅快速柱色谱洗脱,C18固相萃取柱和反相高效液相柱分离得到环肽kahalalid F。HAN等[10]用 (CH2Cl2)∶ (甲醇)(2∶1)反复提取鞘丝藻,得到的粗提液用硅胶真空液相色谱法分离,并且从10%己烷到100%甲醇的乙酸乙酯逐步增加溶剂梯度制备出环肽wewakamide A和guineamide G。除了以上直接将有机试剂作用在海藻原料上的方法外,还可作用在海藻原料提取或纯化后的蛋白上,通过化学试剂破坏蛋白质的肽键和空间结构,得到小分子活性肽。
直接提取法一般用于实验室提取活性肽的实现,但是物理提取对设备的要求高和化学提取提取率较低,多种副产物生成,而且化学试剂的使用不当也会改变产物结构和活性。这些缺陷导致直接提取法难以适应大规模的生产。
生物酶解是制备生物活性肽最快、最安全、最易控制的技术之一,它不仅可以提高蛋白质的功能和生物学性质,而且可以增加低商业价值的副产品的价值。此法利用蛋白酶的特异性催化蛋白质中的肽键(酯键或酰胺键)水解为小分子肽活性物质。这种特异性和水解条件(pH、温度、时间,酶添加量)影响肽链的大小、氨基酸序列以及游离氨基酸的数量,从而影响水解产物的生物活性[18]。
不同的海藻种类具有不同的生物结构,另外还有一些藻类需要特殊的保存方式,由此产生了不同的酶解方法[19]。小球藻类适合于采用单一酶或复合酶直接酶解;大型藻和单细胞藻等存在刚性细胞壁的藻类应先将原料破碎后再进行酶解;对于难以获得和保存的藻类,应先将海藻制成粉末或将其冻融后再酶解。
生物酶解一般常用的有两类酶,一是具有特定活性的蛋白酶,如胃蛋白酶、胰蛋白酶、碱性蛋白酶、中性蛋白酶、木瓜蛋白酶和复合酶等。二是不同的非特定蛋白酶,如来源于灰链霉菌的链酶蛋白酶E和来源于米曲霉的黄曲酶,目前已被用于生产更稳定和有效的生物活性肽,通过减少水解所需的反应时间使其能够获得不同的特性,尤其是肽的组成和分子质量分布。他们能够有目的的剪切肽链来获取所需要的生物活性肽,比较安全高效。除商业酶外,还有一些研究报道了利用粗酶水解蛋白质[20],这表明新的蛋白酶来源在生产海藻活性肽方面具有潜在的应用前景。不同海藻肽的酶解条件及活性举例见表1。
表1 不同海藻肽的酶解条件及活性举例
Table 1 Example of enzymatic hydrolysis conditions and acti ities of different seaweed peptides

来源类别蛋白酶种类及条件(酶底比、酶解温度、酶解时间、pH)功能活性一级序列文献棕榈红藻抗血栓木瓜蛋白酶:20.7 u/mg蛋白、60 ℃、24 h、pH 6.0具有抑制血小板活化因子乙酰水解酶(PAF-AH)的活性(IC50=2.32 mmol/L),可能与ACE-I抑制剂一起用于预防动脉粥样硬化和高血压,维持心脏健康NIGK[24]降血糖胰蛋白酶:1%质量分数、50 ℃、240 min、pH 7.0具有抑制二肽基肽酶(DPP)-I 的活性(IC50在43~159 mmol/L),可用于预防和治疗2型糖尿病ILAPLLAPMAG DHI[25]坛紫菜神经调节胃蛋白酶:0.5%质量分数、37 ℃、30 min、pH 1.2复合酶(胰蛋白酶和胰凝乳蛋白酶质量比为 1∶1):0.25%质量分数、37 ℃、30 min、pH 7.5具有抑制脯氨酰内肽酶(PEP)的活性(IC50低于45.45 mmol/L),辅助进行神经调节-[26]抗菌胃蛋白酶:1%质量分数、37 ℃、3 h、pH 1.8具有抑制金黄色葡萄球菌生长的作用,损伤金黄色葡萄球菌菌体细胞壁和细胞质膜,抑制菌体部分功能性蛋白质合成或者降解菌体部分功能性蛋白质-[27]螺旋藻抗氧化蛋白酶 SM98011:0.06%质量分数、50 ℃、5 min、pH 7.0清除羟基自由基的能力为13.42%LAHICG P[19]龙须菜降血压胰蛋白酶:4%质量分数、37 ℃、8 h、pH 8.0抑制血管紧张素转移酶(ACE)的活性(IC50=474.36 mmol/L),促进脂肪内分泌激素的表达,调节血压Q EY[28]小球藻抗肿瘤胃蛋白酶:2% 质量分数、50 ℃、15 h、pH 2.0具有较强的剂量依赖性抗增殖作用,并诱导AGS细胞G1期后细胞周期阻滞 ECYGPNRPQF[29]
发酵法是利用海藻自身的营养物质培养微生物,同时微生物在生长代谢过程中会产生蛋白酶,这些复杂的蛋白酶系使海藻蛋白水解制备生物活性肽。利用微生物发酵法有众多优点,蛋白酶来源广、繁殖快、微生物资源利用度高[21],水解度高、修饰功能基团、具备更优良的生物活性且得到的生物活性肽分子质量较小,发酵工艺简单、生产成本低、更易于产业化,并且微生物本身也会产生一定营养作用。这些优点使得微生物发酵法在食品和制药工业具有广泛的应用前景。
发酵涉及多种代谢途径,这些代谢途径负责产生代谢产物,这些代谢产物对发酵产品的化学、生化和营养特性有重要贡献。例如乳酸菌的蛋白水解系统由3个主要组成部分组成,与细胞壁结合的蛋白酶,促进蛋白最初水解为寡肽,将寡肽转移到细胞质和细胞内肽酶的特异性转运体,完成水解过程,将寡肽转化为游离氨基酸和(或)低分子肽[22]。微生物产生蛋白水解酶的能力使它们能够在发酵产品制造过程中释放出活性肽。目前在海水鱼,淡水鱼、陆生植物中均有见微生物发酵法制备生物活性肽的报道,但是用此法制备海藻抗肿瘤活性肽的研究还比较少,仅见张明洞[23]采用枯草芽孢杆菌对螺旋藻发酵,制备出具有高活性的螺旋藻肽,当含水量低于7%时,螺旋藻经发酵产生出的肽含量为15%~40%。
由于微生物发酵过程的复杂性,很多微生物的初级代谢产物或次级代谢产物均有毒或对人体有害,活性肽的安全问题和发酵制肽的作用机理也未得到完全解决。无法控制微生物代谢得到一些特殊功能的生物活性肽,此时需要根据生物活性肽的结构选择符合要求的特异性较高的酶。
化学合成法是一种高通量的制备方法,能够在短时间内合成大量的目标肽以供筛选,包括固相合成法和液相合成法。使用固相合成法制备多肽之前首先需要知道目标肽的氨基酸组成和排列方式。从C端(羧基端)向N端(氨基端)重复添加氨基酸的过程,通过连接剂与树脂上的第一氨基酸连接,待合成后切割出完整目标多肽。王竹君[30]采用固相合成法合成已知序列螺旋藻多肽,并证明了合成后多肽的抗肿瘤活性。由于目前分析纯化技术的技术的不断改进和发展,高效液相色谱技术可根据目标肽的性质从复杂的混合肽产物中分离出纯度较高的目标肽,改善了固相合成分离出目标肽杂质较多的缺点,成为目前合成肽的主要方法。成芳[31]使用高效液相色谱合成法成功合成助抗癌活性天然产hapalosin。
但是化学合成法仍然存在副反应多、肽活性低杂肽无法分离、毒性残留等缺点,缩小了生物活性肽的制备范围[21]。当前基因组学及蛋白质组学的发展为大量获得某种特定活性的肽提供了另一种有效方法,即基因重组法。此法很大程度上提高了肽的产量和纯度。但是基因重组技术对于具有营养价值的小分子肽难以合成,而且与化学合成法一样,无法合成未知氨基酸序列的肽。
研究人员针对不同敏感性的海藻抗肿瘤活性肽使用不同的癌细胞株(系)进行活性评价,这些细胞系由于不同的来源具有不同的形态和特征。常用的癌细胞株[32]包括人肝癌细胞HepG2、BEL-7402、SMMC-7721;人乳腺癌细胞株MCF-7、MDA-MB-435、SKBR-3、BT474;人胃癌细胞株SGC-7901,AGS;人肺癌细胞H-460、A549、NCI-H460、H4160;人结肠癌细胞株HT-29、Caco-2、HCT-116、C2BBel;宫颈癌细胞Hela;人卵巢癌耐长春花碱细胞(SK LB1);人前列腺癌细胞株DU145;鼠白血病细胞株L-1210;小鼠白细胞P388;小鼠BALB/C巨噬细胞RAW 264.7细胞;小鼠神经母细胞瘤细胞株神经-2A等。
对癌细胞株经不同浓度及培养时间处理后进行抗肿瘤活性的体外评价,通常使用MTT法和流式细胞术法。
3.1.1 MTT法
MTT法是基于活细胞线粒体脱氢酶活性的检测,采用3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化铵(MTT)体外微孔板法,对海藻抗肿瘤活性肽的抗增殖和细胞毒性作用进行评价[5]。MTT可被活细胞线粒体脱氢酶还原为蓝紫色甲瓒产物,以IC50为指标反映细胞存活率评价海藻抗肿瘤活性肽的抗增殖和细胞毒性作用。
3.1.2 流式细胞术法
由于细胞凋亡是DNA损伤不可修复时细胞死亡的主要类型,在最终决定癌细胞命运中起着关键作用,所以除了评价海藻抗肿瘤肽的抗增殖和细胞毒性作用外,研究人员还对细胞凋亡、坏死和细胞紊乱周期进程进行探究,以期阐明海藻抗肿瘤肽的机制[33]。细胞周期分析通常是用流式细胞术来区分细胞周期的不同阶段(G1 s S s G2/M)。流式细胞术包括PI单染法和Annexin -FITC/PI双染法。细胞被膜联蛋白 和碘化丙啶(PI)通过质膜完整性和通透性的差异来确定细胞是否存活、凋亡或坏死[5]。根据膜联蛋白 检测细胞膜外磷脂酰丝氨酸(PS)的暴露量来确定细胞凋亡的早期阶段;PI染色晚期凋亡和坏死细胞的DNA,而不染色活细胞或早期凋亡细胞的完整质膜这一特点来确定细胞凋亡的晚期阶段。RIEGER[34]等人利用细胞固定过程中细胞通透性的变化,在染色程序后期1%甲醛固定步骤后引入RNase A,促进染色后RNase A进入细胞,从而改善了传统流式细胞术实验可能存在大量假阳性事件的缺陷。
3.1.3 激酶抑制实验
激酶抑制实验也是最广泛的抗肿瘤活性肽筛选的评价方法。激酶作为人体中最丰富的酶之一,人体基因大概编码518种不同的激酶,而且在真核细胞中占据重要的地位[36]。激酶在调节细胞活动和传导细胞信号方面起着核心作用,另外在代谢、细胞生长、凋亡、免疫应答、基因表达、肿瘤发生、细胞分化和增殖、代谢、DNA损伤修复等方面具有重要作用[37]。PKA抑制剂[38]已被发现在体外和体内对多种人类肿瘤细胞株具有抗肿瘤活性,并能增强HI 感染患者的单核细胞功能。
3.1.4 其他体外评价方法
一些研究人员利用荧光显微镜和吖啶橙/溴化乙锭(AO/EB)染色法研究了海藻肽对细胞形态和细胞骨架结构的影响。细胞凋亡还具有一系列典型的形态学特征,如气泡、收缩、染色质浓缩、核碎裂和细胞分裂成膜结合的凋亡小体,可进行形态学观察[35]。凋亡相关蛋白Bax、p53、Caspase-3[33]、细胞色素c、Bcl-2的表达变化,抗凋亡蛋白(Bcl-2、caspase-9)和细胞周期调节蛋白(cyclin A、cyclin E、cyclin-dependent kinase 2(cdk2)、p21和p27)也可用来阐明海藻抗癌活性,通常采用酶联免疫分析。
除上述体外评价以外,还利用具有显著阳性结果的动物模型对海藻抗肿瘤活性肽进行体内评价。体内评价常以荷瘤小鼠为动物模型,小鼠通过皮下接种肿瘤细胞,建立肿瘤体内评价模型[39]。接种24 h后,每天灌胃或注射海藻肽,根据癌细胞类型确定接种传代时间、接种方式和位置。实验结束后处死小鼠,切除肿瘤块并取胸腺、脾脏、肝脏等器官,计算各器官指数,测量肿瘤大小、倍增时间和抑瘤率等。之后用印迹法制片,在显微镜下观察。
海藻抗肿瘤活性肽的活性大小主要取决于其结构特征,如氨基酸组成、序列、长度、总电荷/疏水性等。其中存在的氨基酸主要是缬氨酸、亮氨酸、脯氨酸、丙氨酸等疏水性氨基酸和一个或多个残基赖氨酸。疏水性氨基酸对肿瘤细胞具有选择性和较强的细胞毒性,能增强抗肿瘤肽与肿瘤细胞膜双层外叶的相互作用,所以含有较多疏水性氨基酸的低分子质量多肽也具有较高的抗肿瘤活性;带电(谷氨酸)和杂环氨基酸(脯氨酸)有助于多肽的抗肿瘤特性;肽中正电荷的强度和分子质量的差异可能与细胞毒活性呈正相关。不同海藻来源的抗肿瘤活性肽举例见表2。
直接抑制肿瘤细胞增殖,干扰肿瘤细胞的表达。此为大多数海藻抗肿瘤肽的机制。王竹君等[30]通过对螺旋藻进行酶解,得到9种抗肿瘤肽对肝癌和乳腺癌细胞均具有显著的抑制增殖的活性作用。CHUAN等[29]对绿藻蛋白残渣提取出的肽algae protein waste peptide (APWP)采用流式细胞术法发现此肽能诱导胃癌细胞系AGC死亡并且有明显抑制AGC生长的作用,暴露在APWP下的24 h后,G1期的胃癌细胞减少,亚G1峰出现时间依赖性增加。肽组分在G1期后阻滞了细胞,亚G1期细胞的数量在肽组分给药后24~48 h逐渐增加。
一些抗肿瘤肽是通过直接清除诱导DAN损伤和癌细胞变化的自由基作用的,这种抗肿瘤肽往往也同时具有一定的抗氧化活性[40]。曾巧辉以螺旋藻为原料制备出的多肽组分1、3和4号具有良好的抗氧化活性,同时对胃癌和结肠癌也有比较好的抑制效果。
通过刺激免疫系统,增加免疫系统的干预间接调节肿瘤的发展。在抗肿瘤过程中运用人体本身的调节器官进行干预,促进天然免疫应答。陈美珍等[41]建立H22荷瘤小鼠体外抗肿瘤模型,探讨了龙须菜藻红蛋白抗肿瘤作用与免疫作用之间的关系,发现藻红蛋白能够促进机体的细胞免疫活性和活化免疫细胞,这些免疫细胞同时对肿瘤细胞具有显著杀伤作用。
通过对肿瘤细胞骨架的破坏或改变肿瘤细胞膜的通透性诱导肿瘤细胞凋亡。LUKE等[16]证实鞘丝藻中制备出的环状和线性肽具有抗肿瘤效果,进行肌动蛋白微丝断裂试验后发现,在52 nmol/L时这2种肽均导致了丝状肌动蛋白完全丧失,由于在此浓度下的细胞形态的改变往往会伴随着微丝网络的完全破坏,从而证明此肽是通过细胞微丝网络的破坏,对HCT-116人结肠癌细胞系的IC50=20 nmol/L显示出有效和选择性的抗实体肿瘤活性。
通过对肿瘤细胞内关键细胞器的破坏诱导细胞坏死,SUAREZ等[8]发现,从羽藻中制备的Kahalalide F(KF)对人前列腺癌和乳腺癌细胞有强烈的毒性作用,并且在此肽的作用下这2种癌细胞细胞结构受到严重影响,线粒体、内质网或溶酶体等关键细胞器的完整性受到严重损害。相比之下,核结构得到了保留,染色质和DNA降解没有发生剧烈的变化。说明KF可能在一定程度上诱导线粒体自噬,从而导致坏死细胞死亡。
海藻抗肿瘤肽激活Caspase-3蛋白酶也可诱导肿瘤细胞凋亡[42]。Caspase-3是Caspase家族蛋白酶中的一种肿瘤细胞凋亡的效应者,由Caspase-3介导的特异性蛋白剪切是肿瘤细胞凋亡过程中的重要作用机制,通过激活Caspase-3酶使活化后的Caspase-3酶作用于底物上导致细胞凋亡,并且产生细胞形态学上的改变:染色质固缩,DNA片段化和细胞气泡。
表2 不同海藻来源的抗肿瘤活性肽举例
Table 2 Example of antitumor acti e peptide from different seaweed
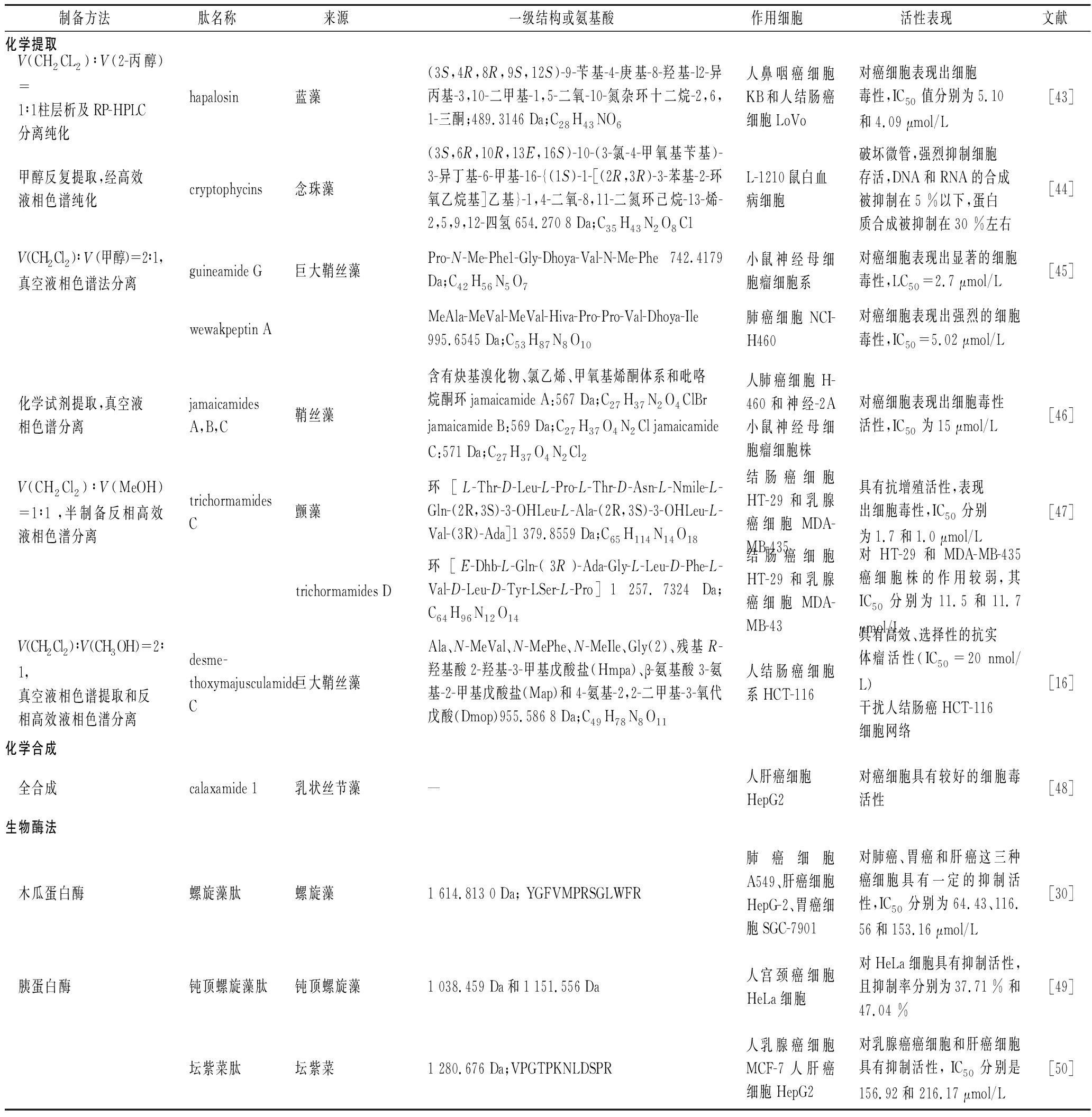
制备方法肽名称来源一级结构或氨基酸作用细胞活性表现文献化学提取 (CH2CL2)∶ (2-丙醇)=1∶1柱层析及RP-HPLC分离纯化hapalosin蓝藻(3S,4R,8R,9S,12S)-9-苄基-4-庚基-8-羟基-l2-异丙基-3,10-二甲基-1,5-二氧-10-氮杂环十二烷-2,6,1-三酮;489.3146 Da;C28H43NO6人鼻咽癌细胞KB和人结肠癌细胞Lo o对癌细胞表现出细胞毒性,IC50值分别为5.10和4.09 μmol/L[43]甲醇反复提取,经高效液相色谱纯化cryptophycins念珠藻(3S,6R,10R,13E,16S)-10-(3-氯-4-甲氧基苄基)-3-异丁基-6-甲基-16-{(1S)-1-[(2R,3R)-3-苯基-2-环氧乙烷基]乙基}-1,4-二氧-8,11-二氮环己烷-13-烯-2,5,9,12-四氢654.270 8 Da;C35H43N2O8C1L-1210鼠白血病细胞破坏微管,强烈抑制细胞存活,DNA和RNA的合成被抑制在5 %以下,蛋白质合成被抑制在30 %左右[44] (CH2Cl2)∶ (甲醇)=2∶1,真空液相色谱法分离guineamide G巨大鞘丝藻Pro-N-Me-Phe1-Gly-Dhoya- al-N-Me-Phe 742.4179 Da;C42H56N5O7小鼠神经母细胞瘤细胞系对癌细胞表现出显著的细胞毒性,LC50=2.7 μmol/L[45]wewakpeptin AMeAla-Me al-Me al-Hi a-Pro-Pro- al-Dhoya-Ile 995.6545 Da;C53H87N8O10肺癌细胞NCI-H460对癌细胞表现出强烈的细胞毒性,IC50=5.02 μmol/L化学试剂提取,真空液相色谱分离jamaicamides A,B,C鞘丝藻含有炔基溴化物、氯乙烯、甲氧基烯酮体系和吡咯烷酮环jamaicamide A:567 Da;C27H37N2O4ClBr jamaicamide B:569 Da;C27H37O4N2Cl jamaicamide C:571 Da;C27H37O4N2Cl2人肺癌细胞H-460和神经-2A小鼠神经母细胞瘤细胞株对癌细胞表现出细胞毒性活性,IC50为15 μmol/L[46] (CH2Cl2)∶ (MeOH)=1∶1 ,半制备反相高效液相色潽分离trichormamides C颤藻环[L-Thr-D-Leu-L-Pro-L-Thr-D-Asn-L-Nmile-L-Gln-(2R,3S)-3-OHLeu-L-Ala-(2R,3S)-3-OHLeu-L- al-(3R)-Ada]1 379.8559 Da;C65H114N14O18结肠癌细胞HT-29和乳腺癌细胞MDA-MB-435具有抗增殖活性,表现出细胞毒性,IC50分别为1.7 和1.0 μmol/L[47]trichormamides D环[E-Dhb-L-Gln-(3R)-Ada-Gly-L-Leu-D-Phe-L- al-D-Leu-D-Tyr-LSer-L-Pro]1 257.7324 Da;C64H96N12O14结肠癌细胞HT-29和乳腺癌细胞MDA-MB-43对HT-29和MDA-MB-435癌细胞株的作用较弱,其IC50分别为11.5和11.7 μmol/L (CH2Cl2)∶ (CH3OH)=2∶1,真空液相色谱提取和反相高效液相色潽分离desme-thoxymajusculamide C巨大鞘丝藻Ala、N-Me al、N-MePhe、N-MeIle、Gly(2)、残基R-羟基酸2-羟基-3-甲基戊酸盐(Hmpa)、β-氨基酸3-氨基-2-甲基戊酸盐(Map)和4-氨基-2,2-二甲基-3-氧代戊酸(Dmop)955.586 8 Da;C49H78N8O11人结肠癌细胞系HCT-116具有高效、选择性的抗实体瘤活性(IC50=20 nmol/L)干扰人结肠癌HCT-116细胞网络[16]化学合成全合成calaxamide 1乳状丝节藻—人肝癌细胞HepG2对癌细胞具有较好的细胞毒活性[48]生物酶法木瓜蛋白酶螺旋藻肽螺旋藻1 614.813 0 Da; YGF MPRSGLWFR肺癌细胞A549、肝癌细胞HepG-2、胃癌细胞SGC-7901对肺癌、胃癌和肝癌这三种癌细胞具有一定的抑制活性,IC50分别为64.43、116.56和153.16 μmol/L[30]胰蛋白酶钝顶螺旋藻肽钝顶螺旋藻1 038.459 Da和1 151.556 Da人宫颈癌细胞HeLa 细胞对HeLa 细胞具有抑制活性,且抑制率分别为37.71 % 和47.04 %[49]坛紫菜肽坛紫菜1 280.676 Da; PGTPKNLDSPR人乳腺癌细胞MCF-7人肝癌细胞HepG2对乳腺癌癌细胞和肝癌细胞具有抑制活性, IC50分别是156.92和 216.17 μmol/L[50]
目前关于海藻抗肿瘤活性肽的作用机制还存在一定的缺陷,仅仅通过细胞实验在诱导癌细胞凋亡和坏死的各种途径方面进行讨论和探究,较少探讨它们对肿瘤细胞生成机制的影响,例如肿瘤细胞DNA、RNA的合成和主要器官蛋白质的合成。如果能够在海藻抗肿瘤肽介导免疫和抗血管生成活性等方面做出更全面的研究,对今后的海藻抗肿瘤活性肽作用机制的系统化也会有更大价值。
海藻肽因有多种对人体健康有益处的生物功能活性而被众多学者广泛研究,其中抗肿瘤功能日益受到重视。我国作为海藻资源丰富的国家,充分利用海藻这一生物活性肽的来源也具有一定社会和经济价值。目前研究已经对海藻抗肿瘤活性肽的评价方法和作用机制进行了广泛的基础性研究,但仍存在着一些局限性。(1)大型海藻抗肿瘤活性肽并未得到全面的研究,需要进一步加深大型海藻肽抗肿瘤功能的研究,改善大型海藻肽的制备工艺,例如制备金属螯合海藻活性肽等。确定海藻活性肽的氨基酸序列及分子结构,提高其抗肿瘤活性。(2)海藻抗肿瘤活性肽虽有进行活性作用机制的研究,但绝大多数局限于细胞水平,通常只是在体外显示了对肿瘤细胞生长具有抑制作用,对于体内模型的抗肿瘤活性并未有足够的实验证明,缺乏安全性、毒理学评估、生物利用率的利用等。(3)关于海藻抗肿瘤活性肽的分子机制也十分有限,大多数研究集中在细胞凋亡和坏死的机制上,而还要加深许多其他方面需要研究才能完全阐明其作用方式与途径,进行膜受体、介导免疫和抗血管生成活性等探究。(4)大多数海藻抗肿瘤活性肽的研究中并未提及肽的保存问题,这对于化学性质不太稳定的肽十分不利。运用当前活性肽保存工艺和运载工艺的发展,包括壳聚糖纳米粒子的包裹和多囊脂质体靶向运载等方法,提高海藻抗肿瘤活性肽的稳定性。未来还需提高海藻肽对肿瘤细胞的靶向治疗能力,以期从天然海藻中获得的肽尽可能被运用到抗肿瘤药品和食品工业当中。
[1] 乔雪,王义鹏,于海宁.抗癌肽的作用机制研究进展[J].生物工程学报,2019,35(8):1 391-1 400.
[2] 李宁,石爱民,刘红芝,等.生物活性肽抗癌活性及其作用机制研究进展[J].中国食品学报,2019,19(11):261-269.
[3] 李克,陈克敏.序言[J]. 中国医学计算机成像杂志,2019,25(5):425-426.
[4] DE CASTRO R J S,SATO,HELIA H. Biologically acti e peptides:Processes for their generation,purification and identification and applications as natural additi es in the food and pharmaceutical industries[J].Food Research International,2015,74:185-198.
[5] KALPA S,JEON Y J.Bio-functionalities of proteins deri ed from marine algae-A re iew[J].Food Research International,2012,48(2):948-960.
[6] CHALAMAIAH M,YU W L,WU J P.Immunomodulatory and anticancer protein hydrolysates (peptides) from food proteins:A re iew[J].Food Chemistry,2018,245:205-222.
[7] 梁艳,吴晓琴,张英.植物肽的化学和生物活性研究进展[J].中国中药杂志,2006(9):709-714.
[8] SUAREZ Y,GONZALEZ L,CUADRADO A,et al.Kahalalide F,a new marine-deri ed compound,induces oncosis in human prostate and breast cancer cells[J].Molecular cancer therapeutics,2003,2(9):863-872.
[9] 陈志华,吴文惠,王幸,等.海藻肽的化学结构特征和活性作用研究进展[J].氨基酸和生物资源,2010,32(2):66-69;79.
[10] HAN B,GOEGER D,MAIER C S,et al.The wewakpeptins,cyclic depsipeptides from a papua new guinea collection of the marine cyanobacterium Lyngbya semipena[J].The Journal of Organic Chemistry,2005,70(8):3 133-3 139.
[11] MUNUSAMY S,CONDE R,BERTRAND B,et al.Biophysical approaches for exploring lipopeptide-lipid interactions[J].Biochimie,2020,170:173-202.
[12] EDWARDS D J,MARQUEZ B L,NOGLE L M,et al.Structure and biosynthesis of the jamaicamides,new mixed polyketide-peptide neurotoxins from the marine cyanobacterium Lyngbya majuscula[J].Chemistry & Biology (Cambridge),2004,11(6):817-833.
[13] LUO S,KANG H S,KRUNIC A,et al.Trichormamides C and D,antiproliferati e cyclic lipopeptides from the cultured freshwater Cyanobacterium cf.Oscillatoria sp.UIC 10045[J].Bioorganic & Medicinal Chemistry,2015,23(13):3 153-3 162.
[14] 孙杰,缪静,朱路英,等.烟台沿海4种常见海藻的氨基酸分析及营养评价[J].安徽农业科学,2008,36(8):3 081-3 082.
[15] NARA T,KAMEI Y,TSUBOUCHI A,et al.Inhibitory action of marine algae extracts on the Trypanosoma cruzi dihydroorotate dehydrogenase acti ity and on the protozoan growth in mammalian cells[J].Parasitology International,2005,54(1):59-64.
[16] SIMMONS T L,NOGLE L M,MEDIA J,et al.Desmethoxymajusculamide C,a cyanobacterial depsipeptide with potent cytotoxicity in both cyclic and ring-opened forms[J].Journal of Natural Products,2009,72(6):1 011-1 016.
[17] HAMANN M T,SCHEUER P J.Kahalalide F:A bioacti e depsipeptide from the sacoglossan mollusk Elysia rufescens and the green alga Bryopsis sp.[J].Journal of the American Chemical Society,1993,115(13):5 825-5 826.
[18] DE CASTRO S,JANSER R, HELIA H,et al.Biologically acti e peptides:Processes for their generation,purification and identification and applications as natural additi es in the food and pharmaceutical industries[J].Food Research International,2015,74:185-198.
[19] 谢倩.螺旋藻的酶解利用研究[D].济南:山东师范大学,2011.
[20] HARNEDY P A,OKEEFFE M B,FITZGERALD R J,et al.Fractionation and identification of antioxidant peptides from an enzymatically hydrolysed Palmaria palmata protein isolate[J].Food Research International,2017,100(1):416-422.
[21] 陈丽娜,温宇旗,韩国庆,等.生物活性肽制备工艺的研究进展[J].农产品加工,2018(17):57-62.
[22] MOHANTY D P,MOHAPATRA S,MISRA S,et al.Milk deri ed bioacti e peptides and their impact on human health-A re iew[J] Saudi J Biol Sci,2016,23(5):577-583.
[23] 张明洞.用螺旋藻制备蛋白激酶、活性肽及蛋白酶的方法:中国,CN200810099924.6[P].2008-09-17.
[24] FITZGERALD C,GALLAGHER E,OCONNOR P M,et al.De elopment of a seaweed deri ed platelet acti ating factor acetylhydrolase (PAF-AH) inhibitory hydrolysate,synthesis of inhibitory peptides and assessment of their toxicity using the Zebrafish lar ae assay[J].Peptides,2013,50:119-124.
[25] HARNEDY P A,OKEEFFE M B,FITZGERALD R J,et al.Purification and identification of dipeptidyl peptidase (DPP) I inhibitory peptides from the macroalga Palmaria palmata[J].Food Chemistry,2015,172:400-406.
[26] 谢雪琼,钟婵,孙乐常,等.利用坛紫菜藻红蛋白制备脯氨酰内肽酶抑制肽[J].食品科学,2019,40(14):123-129.
[27] 刘蕾.坛紫菜(Porphyra haitanensis)中抑菌活性多肽的分离、初步纯化及其作用机理研究[D].青岛:青岛大学,2011.
[28] CAO D Q,L X J,XU X T,et al.Purifcation and identifcation of a no el ACE inhibitory peptide from marine alga Gracilariopsis lemaneiformis protein hydrolysate[J].Eur Food Res Technol,2017,243:1 829-1 837.
[29] SHEIH I,FANG T J,WU T,et al.Anticancer and antioxidant acti ities of the peptide fraction from algae protein waste[J].Journal of Agricultural and Food Chemistry,2010,58(2):1 202-1 207.
[30] 王竹君.螺旋藻抗肿瘤肽的分离及其活性研究[D].广州:华南理工大学,2015.
[31] 成芳.助抗癌活性天然产物Hapalosin类似物库组合构建过程的高效液相色谱分析[D].厦门:厦门大学,2007.
[32] MERAM C,YU W,WU J.Immunomodulatory and anticancer protein hydrolysates (peptides) from food proteins:A re iew[J].Food Chemistry,2018,245:205-222.
[33] OUYANG L,SHI Z,ZHAO S,et al.Programmed cell death pathways in cancer:A re iew of apoptosis,autophagy and programmed necrosis[J].Cell Proliferation,2012,45(6):487-498.
[34] RIEGER A M,NELSON K L,KONOWALCHUK J D,et al.Modified annexin /propidium iodide apoptosis assay for accurate assessment of cell death[J].Journal of isualized Experiments,2011(50):40-40.
[35] 黄蓓.藻胆蛋白色素肽作为光敏剂抗肿瘤作用及其机理的研究[D].合肥:中国科学技术大学,2002.
[36] MANNING G,WHYTE D,MARTINEZ R,et al.The protein kinase complement of the human genome[J]. Science,2002,298(5 600):1 912-1 934.
[37] MCCAULEY J,ZI ANO IC A,SKROPETA D.Bioassays for anticancer acti ities[J].Methods in Molecular Biology (Clifton,N.J.),2013,1 055:191-205.
[38] WANG Z,LI X,SHANG K,et al.T-18,a stemonamide synthetic intermediate inhibits Pim kinase acti ity and induces cell apoptosis,acting as a potent anticancer drug[J].Oncology Reports,2013,29(3):1 245-1 251.
[39] 徐本杰.龙须菜藻红蛋白抗肿瘤作用及其机制的研究[D].汕头:汕头大学,2008.
[40] 曾巧辉.螺旋藻蛋白源生物活性肽的制备及其抗皮肤光老化机理研究[D].广州:华南理工大学,2016.
[41] 陈美珍,杜虹,徐本杰.龙须菜藻红蛋白对H_(22)荷瘤小鼠免疫功能的影响[J].中草药,2010,41(8):1 329-1 332.
[42] 杨滢滢.藻蓝蛋白的分离纯化、酶解及其抗肿瘤活性研究[D].天津:天津商业大学,2009.
[43] STRANTMANN K,BURGOYNE D L,MOORE R E,et al.Hapalosin,a cyanobacterial cyclic depsipeptide with multidrug-resistance re ersing acti ity[J].Journal of Organic Chemistry,1994,59(24):7 219-7 226.
[44] FOSTER B J,FORTUNA M,MEDIA J,et al.Cryptophycin 1 cellular le els and effects in itro using L1210 cells[J].In estigational New Drugs,1998,16(3):199-204.
[45] HAN B,GROSS H,MCPHAIL K L,et al.Wewakamide A and guineamide G,cyclic depsipeptides from the marine cyanobacteria Lyngbya semiplena and Lyngbya majuscula[J].Journal of Microbiology & Biotechnology,2011,21(9):930.
[46] EDWARDS D J,MARQUEZ B L,NOGLE L M,et al.Structure and biosynthesis of the jamaicamides,new mixed polyketide-peptide neurotoxins from the marine cyanobacterium Lyngbya majuscula[J].Chemistry & Biology (Cambridge),2004,11(6):817-833.
[47] LUO S,KANG H S,KRUNIC A,et al.Trichormamides C and D,antiproliferati e cyclic lipopeptides from the cultured freshwater cyanobacterium cf.Oscillatoria sp.UIC 10045[J].Bioorganic & Medicinal Chemistry,2015,23(13):3 153-3 162.
[48] 白德发,廖小建,邱少玲,等.海藻中抗肿瘤活性环肽分离、结构修饰及活性[C].全国第二届海洋与陆地多糖多肽及天然创新药物研发学术会议论文集.漠河:中国生物化学与分子生物学会,中国微生物学会,中华航海医学会,上海市药学会,2015:210-210.
[49] 王雪青,范敏,杨春艳,等.螺旋藻藻蓝蛋白与其酶解物的生物学功能研究[J].食品科学,2008,29(10):433-435.
[50] 白露.坛紫菜多肽的分离纯化及其抗肿瘤活性研究[D].广州:华南理工大学,2016.