表1 实验分组及剂量(45 d)
Table 1 Experimental grouping and dosage(45 d)

组别菌落总数/(CFU·mL-1)动物数量/只灌胃剂量/mL生理盐水0.00360.2MN-002菌粉组1.00×109360.2MN-002发酵乳组1.00×109360.2
注:本实验益生菌按人体剂量的10倍对小鼠进行灌胃
疲劳综合症的症状常包括短期记忆障碍,睡眠障碍和肌肉骨骼疼痛等,严重影响人们的身心健康[1]。随着社会的快速发展,人们生活节奏也逐渐加快,长期生活压力导致人们陷入疲劳,若无法消除或缓解,会造成症状加重甚至诱发其他疾病[2-3]。因此,缓解和抵抗疲劳已经成为困扰现代人的一个热点问题。
目前关于嗜热链球菌多糖的生物活性研究较多,嗜热链球菌衍生的胞外多糖(exopolysaccharides,EPS)具有潜在的抗肿瘤、抗溃疡、免疫调节和降低胆固醇的特性,有助于人类健康[4-5]。但关于嗜热链球菌缓解体力疲劳方面的研究不多,且未见其发酵乳缓解体力疲劳功效的报道。
嗜热链球菌MN-002分离于传统发酵的中国乳制品,具有高产EPS的能力[6]。MN-002菌粉和发酵乳均有提高小鼠非特异性免疫和特异性免疫功效[7],但对于缓解疲劳方面没有进行过探索。因此,本试验以嗜热链球菌MN-002发酵乳和菌粉作为研究对象,通过小鼠运动模型,研究嗜热链球菌MN-002缓解体力疲劳的作用,以期为益生菌资源和相关产品的开发应用提供科学依据。
1.1.1 实验菌种
嗜热链球菌MN-001、MN-002、MN-006、MN-007、MN-009和MN-012,均来源于蒙牛乳业集团研发中心菌种保藏库。
1.1.2 实验动物
实验动物为SPF级昆明小鼠,雄性,平均体重为(20±2) g,共108只,随机分为对照组、发酵乳组、菌粉组3组饲喂,购于内蒙古大学实验动物研究中心。
1.2.1 发酵乳的制备
MN-002菌株在12%(质量分数)脱脂乳培养基中活化3代,以2%接菌量接种于12%脱脂乳,于37 ℃发酵18 h,4 ℃冷却6~8 h后,在M17固体培养基培养48 h并检测发酵乳中菌落总数,利用0.01 mol/L、pH 7.4的磷酸盐缓冲液(phosphate buffer solution,PBS)调整其菌数为1.0×109 CFU/mL,按用量分装4 ℃保存备用。
1.2.2 MN-002菌粉的预处理
将MN-002菌粉在M17固体培养基培养48 h并检测发酵剂活菌数,利用0.01 mol/L、pH 7.4的PBS调整其菌数为1.0×109 CFU/mL,按用量分装4 ℃保存备用。
1.2.3 产胞外多糖菌株能力检测
参照王凡等[8]的实验方法,以葡萄糖为标准溶液,葡萄糖质量浓度(μg/mL)X为横坐标,吸光度Y为纵坐标绘制标准曲线。采用苯酚-硫酸法测定多糖含量。
1.2.4 MN-002抗疲劳功能评价
实验动物适应性饲养7 d、待体重均达(20±2) g后将小鼠随机分为3组,分组饲喂,自由饮水,自由采食。受试组小鼠每日1次灌胃,对照组以同样的方法给予生理盐水,连续45 d,如表1所示。
表1 实验分组及剂量(45 d)
Table 1 Experimental grouping and dosage(45 d)

组别菌落总数/(CFU·mL-1)动物数量/只灌胃剂量/mL生理盐水0.00360.2MN-002菌粉组1.00×109360.2MN-002发酵乳组1.00×109360.2
注:本实验益生菌按人体剂量的10倍对小鼠进行灌胃
本研究通过使小鼠进行负重游泳判断小鼠运动耐力的变化,并通过检测小鼠血清尿素、肝糖原、血乳酸3项指标对MN-002缓解小鼠疲劳的功效进行评估。
1.2.4.1 负重游泳实验
参考LIU等[9]的实验方法进行小鼠负重游泳实验,记录小鼠自由泳开始至死亡的时间。受试样品组负重游泳时间显著长于对照组(P<0.05),表明可有效缓解小鼠体疲劳,标记结果呈阳性(+)。
1.2.4.2 血清尿素氮的含量测定
参考WYBENGA等[10]检测血清尿素氮的实验方法。受试样品血清尿素含量显著低于对照组(P<0.05),表明可有效调节血清尿素氮含量,标记结果呈阳性(+)。
1.2.4.3 肝糖原
末次给予受试样品30 min后,处死小鼠,取肝脏。用蒽酮法试剂盒检测肝糖原[11]。受试样品组肝糖原含量显著高于对照组(P<0.05),表明可有效缓解肝糖原消耗,标记结果呈阳性(+)。
1.2.4.4 血乳酸
末次给予受试样品30 min后,在30 ℃水中不负重游泳10 min。采3次血:第1次,游泳前采;第2次,游泳10 min后;第3次,休息20 min后。用乳酸试剂盒检测血乳酸。计算3个时间点血乳酸曲线下面积。受试样品组曲线下面积显著小于对照组(P<0.05),表明可有效缓解血乳酸产生,标记结果呈阳性(+)[12]。
缓解疲劳功效判定:负重游泳结果显示阳性(+),且血乳酸、血清尿素氮、肝糖原3项中任意2项显示阳性(+),可判定嗜热链球菌MN-002具有缓解体力疲劳功能。
试验结果采用SPSS 23统计软件进行处理,采用单因素方差分析进行多组间差异比较,采用t检验进行两两比较,以P<0.05为具有统计学意义,实验数据均以x±s表示。
2.1.1 标准曲线
由图1可获得葡萄糖标准曲线方程为y=0.008 1x+0.004 3,R2=0.999 2。
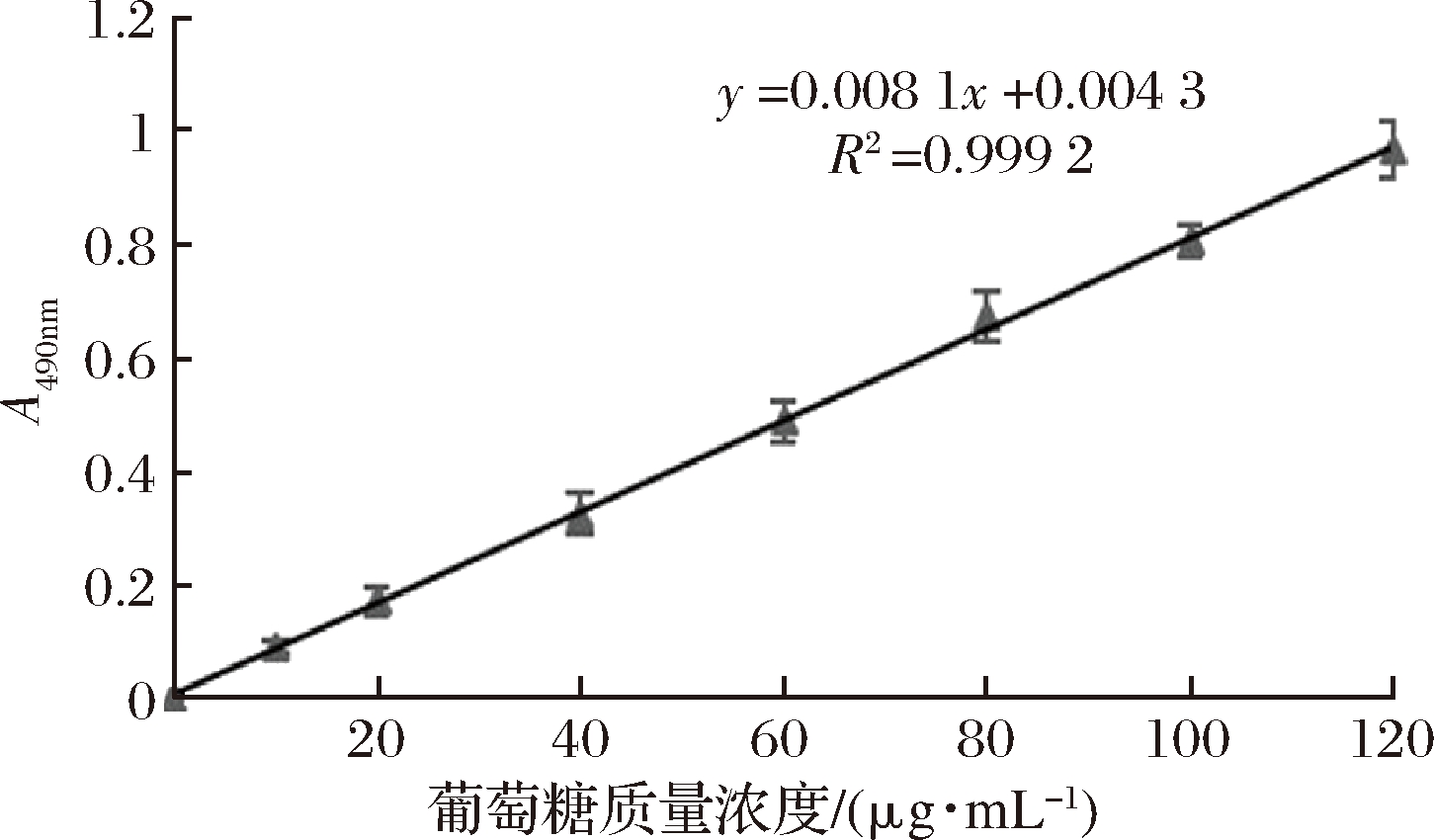
图1 葡萄糖标准曲线
Fig.1 Standard curve of glucose
2.1.2 菌株产胞外多糖检测
如表2所示,6株菌的胞外多糖产量均达到90 mg/L,其中,嗜热链球菌MN-002具有最强的产胞外多糖能力,其发酵液中EPS的含量达到了(495.72±15.86) μg/mL,约是其他菌株产量的5倍。
表2 菌株的EPS产量 单位:μg/mL
Table 2 EPS yield of strains

菌株编号 胞外多糖产量MN-00197.40±1.91cMN-002495.72±15.86aMN-00697.56±5.98cMN-007107.89±4.43bMN-00999.68±3.71bcMN-012118.56±5.06b
注:表中不同小写字母表示差异显著
由表3和图2可知。3组小鼠的体重在饲喂期间不断升高,45 d均增重约20 g,且3组间各时间点的体重都没有显著性差异,上升趋势几乎一致,结果表明,发酵乳和菌粉安全无毒,而且无其他增肥等不良效果。
表3 小鼠体重记录表 单位:g
Table 3 The weight of mouse
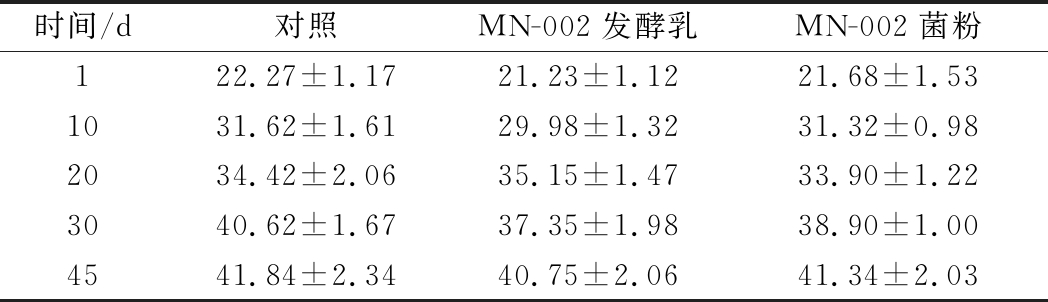
时间/d对照MN-002发酵乳MN-002菌粉122.27±1.1721.23±1.1221.68±1.531031.62±1.6129.98±1.3231.32±0.982034.42±2.0635.15±1.4733.90±1.223040.62±1.6737.35±1.9838.90±1.004541.84±2.3440.75±2.0641.34±2.03
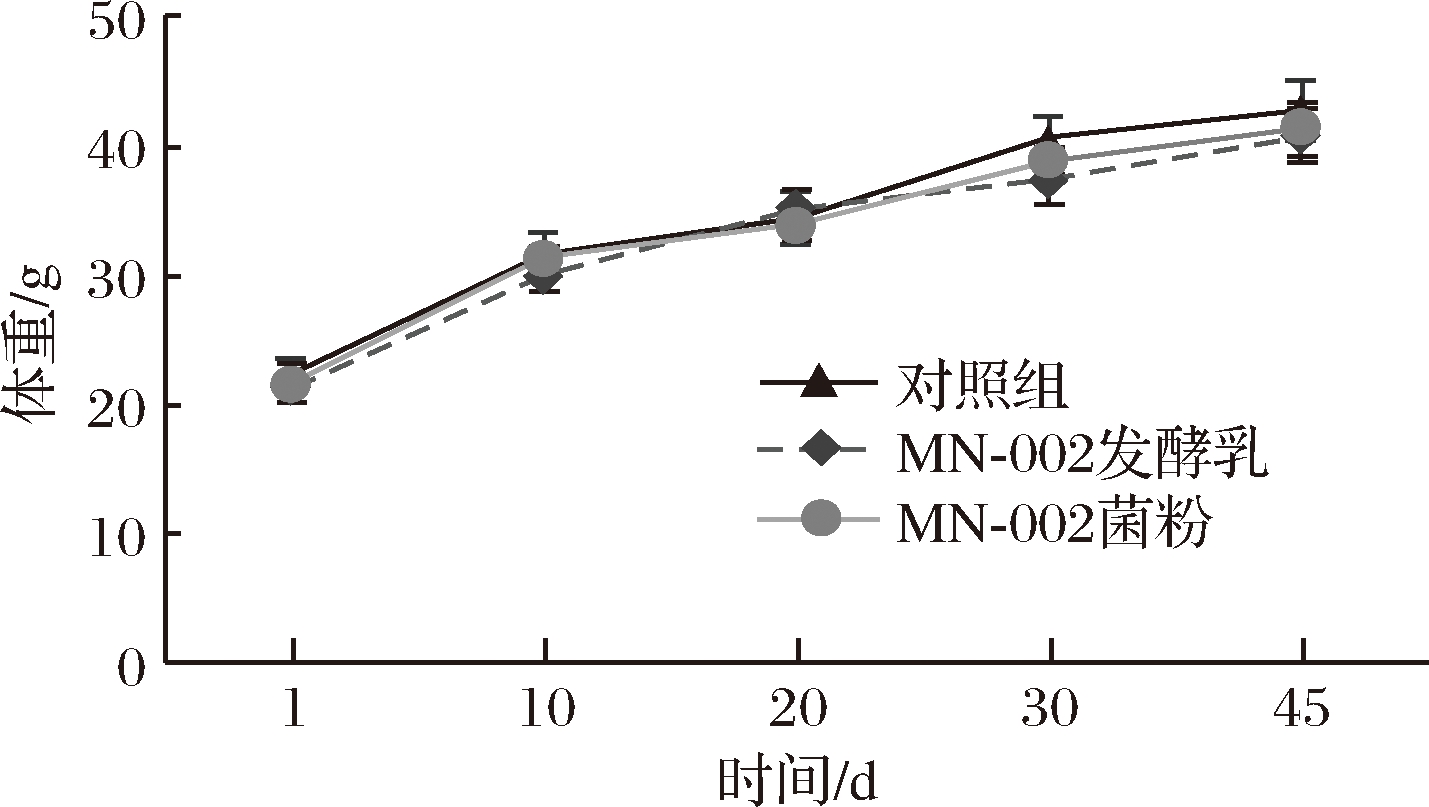
图2 饲喂期间小鼠体重变化曲线(N=12)
Fig.2 Weight curve of mouse during feeding(N=12)
对运动耐力的调节作用是缓解疲劳能力加强的直接表现,游泳时间直接反映了小鼠的疲劳程度。由图3可知,MN-002发酵乳和MN-002菌粉实验组小鼠负重游泳时间均显著长于对照组(P<0.05),比对照组分别延长了1.08 min和2.95 min;同时菌粉组小鼠负重游泳时间显著长于发酵乳组(P<0.05)。发酵乳组和菌粉组负重游泳实验均显示为阳性,而且菌粉组要比发酵组具备更优的抗疲劳能力。
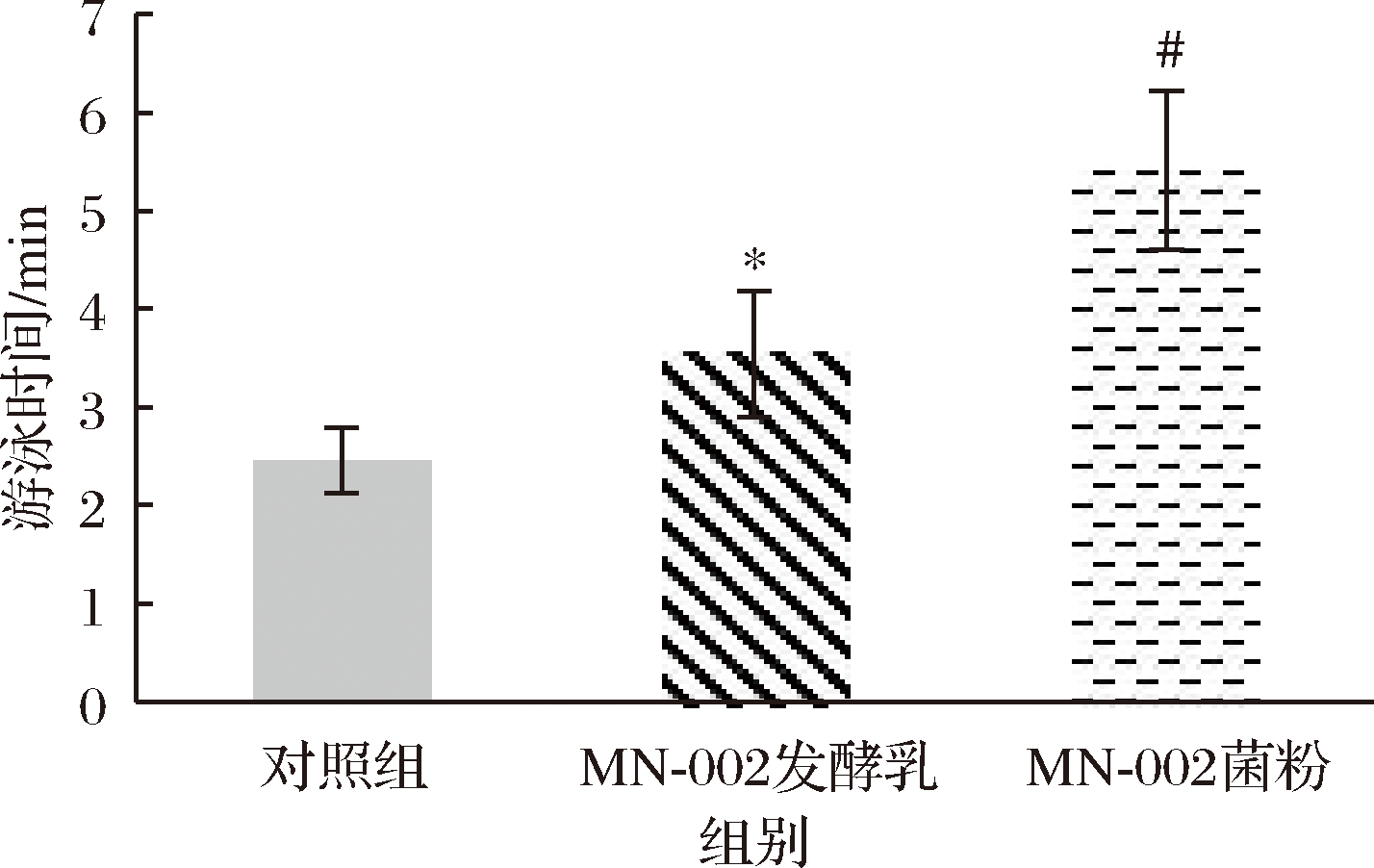
图3 小鼠游泳时间变化
Fig.3 Swimming time of mouse
注:N=12;*代表本组与对照组相比有显著差异(P<0.05);#代表本组分别与对照组、MN-002发酵乳组相比有显著差异(P<0.05)(下同)
由图4可知,发酵乳实验组和菌粉实验组肝糖原含量显著高于对照组(P<0.05),分别有59.9%和88.0%的增量;此外,菌粉组肝糖原含量比发酵乳组显著高出17.5%(P<0.05)。发酵乳组和菌粉组肝糖原实验均显示阳性,但菌粉抗疲劳效果略优于发酵乳。

图4 肝糖原含量变化
Fig.4 Hepatic glycogen content changes
图5结果显示MN-002发酵乳和菌粉组小鼠的血清尿素氮均显著低于对照组(P<0.05),分别比对照组降低了25.4%和15.6%;而且发酵乳组与菌粉组的血清尿素氮含量水平并没有显著差异(P>0.05)。该结果表明,发酵乳组和菌粉组血清尿素氮实验结果均显示为阳性,且发酵乳和菌粉调节血清尿素含量的效果相近。
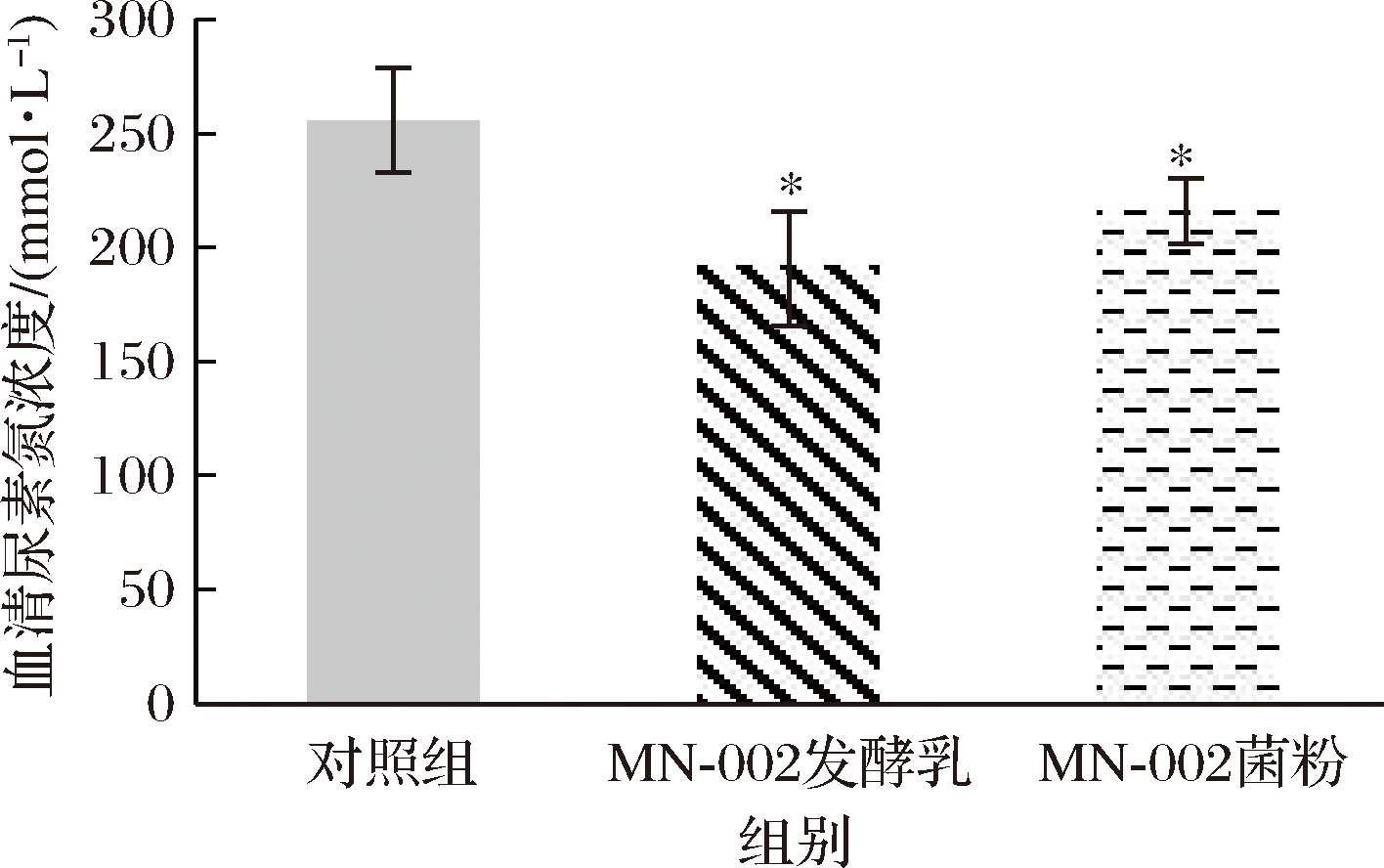
图5 血清中尿素含量变化
Fig.5 Changes in serum urea content
注:N=12;*表示本组与对照相比差异显著(P<0.05)(下同)
由图6可知,发酵乳实验组血乳酸曲线下面积显著降低了7.2%(P<0.05);菌粉实验组血乳酸曲线面积与对照组相比也显著降低(P<0.05)。菌粉和发酵乳显著降低血乳酸含量。
综上,得出判定结果如表4所示,MN-002菌粉和发酵乳组负重实验及3项辅助生化指标均显著变化,因此,MN-002菌粉和发酵乳的抗疲劳结果均判定为阳性。
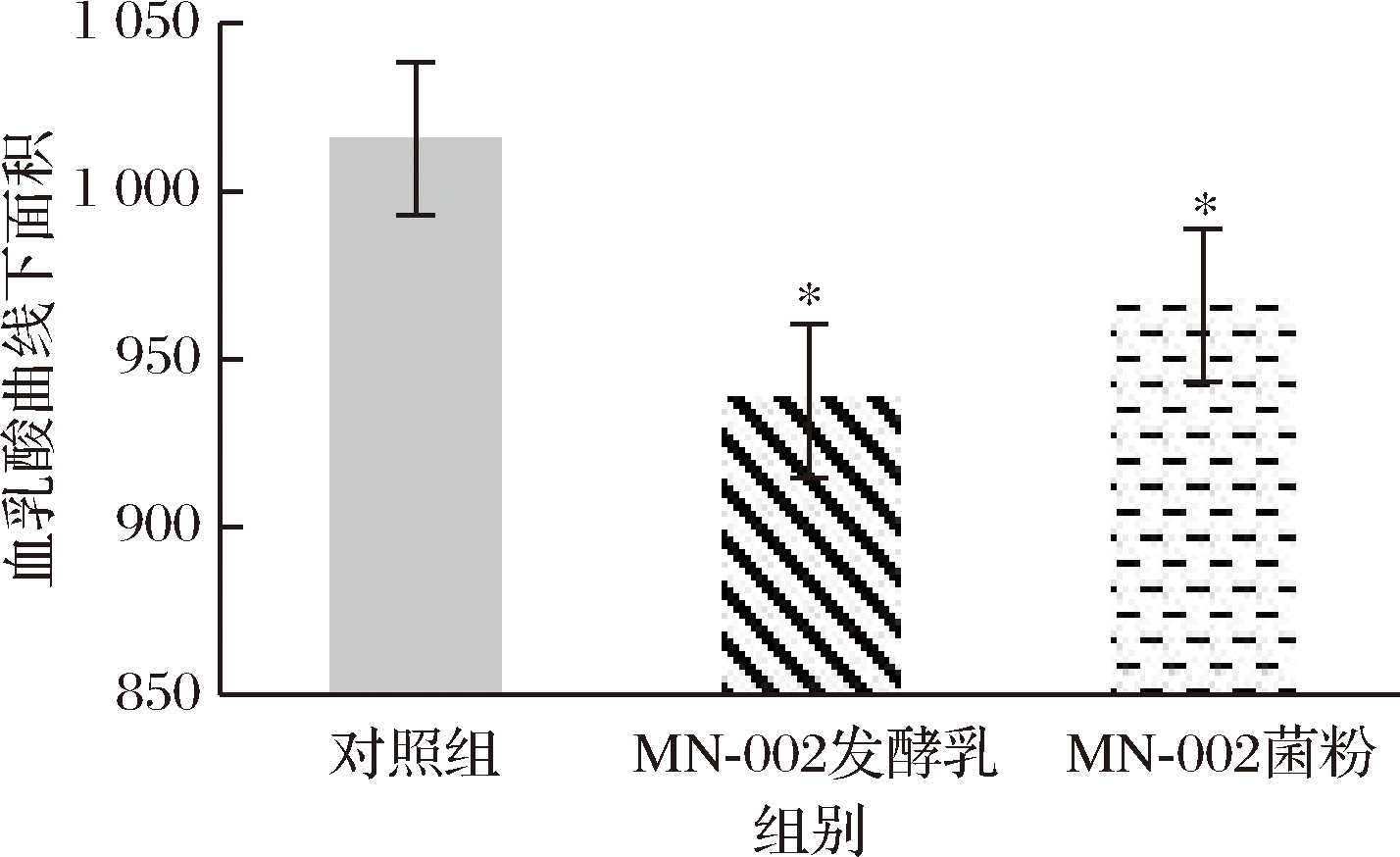
图6 血乳酸曲线下面积柱形图
Fig.6 Area column chart under blood lactate curve
表4 试验结果判定表
Table 4 Result determination

试验组别负重游泳实验辅助实验生化指标血清尿素肝糖原血乳酸抗疲劳结果发酵乳+++++菌粉 +++++
注:+表示试验结果呈阳性,-表示试验结果呈阴性
疲劳的定义是工作学习过程中执行能力降低和达成效率降低的状态。同时会伴随身体或心理疲惫的感觉[9],而运动则是导致身体疲劳的关键因素之一。运动耐力直接且客观反映了疲劳程度[13],负重游泳试验结果表明,发酵乳和菌粉组小鼠负重游泳时间较对照组显著延长(P<0.05),说明嗜热链球菌MN-002能够提高小鼠的运动耐力,具有一定的延缓疲劳活性,同时,其作为菌粉的抗体力疲劳效果显著优于发酵乳。
肌糖原的分解是运动能量的初始来源,剧烈运动会产生能量耗尽,后期的能量则主要来自肝糖原[14]。肝糖原是疲劳状态的敏感指标。结果显示,嗜热链球菌MN-002可减缓运动过程中肝糖原消耗,进而延缓疲劳产生,提高运动耐受力,有助于改善运动的代谢控制和能量代谢的激活[15]。同样,菌粉组的调节效果显著优于发酵乳,与负重游泳实验结果相一致。肝糖原的积累可能是导致运动耐受能力增加的关键因素。
通过无氧糖酵解,运动过程中获取能量的同时,体内会产生和积累大量代谢产物,包括乳酸[16]。尿素在肝脏中形成,是蛋白质代谢的最终产物,其含量与运动耐量呈现负相关关系。即血清尿素含量越高,表明机体适应运动耐受性越弱[17]。因此,血乳酸和血清尿素氮都是缓解疲劳的重要检测指标。发酵乳组血清尿素氮和血乳酸含量显著下降,说明MN-002发酵乳和菌粉有效降低了蛋白质的分解代谢,延缓了乳酸在体内的堆积,增加了运动负荷的适应能力,加速代谢产物清除,促进疲劳恢复。
嗜热链球菌MN-002可产生大量EPS,是其他菌株产量的近5倍,包含76%~81%的酸性EPS和12%~16%的中性EPS。多糖具有调节免疫、抗疲劳、抗肿瘤、抗氧化等生物活性[18-21],可通过促进糖原合成、减少运动代谢产物、增加耐缺氧能力等来提高机体的抗疲劳能力,对于预防与消除运动性疲劳有重要作用[22]。枸杞、五味子和黄芪多糖对正常小鼠具有抗疲劳效果,最低有效剂量均<50 mg/(kg·d),而人参、土党参和黄秋葵多糖的有效剂量均为100 mg/(kg·d)[23-26]。推测EPS可能是嗜热链球菌MN-002提高小鼠运动耐力、增加肝脏中肝糖元储备量、降低血乳酸、血清尿素氮含量的功能因子,其发挥功能的具体分子机制需要进一步探究。
综上所述,6株乳酸菌中嗜热链球菌MN-002产胞外多糖能力最强,高达495.72 μg/mL,显著高于其他菌株;在不影响小鼠体重的前提下,高产胞外多糖的MN-002发酵乳和菌粉均有缓解小鼠体力疲劳的功效,活菌数有效剂量均为2×108 CFU/d;相较于发酵乳组,菌粉组抗疲劳和调节肝糖原的效果更优,而发酵乳组调节血乳酸的效果更好,它为嗜热链球菌MN-002的应用及产品开发奠定了基础。
[1] FUKUDA K, STRAUS S E, HICKIE I, et al. The chronic fatigue syndrome: A comprehensive approach to its definition and study. International Chronic Fatigue Syndrome Study Group[J]. Ann Intern Med, 1994, 121(12):953-959.
[2] AKAZAWA K H, CUI Y, TANAKA M, et al. Mapping of regional brain activation in response to fatigue-load and recovery in rats with c-Fos immunohistochemistry[J]. Neurosci Res, 2010, 66(4): 372-379.
[3] CHAUDHURI A, BEHAN P O. Fatigue in neurological disorders [J]. Lancet, 2004, 363(9 413):978-988.
[4] DUBOC P, MOLLET B. Applications of exopolysaccharides in the dairy industry[J]. Int Dairy J, 2001, 11(9):759-768.
[5] RUASMADIEDO P, HUGENHOLTZ J, ZOON P. An overview of the functionality of exopolysaccharides produced by lactic acid bacteria [J]. Int Dairy J, 2002, 12(2):163-171.
[6] KANG X, LING N, SUN G, et al. Complete genome sequence of Streptococcus thermophilus strain MN-ZLW-002[J]. Journal of Bacteriology, 2012, 194(16):4 428-4 429.
[7] 康小红, 张兰威, 孙国庆, 等. 一种嗜热链球菌胞外多糖及其制备和检测方法:中国,CN102702372B[P].2012-10-03.
[8] 王凡, 陈建国, 李周勇, 等.甘南藏族传统发酵乳中高产胞外多糖菌株筛选及发酵特性研究[J].食品科技,2019,44(7):10-15.
[9] LIU J, DU C, WANG Y, et al. Anti-fatigue activities of polysaccharides extracted from Hericium erinaceus[J]. Experimental and Therapeutic Medicine, 2015, 9(2):483-487.
[10] WYBENGA D R, GIORGIO J D, PILEGGI V J. Manual and automated methods for urea nitrogen measurement in whole serum [J]. Clin Chem, 1971, 17(9): 891-895.
[11] SOTELO-FÉLIX J I D, MARTINEZ-FONG D, MURIEL P, et al. Evaluation of the effectiveness of Rosmarinus officinalis (Lamiaceae) in the alleviation of carbon tetrachloride?induced acute hepatotoxicity in the rat[J]. J Ethnopharmacol, 2002, 81(2): 145-154.
[12] SHANG Y, CHENG J, QI J, et al. Scutellaria flavonoid reduced memory dysfunction and neuronal injury caused by permanent global ischemia in rat[J]. Pharmacol Biochem Behav, 2005, 82(1): 67-73.
[13] ZHANG Gang, ZHOU Simin, TIAN Junhuai, et al. Anti-fatigue effects of methazolamide in high-altitude hypoxic mice[J]. Tropical Journal of Pharmaceutical Research, 2012, 11 (2): 209-215.
[14] ANAND T, KUMAR G P, PANDAREESH M D, et al. Effect of bacoside extract from Bacopa monniera on physical fatigue induced by forced swimming [J]. Phytother Res, 2012, 26(4): 587-593.
[15] XU C, LV J, LO Y M, et al. Effects of oat β-glucan on endurance exercise and its anti-fatigue properties in trained rats [J]. Carbohydr Polym, 2013, 92(2): 1 159-1 165.
[16] IKEUCHI M, KOYAMA T, TAKEI S, et al. Effects of benzylglucosinolate on endurance capacity in mice [J]. J Health Sci, 2009, 55(2): 178-182.
[17] TANG W, ZHANG Y, GAO J, et al. The anti-fatigue effect of 20 (R)-ginsenoside Rg3 in mice by intranasally administration[J]. Biol Pharm Bull, 2008, 31(1): 2 024-2 027.
[18] CHO C W, HAN C J, RHEE Y K, et al. Cheonggukjang polysaccharides enhance immune activities and prevent cyclophosphamide-induced immunosuppression[J]. Int J Biol Macromol, 2015, 72: 519-525.
[19] GAO H, ZHANG W, WANG B, et al. Purification, characterization and anti-fatigue activity of polysaccharide fractions from okra (Abelmoschus esculentus (L.) Moench)[J]. Food Funct, 2018,9(2):1 088-1 101.
[20] WANG J, BAO A, MENG X, et al. An efficient approach to prepare sulfated polysaccharide and evaluation of anti-tumor activities in vitro[J]. Carbohydrate Polymers, 2018,184:366-375.
[21] 兰美华, 吴红彦. 中药植物多糖抗氧化作用研究进展[J]. 实用中医药杂志, 2012, 28(4):326-327.
[22] 董碧莲, 蔡延渠, 吕莉,等. 中药多糖增强免疫、抗疲劳作用的研究进展[J]. 2019,41(5):1 119-1 124.
[23] 胡馨予, 赵冰, 孙晓琪,等.枸杞子多糖抗疲劳活性研究[J]. 食品科技,2015,40(7):197-200.
[24] 何忠梅, 管春红, 李盛钰. 植物乳杆菌C88联合短梗五加多糖抗疲劳作用[J].2016,41(2):99-103.
[25] 吴铭, 周桃英, 陈年友,等.黄芪多糖抗疲劳作用研究[J].湖北农业科学,2014,53(1):175-177.
[26] 林华, 徐瑞, 田明建,等.人参茎叶多糖对大鼠血清自由基清除能力及抗疲劳能力的影响[J].辽宁师范大学学报(自然科学版),2015, 38(4):555-560.