表1 胶囊组成配方
Table 1 Composition of capsules

编号卡拉胶质量浓度/(g·L-1)果胶-壳聚糖聚合物质量浓度/(g·L-1)淀粉质量浓度/(g·L-1)果胶-壳聚糖占固形物质量分数/%C120182230C220241640C320301050C420360460
注:果胶-壳聚糖聚合物的质量是指脱水干燥至恒重后的质量
在国内,由于“毒胶囊”事件的连续发生[1],人们“谈药色变”;在国外,上世纪 90 年代英国曾爆发大规模疯牛病事件,欧美国家一度“闻牛色变”,作为衍生物的明胶产业也遭受打击,非明胶空心胶囊的开发也早已提上日程[2-4]。靶向给药系统,可使药物递送或浓集于特定靶部位和靶器官,从而避免药物作用于全身作用带来的毒副反应,是最新型的第4代药物剂型[5]。结肠近端容易发生病变,结肠靶向给药也是目前研究的热点,但是目前市场上的结肠靶向空心胶囊还存在一些问题,pH依赖型[6]或时间依赖型[7]结肠靶向胶囊,定位不够准确;菌群/酶触发型空心胶囊用明胶胶囊包衣而成,但是包衣所用的材料为偶氮类化合物[8],存在一定的毒副作用;近年来多糖类化合物开始应用,但是制备工艺复杂,甚至有3层包衣[9]。果胶-壳聚糖聚合物是近期研究的热点,原料丰富,天然安全,且具有在胃中不被降解,在结肠中可被降解的特性,因此将果胶-壳聚糖聚合物作为结肠靶向空心胶囊的新材料,旨在为果胶-壳聚糖的应用提供技术依据。
卡拉胶,港阳香化集团;淀粉,大米淀粉,江西金农生物科技有限公司;牛血清、胰酶粉(胰蛋白酶≥4 000 U/g)、胰淀粉酶≥3 000 U/g、胰脂肪酶≥7 000 U/g,美国Sigma-Aldrich公司;胃蛋白酶≥3 000 NFU/mg,广州齐云生物技术有限公司;实验中所用试剂H3PO4、磷酸盐、甘油均为分析纯。
DZF-6 020真空干燥箱,上海一恒科学仪器有限公司;SHB-3水循环式真空泵,西安仪创实验室仪器设备有限公司;PS 811型外径千分尺,德国帕斯特集团有限公司;PHS-25酸度计,上海雷磁仪器厂;XMTD-204数显水浴恒温振荡器,常州普天仪器制造有限公司;UV-5 100紫外分光光度计,日本Shimadzu公司;QA-HPZ-30恒温恒湿培养箱,东莞捷程仪器设备有限公司;空心胶囊模具(1号),绍兴拓普机械有限公司。
1.3.1 果胶-壳聚糖聚合物的制备
在室温条件下,将果胶溶于水中,制备质量浓度为50 g/L的果胶溶液,将壳聚糖溶于0.3%(体积分数)乙酸水溶液中,制备质量浓度为10 g/L的壳聚糖乙酸溶液,然后将壳聚糖溶液缓慢加入到果胶溶液中,边加边搅拌,得到果胶壳聚糖质量比为1∶3的溶液,待反应完全以20 000 r/min的速度匀浆,室温放置48 h,然后将反应物离心,弃去上清液,反复水洗,离心,得果胶-壳聚糖聚合物。
1.3.2 果胶-壳聚糖结肠靶向空心胶囊的制备
将淀粉溶于水中,搅拌并加热到70~80 ℃[10],保持5~8 min使糊化;加入卡拉胶搅拌至溶解完全,再缓慢加入果胶-壳聚糖聚合物,加水稀释溶液调整胶液浓度,并加入甘油作为增塑剂;最后将溶液在(80±5) ℃加热20~30 min,搅拌均匀后真空脱气
用不锈钢模具将果胶-壳聚糖/卡拉胶/淀粉混合溶液在55~60 ℃条件下蘸胶,模具取出翻转2圈,使胶液均匀涂抹于模具上,稍冷后将模具置于真空干燥箱中干燥12 h,脱模、切割并加盖密封。
1.3.3 果胶-壳聚糖聚合物含量对药物释放度的影响
卡拉胶质量浓度为20 g/L,胶体总固形物质量浓度为60 g/L,调整果胶-壳聚糖聚合物和淀粉的质量浓度,使果胶-壳聚糖占固形物比例为30%、40%、50%、60%(质量分数),见表1。按1.3.2方法制备果胶-壳聚糖结肠靶向空心胶囊,考察果胶-壳聚糖聚合物占固形物的比例对胶囊药物释放度的影响。
表1 胶囊组成配方
Table 1 Composition of capsules

编号卡拉胶质量浓度/(g·L-1)果胶-壳聚糖聚合物质量浓度/(g·L-1)淀粉质量浓度/(g·L-1)果胶-壳聚糖占固形物质量分数/%C120182230C220241640C320301050C420360460
注:果胶-壳聚糖聚合物的质量是指脱水干燥至恒重后的质量
1.3.4 果胶-壳聚糖结肠靶向空心胶囊制备工艺优化
(1)果胶-壳聚糖聚合物的比例对胶囊性能的影响
卡拉胶质量浓度为20 g/L,胶体总固形物质量浓度为60 g/L,调整加入的果胶-壳聚糖聚合物量占胶液总固形物的比例分别为40%、45%、50%(质量分数),加入2%(体积分数)的甘油作为增塑剂,按1.3.2方法制备果胶-壳聚糖结肠靶向空心胶囊,考察果胶-壳聚糖聚合物占胶液固形物的比例对胶囊水蒸气透过系数的影响。
(2)甘油含量对胶囊性能的影响
卡拉胶质量浓度20 g/L,果胶-壳聚糖聚合物质量浓度为30 g/L,淀粉质量浓度为10 g/L,调整甘油含量占胶液的体积分数分别为0.5%、1%、1.5%、2%、2.5%,按1.3.2方法制备果胶-壳聚糖结肠靶向空心胶囊,考察甘油含量对胶囊水蒸气透过系数的影响。
(3)干燥温度对胶囊性能的影响
卡拉胶质量浓度为20 g/L,果胶-壳聚糖聚合物浓度为30 g/L,淀粉质量浓度为10 g/L,加入2%(体积分数)的甘油作为增塑剂,按1.3.2方法制备果胶-壳聚糖结肠靶向空心胶囊,考察干燥温度40、50、60、70、80 ℃对胶囊水蒸气透过系数的影响。
(4)果胶-壳聚糖结肠靶向空心胶囊制备的响应面优化试验
根据单因素试验结果,采用响应面软件Design-Expert 6.0对果胶-壳聚糖聚合物结肠靶向空心胶囊制备条件进行Box-Benhnken优化,设计3因素3水平的响应面试验,以空心胶囊的水蒸气透过系数为指标对制备条件进行优化。试验因素水平编码如表2所示。
表2 空心胶囊制备工艺参数
Table 2 Extraction parameter of the bioactive protein from goat placenta
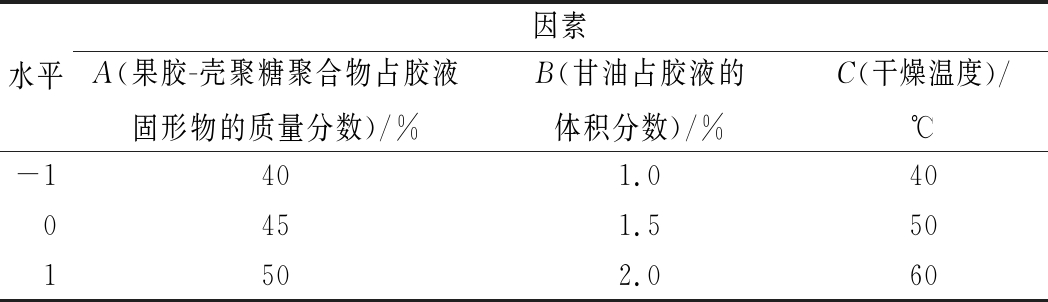
水平因素A(果胶-壳聚糖聚合物占胶液固形物的质量分数)/%B(甘油占胶液的体积分数)/%C(干燥温度)/℃-1401.0400451.5501502.060
1.3.5 测定方法
1.3.5.1 体外模拟药物释放度的测定
模拟胃液(simulated gastric fluid,SGF)的配制:1 g 胃蛋白酶溶解于100 mL HCl(0.01 mol/L)溶液中,pH 1.5;
模拟小肠液(simulated intestinal fluid,SIF)的配制:1 g胰酶粉溶于100 mL 磷酸盐缓冲(0.05 mol/L)溶液中,pH 6.8;
模拟结肠液(simulated colonic fluid,SCF)的配制:将SD大鼠麻痹后把结肠从腹部取出,在充氮环境中收集结肠内容物30 g溶于100 mL磷酸盐缓冲(0.05 mol/L)溶液中,pH 7.8。
以牛血清白蛋白(bovine serum albumin,BSA)为模拟药物来分析该胶囊的药物释放特征。每个胶囊填充25 mg BSA并密封,然后放入装有模拟胃液的容器中2 h,取出水洗后放入模拟小肠液3 h,之后再次取出水洗后放入模拟结肠液9 h。整个过程溶液放置在37 ℃恒温水浴锅中并以100 r/min振荡,每30 min吸取5 mL模拟液测定1次BSA的含量,同时补足对应的新鲜模拟液5 mL。
溶液中BSA的含量采用紫外分光光度法进行测定。分别配制质量浓度为0.1、0.2、0.4、0.6、0.8、1.0 mg/mL BSA溶液作为标准溶液,在280 nm条件下测定吸光度,绘制标准曲线。测定在 t 时刻取出的模拟液的吸光度,并根据吸光度计算出BSA的含量,BSA释放率(RB)的计算如公式(1)所示:
(1)
式中:Rt,BSA在t时刻的累积释放量;Mi,BSA的原始质量(25 mg)。
1.3.5.2 水蒸气透过系数(water vapor permeability,WVP)的测定
参照王静平[11]采用的杯式法进行测定。
1.3.5.3 胶囊规格尺寸的测定
长度的测定:用游标卡尺测量胶囊帽和胶囊体的长度,精确到0.02 mm。
厚度的测定:用外径千分尺于被测聚合膜上随机选5点进行测量,取平均值得膜厚度,精确到0.01 mm。
1.3.5.4 含水量的测定
根据《中国药典》[12]2010版中含水量的测定方法进行测定。
1.3.5.5 脆碎率的测定
根据《中国药典》[12]2010版中脆碎率的测定方法进行测定。
1.3.6 数据分析方法
采用SPSS统计软件进行数据分析,组间均值比较用单因素方差分析(one-way ANOVA),结果用平均值±标准误差表示。
根据表1中的胶囊配方制备胶囊,以BSA作为模拟药物测定空心胶囊的药物释放特性,考察果胶-壳聚糖聚合物比例对药物释放度的影响,见图1。
由图1可知,在模拟胃液里,4种配方制备的胶囊药物都没有释放;在模拟小肠液中,BSA以缓慢的速度释放出来,C1样品释放率最高,达到53.12%,C2、C3、C4的释放率分别达到9.89%、6.82%和2.47%,在模拟结肠液中,BSA被快速释放出来,C1样品内BSA在第5小时的释放率达到最高值,为95.08%,C2和C3样品内BSA在第5.5小时达到最大,释放率分别为92.46%和93.33%,而C4内BSA最大释放率为90.93%,发生在第7 h,之后BSA释放率缓慢下降。因此,果胶-壳聚糖聚合物占胶液中固形物的最佳比例为40%~50%。
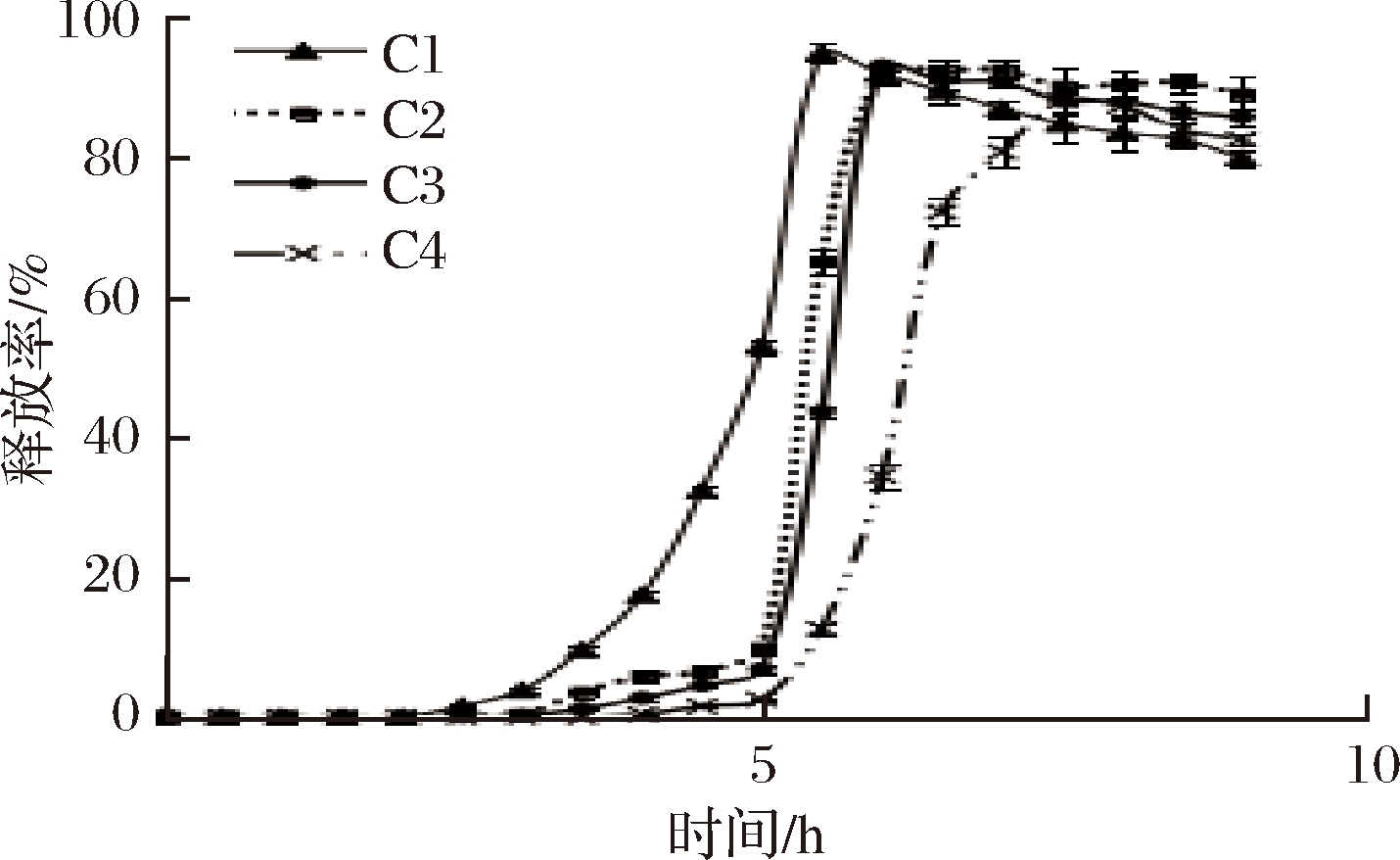
图1 BSA体外模拟释放率
Fig.1 Release of BAS from capsule in vitro
2.2.1 果胶-壳聚糖聚合物含量对胶囊水蒸气透过系数的影响
由图2可知,随着果胶-壳聚糖聚合物含量的增加,胶囊的水蒸气透过系数逐渐降低,说明果胶-壳聚糖聚合物含量与胶囊的透水气性有着直接的关系,而卡拉胶和淀粉的的阻水性相对较差,当果胶-壳聚糖聚合物在固形物中的比例(质量分数)增加时,胶囊的阻水性也会增强。

图2 果胶-壳聚糖聚合物含量对胶囊水蒸气透过系数的影响
Fig.2 Effect of pectin-chitosan ploymer on the WVP of capsule
2.2.2 甘油含量对胶囊水蒸气透过系数的影响
由图3可知,随着甘油含量的增加,水蒸气透过系数呈现出先减小后增加的趋势,当甘油含量为1%(体积分数)时,水蒸气透过系数最小,之后随着甘油含量的增加,水蒸气透过系数逐渐增加。原因可能是甘油可以很容易地插入到大分子物质之间,从而增强聚合物中的刚性结构,增强了阻水性能;随着甘油含量的逐渐增加,甘油分子的亲水特性增加了聚合膜的含水量,从而使聚合膜的水蒸气渗透性能增加[13-14]。

图3 甘油含量对胶囊水蒸气透过系数的影响
Fig.3 Effect of glycerol on the WVP of capsule
2.2.3 干燥温度对胶囊水蒸气透过系数的影响
由图4可知,随着干燥温度的增加,水蒸气透过系数呈现出先减小后增加的趋势,当干燥温度为60 ℃时,水蒸气透过系数最小,之后随着干燥温度的增加,水蒸气透过系数逐渐增加。原因可能是干燥温度的升高加剧了胶液中大分子聚合物链段的运动,从而形成致密度高的立体网状结构;也可能是加热改变了胶液中大分子的结构,从而增加了可与其他物质进行作用的氢键,聚合膜结构变得致密,从而WVP减小。但是当温度继续升高时,大分子聚合物内部的链段运动加速,聚合物还未形成均匀立体网状结构就已经沉积下来,形成气孔和裂纹从而使WVP增加[15-16]。
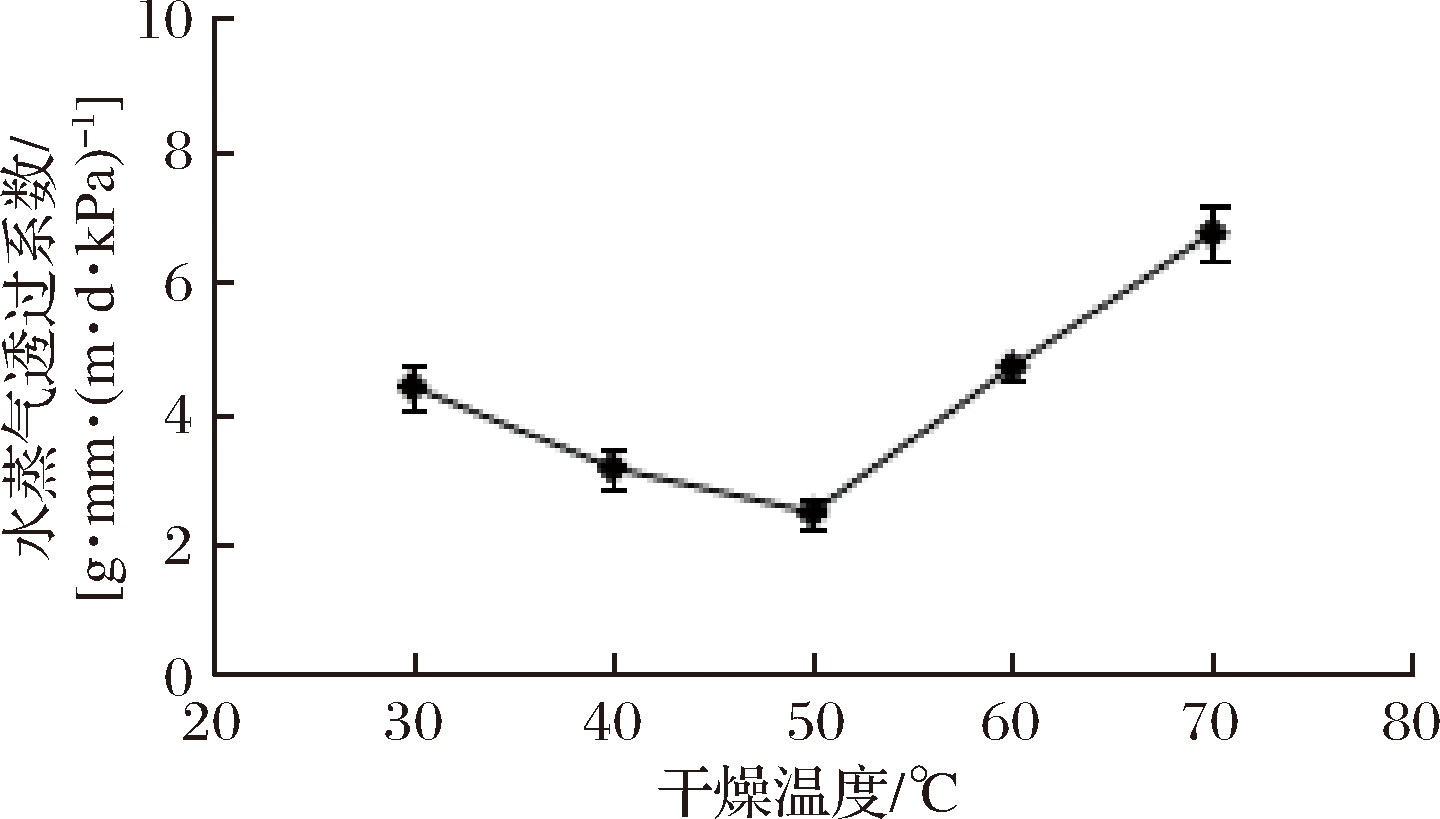
图4 干燥温度对胶囊水蒸气透过系数的影响
Fig.4 Effect of drying temperature on the WVP of capsule
2.2.4 果胶-壳聚糖结肠靶向胶囊制备工艺的响应面优化
(1)回归模型建立及方差分析
根据单因素试验结果确定影响因素及其水平,响应面试验设计及结果见表3。试验结果采用Design-Expert 8.0.6软件进行多元回归拟合得到水蒸气透过系数与各因素的二次方程模型。
水蒸气透过系数与各因素的二次方程模型:
Y=3.28-0.44×A-0.11×B+0.79×C+0.14×A×B+0.50×A×C+0.29×B×C-0.21×A2+0.70 × B2+1.48×C2
式中:Y,水蒸气透过系数,g·mm/(m·d·kPa);A,果胶-壳聚糖聚合物占胶液固形物的质量分数,%;B,甘油占胶液的体积分数,%;C,干燥温度,℃。
表3 响应面实验设计及结果
Table 3 Experimental values for the optimization of the fermentation conditions by RSM
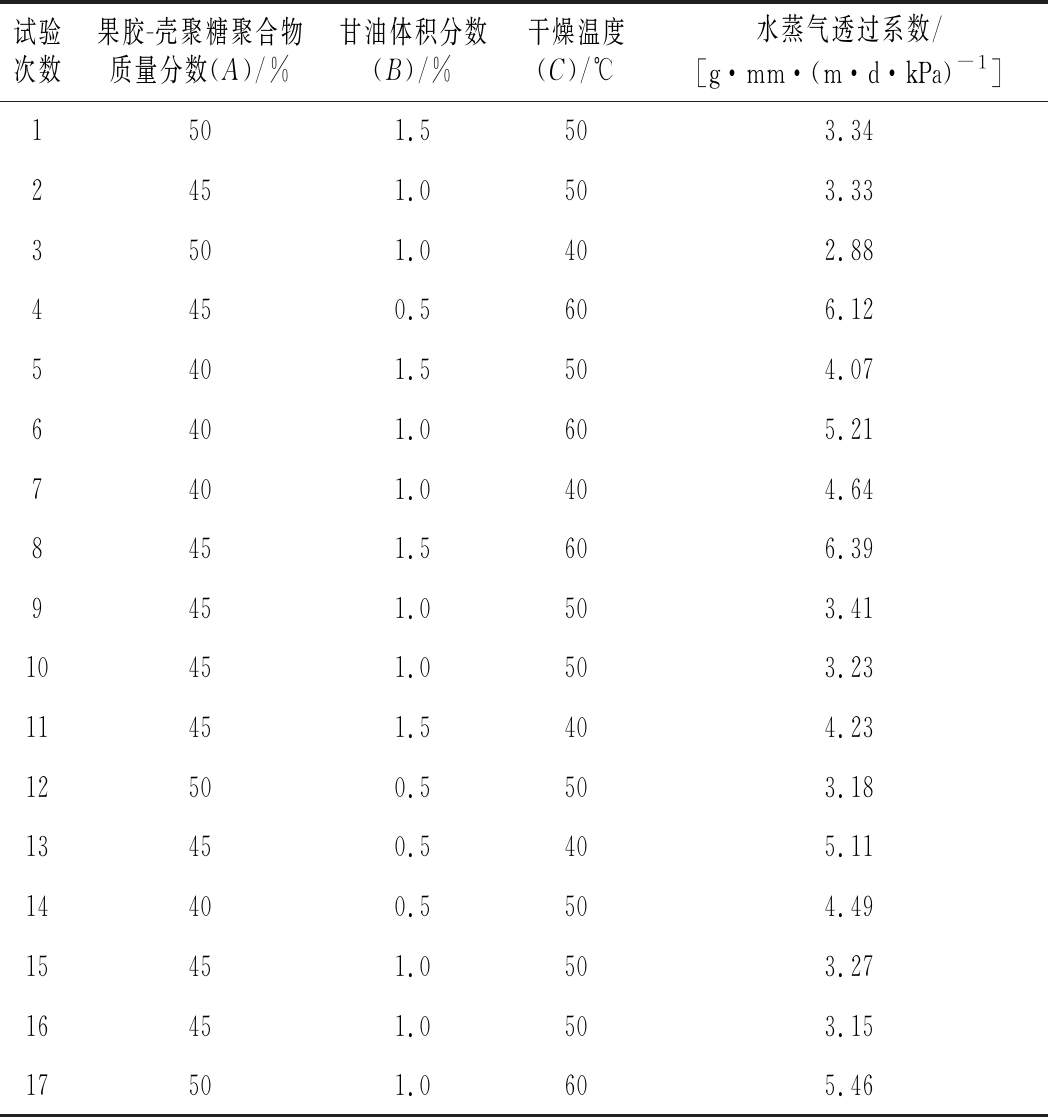
试验次数果胶-壳聚糖聚合物质量分数(A)/%甘油体积分数(B)/%干燥温度(C)/℃水蒸气透过系数/[g·mm·(m·d·kPa)-1]1501.5503.342451.0503.333501.0402.884450.5606.125401.5504.076401.0605.217401.0404.648451.5606.399451.0503.4110451.0503.2311451.5404.2312500.5503.1813450.5405.1114400.5504.4915451.0503.2716451.0503.1517501.0605.46
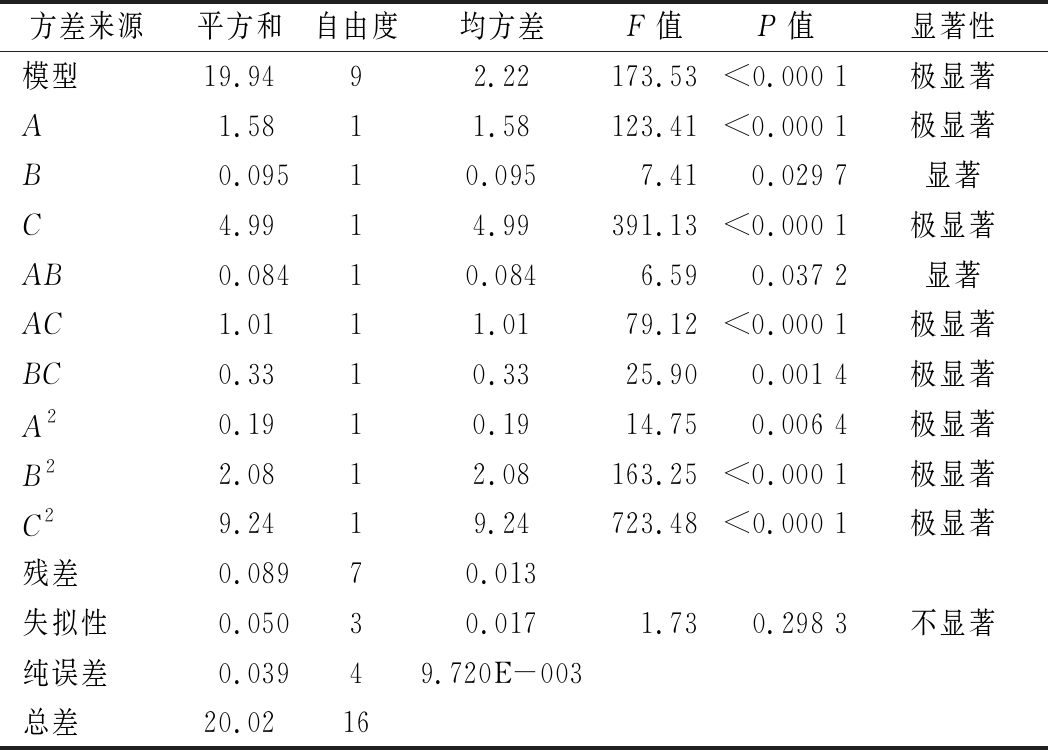
试验数据的方差分析结果见表4,所得回归方程极显著,且失拟检验不显著,说明回归模型很理想,用方程拟合3个因素与水蒸气透过系数之间的关系是可行的的,实验误差小,可以用该回归模型代替试验真实点对试验结果进行分析。由回归方程和方差分析数据可知,回归方程的一次项3因素(A、B、C)对水蒸气透过系数有不同程度的影响,因素A、因素C对水蒸气透过系数影响极显著(P<0.01),因素B对产物的免疫活性影响显著(P<0.05);回归方程的二次项A2、B2、C2以及交互项中的AC、BC也对水蒸气透过系数影响极显著(P<0.01),交互项中的AB对水蒸气透过系数影响显著(P<0.05)。这表明各因素对响应值的影响不是简单的线性关系,而是呈二次关系,且3因素之间存在显著的交互作用。
表4 响应面方差分析结果
Table 4 Statistic analysis for the response surface quadratic model obtained from RSM design
方差来源平方和自由度均方差F值P值显著性模型19.9492.22173.53<0.000 1极显著A1.5811.58123.41<0.000 1极显著B0.09510.0957.410.029 7显著C4.9914.99391.13<0.000 1极显著AB0.08410.0846.590.037 2显著AC1.0111.0179.12<0.000 1极显著BC0.3310.3325.900.001 4极显著A20.1910.1914.750.006 4极显著B22.0812.08163.25<0.000 1极显著C29.2419.24723.48<0.000 1极显著残差0.08970.013失拟性0.05030.0171.730.298 3不显著纯误差0.03949.720E-003总差20.0216
注:表中P<0.05表明模型或考察因素有显著影响;P<0.01表明影响高度显著
(2)不同独立变量间响应面立体图
分别将模型中的果胶-壳聚糖聚合物质量分数、甘油体积分数及干燥温度其中1个因素固定在中间水平,得到另外2个因素交互作用对水蒸气透过系数的子模型,并根据模型绘制三维曲面图,水蒸气透过系数的响应面及等高线如图5所示。
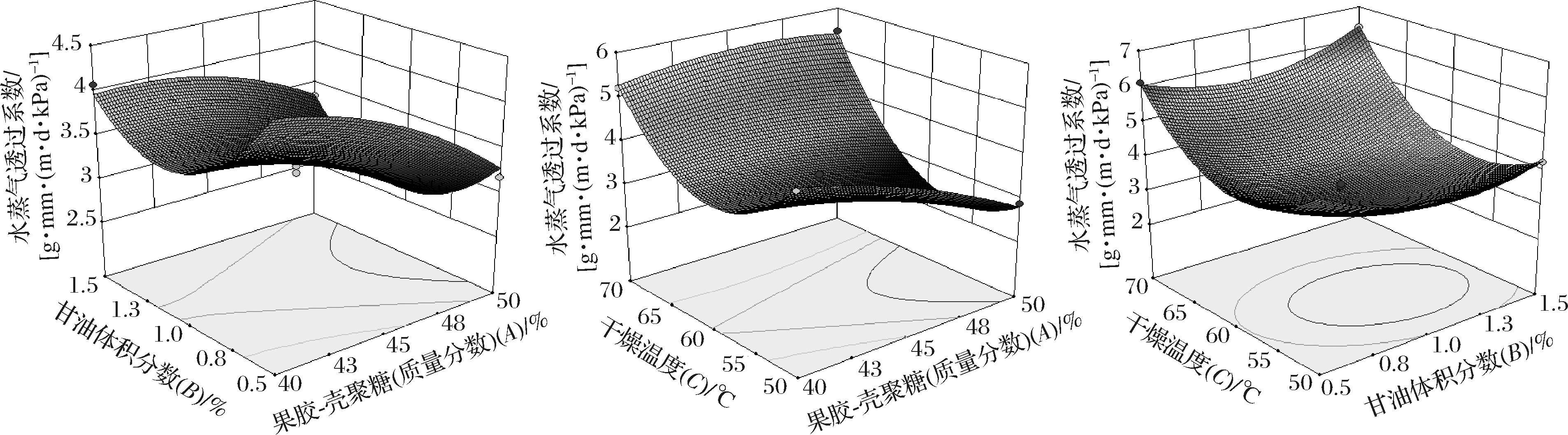
图5 各因素交互作用对空心胶囊水蒸气透过系数影响的响应面
Fig.5 Response surface of interaction of various factors on capsule WVP
利用Design Expert 8.0.6软件进行分析计算,可得到果胶-壳聚糖结肠靶向空心胶囊的最佳制备条件为果胶-壳聚糖聚合物占胶液固形物的质量分数(A)为50%,甘油占胶液的体积分数(B)为1%,干燥温度(C)为46 ℃,预测制备的空心胶囊水蒸气透过系数为2.34 g·mm/(m·d·kPa)。
(3)试验模型验证
采用上述优化后的胶囊制备工艺条件,进行验证试验,测得水蒸气透过系数达到2.39±0.12,与预测值2.34误差在1%以内,说明采用该方法优化得到的胶囊制备工艺条件参数准确可靠,运用试验建立的数学模型进行预测在实践中是切实可行的。
采用蘸胶法制备的胶囊如图6所示,胶囊呈黄白色,透明,表面光滑,无薄头、瘪头、梅花头、皱纹等现象。体长,帽长,体外径和帽外径分别为(16.60±0.5)、(9.80±0.5)、(6.63±0.5)和(6.91±0.5) mm,含水率为(10.06±0.83)%,脆碎率为0。

图6 空心胶囊
Fig.6 Photo of capsule
(1)通过对药物释放率的测定,分析了果胶-壳聚糖聚合物比例对药物释放度的影响,当其含量占胶液中固形物的比例为40%~50%时,以BSA为模拟药物,制备的胶囊在模拟胃液里药物都不释放,在小肠液中的药物释放率为(6.82±0.54)%~(9.89±0.98)%,在结肠液中的药物总释放率达到(92.46±1.50)%~(93.33±0.63)%,达到结肠靶向给药胶囊的要求。
(2)以水蒸气透过系数为响应指标,对果胶-壳聚糖结肠靶向胶囊的制备工艺和配方进行单因素和响应面分析,得到最佳制备条件为果胶-壳聚糖聚合物占胶液固形物的质量分数为50%,甘油占胶液的体积分数为1%,干燥温度为46 ℃,在此条件下制备的空心胶囊水蒸气透过系数为(2.39±0.12) g·mm/(m·d·kPa),透气系数差,有利于内容物稳定性的增加,各项指标符合国标要求。
(3)采用本文方法制备的结肠靶向空心胶囊工艺简单,原料天然,脆碎度更低,但是不如现有胶囊光滑、坚硬,松紧度稍差,需要进一步改进。
[1] 张奇锋, 姜淦. 胶囊行业之殇[N]. 广东科技报, 2012-04-21(6).
[2] 华慧颖, 王少鹏, 廖威,等. 豆粕提取物用于药用空心胶囊制作的研究[J]. 明胶科学与技术, 2011, 31(1):7-10.
[3] RODRIGUEZ-PATINO J M, MOLINA-ORTIZ S E, S NCHEZ C C, et al. Behavior of soy globulin films at the air-water interface, structure and dilatational properties of spread films[J]. Industrial and Engineering Chemistry Research, 2003, 42(21): 5 011-5 017.
NCHEZ C C, et al. Behavior of soy globulin films at the air-water interface, structure and dilatational properties of spread films[J]. Industrial and Engineering Chemistry Research, 2003, 42(21): 5 011-5 017.
[4] WANG M J, XIE Y L, CHEN Z J , et al. Optimizing preparation of NaCS-chitosan complex to form a potential material for the colon-Specific drug delivery system[J]. Journal of Applied Polymer Science, 2010, 117(5):3 001-3 012.
[5] MAESTRELLI F, CIRRI M, CORTI G, et al. Development of enteric-coated calcium pectinate microspheres intended for colonic drug delivery[J]. European Journal of Pharmaceutics & Biopharmaceutics, 2008, 69(2): 508-518.
[6] MOGHIMIPOUR E, DORKOOSH F A, REZAEI M, et al. In vivo evaluation of pH and time-dependent polymers as coating agent for colonic delivery using central composite design[J]. Journal of Drug Delivery Science and Technology, 2018, 43:50-56.
[7] SANGALLI M E, MARONI A, ZEMA L, et al. In vitro and in vivo evaluation of an oral system for time and/or site-specific drug delivery[J]. Joumal of Controlled Release, 2001, 73(1):103-110.
[8] TOZAKI H, NISHIOKA J, KOMIKE J, et al. Enhanced absorption of insulin and (Asu(1,7)) eel-calcitonin using novel azopolymer-coated pellets for colon-specific drug delivery[J]. Journal of Pharmaceutical Sciences, 2001, 90(1):89-97.
[9] 傅红兴, 李慧, 万常伟,等. 吲哚美辛结肠靶向胶囊的制备及体外释药评价[J].中国现代应用药学, 2013, 30(9):984-988.
[10] 吴颖. 新型淀粉膜的制备及其结构和性能的研究[D]. 天津:天津大学, 2009.
[11] 王静平. 添加海藻酸钠的可食性淀粉膜的研究[D]. 天津:天津大学, 2007.
[12] 国家药典委员会.中华人名共和国药典[M].北京:中国医药科技出版社,2010.
[13] AL-HASSAN A A, NORZIAH M H. Starch-gelatin edible films: Water vapor permeability and mechanical properties as affected by plasticizers[J]. Food Hydrocolloids, 2012, 26(1): 108-117.
[14] 王利强, 贾超, 卢立新,等. 正交试验优化马铃薯淀粉基复合膜制备工艺及包装性能测定[J]. 食品科学, 2013, 34(14):80-85.
[15] 宫志强, 李彦春, 祝德义,等. 干燥温度对壳聚糖-明胶复合膜性能的影响[J]. 食品科技, 2008, 33(4): 92-94;102.
[16] 李梦琴, 艾志录, 张平安,等. 干燥温度对谷朊粉膜性能的影响[J]. 食品科学, 2005, 26(4): 123-126.