黑曲霉群(Aspergillus niger group)是曲霉属(Aspergillus)环绕亚属(Subgen.Circumdati)黑色组(Sect.Nigri)的一组具有不同程度的黑褐色、红褐色、橄榄褐色和暗褐色等至黑色分生孢子头的菌群,即Raper & Fennell(1965)分类系统中的Aspergillus niger group[1]。黑曲霉群菌种在自然界分布极为普遍,也是常见引起食品和饲料等腐败变质的植物病害真菌,但某些菌种因具有重要的经济利用价值而被广泛用于食品、医药等工业[2]。20世纪80年代,美国食品药品管理局(Food and Drug Administration,FDA)将黑曲霉列入一般认为是安全的菌种(generally recognized as safe,GRAS)进行管理,并将其广泛用于淀粉酶、脂肪酶、柠檬酸和葡萄糖酸等几十种食品添加剂的生产[3-6]。据报道,已知的黑曲霉群菌种主要来源于土壤,但近年来,越来越多的研究发现黑曲霉群菌种可普遍从污染的葡萄、咖啡和可可及其制品等中分离[7-11]。
黑曲霉群菌种作为食品发酵工业常用菌和食品中常见的腐败菌,已有许多分类学家对其系统发育和分类学关系进行了比较全面的研究,但黑曲霉群菌种的正确分类和鉴定仍然是目前分类学研究中较为困难的一类[10, 12-15]。截止到2019年,黑曲霉群中已有27种黑曲霉的分类学地位被确定。此外,已有研究表明,该类群菌种生物多样性复杂,难以通过形态学进行鉴定,需要结合生理学分析、细胞外分泌物类型、分子生物学手段等进行综合鉴定[10, 12-21]。FRISVAD等[16]总结了不同鉴定方法在曲霉属(包括黑曲霉群)菌种分类鉴定和系统发育中的应用情况,具体见表1。分别阐述形态学、生理特征、细胞外分泌物特征、分子生物学特征和全基因组测序等技术在该类菌种分类鉴定中的具体应用情况。
表1 不同鉴定技术在曲霉属真菌分类鉴定和系统发育中的应用情况
Table 1 Application of different identification technologies used to characterize Aspergillus strains for taxonomic and phylogenetic purposes

鉴定特征专用仪器和设备一般实验室是否配备鉴定结果可信度应用情况微观形态显微镜是++++宏观形态照相机、比色计是++++生理特征培养箱等是++挥发性次级代谢产物GC很少实验室配备+不常用非挥发性次级代谢产物TLC个别实验室配备++不常用HPLC-DAD很少实验室配备+++不常用HPLC-MS很少实验室配备+++不常用diMS很少实验室配备++不常用胞外酶GE、CE很少实验室配备+不常用DNA序列测定PCR仪、测序仪个别实验室配备+++
注:GC,气相色谱; TLC,薄层色谱;HPLC,高效液相色谱;DAD,二极管阵列检测;MS,质谱;diMS,质谱直接进样;GE,凝胶电泳;CE,毛细管电泳; PCR,聚合酶链式反应
1 不同分类和鉴定方法的研究现状
1.1 形态学特征
通常来说,以菌落的宏观形态和微观形态为基础的传统形态学特征数据是曲霉属真菌菌种分类和鉴定的主要依据。但考虑到菌落形态受培养条件(培养基和培养温度等)的影响易发生改变,因此,如何确保待鉴定菌种与参考模式菌种的培养条件一致性是进行正确鉴定的前提。我国的曲霉属真菌鉴定学专著《中国真菌志 第5卷曲霉属及其相关有性型》推荐黑曲霉群菌种鉴定的培养基为查氏琼脂(czapek agar,CA)、查氏酵母膏琼脂(czapek yeast extract agar,CYA)和麦芽汁琼脂(malt extract agar,MEA),培养温度为25 ℃,变化范围为22~27 ℃,培养时间为5、7、10和14 d或更长时间[1]。真菌学分类和鉴定领域的国际权威专家推荐黑曲霉群菌种鉴定的培养基为CYA、MEA和氯硝胺18%甘油(dichloran glycerol,DG18)琼脂,培养温度为15、25和37 ℃,培养时间为7和14 d 或更长时间[13-16]。此外,对于某些难以通过上述培养基进行区分的菌种,还可选择肌酸蔗糖琼脂(creatine sucrose agar,CREA)、麦芽汁提取物啶酰菌胺琼脂(malt extract agar-boscalid,MEA-B)、酵母提取物蔗糖琼脂(yeast extract sucrose agar,YES)和燕麦琼脂(oatmeal agar,OAT)等,培养温度还可选择18、21、30、33和40 ℃等[13-14, 22-24]。
黑曲霉群菌种形态学鉴定的主要依据为待鉴定菌种在推荐的培养条件下的宏观形态和微观形态特征[1-2, 13-24]。其中菌落的宏观形态特征主要包括菌落的生长速度(以菌落直径来表示)、菌落的边缘是否整齐或有不规则缺裂、菌落的颜色及其变化、菌落的质地(丝绒状、絮状、绳状)、菌落的基部菌丝体薄或厚,柔软或坚韧,平坦、褶皱或具沟纹、菌落的表面是否产生无色或具有不同颜色的液滴、菌落的反面无色或具不同颜色,是否可以产生菌核等[1-2, 13-24]。菌落的微观形态特征主要包括菌落在显微镜下的分生孢子梗包括足细胞、分子孢子头、分生孢梗茎、顶囊、梗基、瓶梗和分生孢子等的形状、大小、颜色、表面纹饰等,同时还要观察产孢结构具体特征如产孢细胞的层数、长度和颜色等[1-2, 13-23]。黑曲霉群菌种一般具有黑色、黑褐色、紫褐色等的分生孢子头,分生孢子头一般为球形、辐射形或分裂成几个柱状结构;分生孢梗茎一般为光滑无色或近顶囊处带暗褐色;顶囊球形或近球形,有时呈暗褐色;产孢结构为单层或双层或同时存在单层或双层产孢细胞;分生孢子球形、近球形、椭圆形或横向扁平,光滑或不同程度的粗糙至具刺或纵向条纹;有的菌种可以产生菌核,菌核一般为球形或近球形,初为白色至奶油色,老后颜色变暗[1-2, 13-24]。
1.2 细胞外分泌物的特征
作为对外界生物和非生物环境的反应而产生的细胞外泌物的特征,也成为近年来黑曲霉群菌种分类和鉴定过程中常采用的重要依据[15]。该类物质主要包括次级代谢产物、过量合成的有机酸、积累的碳水化合物(例如海藻糖和多元醇)、胞外酶(extracellular enzymes)、疏水蛋白(hydrophobins)、黏附素(adhesins)、扩张素(expansins)和伴侣蛋白(chaperones)以及某些可能参与避免真菌繁殖结构被昆虫、螨类和其他动物食用的聚酮类和生物碱等[25]。通常分泌到细胞外或聚集在细胞壁上,并随着环境条件的变化而改变。对于那些能够分泌到细胞外的次级代谢产物如真菌毒素和抗菌素等,因具有高度的种属特异性,常被用于黑曲霉群菌种的分类和鉴定[26-27]。此外,黑曲霉群的不同种/株产生的次级代谢产物的差异也得到了全基因组测序研究的支持,即从基因组水平研究可知,黑曲霉群的不同种/株之间次级代谢产物产生能力的差异往往与基因组水平上携带的聚酮与非核糖体肽合成酶基因的数量和相似性密切相关[28-30]。
近年来,随着GC、HPLC、GC-MS、HPLC-MS等技术飞速发展,使得通过检测一种或几种特定的生物标志物而辅助于黑曲霉群菌种的分类和鉴定越来越成为可能。目前,可用于黑曲霉群菌种分类和鉴定且相对易于检测的细胞外泌物主要有neoxaline、黑麦酮酸类(secalonic acid)(包括黑麦酮酸D和F等)、环棒麦角素(cycloclavine)、狐茅麦角碱(festuclavine)、曲地酸(asterric acid)、dihydrogeodin、erdin(土曲霉素)、tensiol A和B、萘并-γ-吡喃酮类化合物(naphtho-γ-pyrones)、赭曲霉毒素(ochratoxins)(包括OTA、OTB、OTα和OTβ)、伏马菌素(fumonisins)(包括FB2、FB4和FB6等)和funalenone等[13]。但考虑到黑曲霉群菌种产生的次级代谢产物具有种属差异并与培养条件密切相关,尤其是培养温度、培养时间、培养基组成等,例如并非所有的黑曲霉群菌种都可以产生OTA,且黑曲霉产生OTA能力和产量与其培养条件密切相关,因此科学合理的实验方案的设计是利用外泌物的特征进行黑曲霉群菌种鉴定的难点[31]。此外,有许多结构尚不清楚但能在黑曲霉群的一个或多个物种中检测到的次级代谢产物,也可以很好的辅助用于黑曲霉群菌种的分类和鉴定。所以,总体来看,细胞外分泌物的特征是未来黑曲霉群菌种分类和鉴定过程中一个很好的补充方法。
1.3 分子生物学鉴定
已有的研究证明,黑曲霉群菌种作为难以分类和鉴定的种群,为了保证鉴定结果的可靠性,除了依靠形态学和细胞外分泌物的特征外,仍需结合限制性片段长度多态性(restriction fragment length polymorphism,RFLP)、PCR-RFLP、扩增片段长度多态性(amplified fragment length polymorphism,AFLP)、单链构象多态性(single strand conformation polymorphism,SSCP)、序列分析、引物特异性PCR和实时定量荧光PCR(quantitative real-time PCR,qRT-PCR)等多种分子生物学技术的鉴定结果进行综合判断[32-54],具体情况见表2。
表2 分子生物学技术在黑曲霉群菌种鉴定中的应用情况
Table 2 Application of molecular biology technology in identification of A. niger group

分子生物学技术目标基因应用范围文献RFLPpelA、pelB和pki能够区分黑曲霉和塔宾曲霉的鉴定[32]RFLPpelD所有分离株中相对保守,不能用于鉴定。[33]RFLPrDNA能够区分黑曲霉、塔宾曲霉、巴西曲霉、炭黑曲霉、日本曲霉、A. ellipticus和A. aculeatus[2,34]RFLP线粒体DNA能够将黑曲霉和巴西曲霉与塔宾曲霉区分开,日本曲霉与A. aculeatus区分开[34-35]PCR-RFLPITS、IGS、benA能够将黑曲霉群菌种的OTA潜在产毒株与非产毒株[36-39]AFLP能够区分已知的大多数黑曲霉群菌种[40-42]PCR-SSCP能够区分黑曲霉、巴西曲霉和塔宾曲霉在内的11种黑曲霉[43]引物特异性PCRITS能够将黑曲霉区分为4个不同的组[16]引物特异性PCRCytb能够用于推断日本曲霉、A.aculeatus、黑曲霉、塔宾曲霉、炭黑曲霉和A.ellipticus的系统发育关系[45]引物特异性PCRCoX I和线粒体DNA具有种内和种间变异性,不能用于黑曲霉群菌种的分类和鉴定[46]引物特异性PCRIGS序列变异性太高,不能够用于黑曲霉群菌种的分类和鉴定[13]引物特异性PCR丙酮酸激酶、果胶裂解酶、聚半乳糖醛酸酶、翻译起始因子2、转录延伸因子1-α和RNA聚合酶2仅能区分2种至5种黑曲霉[44-53]
RFLP是最早用于黑曲霉群新种鉴定的分子生物学技术。KUSTERS-VAN等[32-33]采用RFLP技术探讨了果胶裂合酶基因(pelA、pelB、pelD)和丙酮酸激酶基因(pki)作为DNA杂交实验的探针用于黑曲霉群菌种快速鉴定的可行性。结果发现,pelD基因在黑曲霉群的所有分离株中具有保守性,不能用于黑曲霉群菌种的鉴定,pelA和pelB可用于黑曲霉和塔宾曲霉的鉴定。KUSTERS-VAN等[32]和VARGA等[34]发现Sma I内切酶消化rDNA后可将黑曲霉、塔宾曲霉、巴西曲霉、炭黑曲霉、日本曲霉、A. ellipticus和A.aculeatus区分开。VARGA等[34]和HAMARI等[35]发现用Hae III/Bg III消化线粒体DNA可将黑曲霉和巴西曲霉与塔宾曲霉区分开,日本曲霉与A. aculeatus区分开。随后陆续报道了PCR-RFLP用于黑曲霉群菌种鉴定的可行性,尤其是发现采用Rsa I消化ITS基因、Hinf I消化IGS基因和Rsa I消化β-微管蛋白(beta-tubulin,benA)基因时可将黑曲霉群菌种的OTA潜在产毒株与非产毒株区分开[36-39]。PERRONE等[40-42]发现AFLP技术可以鉴定已知的大多数黑曲霉群菌种。SUSCA等[43]采用PCR-SSCP技术鉴定了包括黑曲霉、巴西曲霉和塔宾曲霉在内的11种黑曲霉。
基于管家基因如核糖体RNA基因及其内转录间隔区(internal transcribed spacer,ITS)和基因内间隔区(intergenic spacer,IGS)、线粒体细胞色素b(mitochondrial cytochrome b,Cytb)、benA、钙调蛋白(calmodulin,CaM)和细胞色素氧化酶I(cytochrome oxidase I,Cox I)建立的DNA序列分析和引物特异性PCR分析是目前黑曲霉群菌种分类和鉴定时最常用的分子生物学方法[44-53]。下面对DNA序列分析方法的可行性进行详细讨论。FRISVAD等[16]经过大量的实验研究表明,受序列变异度的影响,ITS序列仅能将黑曲霉群菌种大致区分为4个组:(1)黑曲霉和A.lacticoffeatus;(2)巴西曲霉(A.brasiliensis);(3)A.costaricaensis;(4)塔宾曲霉、臭曲霉、A.vadensis 和A.pipers,且大多数具有单层产孢结构的菌种都具有相同的ITS序列,如日本曲霉、A.aculeatus 和 A.uvarum。YOKOYAMA等[45]通过对黑曲霉群12个种的32株黑曲霉的线粒体基因Cytb的402个核苷酸序列和133个氨基酸序列分析,发现通过Cytb的氨基酸序列差异可以推断日本曲霉、A.aculeatus、黑曲霉、塔宾曲霉、炭黑曲霉和A.ellipticus的系统发育关系,但是不能通过Cytb基因的核苷酸序列差异推断塔宾曲霉和黑曲霉的系统发育关系。GEISER等[46]基于Cox I和线粒体DNA基因的核苷酸序列对8个种42株黑曲霉的系统发育关系分析可知,基于CoX I和线粒体DNA构建的系统发育树均具有种内和种间变异性,不能用于黑曲霉群菌种的分类和鉴定;此外,SAMSON等[13]基于IGS序列差异分析发现,该区域的核苷酸序列变异性太高,不能用于黑曲霉群菌种的鉴定。同时,基于丙酮酸激酶、果胶裂解酶、聚半乳糖醛酸酶、翻译起始因子2、转录延伸因子1-α和RNA聚合酶2等基因的分子鉴定技术仅能区分2~5种黑曲霉,也不建议用于黑曲霉群菌种的分类和鉴定[44-53]。大量研究证实,已知的黑曲霉群菌种中除了黑曲霉与A.lacticoffeatus可以通过在GenBank数据库中下载已经公布菌株的benA基因的核苷酸序列,并构建系统发育树进行初步鉴定外,其余绝大多数菌株均需要通过下载已经公布菌株的CaM核苷酸序列并构建系统发育树进行初步鉴定。但考虑到GenBank数据库是一个公共、开放的数据库可以接受上传的所有序列,并将其用于菌种的分类鉴定或系统发育分析,但GenBank数据库并不负责上传序列真实性或正确性的判断,因此在利用从GenBank数据库中下载的序列进行系统发育树构建时会出现因序列错误而引起鉴定错误。为了去除错误的序列并保证鉴定结果的可靠性,建议采用基因参考序列数据库(reference sequence database,RefSeq)中公布的序列信息进行系统发育树(http://www.ncbi.nlm.gov/refseq/)的构建[7]。
ATOUI 等[47]、SUSCA等[48]和PERRONE等[49]基于管家基因的引物特异性PCR对黑曲霉群不同菌种的研究发现,不同管家基因的鉴定能力不同,如针对聚酮合成酶(polyketide synthase,PKS)AT结构域的特异性引物可以特异性的鉴定炭黑曲霉,而针对CaM的特异性引物可以特异性的鉴定黑曲霉和炭黑曲霉。此外,即使是对同一个管家基因,引物序列的不同也会产生不同的鉴定能力,如ITS序列。GONZALEZ-SALGADO等[50]和HAUGLAND等[51]采用ITS/NIG、ITS1/JAP、ITS1/HET和ITS1/ELL可分别特异性的扩增黑曲霉、塔宾曲霉、日本曲霉、A.heteromorphus和A.ellipticus。针对PKS序列的不同位置设计不同的引物时,仅能鉴定可产OTA的炭黑曲霉潜在产毒株或同时鉴定产OTA的炭黑曲霉和黑曲霉的潜在产毒株[52-53]。
综上可知,分子生物学技术是黑曲霉群菌种分类和鉴定中必不可少的重要组成部分,但每种分子生物学鉴定方法都难以实现系统、全面和准确的鉴定。目前来说,基于管家基因的序列测定是最为常用的方法,CaM和benA结合能鉴定黑曲霉群的绝大多数菌种,但ITS序列和其他管家基因的鉴定水平有限难以实现精准鉴定。所以,在实际的鉴定中有必要结合多种管家基因的鉴定结果进行综合判断。
1.4 生理特征
用于黑曲霉群菌种分类和鉴定研究的生理特征分析,主要是指菌种对不同营养物质如碳源、氮源、无机盐等的利用能力差异。已有研究证实,黑曲霉、塔宾曲霉、臭曲霉、日本曲霉和A. vadensis在7种不同碳源上的生长曲线各不相同,但黑曲霉和塔宾曲霉的碳源利用情况最相似;相比于其他菌种,黑曲霉和塔宾曲霉对甘油、D-半乳糖醛酸盐和乙酸盐的利用能力均较差,臭曲霉和日本曲霉对木糖醇的利用能力较差,塔宾曲霉对柠檬酸的利用能力较差[54]。SAMSON等[13]对已经被鉴定的19种黑曲霉的研究发现,CREA作为一种半选择性培养基,可以将黑曲霉群菌种区分为不同的组。对于可以产生双层小梗的菌种如黑曲霉及其近缘种包括巴西曲霉、臭曲霉、塔宾曲霉、A.vadensis、A. sclerotioniger、A. costaricaensis、A. piperis 和A.lacticoffeatus来说,其在CREA培养基上的生长速度适中,产酸能力较强,可在菌落周围形成黄色的大晕环;而对A. ellipticus、A. heteromorphus 和A. homomorphus来说,在CREA培养基上的生长速度较快,但产酸能力相对前者较弱。此外,对于可以产生单层小梗的菌种来说,CREA可以很好的将日本曲霉、A.uvarum、A.aculeatus和A.aculeatinus区分开,具体生长情况如下:A.uvarum在CREA培养基上生长不良、产酸能力有限,而A.aculeatus和日本曲霉在CREA培养基上生长良好、产酸能力中等;A.aculeatinus在CREA培养基上生长速度较快且产酸能力也很强。POLLASTRO等[55]开发的半选择性培养基MEA-B(含10 mg/L的啶酰菌胺)可将多种黑曲霉区分开,如在MEA-B培养基上培养3 d后,只有炭黑曲霉、A. sclerotioniger、A. homomorphus 和A. sclerotiicarbonarius生长状态良好,而A. ellipticus、黑曲霉、巴西曲霉、A. vadensis、A.piperis 和A. costaricaensis等均未在MEA-B培养基上观察到菌落生长,继续培养7 d后,许多菌株可恢复生长,但只有炭黑曲霉、A.sclerotioniger 和A. sclerotiicarbonarius 能够产生孢子。更重要的,根据A. ibericus与炭黑曲霉在MEA-B培养基上的生长状态,可以将与炭黑曲霉亲缘关系很近但不能产生OTA的A. ibericus与炭黑曲霉区分开。
已有研究证实,生理特征分析被成功用于2种具有重要工业利用价值且亲缘关系较近的黑曲霉和泡盛曲霉(A.awamori)的鉴定[14]。将2种菌的28株菌接种在仅含0.2%碳源的基本培养基上,分析了其对30种碳源包括葡萄糖、D-半乳糖、半乳糖、D-来苏糖、L-山梨糖、L-鼠李糖、乳糖、eritrit、galactit、L-缬氨酸、L-β-苯丙氨酸、L-色氨酸、L-苏氨酸、L-丝氨酸、L-半胱氨酸、L-天冬酰胺、L-酪氨酸、L-赖氨酸、L-组氨酸、L-瓜氨酸、顺式乌头酸、香兰素(vanillin)、香兰素酸(vanillin acid)、L-抗坏血酸、D-氨基葡萄糖、双甘氨肽、水杨苷、果胶、松三糖和α-酮戊二酸的利用情况[14]。结果发现,2种菌除了在分别以L-山梨糖和2-脱氧-D-葡萄糖作为唯一碳源的培养基上的生长情况不同外,黑曲霉和泡盛曲霉具有非常相似的碳源利用情况,具体情况如下:以L-山梨糖作为唯一碳源时黑曲霉的生长速度明显低于泡盛曲霉,以2-脱氧-D-葡萄糖作为唯一碳源时,所测定的黑曲霉菌株生长状况良好,但有86.7%的泡盛曲霉未被观察到生长[14]。
综上可知,在特定的培养条件下,同种的黑曲霉具有相似的生理特征,但是不同种黑曲霉对营养物质的利用情况差异较大。基于生理特征的差异的分类和鉴定也是未来黑曲霉群菌种分类和鉴定领域的一个新的发展方向。
1.5 全基因组测序分析
截止到2019年8月,全世界范围内已经完成全基因组测序并公布的黑曲霉群菌种有5种17株,主要包括12株黑曲霉、1株泡盛曲霉、2株塔宾曲霉、1株日本曲霉、1株炭黑曲霉。其中最早完成测序的为柠檬酸生产常用菌黑曲霉ATCC 1015,公布日期为2011年10月12日;接着为黑曲霉SH-2,公布日期为2014年4月17日,其余15株均在近3年完成的测序,且17株菌中有6株菌为我国科学家负责完成测序工作。黑曲霉的基因组大小范围为31.85~36.45 Mb,GC含量范围为48.8%~51.6%。
但目前对于全基因组序列测定结果与传统的形态学、生理学、分子生物学技术等检测方法的对比分析,尚缺乏足够的数据支持,且对于许多最新报道、已经被鉴定的多种黑曲霉群菌株来说,也缺乏全基因组序列分析结果,后续研究中均有待于进一步加强全基因组序列的分析。
2 总结与展望
黑曲霉群菌种作为具有重要工业应用价值和常见的植物致病性真菌,其分类和鉴定工作一直是鉴定学中的热点和难点问题,迫切需要结合形态学、生理特征、DNA序列特征以及细胞外分泌物的特征等进行综合分析。此外,为了保证鉴定结果的可靠性,需要进一步加强对生理特征、细胞外泌物特征、分子生物学特征尤其是全基因组序列特征在菌种分类和鉴定工作中的应用。在此基础上,期望通过国际合作制定出一套可以适合黑曲霉群菌种分类和鉴定以及可以描述物种特征的最低判定标准或规范。
[1] 齐祖同.中国真菌志:第五卷曲霉属及其相关有性型[M]. 北京:科学出版社,1997:91-103.
QI Z T. Annals of Chinese fungi:Volume 5 Aspergillus and its associated sexual types[M]. Beijing:Science Press, 1997:91-103
[2] VARGA J,KEVEI F,HAMARI Z,et al.Genotypic and phenotypic variability among black aspergilla.In:Integration of modern taxonomic methods for Penicillum and Aspergillus classification.(Samson RA,Pitt JI,eds)[M].Amsterdam:Harwood Academic Publishers,2000,397-411.
[3] FAO/WHO.Toxicological evaluation of certain food additives[C].The 31 st meeting of the Joint FAO/WHO Expert Committee on Food Additives,World Health Organization,Geneva,1987.
[4] FAO/WHO.Toxicological evaluation of certain food additives[C].The 35th meeting of the Joint FAO/WHO Expert Committee on Food Additives,World Health Organization,Geneva,1990.
[5] FAO/WHO.Compendium of food additive specifications,vol 1 and 2.Food and Nutrition Paper no.51/1 and 51/2.Food and Agricultural Organization of the United Nations,World Health Organization,Rome,1992.
[6] 郭鲁宏, 杨顺楷.黑曲霉产生的酶类及其应用[J].天然产物研究与开发,1997,10(4):87-93.
GUO L H,YANG S K.Enzymes produced by Aspergillus niger and their applications[J].Natural Product Research and Development,1997,10(4):87-93.
[7] FUNGARO M H P,FERRANTI L S,MASSI F P,et al.Aspergillus labruscus sp.nov.a new species of Aspergillus section Nigri discovered in Brazil[J].Scientific Reports,2017,7(1):6 203.
[8] SUSCA A,PROCTOR R H,BUTCHKO R A E,et al.Variation in the fumonisin biosynthetic gene cluster in fumonisin-producing and nonproducing black aspergilli[J].Fungal Genetics and Biology,2014,73:39-52.
[9] NOONIM P,MAHAKARNACHANAKUL W,NIELSEN K F,et al.Fumonisin B2 production by Aspergillus niger in Thai coffee beans[J].Food Additives and Contaminants,2009,26(1):94-100.
[10] FERRACIN L M,FRISVAD J C,TANIWAKI M H,et al.Genetic relationships among strains of the Aspergillus niger aggregate[J].Brazilian Archives of Biology and Technology,2009,52:241-248.
[11] SØRENSEN A,LÜBECK P S,LÜBECK M,et al.Aspergillus saccharolyticus sp.nov.,a new black Aspergillus species isolated in Denmark[J].International Journal of Systematic and Evolutionary Microbiology,2011,61(Pt12):3 077-3 083.
[12] ABARCA M L,ACCENSI F,CANO J,et al.Taxonomy and significance of black aspergilla[J].Antonie Van Leeuwenhoek,2004,86(1):33-49.
[13] SAMSON R A,NOONIM P,MEIJER M,et al.Diagnostic tools to identify black aspergilla[J].Studies in Mycology,2007,59:129-145.
[14] VARGA J,FRISVAD J C,KOCSUBÉ S,et al.New and revisited species in Aspergillus section Nigri[J].Studies in Mycology,2011,69:1-17.
[15] SAMSON R A,VISAGIE C M,HOUBRAKEN J,et al.Phylogeny,identification and nomenclature of the genus Aspergillus[J].Studies in Mycology,2014,78:141-173.
[16] FRISVAD J C,LARSEN T O,VRIES R de,et al.Secondary metabolite profiling,growth profiles and other tools for species recognition and important Aspergillus mycotoxins[J].Studies in Mycology,2007,59:31-37.
[17] MURAKAMI H.A brief history of classification of the black aspergilli including the Kuro-koji molds.Taxonomic studies on Japanese industrial strains of the Aspergillus (Part 24)[J].Journal of the Society of Brewing Japan,1976,71:952-956.
[18] MURAKAMI H,YOSHIDA K.Grading of morphological characters of the black aspergilli.Taxonomic studies on Japanese Industrial strains of the Aspergillus (Part 27)[J].Journal of the Society of Brewing Japan,1979,74:328-331.
[19] MURAKAMI H,YOSHIDA K.Grading of physiological characters of the black aspergilli.Taxonomic studies on Japanese Industrial strains of the Aspergillus (Part 28)[J].Journal of the Society of Brewing,Japan,1979,74:459-461.
[20] MURAKAMI H,YOSHIDA K,YOSHIDA K,et al.Tables of mycological characters of the representative strains of the black aspergilli.Taxonomic studies on Japanese industrial strains of the Aspergillus (Part 30)[J].Journal of the Society of Brewing Japan,1979,74:466-470.
[21] AL-MUSALLAM A.Revision of the black Aspergillus species[D].Utrecht:Utrecht University,Baarn,1980.
[22] PERRONE G,VARGA J,SUSCUA A,et al.Aspergillus uvarum sp.nov.an uniseriate black Aspergillus species isolated from grapes in Europe[J].International Journal of Systematic and Evolutionary Microbiology,2008,58(4):1 032-1 039.
[23] NOONIM P,MAHAKARNCHANAKUL W,VARGA J,et al.Two novel species of Aspergillus section Nigri from Thai coffee beans[J].International Journal of Systematic and Evolutionary Microbiology,2008,58(7):1 727-1 734.
[24] FUNGARO M H P,FERRANTI L S,MASSI F P,et al.Aspergillus labruscus sp.nov.a new species of Aspergillus section Nigri discovered in Brazil[J].Scientific Reports,2017,7(1):6 203.
[25] ROHLFS M,OBMANN B,PETERSEN R.Competition with filamentous fungi and its implication for a gregarious lifestyle in insects living on ephemeral resources[J].Ecological Entomology,2005,30(5):556-563.
[26] FRISVAD J C,BRIDGE P D,ARORA D K.Chemical fungal taxonomy[M].New York:Marcel Dekker,1998.
[27] LARSEN T O,SMEDSGAARD J,NIELSEN K F,et al.Phenotypic taxonomy and metabolite profiling in microbial drug discovery[J].Natural Product Reports,2005,22(6):672-693.
[28] GALAGAN J E,CALVO S E,CUOMO C,et al.Sequencing of Aspergillus nidulans and comparative analysis with A.fumigatus and A.oryzae[J].Nature,2005,438:1 105-1 115.
[29] NIERMAN W H,PAIN A,ANDERSON M J,et al.Genomic sequence of the pathogenic and allergenic filamentous fungus Aspergillus fumigatus[J].Nature,2005,438:1 151-1 156.
[30] PEL H J,DE WINDE J H,ARCHER D B,et al.Genome sequencing and analysis of the versatile cell factory Aspergillus niger CBS 513.88[J].Nature Biotechnology,2007,25:221-231.
[31] FRISVAD J C,NIELSEN K F,SAMSON R A.Recommendations concerning the chronic problem of misidentification of mycotoxigenic fungi associated with foods and feeds[J].Advances in Experimental Medicine and Biology,2006,571:33-46.
[32] KUSTERS-VAN SOMEREN M A,KESTER H CM,SAMSON R A,et al.Variation in pectinolytic enzymes in black aspergilli:A biochemical and genetic approach.In:Modern concepts in Penicillium and Aspergillus classification(Samson RA,Pitt JI,eds).[M].New York:Plenum Press,1990,321-334.
[33] KUSTERS-VAN SOMEREN M A,SAMSON R A,VISSER J.The use of RFLP analysis in classification of the black aspergilli:Reinterpretation of Aspergillus niger aggregate[J].Current Genetics,1991,19(1):21-26.
[34] VARGA J,KEVEI F,FEKETE C,et al.Restriction fragment length polymorphisms in the mitochondrial DNAs of the Aspergillus niger aggregate[J].Mycological Research,1993,97(8):1 207-1 212.
[35] HAMARI Z,KEVEI F,KOVáCA E,et al.Molecular and phenotypic characterization of Aspergillus japonicus and Aspergillus aculeatus strains with special regard to their mitochondrial DNA polymorphisms[J].Antonie Van Leeuwenhoek,1997,72:337-347.
[36] MEDINA A,MATEO R,LOPEZ-OCANA L,et al.Study of Spanish grape mycobiota and ochratoxin A production by Isolates of Aspergillus tubingensis and other members of Aspergillus section Nigri[J].Applied and Environmentral Microbiology,2005,71(8):4 696-4 702.
[37] BAU M,CASTELLA G,BRAGULAT M R,et al.RFLP characterization of Aspergillus niger aggregate species from grapes from Europe and Israel[J].International Journal of Food Microbiology,2006,111:S18-S21.
[38] MARTINEZ-CULEBRAS P V,RAMON D.An ITS-RFLP method to identify black Aspergillus isolates responsible for OTA contamination in grapes and wine[J].International Journal of Food Microbiology,2007,113(2):147-153.
[39] ZANZOTTO A,BURRUGNO S,MARCIANO P.Digestion of DNA regions to discriminate ochratoxigenic and non-ochratoxigenic strains in the Aspergillus niger aggregate[J].International Journal of Food Microbiology,2006,110(2):155-159.
[40] PERRONE G,MULE G,SUSCA A,et al.Ochratoxin A production and amplified fragment length polymorphism analysis of Aspergillus carbonarius, Aspergillus tubingensis,and Aspergillus niger strains isolated from grapes in Italy[J].Applied and Environmentral Microbiology,2006,72(1):680-685.
[41] PERRONE G,SUSCA A,EPIFANI F,et al.AFLP characterization of Southern Europe population of Aspergillus section Nigri from grapes[J].International Journal of Food Microbiology,2006,111:S22-S27.
[42] PERRONE G,STEA G,EPIFANI F,et al.Aspergillus niger contains the cryptic phylogenetic species A.awamori[J].Fungal Biology,2011,115(11):1 138-1 150.
[43] SUSCA A,STEA G,PERONE G.Rapid polymerase chain reaction (PCR)-single-stranded conformational polymorphism (SSCP) screening method for the identification of Aspergillus section Nigri species by the detection of calmodulin nucleotide variations[J].Food Additives and Contaminants,2007,24(10):1 148-1 153.
[44] VARAGA J,KOCSUBÉ S,T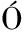 TH B,et al.Aspergillus brasiliensis sp.nov.,a biseriate black Aspergillus species with world-wide distribution[J].International Journal of Systematic and Evolutionary Microbiology,2007,57(Pt 8):1 925-1 932.
TH B,et al.Aspergillus brasiliensis sp.nov.,a biseriate black Aspergillus species with world-wide distribution[J].International Journal of Systematic and Evolutionary Microbiology,2007,57(Pt 8):1 925-1 932.
[45] YOKOYAMA K,WANG L,MIYAJI M,et al.Identification,classification and phylogeny of the Aspergillus section Nigri inferred from mitochondrial cytochrome b gene[J].FEMS Microbiology Letters,2006,200:241-246.
[46] GEISER D M,KLICH M A,FRISVAD J C,et al.The current status of species recognition and identification in Aspergillus[J].Studies in Mycology,2007,59:1-10.
[47] ATOUI A,MATHIEU F,LEBRIHI A.Targeting a polyketide synthase gene for Aspergillus carbonarius quantification and ochratoxin A assessment in grapes using real-time PCR[J].International Journal of Food Microbiology,2007,115(3):313-318.
[48] SUSCA A,STEA G,MULE G,et al.Polymerase chain reaction (PCR) identification of Aspergillus niger and Aspergillus carbonarius based on the calmodulin gene[J].Food Additives and Contaminants,2007,24(10):1 154-1 160.
[49] PERRONE G,SUSCA A,STEA G,et al.PCR assay for identification of Aspergillus carbonarius and Aspergillus japonicus[J].European Journal of Plant Pathology,2004,110(5-6):641-649.
[50] GONZALEZ-SALGADO A,PATNO B,VAZQUEZ C,et al.Discrimination of Aspergillus niger and other Aspergillus species belonging to section Nigri by PCR assays[J].FEMS Microbiology Letters,2005,245(2):353-361.
[51] HAUGLAND RA,VESPER S.Method of identifying and quantifying specific fungi and bacteria.US Patent No.6387652[P].2001-07-13.
[52] LEBRIHI A,MATHIEU F,BORGIDA L P,et al.Method for the detection of ochratoxin A-or citrinin-producing fungi.European patent No.EP1329521[P].2003-07-23.
[53] DOBSON A,O″CALLAGHAN J.Detection of ochratoxin A producing fungi.Patent No.WO 2004/072224 A2[P].2004-02-12.
[54] MURAKAMI H,YOSHIDA K,YOSHIDA K,et al.Tables of mycological characters of the representative strains of the black aspergilli.Taxonomic studies on Japanese industrial strains of the Aspergillus (Part 30)[J].Journal of the Society of Brewing Japan,1979,74(7):466-470.
[55] POLLASTRO S,DE MICCOLIS R M,FARETTA F.A new semi-selective medium for the ochratoxigenic fungus Aspergillus carbonarius[J].Journal of Plant Pathology,2006,88(1):107-112.