多糖广泛存在于自然界,是一种功能多样的天然大分子物质。从天然植物、真菌中提取的多糖具有抗氧化、抗肿瘤等多种生物活性,并可作为添加剂用于食品工业、生物医学等领域,是用途极其广泛的天然物质[1-3]。多糖由多个单糖分子通过糖苷键连接而成,其分子链长、聚合度大,并且支链多带有羟基,易形成分子间氢键,图1所示为几种常见多糖的糖单元结构。多糖特殊的结构导致其在水中的溶解性较差,部分多糖甚至不溶于水[4-5],改善多糖溶解特性有利于其更广泛的应用。许多从天然药物中提取的活性多糖需溶解在水中才能被人体吸收,继而实现生物活性的表达,如菌核侧耳多糖具有免疫调节与抗肿瘤活性,但该种多糖几乎不溶于水,不易被人体吸收[6],故有必要提高其溶解性。多糖溶解性的改善意味着其亲水性、保水性的提高,这些性质的改善可为多糖赋予更多样的功能,羧甲基淀粉(carboxmethyl starch,CMS)相比原淀粉具有较强的吸水性与溶胀性,可作为高效崩解剂用于药物制剂中[7]。衍生化获得的水溶性羧甲基纤维素(carboxmethyl starch,CMC)则常用于食品加工中,防止食品中水分挥发并提高口感[8]。在工业应用上,多糖溶解性的提高还意味着多糖溶解所需时间与能耗的降低,能减少多糖使用成本,提高其使用便捷性。因此,多糖溶解性改善的研究在科研和工业应用中意义重大。
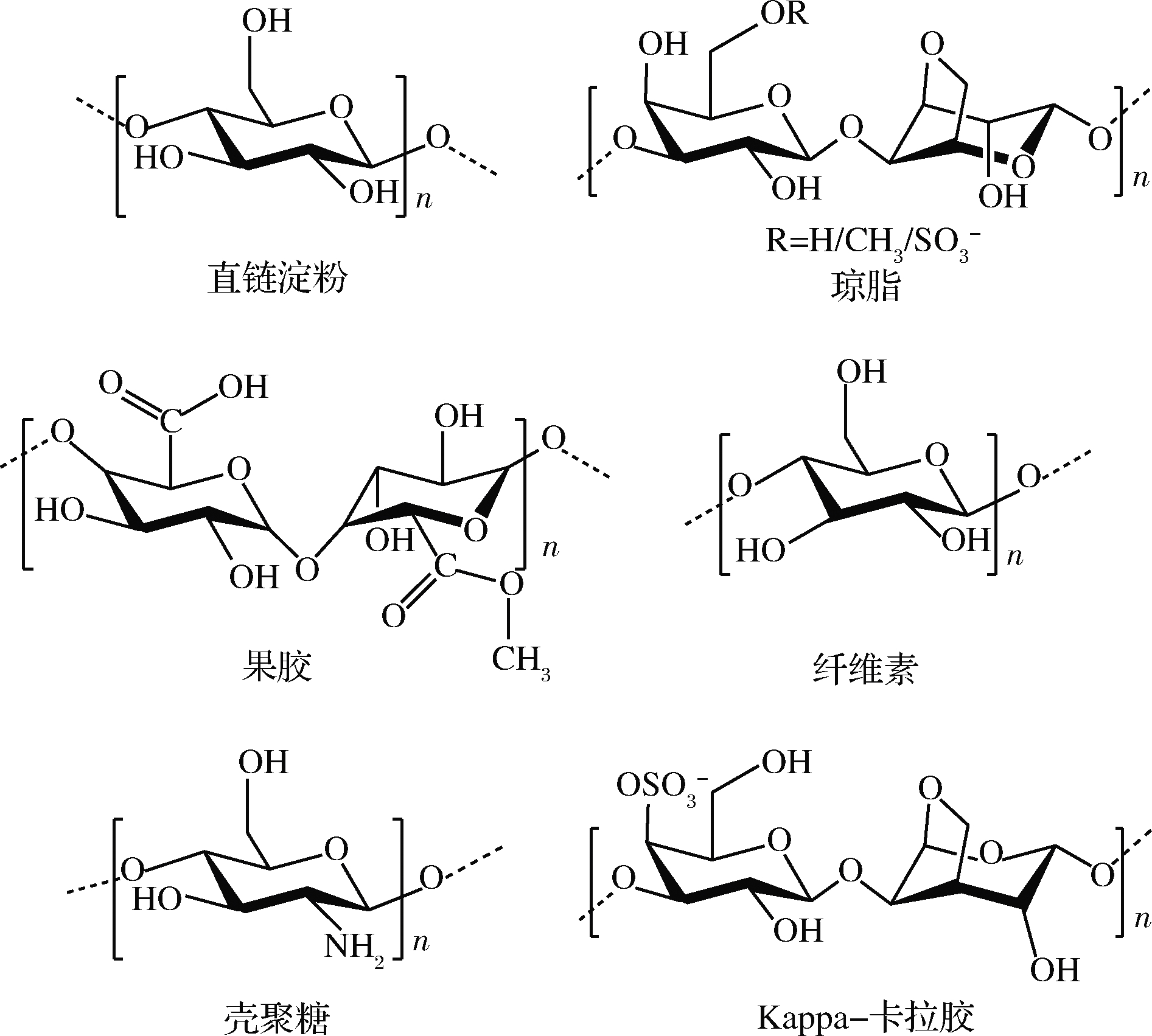
图1 几种常见多糖的糖单元结构
Fig.1 Structure of repeating units of common polysaccharides
大量研究表明,超声处理、酸处理、添加助溶剂、羧甲基化和羟烷基化等方法对改善多糖在水中溶解性具有较好的效果,同时对多糖的生物活性、黏度、凝胶化能力等性质起到一定程度的调控作用,在多糖改性研究中潜力巨大[9-10]。根据其改性特点及其对多糖结构性质影响,本文将其归纳为物理法、降解法和衍生化法三类,并进一步对比改性前后的多糖结构性能变化,考察各类方法优缺点,以期为多糖溶解性改善研究及其工业化应用提供参考依据。
1 物理法
物理法对多糖结构、性质影响较小,且工艺简单、操作灵活,常被用于多糖溶解性改善研究。近年来,多糖的物理改性研究集中于微细化处理与添加助溶剂2种方法。微细化处理是通过高压均质等物理手段对多糖颗粒施加机械作用,以获得粒径小、粒度均匀的颗粒,所获颗粒越小、比表面积越大,其溶解度越高[10]。助溶剂法则通过将多糖与第三组分物理混合的方式,提高多糖的溶解度[11]。
1.1 高压均质处理
高压均质处理是工业常用的微细化处理方法,利用高压作用产生的剪切、撞击和涡旋等机械作用使物料超微细化。高压均质处理对物料施加的强机械作用可显著降低淀粉、纤维素等多糖的颗粒粒径,并改善其颗粒形貌,从而提高其溶解性能。APOSTOLIDIS等[12]通过高压均质设备对淀粉进行改性。由扫描电子显微镜结果看出,均质处理后淀粉平均粒径由7.5 μm降至0.5 μm。随着均质压力的提高,淀粉颗粒表面出现孔隙、沟壑等形貌,颗粒比表面积增大,溶解度提高。侯淑瑶等[13]使用高压均质处理制备纳米级淀粉,在均质压力80 MPa、均质次数25次、淀粉质量浓度3.2 g/100mL条件下获得平均粒径为214.3 nm的椭圆形纳米淀粉颗粒,得率为46.12%,均质后淀粉粒径呈正态分布,均匀性提高,颗粒结构变得疏松、吸水性增强。
高压产生的机械作用使多糖分子间氢键受到破坏,结晶度降低,此外,均质处理带来的均匀化与微细化,还使多糖复配稳定性与相容性提高。SHAHBAZI等[14]将高压均质后的淀粉与卡拉胶复配成膜。改性淀粉与卡拉胶间显示出良好的互溶性,均质处理后,改性淀粉部分结晶峰明显减弱,淀粉结晶度下降,更易于与卡拉胶形成氢键,提高成膜稳定性。LIN等[15]使用不同压力对细菌纤维素进行处理,结果表明,纤维素悬浊液的稳定性及持水性提高,体系的水分逸散速率降低,不易在长期的贮存中失水。
高压均质处理中常通过调节均质压力与处理次数来对物料品质进行调控。工业上一般采取较为温和的均质压力与较少的均质次数对多糖进行处理,以降低机械作用对多糖结构性质的破坏。
1.2 助溶剂法
助溶剂是工业常用的提高特定物质溶解能力的第三类物质,通过与难溶物在溶剂中形成可溶性的分子间络合物或复盐等,增加难溶物在溶剂中的溶解度[16]。使用助溶剂一般可数倍甚至数百倍提高溶质的溶解度。MADGULKAR等[11]使用葡萄糖、果糖等糖类作为水难溶性药物克霉唑的载体,将其溶解度提高至原来的800倍。助溶剂虽能提高溶质的溶解度,但助溶机理较复杂,许多机理至今尚未探明。PARUTA [17]发现助溶剂使溶剂的极性上升,认为助溶剂作用机理与助溶剂对溶剂的极性作用有关。STENNER等[18]研究了蔗糖和多元醇对卡拉胶溶解和凝胶化的影响,提出糖助溶剂作用机理应与体系中的氢键有关。
由于缺乏统一的助溶机理,关于助溶剂的选择尚无清晰明确的规律。常用助溶剂包括易溶的糖、低级醇以及表面活性剂等。用于多糖类物质的助溶剂多根据经验选用,因多糖在醇溶液中会产生沉淀,醇类助溶剂对多糖效果不理想。考虑到多糖分子带有大量羟基,可与助溶剂在氢键的相互作用下发生相互缔合或包覆从而提高溶解度,故通常考虑从易溶的低分子质量糖中筛选多糖的助溶剂。丛峰松[19]将琼脂粉与蔗糖助溶剂混合煮沸后经冻融处理,将琼脂的溶解温度由95 ℃降至80 ℃,溶解时间缩短一半。SMAN[20]对淀粉在蔗糖溶液中溶解度提高这一现象进行解释。证明蔗糖溶液能有效溶解淀粉、影响淀粉的吸水膨胀性能,而多糖的溶胀率与其溶解性和持水性有关,溶胀率的上升说明其溶解度上升。
除传统形式的助溶剂,一些新型助溶剂逐渐为人所关注。XU等[21]使用离子液体作为助溶剂,将室温下的纤维素溶解度由1%提高至15%,纤维素在离子液体中的溶解度取决于氢键接受其阴离子的能力。助溶剂对改善多糖溶解性效果显著且无毒无害、廉价易得,但由于助溶机理尚不明确,今后的研究可侧重于助溶机理的探究与模型建立,减少体系中第三组分的引入,以提高改性多糖的使用范围。
物理法工艺简单灵活,对多糖结构性质影响小,也正因如此,物理法对多糖改性效果较有限,故工业上不建议单独使用物理处理法,而是通过与超声处理、衍生化法结合使用,提高处理效果并降低其他方法的处理压力。
2 降解法
多糖的糖单元一般由糖苷键连接而形成大分子长链,该种结构使得多糖对酸性与强机械作用等环境缺乏耐受性,在这些环境下,糖苷键易被破坏断裂,使多糖分子质量降低、聚合度下降。因低分子质量糖在水中的溶解性更好,通过控制多糖降解的程度以提高其溶解性不失为一种有效的溶解性改善思路。基于此,多糖溶解性改善研究中常使用超声处理与酸处理对多糖进行降解。图2是以纤维素为例的降解示意图。
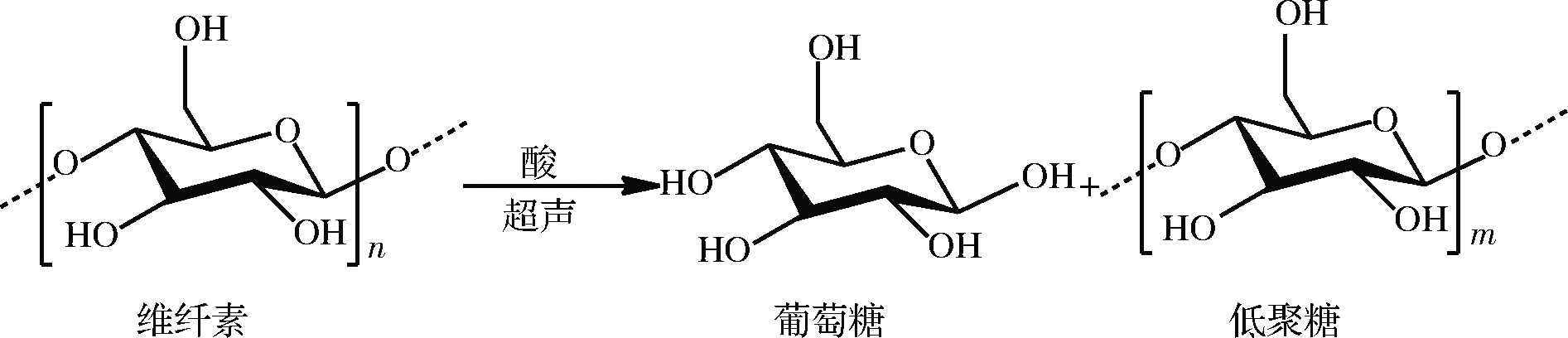
图2 纤维素降解示意图(m<n)
Fig.2 Degradation of cellulose
2.1 超声降解法
超声波频率高、能量大,在传播过程中对介质产生空化效应与自由基效应,由此引起的强机械作用和氧化还原作用使多糖糖苷键断裂,可在中性条件和低温环境下实现多糖降解[22-23]。机械作用对高分子质量多糖效果更显著,而自由基作用对低分子质量多糖更有效,通过控制超声功率强弱与作用时间,对多糖分子链进行较均匀且精细的断裂降解。
超声处理可改变多糖结晶结构,使颗粒变得松散,提高水分与多糖的有效接触,从而提高多糖溶解度与溶胀率。SUJKA等[24]使用20 kHz、170 W的超声波对4种作物淀粉进行处理,发现超声使淀粉颗粒表面出现裂纹。超声处理后,4种淀粉溶解度均出现5%~10%的提高,同时,颗粒吸水性以及溶胀能力提高,糊黏度降低。李公斌[25]研究了黑木耳多糖经超声处理后的性质变化,发现木耳多糖经超声处理后由难溶变为易溶,溶解性随超声作用时间的延长而提高。JAMBRAK等[26]使用24 kHz的超声波对淀粉进行处理,发现超声可破坏淀粉颗粒的结晶区域,使淀粉吸水性增加,从而提高了淀粉颗粒的溶胀能力与溶解度。并且温度条件对超声处理影响显著,70 ℃下处理15 min后的淀粉的溶胀能力比20 ℃下提高4~6倍。
多糖在超声条件下降解的速率常数与其分子质量有关,分子质量越高则降解速率越高。此外,超声降解多糖的分子质量有一定范围,分子质量过低时,超声作用不足以使糖苷键断裂,故超声处理可控制多糖分子质量分布,提高降解均一性。LII等[27]在研究琼脂糖与卡拉胶的超声降解动力学时发现,降解速率常数k与多糖分子质量有关,多糖分子质量越高,降解速率常数越高,并且螺旋交联状态的分子链相对杂乱,前者对超声有更强的抵抗力,故杂乱状态的分子链更易于超声降解。WONG等[28]发现纤维素经超声处理后分子质量和结晶度指数下降。并且超声降解所得产物分子质量分布均匀,最低分子质量在46 kDa左右。
超声降解法工艺简单高效,产物分子质量分布均匀,对降低多糖的溶解温度有一定的效果,但处理后多糖长链在一级结构上受到了破坏,分子质量出现不可逆的下降,对琼脂、卡拉胶等多糖的凝胶性能影响较大。故采用超声处理法改善多糖溶解性时,需根据不同多糖理化性质差异,控制降解程度,以获得最优性质产品。
2.2 酸解法
多糖分子链中的糖苷键对酸不稳定,容易酸解断键,当溶液中的pH低于一定值时,多糖由复杂多聚糖水解还原为低聚糖,分子质量降低。酸解法工艺简单,酸液可多次利用,成本低廉,被大量用于多糖降解研究[29]。
酸处理可降低多糖分子质量,形成溶解性更好的小分子短链,使多糖溶解性提高。夏和咏等[30]将琼脂分散于水中形成悬浊液后,投入适量食品级酸在60~90 ℃条件下处理2~4 h,经过滤、干燥后获得65 ℃溶解的速溶琼脂,溶解温度较改性前降低30 ℃。DOU等[31]使用混酸对壳聚糖热塑性进行改善,发现随着酸浓度的增加,结晶度总体呈下降趋势,说明酸处理能降低壳聚糖分子的有序性,提高溶解性。酸处理后壳聚糖材料水接触角减小,当酸浓度为壳聚糖质量的7.5%以上时,水接触角较原壳聚糖降低5.26%,说明酸处理提高了壳聚糖的亲水性。
多糖在酸中降解的程度与所用酸的强弱和反应温度有关。CHIRAPART等[32]使用H2SO4、草酸、醋酸及柠檬酸对琼脂进行酸解,结果显示,酸处理对琼脂物化性质影响显著,过高的酸浓度与反应温度均会使得降解速率过快,降解程度难以控制,使琼脂性能急剧降低。此外,通过控制酸解程度,可降低琼脂分子中的![]() 含量,提高琼脂品质。杭志喜等[33]对小麦秸秆纤维素的稀酸降解进行了研究,发现酸在降解反应中起催化剂作用,提高酸的质量分数不能提高反应转化率,而应通过提高多糖与酸的有效接触面积来实现。
含量,提高琼脂品质。杭志喜等[33]对小麦秸秆纤维素的稀酸降解进行了研究,发现酸在降解反应中起催化剂作用,提高酸的质量分数不能提高反应转化率,而应通过提高多糖与酸的有效接触面积来实现。
在实际应用中,酸降解工艺不可避免地存在反应器腐蚀、废水处理困难等问题,并且降解后的产物分子质量分布宽、均一性差且分离困难。为解决上述问题,HUANG等[34]采用固体酸催化剂代替液体酸进行酸解反应,减少了废液产生并提高了催化剂的回收率。目前这一思路尚停留于实验室阶段,有待进一步探索。
超声处理与酸处理是较为常用的多糖降解方法,相比酶解法的使用成本更低、操作更简便。但就改善多糖溶解性的途径而言,降解法仍是一种以牺牲多糖分子质量换取水溶性提高的方法,故降解法更适用于对分子质量要求不高的工艺中。
3 衍生化法
衍生化法属于多糖的化学改性手段,通过使用不同的衍生化试剂在多糖支链羟基上接入烷基、羧甲基或羟烷基等基团,实现多糖的特定改性。通过引入亲水性和大位阻基团可降低多糖结晶度,提高溶解性。
3.1 氧化
多糖在氧化剂存在的条件下同时发生支链氧化和主链降解2种反应,含硫酸酯基的多糖还伴有脱硫化反应[35]。图3是以直链淀粉为例的氧化示意图。
支链氧化可引入亲水性的醛基和羧基,主链降解则使多糖分子质量降低,2种反应类型均可提高多糖溶解性,但与支链氧化相比,主链降解反应对多糖分子结构、物化性质影响较显著,故氧化处理一般需抑制主链的降解而促进支链反应。通过对氧化剂和反应条件的调控,可调整多糖分子在氧化过程中2种反应的程度[36]。在低氧化剂浓度与低温条件下主要进行支链羟基的氧化反应,高温和高氧化剂浓度则有利于降低产物分子质量[9]。ZHANG等[35]使用H2O2对琼脂处理,结果显示,氧化琼脂支链硫酸酯基含量降低至0.21%,较改性前降低73.4%,凝胶强度提高30.9%,同时,氧化琼脂分子质量、凝胶溶胶温度、溶解温度降低,白度与凝胶透明度提高。CHEN等[37]使用NaClO作为氧化剂对微晶纤维素进行氧化处理,氧化后微晶纤维素出现更多裂纹,表面更粗糙,氧化微晶纤维素的溶解度由0%提高至78.24%。氧化微晶纤维素与羟丙基淀粉制备成膜后,膜拉伸强度较原纤维素提高249.42%,在水中溶解所需时间缩短至60 s。
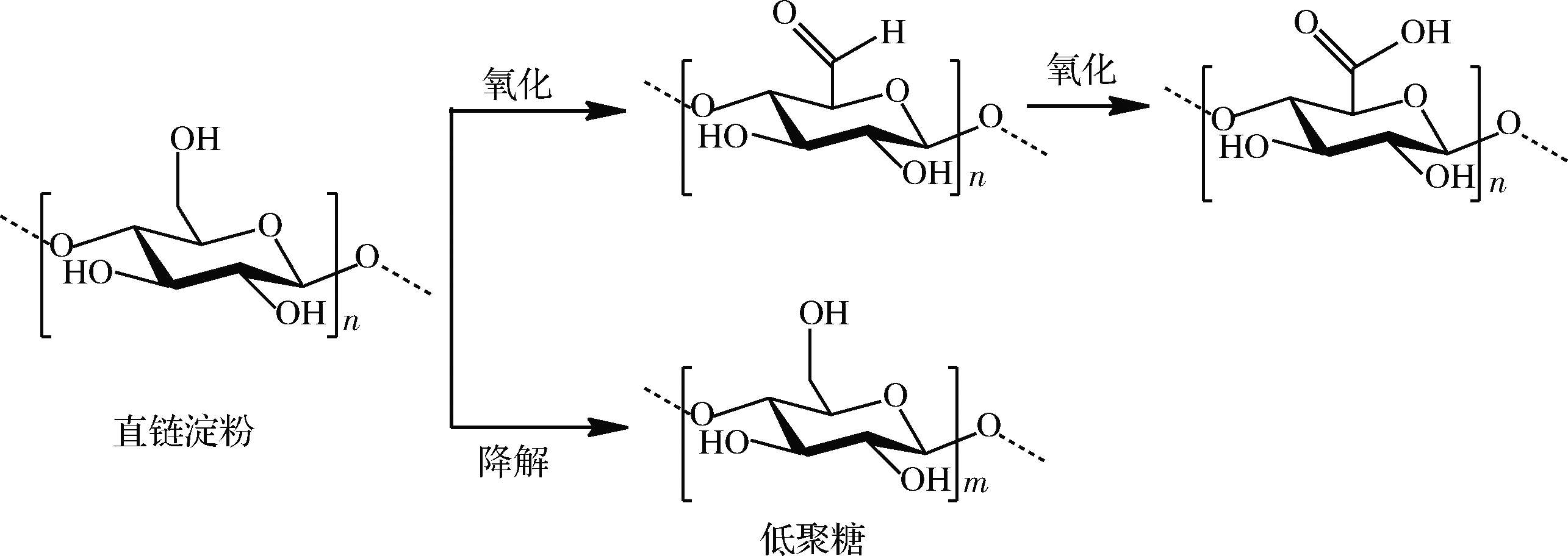
图3 直链淀粉氧化示意图(m<n)
Fig.3 Oxidation of amylose
工业上常用低浓度的NaClO和H2O2进行氧化反应,氧化程度易于调控,同时可利用氧化剂破坏反应物中的发色基团,提高产物的白度品质。陈会景等[38]用H2O2为氧化剂制备氧化琼脂,在80 ℃、4 h以及0.2%(体积分数)H2O2用量下,将琼脂粉末白度由54%提高至58%。李晓文等[39]通过正交实验法对H2O2漂白马铃薯淀粉工艺进行优化,将淀粉白度提高3%~10%。所获最优工艺条件为H2O2的用量为4%(体积分数), 漂白时间为50 min,温度40 ℃,料液pH值为6,此条件下淀粉性质无明显变化。
氧化工艺简单有效,在改善多糖溶解性的同时还可提升材料的抗菌性[36]、抗氧化性等性能,但对大部分植物多糖而言,其糖单元上的氧化可接入位点少,支链与主链反应程度难以精细调控,氧化反应稳定性和重复性有待进一步提高。
3.2 羧甲基化
多糖支链羟基经碱活化后,与羧甲基化试剂进行醚化反应,可实现在多糖分子支链上引入羧甲基的目的。琼脂羧甲基化反应示意如图4所示,羧甲基化可发生在1~4位的羟基上。
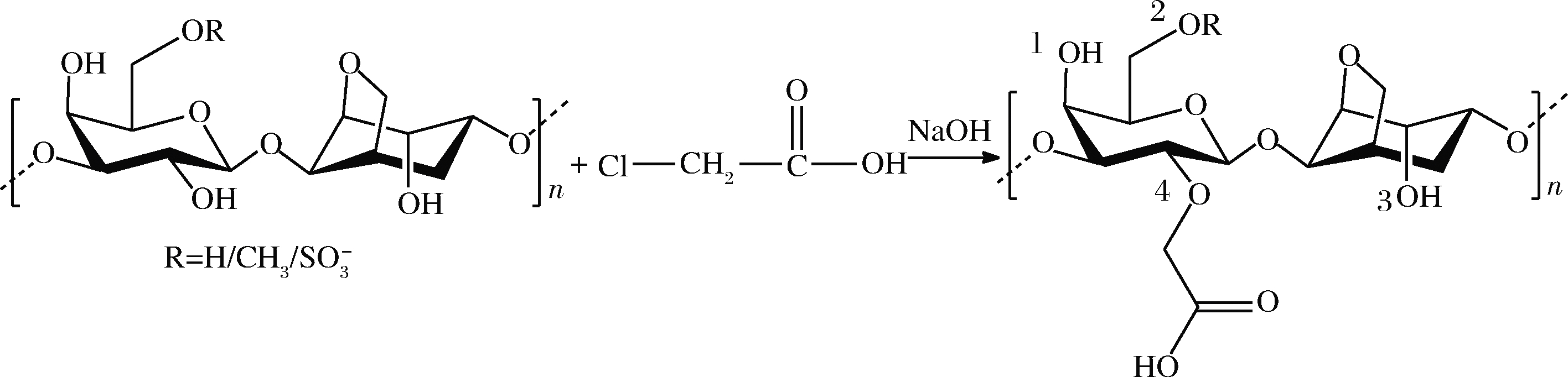
图4 琼脂羧甲基化示意图
Fig.4 Carboxymethylation of agar
由于羧基优异的亲水性和空间位阻作用,羧甲基化可有效减少分子内氢键的形成,极大提高多糖溶解性。CAO等[40]制备了不同取代度的羧甲基琼脂并对其性能进行了研究,发现随着取代度的上升,羧甲基琼脂的溶解温度逐渐下降,取代度为0.495时,溶解温度降低至44 ℃。此外,羧甲基琼脂的凝胶溶胶温度、凝胶强度以及溶液表观黏度下降,凝胶弹性和吸湿性提高。CHAUDHARY等[41]通过微波辅助合成羧甲基琼脂糖。发现羧甲基化取代度>0.69的样品可在室温条件下溶解,并在7 ℃以下凝胶。羧甲基化琼脂糖颗粒表面孔道增多,有利于水分子进入。魏红[42]对黑木耳多糖进行羧甲基化修饰,衍生化后,黑木耳多糖溶解度由0.1 mg/mL提高至0.6 mg/mL,此外,相对未改性的黑木耳多糖,羧甲基多糖对羟自由基、1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)自由基、2,2′-联氮-双-3-乙基苯并噻唑啉-6-磺酸[2,2′-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS]自由基表现出一定的清除作用,说明羧甲基多糖抗氧化活性提高。
取代度是衡量衍生化程度的重要指标,其数值大小间接反映了改性多糖的溶解性高低,如何在不对多糖性质造成明显破坏的条件下获取高取代度是羧甲基化工艺研究的主要目的。![]() 等[43]研究了淀粉非均相羧甲基化反应中的物料配比、反应时间、反应温度等参数对羧甲基淀粉取代度的影响,发现反应温度对取代度影响最大,58 ℃下取代度最高,此外,NaOH质量比、反应体系中的乙醇含量以及反应时间存在最优值。GE等[44]通过微波辅助合成羧甲基壳聚糖,发现微波作用可显著提高羧甲基化反应速率,将反应时间缩短至30 min以内,所得最优反应条件为氯乙酸与壳聚糖质量比为8∶1,碱化时间2 h,反应温度100 ℃,微波功率为260 W,该条件下取代度为0.85。
等[43]研究了淀粉非均相羧甲基化反应中的物料配比、反应时间、反应温度等参数对羧甲基淀粉取代度的影响,发现反应温度对取代度影响最大,58 ℃下取代度最高,此外,NaOH质量比、反应体系中的乙醇含量以及反应时间存在最优值。GE等[44]通过微波辅助合成羧甲基壳聚糖,发现微波作用可显著提高羧甲基化反应速率,将反应时间缩短至30 min以内,所得最优反应条件为氯乙酸与壳聚糖质量比为8∶1,碱化时间2 h,反应温度100 ℃,微波功率为260 W,该条件下取代度为0.85。
羧甲基化研究起步早,现有工艺已较为成熟,羧甲基淀粉、羧甲基壳聚糖、羧甲基纤维素等多糖衍生物的制备已实现工业化。羧甲基化对降低多糖黏度、溶解温度效果显著,并可提高多糖的成膜特性、抗氧化性等性质。羧甲基化法存在的不足在于羧甲基之间形成氢键作用弱于羟基氢键,且羧甲基空间位阻作用会阻碍多糖链的相互交联,影响琼脂、卡拉胶一类多糖的凝胶性能。故多糖改性实际应用中不宜一味追求高取代度,而应综合多糖自身性质来选择工艺。
3.3 羟烷基化
羟烷基化是在多糖羟基氧原子上引入烷基和羟基,生成醚类化合物的反应过程。与羧甲基化类似,羟烷基具有较强的亲水性与空间位阻作用,可提高多糖分子的亲水性并降低其结晶度和有序性,使颗粒松散,易于水分渗入[45]。纤维素羟乙基化反应原理如图5所示,由于所接入的羟乙基羟基上的化学环境与原羟基相似,故羟乙基羟基上可再进行羟乙基化反应。
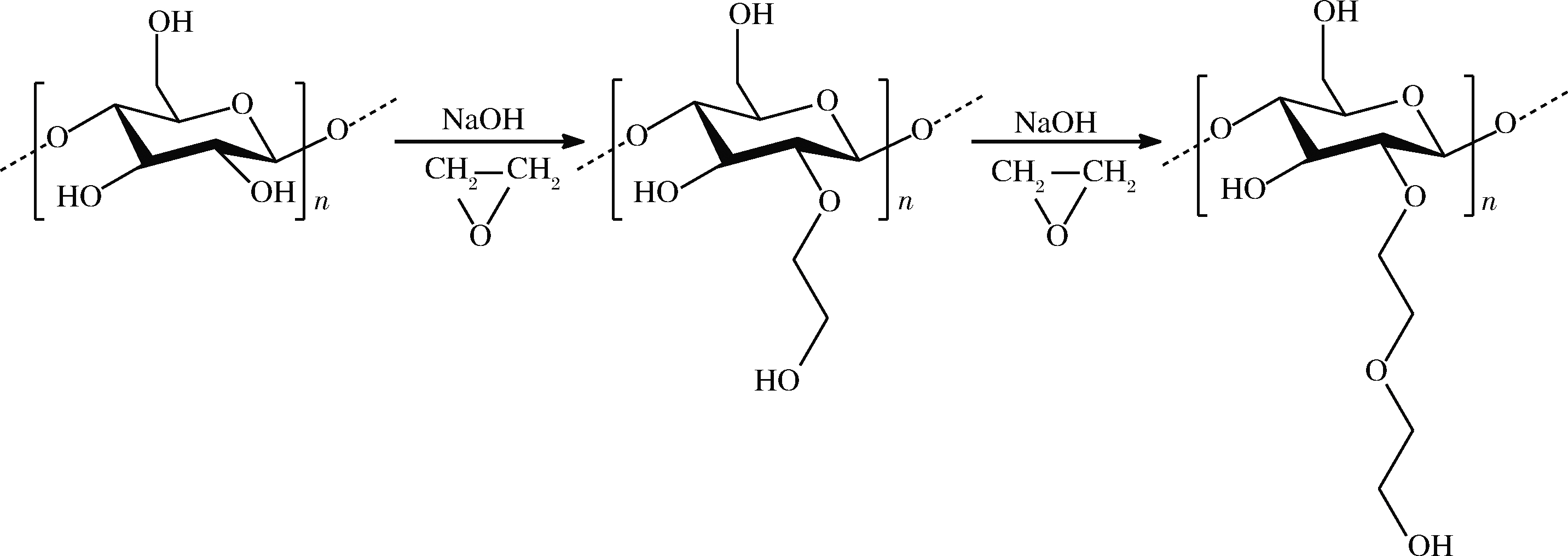
图5 纤维素羟乙基化反应示意图
Fig.5 Hydroxylalkylation of cellulose
ZHANG等[46]以环氧丙烷为醚化剂,制备出了不同取代度的羟丙基琼脂,随着取代度的上升,羟丙基琼脂溶解温度、凝胶溶胶温度以及凝胶强度下降,获得羟丙基琼脂最高摩尔取代度为0.557,溶解温度由改性前的90 ℃降至80 ℃。LAWAL[47]对淀粉的羟丙基化进行了研究,发现随着环氧丙烷用量的提高,淀粉溶解度、溶胀能力提高,溶液浊度下降。羟丙基的空间位阻效应可减少淀粉粘结与成链交联,同时使得淀粉颗粒变得松散,溶胀容量提高。当取代度为0.16时,溶解度提高5%~10%。ZHOU等[48]以均相反应体系合成了羟乙基纤维素,当摩尔取代度>0.57时,羟乙基纤维素表现出明显的水溶性,并形成高黏度溶液。由13C核磁共振谱图分析可知,糖单元上C-2、C-6位上的取代度高于C-3位,说明受羟烷基空间位阻的影响,取代更易于发生在位阻小的碳原子上。
羟烷基化形成的醚键稳定性高,在水解、氧化、羧甲基化反应过程中不易断裂,受电解质和pH影响小,改性后的多糖能被进一步用于衍生化、氧化降解等改性过程,能适应造纸、纺织、食品工程、生物医药的要求[49]。ZHANG等[50]通过羟烷基化法将琼脂糖的凝胶化温度由36 ℃降至30 ℃以下,提高了琼脂糖在热敏性生物活性研究领域的应用性。HU等[51]将壳聚糖与羟丁基壳聚糖经过物理混合后真空冷冻干燥处理,获得一种多孔海绵状结构。该种结构孔隙率高(约85%)并具有优异的抗菌性能,相对单一壳聚糖材料,混合后海绵结构的吸水率提高25倍,由大鼠体内试验证明,强亲水性有助于该材料吸收血液中的湿分,促进血液凝结,说明羟丁基材料可用于促进伤口愈合。SIMON等[52]研究了羟丙甲纤维素与羟丙基淀粉复合膜的流变学性能,指出淀粉与纤维素相容性较差,羟丙基化改性后可提升两者相容性。
衍生化法改善多糖溶解性效果显著,根据需要还可对多糖黏度、凝胶透明度、凝胶溶胶温度等性质进行针对性调控,是一种极具潜力的多糖改性方法。但另一方面,衍生化法多采用非均相反应体系,由于涉及扩散传质影响,反应时存在取代不均匀问题,使多糖起始溶解温度与完全溶解温度区间大,溶解耗时长。该缺陷长期为科研人员所忽略,亟待解决。
4 结语
综上,物理法、降解法和衍生化法均可改善多糖溶解性,所述工艺出发点多为降低颗粒直径、降解获得溶解性的小分子糖或引入亲水性基团,涉及多糖结构与官能团的改变,对多糖物化性质影响也各有不同。就研究现状来看,所提及的工艺尚存在一定局限性,故针对目前存在的问题提出几个研究方向以供探讨。
(1)探明多糖改性机理:目前的改性研究仅停留于可确定一种工艺对改善多糖溶解性有效,其效果缘何机理尚未完全探明。如衍生化法处理后多糖普遍存在分子质量降低、结晶度下降以及颗粒形貌改变等性质变化,溶解性的提升可能是其中多种缘由共同作用的结果,对改性机理的探究可为后续的研究和应用提供基本理论支持。
(2)反应程度的精确调控:多糖改性质量的调控基本只能通过调整反应基本参数实现,对涉及多糖结构变化的反应难以精确调控,例如羟丙基化时,在羟丙基的羟基位上仍可进行接枝反应,其衍生化程度难以调控。对反应特性进行深入研究有利于实现对多糖品质的控制与调整,提高反应稳定性。
(3)提高非均相反应的均一性:多糖改性反应多采用固液非均相反应体系,反应过程涉及反应液在颗粒内外的传质传热以及颗粒直径的变化,由于缺乏对该种非均相反应特性的认识,多糖改性效果稳定性差,取代、降解程度不均匀。故建立相应的反应与传质模型,探明多糖反应过程中传质传热与反应特性,对扩大该改性方法的使用范围以及实现工业化有重要意义。
[1] GONG P, WANG S, LIU M, et al.Extraction methods, chemical characterizations and biological activities of mushroom polysaccharides:A mini-review[J].Carbohydrate Research, 2020, 494:108 037.
[2] KAKAR M U, NAVEED M, SAEED M, et al.A review on structure, extraction, and biological activities of polysaccharides isolated from Cyclocarya paliurus (Batalin) Iljinskaja[J].International Journal of Biological Macromolecules, 2020, 156:420-429.
[3] KHALIL H P S A, SAURABH C K, TYE Y Y, et al.Seaweed based sustainable films and composites for food and pharmaceutical applications:A review[J].Renewable & Sustainable Energy Reviews, 2017, 77:353-362.
[4] TORRES P, SANTOS J P, CHOW F, et al.A comprehensive review of traditional uses, bioactivity potential, and chemical diversity of the genus Gracilaria (Gracilariales, Rhodophyta)[J].Algal Research, 2019, 37:288-306.
[5] RAMASAMY U R, GRUPPEN H, KABEL M A.Water-holding capacity of soluble and insoluble polysaccharides in pressed potato fibre[J].Industrial Crops and Products, 2015, 64:242-250.
[6] LIU Y, MEI H, SU Y, et al.Inhibitory effects of Pleurotus tuber-regium mycelia and bioactive constituents on LPS-treated RAW 264.7 cells[J].Journal of Functional Foods, 2014, 7:662-670.
[7] 张立军, 高俊刚.玉米羧甲基淀粉崩解剂的合成及性能改进[J].化学世界, 2004, 45 (10):537-539.
ZHANG L J, GAO J G.Synthesis and properties of carboxymethyl corn starch[J].Chemical World,2004,45(10):537-539.
[8] 张丽平, 余晓琴.羧甲基纤维素钠(CMC)在食品工业应用的情况和研究动态[J].中国食品添加剂, 2006(1):118-125.
ZHANG L P, YU X Q.Application of CMC in food industry and its development[J].China Food Additives, 2006(1):118-125.
[9] 陈蕾, 吴皓.多糖降解方法的研究进展[J].中华中医药学刊, 2008, 26 (1):133-135.
CHEN L, WU H.Research advances in degradation of polysaccharides[J].Chinese Archives of Traditional Chinese Medicine, 2008,26(1):133-135.
[10] SARFRAZ R M, BASHIR S, MAHMOOD A, et al.Application of various polymers and polymers based techniques used to improve solubility of poorly water soluble drugs:A review[J].Acta Poloniae Pharmaceutica, 2017, 74 (2):347-356.
[11] MADGULKAR A, BANDIVADEKAR M, SHID T, et al.Sugars as solid dispersion carrier to improve solubility and dissolution of the BCS class II drug:Clotrimazole[J].Drug Development & Industrial Pharmacy, 2016, 42 (1):28-38.
[12] APOSTOLIDIS E, MANDALA I.Modification of resistant starch nanoparticles using high-pressure homogenization treatment[J].Food Hydrocolloids, 2020, 103:105 677.
[13] 侯淑瑶, 代养勇, 刘传富, 等.高压均质法制备甘薯纳米淀粉及其表征[J].食品工业科技, 2017, 38 (12):233-238;242.
HOU S Y, DAI Y Y, LIU C F, et al.Preparation and characterization of sweet potato starch nanoparticles by high pressure homogenization[J].Science and Technology of Food Industry,2017,38(12):233-238;242.
[14] SHAHBAZI M, MAJZOOBI M, FARAHNAKY A.Physical modification of starch by high-pressure homogenization for improving functional properties of κ-carrageenan/starch blend film[J].Food Hydrocolloids., 2018, 85:204-214.
[15] LIN D, LI R, LOPEZ-SANCHEZ P, et al.Physical properties of bacterial cellulose aqueous suspensions treated by high pressure homogenizer[J].Food Hydrocolloids., 2015, 44:435-442.
[16] JOUYBAN A.Review of the cosolvency models for predicting solubility of drugs in water-cosolvent mixtures[J].Journal of Pharmacy & Pharmaceutical Sciences, 2008, 11 (1):32-58.
[17] PARUTA A N.Solubility of several solutes as a function of the dielectric constant of sugar solutions[J].Journal of Pharmaceutical Sciences, 1964, 53 (10):1 252-1 254.
[18] STENNER R, MATUBAYASI N, SHIMIZU S.Gelation of carrageenan:Effects of sugars and polyols[J].Food Hydrocolloids, 2016, 54:284-292.
[19] 从峰松.速溶琼脂的制备方法:中国,CN1793184A[P].2005-12-29.
CONG F S.Preparation of instant agar:China, CN1793184A[P].2005-12-29.
[20] SMAN R G M V D.Theoretical investigation of the swelling of polysaccharide microgels in sugar solutions[J].Food & Function, 2018, 9 (5):2 716-2 724.
[21] XU A, ZHANG Y, ZHAO Y, et al.Cellulose dissolution at ambient temperature:Role of preferential solvation of cations of ionic liquids by a cosolvent[J].Carbohydrate Polymers, 2013, 92 (1):540-544.
[22] 马晓彬, 张丽芬, 徐玉亭, 等.多糖超声物理改性的研究进展[J].中国食品学报, 2015, 15 (10):163-169.
MA X B, ZHANG L F, XU Y T.Research progress on the application of ultrasound technology in physical modification of polysaccharides[J].Journal of Chinese Institute of Food Science and Technology,2015,15(10):163-169.
[23] ![]() S, STASZEWSKA D U.Kinetics of ultrasonic degradation and polymerisation degree distribution of sonochemically degraded chitosans[J].Carbohydrate Polymers, 2004, 56 (4):489-498.
S, STASZEWSKA D U.Kinetics of ultrasonic degradation and polymerisation degree distribution of sonochemically degraded chitosans[J].Carbohydrate Polymers, 2004, 56 (4):489-498.
[24] SUJKA M, JAMROZ J.Ultrasound-treated starch:SEM and TEM imaging, and functional behaviour[J].Food Hydrocolloids., 2013, 31 (2):413-419.
[25] 李公斌.黑木耳多糖分子修饰及功能与应用研究[D].哈尔滨:东北林业大学, 2006.
LI G B.Application, function, and molecular modification of Auricularia auricula[D].Harbin:Northeast Forestry University,2006.
[26] JAMBRAK A R, HERCEG Z, ![]() D, et al.Ultrasound effect on physical properties of corn starch[J].Carbohydrate Polymers, 2010, 79 (1):91-100.
D, et al.Ultrasound effect on physical properties of corn starch[J].Carbohydrate Polymers, 2010, 79 (1):91-100.
[27] LII C H, CHEN C H, YEH A I, et al.Preliminary study on the degradation kinetics of agarose and carrageenans by ultrasound[J].Food Hydrocolloids., 1999, 13 (6):477-481.
[28] WONG S S, KASAPIS S, HUANG D.Molecular weight and crystallinity alteration of cellulose via prolonged ultrasound fragmentation[J].Food Hydrocolloids, 2012, 26 (2):365-369.
[29] WANG Y Z, ZHANG X H, ZHANG J H.New insight into the kinetic behavior of the structural formation process in agar gelation[J].Rheologica Acta, 2013, 52 (1):39-48.
[30] 夏和咏, 邹辉, 夏静.一种低温速溶琼脂的精制方法:中国,CN108264584A[P].2018-01-31.
XIA H Y, ZOU H, XIA J.A refining method of low temperature instant agar:China,CN108264584A[P].2018-01-31.
[31] DOU X Y, LI Q, WU Q X, et al.Effects of lactic acid and mixed acid aqueous solutions on the preparation, structure and properties of thermoplastic chitosan[J].European Polymer Journal, 2020, 134:109 850.
[32] CHIRAPART A, OHNO M, UKEDA H, et al.Effects of partial acid hydrolysis on physical and chemical properties of agar from a newly reported Japanese agarophyte (Gracilariopsis lemaneiformis)[J].Journal of Applied Phycology, 1997, 9 (1):73-76.
[33] 杭志喜, 崔海丽.稀酸降解植物纤维素的研究[J].安徽工程科技学院学报(自然科学版), 2005, 20 (2):16-19.
HANG Z X, CUI H L.Degrading plant cellulose by thin acid[J].Fournal of Anhui University Of Technology and Science(Natural Science),2005,20(2):16-19.
[34] HUANG Y B, FU Y.Hydrolysis of cellulose to glucose by solid acid catalysts[J].Green Chemistry, 2013, 15 (5):1 095-1 111.
[35] ZHANG C, AN D, XIAO Q, et al.Preparation, characterization, and modification mechanism of agar treated with hydrogen peroxide at different temperatures[J].Food Hydrocolloids, 2020, 101:105 527.
[36] ZHU M J, GE L M, LYU Y B, et al.Preparation, characterization and antibacterial activity of oxidized κ -carrageenan[J].Carbohydrate Polymers, 2017, 174:1 051-1 058.
[37] CHEN J, CHEN F S, MENG Y H, et al.Oxidized microcrystalline cellulose improve thermoplastic starch-based composite films:Thermal, mechanical and water-solubility properties[J].Polymer, 2019, 168:228-235.
[38] 陈会景, 付爽, 林坤辉, 等.过氧化氢氧化琼脂的制备及其性能表征[J].食品安全质量检测学报, 2018, 9 (8):1 893-1 900.
CHEN H J, FU S, LIN K H, et al.Preparation and properties of oxidized agar with H2O2 treatment[J].Journal of Food Safety & Quality,2018,9(8):1 890-1 900.
[39] 李晓文, 熊兴耀.双氧水在超细化马铃薯淀粉漂白工艺中的应用[J].食品科技, 2007, 54 (7):54-57.
LI X W, XIONG X Y.Study on bleach technics for micronization potato starch by using H2O2[J].FOOD SCIENCE AND TECHNOLOGY,2007,7:54-57.
[40] CAO M Z, LIU X, LUAN J M, et al.Characterization of physicochemical properties of carboxymethyl agar[J].Carbohydrate Polymers, 2014, 111:449-455.
[41] CHAUDHARY J P, KONDAVEETI S, GUPTA V, et al.Preparation and functional evaluation of agarose derivatives[J].Journal of Applied Polymer Science, 2014, 131 (16):1-10.
[42] 魏红.黑木耳多糖的羧甲基化修饰及抗氧化活性研究[D].镇江:江苏大学, 2010.
WEI H.Carboxymethylated derivative and their antioxidant activities of polysaccharides from Auricularia auricular[D].Zhenjiang:Jiangsu University,2010.
[43] ![]() S.Synthesis of carboxymethyl starch[J].Starch-Stãrke, 2000, 52 (11):413-419.
S.Synthesis of carboxymethyl starch[J].Starch-Stãrke, 2000, 52 (11):413-419.
[44] GE H C, LUO D K.Preparation of carboxymethyl chitosan in aqueous solution under microwave irradiation[J].Carbohydrate Research, 2005, 340 (7):1 351-1 356.
[45] KAUR L, SINGH N, SINGH J.Factors influencing the properties of hydroxypropylated potato starches[J].Carbohydrate Polymers, 2004, 55 (2):211-223.
[46] ZHANG X, LIU X, CAO M, et al.Preparation of hydroxypropyl agars and their properties[J].Carbohydrate Polymers, 2015, 129:87-91.
[47] LAWAL O S.Starch hydroxyalkylation:Physicochemical properties and enzymatic digestibility of native and hydroxypropylated finger millet (Eleusine coracana) starch[J].Food Hydrocolloids, 2009, 23 (2):415-425.
[48] ZHOU J P, QIN Y, LIU S L, et al.Homogenous synthesis of hydroxyethylcellulose in NaOH/urea aqueous solution[J].Macromolecular Bioscience, 2005, 6 (1):84-89.
[49] 张本山, 余欢, 汪建平, 等.羟丁基化水平对玉米淀粉理化性质的影响[J].现代食品科技, 2014, 30 (12):85-91.
ZHANG B S, YU H, WANG J P, et al.Effects of the degree of substitution during hydroxybutylation on the physicochemical characteristics of maize starch[J].Modern Food Science & Technology,2014,30(12):85-91.
[50] ZHANG N, WANG J L, YE J, et al.Oxyalkylation modification as a promising method for preparing low-melting-point agarose[J].International Journal of Biological Macromolecules, 2018, 117:696-703.
[51] HU S H, BI S C, YAN D, et al.Preparation of composite hydroxybutyl chitosan sponge and its role in promoting wound healing[J].Carbohydrate Polymers, 2018, 184:154-163.
[52] SIMON G, ZHANG N, LIU H, et al.Rheological and gel properties of hydroxypropyl methylcellulose/hydroxypropyl starch blends[J].Colloid & Polymer Science, 2015, 293:229-237.