3D打印是一种基于材料的逐层沉积形成三维结构的辅助制造技术,与传统制造技术不同,它可以方便地获得所需产品的辅助制造技术。3D打印所进行的复杂对象的快速制造,特别是不受设计复杂性的影响,在新的未经测试的几何设计中提供了巨大的潜力[1]。
在食品设计和生产领域,3D打印具有成本低、简单和快速的原型优势。原材料是决定3D食品打印质量的决定因素,它应该是可食用的,且具有可接受的可塑性。
由于材料特性是3D打印产品质量的重要基础,对3D食品打印适用材料理论研究的不足制约了该技术在食品领域的发展。用于3D食品打印的材料包括面团、巧克力和奶酪等[2-3]。FENG等[4]揭示了豌豆蛋白对马铃薯淀粉基3D打印材料在颗粒结构、晶体结构、化学结构、结构特性和热性能方面的影响。LIU等[5]研究了土豆泥的流变特性和3D打印适应性。然而现有的研究大多集中在用于3D食品打印(如面团)混合材料的表观特性上。为了扩大适用于3D打印的材料,有必要对材料的各种理化结构特性进行深入研究。淀粉具有来源广泛、价格便宜、无毒无害等优势[6-8],作为主食、装饰、调味品皆可。同时它也是很好的食品基材,方便和其他食品组分混合成型,并通过3D打印这一加工手段可以制得丰富多彩的食品产品,故本试验采用淀粉作为3D打印原料。
本试验以马铃薯淀粉、小麦淀粉和玉米淀粉为3D打印材料,对产品的加工性能和质量进行了研究。采用外观形态、颜色、黏度、碘吸收光谱、傅里叶变换红外光谱 (fourier transform infrared spectroscopy, FT-IR)、质构分析和微观结构等理化性质和结构特征对产品质量进行评价,以寻找最适合进行3D打印的单一淀粉原料。
1 材料与方法
1.1 实验材料
玉米淀粉,上海风味实业有限公司;新鲜的马铃薯(Favorita)、小麦面粉,购于超市;采用水洗法提取小麦淀粉;按照CORREA等[3]描述的方法提取淀粉。所有提取的湿淀粉在(45±0.3)℃下热风干燥48 h后进一步利用。
1.2 仪器与设备
3D食品打印机,Shinnove-S2 customized, Shinnove scientific and technical Co. Ltd., Hangzhou, China;TA-XT Plus质构仪,Stable Micro Systems Ltd., Surrey,UK;SEM-450扫描电镜,Thermo Fisher Scientific Inc., Oregon;Vetex70傅里叶红外光谱, Bruker Co., Germany;CR-310色差计,Minolta Co. Tokyo, Japan; RVA-Techmaster快速黏度分析仪,Perten Co., Sweden。
1.3 样品制备
分别将每种淀粉与蒸馏水按照1∶4的质量比,于混合水浴中加热。在80 ℃下搅拌40 min,保证100%的淀粉糊化。
1.4 3D打印
在本研究中使用高温定制版3D食品打印机。选择1.2 mm的塑料喷嘴。挤出柱温度为45 ℃,单层高度为0.7 mm,喷嘴移动速度为30 mm/s。本实验3D打印的模型为剑龙。用游标卡尺测量了剑龙打印产品的长度、宽度和高度。每一批至少重复3次。
1.5 质构分析
利用质构仪 (TA-XT Plus,Stable Micro Systems Ltd., Surrey,UK)对在饱和NaCl溶液的氛围中平衡了不同贮存期 (0、 6、 24 h) 的打印样品进行了全质构分析(texture profile analysis, TPA)。试验采用圆柱形探头 (P/0.5R),将样品压缩到初始高度的25% (1.00 mm),然后用5 kg的测力传感器以1 mm/s的十字头速度减压。TPA测量由2个压缩/解压缩周期组成,以1 mm/s的速率间隔5 s。记录的TPA指标为硬度、弹性和凝聚力。对每一批进行3次测量。
1.6 扫描电镜
通过扫描电镜(scanning electron microscope, SEM)扫描经过糊化后和打印后产品的微观结构。将冻干后的淀粉和3D打印的样品粉末用导电两面胶纸固定在样品座上,使用真空镀膜仪喷镀导电层,然后在加速电压5 kV,放大 5 000倍下进行电镜观察。
1.7 傅里叶红外光谱分析仪(fourier transform infrared spectroscopy,FT-IR)分析
FT-IR设备用于测定样品图谱。糊化和打印后淀粉在波长4 000~400 cm-1范围内的红外光谱,温度为(20±0.2)℃, 使用KBr的光谱作为背景。此外,通过仪器软件除去KBr的背景效应。将冻干样品粉末 (3 mg) 与KBr (300 mg) 混合并在研钵中研磨成细粉,然后将其压成切片。每批次测量3次以进行统计分析。
1.8 碘吸收光谱和蓝值
蓝色值 (BV) 和碘结合波长最大值 (λmax)根据KLUCINEC[9]的方法测定。将每种原淀粉、糊化后和3D打印后的淀粉样品(40 mg) 分散在含有10%尿素的10.0 mL DMSO中10 min。然后将样品分散在沸水浴中20 min并迅速冷却至室温 (25 ℃)。取试样 (1.0 mL) 加入12 mL I2-KI水溶液 (2.0 mg I2/mL和20.0 mg KI/mL) 于100 mL容量瓶中,用蒸馏水将混合物定容至100 mL并立即混匀。使用分光光度计从400~700 nm扫描所有样品。记录635 nm (λmax) 和520 nm的吸光度,重复测量3次。
1.9 颜色测定
使用色差计 (CR-310,Minolta Co.) 进行颜色测试。使用白板校准后,可以得到样品的L*(亮度)、a*(红度)和b*(黄度)。以原淀粉作为参照,重复测量10次。通过公式 (1) 计算与颜色坐标的色差 (ΔE):
(1)
1.10 快速黏度分析
用快速黏度分析仪 (RVA-Techmaster, Perten Co., Sweden)对所有原淀粉的糊化特性进行评价。将3.0 g淀粉置于RVA样品罐中并加入25 g蒸馏水,使用AACC 61-02.01(美国临床化学协会)预编译的参数[10]。
1.11 数据分析
用社会科学SPSS 18.0软件包 (IBM, Chicago, IL, U.S.A) 进行统计分析,并用单向ANOVA和Duncan多重比较法确定变量在95%置信水平下对均值是否有显著影响。此外,使用OriginPro 8.5 (OriginLab,Northampton,U.S.A.)绘制所有的统计图形。
2 结果与讨论
2.1 3D打印产品的形态分析
使用马铃薯、小麦和玉米淀粉经3D打印后的剑龙如图1所示。
小麦和玉米淀粉打印模型显示出相对完整的形态结构,具有明显的模型边缘和更好的准确性。然而马铃薯淀粉打印的模型边缘由于黏连而发生变形。由于淀粉的黏度和糊化的影响,由小麦和玉米淀粉制作的模型也比由马铃薯更光滑。较高的黏度和较快的糊化速率会增加挤出和成型的难度,并使得样品黏附在3D打印机的内壁上。
打印样本的准确度越高,产品的质量越好。本试验目标CAD模型的长度、宽度和高度分别为70.90、 28.90和10.00 mm。如表1所示,小麦淀粉样品尺寸为70.89、25.74和10.15 mm。相比之下,与CAD模型相比,通过马铃薯和玉米淀粉打印的样品尺寸发生略微收缩。产品中也出现一些空洞,同时剑龙脊柱的边界并不明显。而马铃薯淀粉制备的产品由于易回生和黏度高,其差异更显著。如前所述,较高的黏度会使物料由于黏粘而难以挤出,淀粉的回生会从聚合物网络中排出水而产生脱水收缩,从而缩小打印样品的体积尺寸[10-12]。

a-马铃薯淀粉;b-小麦淀粉;c-玉米淀粉
图1 使用3种淀粉的打印样品
Fig.1 Printed samples using three kinds of starches
(比例尺均为10 mm长)
表1 三种淀粉3D打印模型与CAD模型的尺寸
Table 1 3D structures analysis of samples using three
kinds of starches

样品长/mm宽/mm高/mm模型70.9028.7010.00马铃薯淀粉70.12±0.07d25.29±0.05d10.14±0.05b小麦淀粉70.89±0.05a25.74±0.03b10.15±0.02b玉米淀粉70.42±0.03c25.62±0.02c10.28±0.03a
注:P<0.05水平下,同一列中具有不同字母的值显著不同(下同)
2.2 3D打印对淀粉碘蓝值的影响
淀粉的碘结合通常用于估计淀粉样品中直链淀粉的含量。较高的BV表明直链淀粉含量较高[13]。与原淀粉相比,糊化会增加淀粉的BV。此外,由于挤出过程影响,打印过程也会增加BV(表2)。
表2 三种原淀粉、糊化后与打印后淀粉的碘蓝值
Table 2 Iodine absorbance spectrum parameters of
starches, for a single starch batch
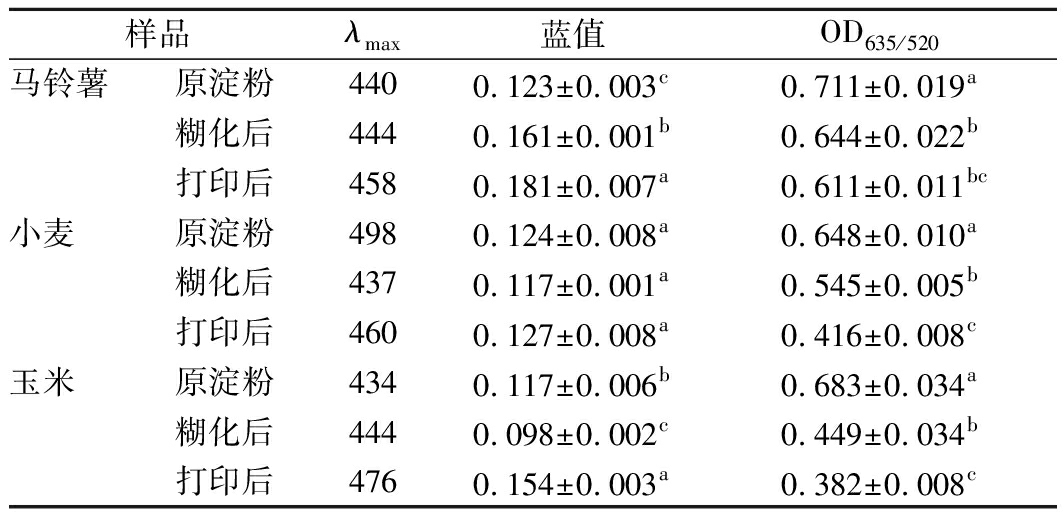
样品λmax蓝值OD635/520马铃薯原淀粉4400.123±0.003c0.711±0.019a糊化后4440.161±0.001b0.644±0.022b打印后4580.181±0.007a0.611±0.011bc小麦原淀粉4980.124±0.008a0.648±0.010a糊化后4370.117±0.001a0.545±0.005b打印后4600.127±0.008a0.416±0.008c玉米原淀粉4340.117±0.006b0.683±0.034a糊化后4440.098±0.002c0.449±0.034b打印后4760.154±0.003a0.382±0.008c
注:λmax,最大碘吸收波长;BV,蓝色值
直链淀粉含量对3D打印样品特征的影响包括颜色、尺寸收缩和流变学特性。一定含量的直链淀粉使淀粉容易回生,导致样品易于硬化和收缩。然而,回生有利于淀粉凝胶成型,增强淀粉凝胶的稳定性。
λmax和OD635 / 520反映了淀粉的碘结合能力。淀粉的最大吸光度λmax根据聚合物链的聚合度(degree of polymerization, DP)而变化。随着葡聚糖链长度的增加,淀粉分子可以容纳的碘分子数量也有所增加[14]。然而,包括水分含量、晶体结构、DP和葡聚糖链等在内的复杂因素会改变λmax和OD635/520,可以观察到打印后OD635/520值降低,这表明回生淀粉的螺旋腔中的可用空间较少,是样品淀粉碘结合能力较低的原因[15]。
2.3 不同淀粉3D打印产品色泽分析
表3显示了湿淀粉、糊化淀粉和打印样品的颜色变化。糊化处理和打印处理对色泽均有显著影响。从表3可以看出,由于淀粉凝胶形成、淀粉糊化和再结晶/回生过程中,L*值显著降低,从而导致凝胶在冷却和挤压过程中释放水分。随着淀粉颗粒的膨胀和胶凝,凝胶变得更加不透明,从而引起凝胶b*值的一些变化[16]。总之,当使用原淀粉作为参考进行淀粉加热处理时,ΔE值显著增加。然而,打印处理(挤出)引起ΔE的较小变化,推断出3D打印对样品色泽影响不大。与原淀粉相比,使用马铃薯淀粉的打印淀粉凝胶显示出最高的ΔE值 (58.36),因为直链淀粉含量会影响淀粉凝胶的亮度以改变颜色,这与马铃薯淀粉具有最高直链淀粉含量(表2)的结果一致。
表3 三种原淀粉、糊化后与打印后淀粉的颜色变化
Table 3 Iodine absorbance spectrum parameters of
starches, for a single starch batch

样品L∗a∗b∗ΔE马铃薯原淀粉56.00±0.01a-2.37±0.02c1.92±0.01a-糊化后46.35±0.29b-1.88±0.05b-0.21±0.06b42.78±0.29b打印后29.01±0.09c-0.26±0.03a-1.28±0.03c58.36±0.10a小麦原淀粉58.97±0.04a-2.57±0.02c2.91±0.01a-糊化后41.19±0.14b-1.96±0.02b-2.65±0.03b48.36±0.14b打印后33.43±0.01c-1.22±0.03a-3.32±0.02c55.45±0.01a玉米原淀粉97.54±0.08a0.42±0.03a1.71±0.04a-糊化后72.47±0.05b0.18±0.04b-3.69±0.02c17.25±0.05b打印后71.70±0.02c0.09±0.04c-2.55±0.01b17.19±0.02a
2.4 淀粉的流体特性研究
黏度特性反映糊化淀粉的流体性质以及产品的可打印性和质量。马铃薯、小麦和玉米淀粉的黏度特性如图2所示。糊化温度 (Ptemp, ℃),峰值黏度 (PV, cP),峰值时间 (PT, min),谷值黏度 (TV,cP),衰减值 (BV, cP),回生值 (SV, cP)和最终黏度 (FV, cP) 用于表示黏度特性(表4)。
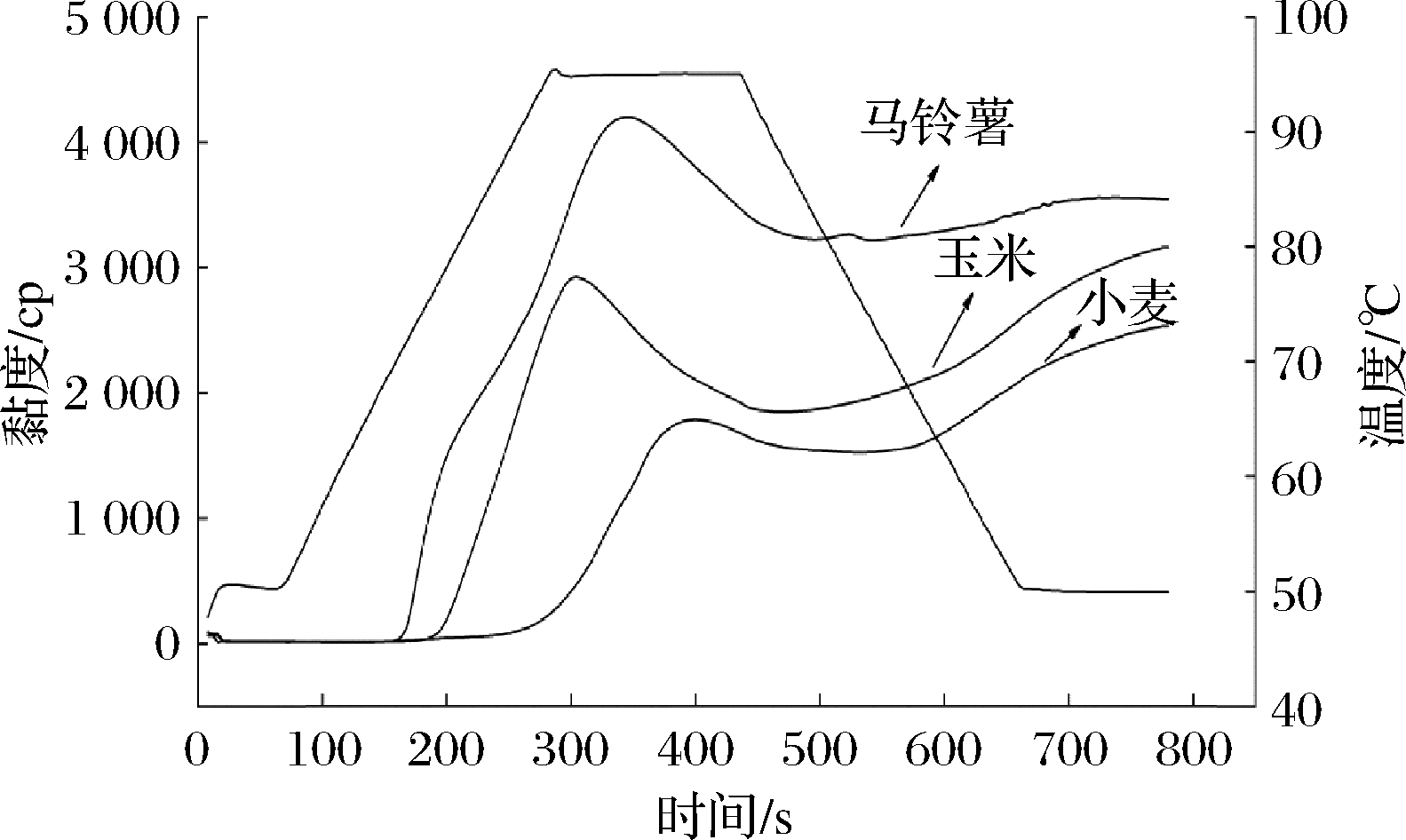
图2 三种原淀粉的快速黏度分析(14%)
Fig.2 RVA curves for starch pastes (14%) of
potato, wheat and corn starches
适用于3D挤出打印的食品材料应该是具有合适的剪切稀化行为的假塑性流体形式,并且易于在适当的剪切力下从打印机喷嘴挤出,并且能够在挤出后快速结构恢复固化。通过分析流变和黏度特性可得出材料的支撑能力、储存特性、可挤出性和可打印性[17]。CORREA等[3]和MOO-HUCHIN等[4]的研究结果表明了马铃薯、小麦和玉米淀粉凝胶的假塑性特征。
马铃薯淀粉显示出最高的黏度(峰值黏度、谷值黏度和最终黏度)。马铃薯、小麦和玉米淀粉糊的黏度差异可归因于淀粉颗粒大小和形状、以及直链淀粉含量的差异。高黏度材料易于黏在进料管内壁上并阻塞喷嘴,使得挤出更加困难并导致最终产品形状的不精确生产[17]。小麦和玉米淀粉具有较高的糊化温度和较低的黏度,其热稳定性优于马铃薯淀粉。由表4还可以看出,马铃薯淀粉的回生值最低(305±45),这说明玉米和小麦淀粉打印的样品比马铃薯的稳定性好,因为马铃薯淀粉分子中磷脂的存在使其难以回生。马铃薯淀粉的高直链淀粉含量可能是黏度图2中观察到的回生黏度急剧增加的原因。黏度特性可用于估算3D挤出产品的性能,由马铃薯淀粉制备的样品由于较高的黏度和较慢的回生速率而显示打印精度降低。
表4 三种原淀粉的快速黏度分析(14%)
Table 4 Pasting properties under three kinds of native starches

样品Ptemp/℃PV/cPPT/minTV/cPBV/cPSV/cPFV/cP马铃薯淀粉70.21±0.08c4 246±46a5.7±0.1b3 242±22a1 005±24a305±45c3 547±45a小麦淀粉91.28±0.08a1 811±51c6.6±0.0a1 530±55c281±14c1 028±18b2 558±63c玉米淀粉76.12±0.92b2 848±71b5.1±0.1c1 860±38b988±78b1 234±66a3 094±68b
2.5 红外光谱分析
FT-IR可用于分析淀粉分子中的短程有序结构。晶型、链构象和螺旋结构的变化改变了红外能量的吸收[18]。如图3所示,糊化淀粉和打印后淀粉的红外光谱无显著性差异。

a-马铃薯淀粉;b-小麦淀粉;c-玉米淀粉
图3 三种原淀粉、糊化后和3D打印后淀粉的FT-IR
Fig.3 FT-IR spectra for a single starch batch
在原淀粉、糊化和打印后的淀粉之间存在一些类似的典型峰。光谱显示在波数574、930、1 016~1 022、1 048、1 080、1 154、1 365、1 420、1 644、2 930和3 380 cm-1附近有高吸收,证实了样品的碳水化合物性质[19]。3 400和2 930 cm-1的吸收分别归因于马铃薯、小麦和玉米淀粉的O—H和H—C—H键伸展,而1 644 cm-1处的峰值可能归因于碳水化合物中COO—伸缩振动[20-21]。而1 369~1 420 cm-1的波段由于C—H弯曲振动; 1 156和1 080 cm-1处的峰主要归因于淀粉中C—O—H的C—O伸展; 574和930 cm-1处的峰归因于吡喃糖环[22]。
1 047和1 022 cm-1处的峰分别与淀粉的有序和无定形结构相关[22]。在先前的研究中,观察到1 022 cm-1处的峰强度随糊化的进行而增强(有序结构的损失),并且在回生过程中减弱(重新排序)[23]。不在1 100~1 000 cm-1处的峰变化表明淀粉分子(葡萄糖)上的C—O—C键因淀粉颗粒的凝胶化而断裂。分析FT-IR光谱可以看出在打印过程中没有官能团消失或出现,这表明在3D打印中没有产生新物质,这与FENG等[7]的发现一致。
2.6 不同淀粉3D打印产品质构分析
图4显示了由马铃薯、小麦和玉米淀粉制成的打印样品在分别存放0、6和24 h后进行TPA试验后得到的硬度、弹性和内聚性等质构特征。
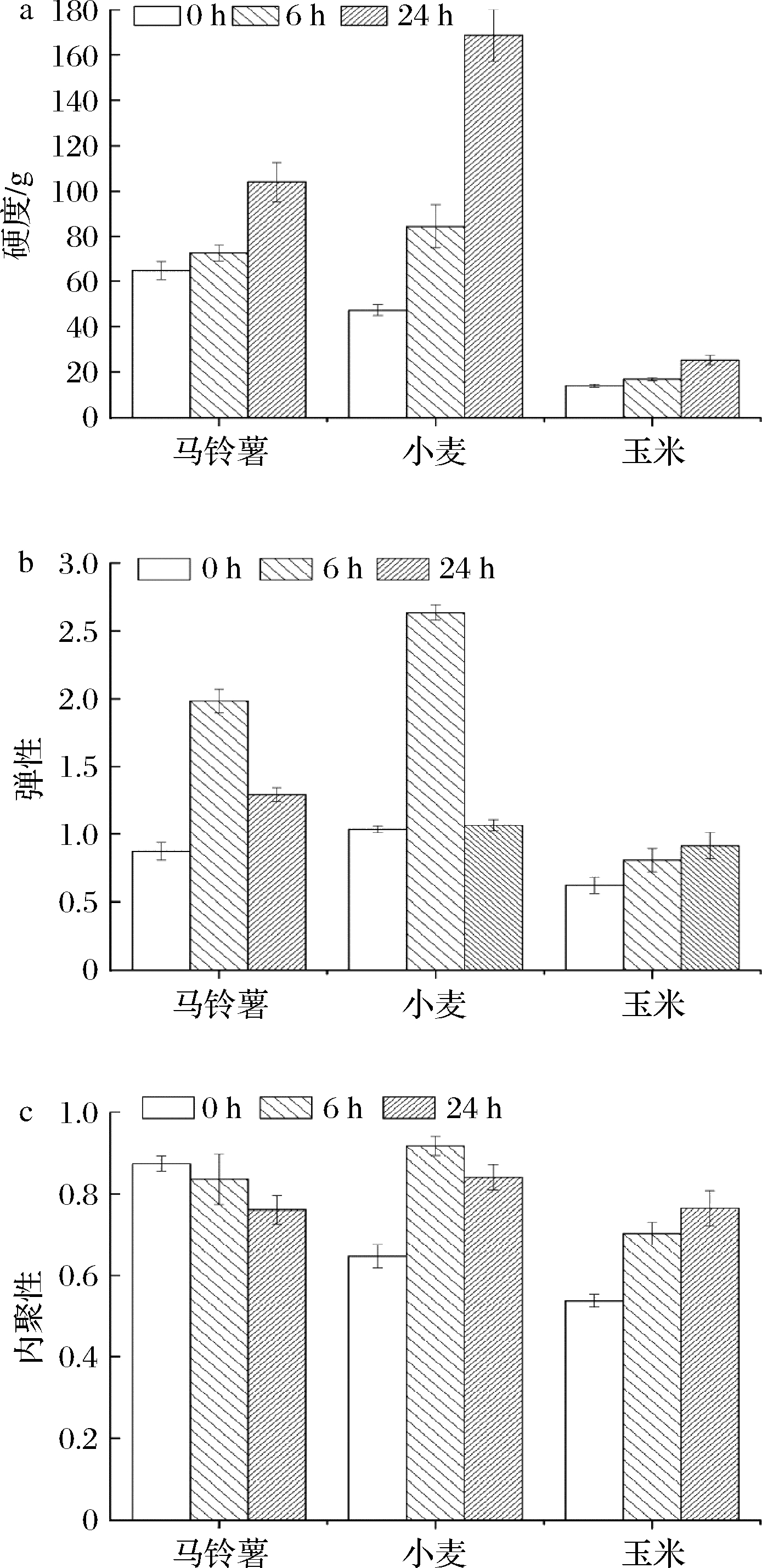
a-硬度;b-弹性;c-黏附性
图4 三种淀粉的3D打印模型在储存24 h过程
中的质构变化
Fig.4 Textural properties including hardness,
springiness and cohesiveness, for printed samples
using three kinds of starches during 24 h storage
硬度可以反映3D打印后材料的形状保持和挤出特性。所有打印样品的硬度在储存24 h后都逐渐增加(图4-a)。SINGH等[24]的研究结果表明淀粉凝胶的硬度主要是由回生引起的,与淀粉凝胶的脱水缩合和淀粉的重结晶有关。24 h后通过小麦淀粉凝胶打印的样品由于较短的链而具有较硬的质地,在保存后具有较高的脱水倾向。
弹性与淀粉的结构和含水量有关。在使用马铃薯和玉米淀粉的2个打印样品中观察到,随着回生,弹性值的先增加然后减少。淀粉的结构在长期储存后变得坚韧和致密。这种现象导致水分流失并降低样品的弹性。在长时间储存(24 h)后,形成脆弱的结构,这导致马铃薯和玉米样品的弹性降低。相反,由小麦淀粉制成的样品的弹性略有增加,因为该测定中使用的小麦淀粉难以回生,这与SV数据拟合。
内聚性是指内部淀粉颗粒之间的黏合力,其表现出与黏度的相关性。由马铃薯淀粉制成的样品内聚性不断上升,这表明未达到最终黏度,且马铃薯淀粉难以回生。作为对比,在储存6 h后,小麦淀粉打印的样品内聚性开始下降,这表明淀粉发生了回生。玉米淀粉的内聚性不断降低,可以推断出玉米淀粉容易回生,这与RVA分析的SV数据吻合。
凝胶强度差异的原因可能在于小麦淀粉的直链淀粉含量高于其他淀粉含量。研究发现,某些植物物种的直链淀粉含量与淀粉凝胶强度/黏度之间存在正相关性[25]。总之,与研究的其他淀粉凝胶相比,小麦淀粉打印样品在冷却时易形成高浓度凝胶。
2.7 三维打印对样品微观结构的影响
样品的微观结构如图5所示,糊化和挤出处理的所有淀粉均形成连续且均匀的微观结构。然而,与糊化淀粉相比,3D打印样品显示出更紧凑的结构,表明3D打印使产品结构紧凑,有利于维持形状。除挤出外,脱水收缩和回生均可有助于形成牢固结构。与小麦和玉米相比,来自马铃薯的糊化和打印淀粉具有更多的孔隙,因为它具有更高的形状度。较高的形状度不仅会降低打印产品的精度,还会导致产品的结构松散,不利于产品制造和储存。

a-糊化马铃薯淀粉;b-打印马铃薯淀粉; c-糊化小麦淀粉;
d-打印小麦淀粉;e-糊化玉米淀粉;f-打印玉米淀粉
图5 三种淀粉糊化后和打印后的扫描电镜(5 000倍)
Fig.5 SEM micrographes (5 000×) for three kinds of
gelatinized and printed samples
3 结论
本试验成功验证了淀粉3D打印的可行性,且产品具有较好的准确性和重现性。用马铃薯和玉米淀粉制作的3D打印模型产生了显著的尺寸收缩,而使用小麦淀粉制作的3D打印模型与实际模型最接近。打印处理也改变了原淀粉的颜色。分析数据显示小麦淀粉凝胶易于在3D打印机上挤出。
与糊化过程相比,打印操作不会对淀粉结构造成改变,且所有3D打印模型的表面都变得更加光滑,网络结构更加规整、致密,表明打印处理可能引起直链淀粉交联,减少空隙,使聚集凝胶结构在一定程度上转变为细链凝胶网络。基于以上研究结果,可以初步确定小麦淀粉更适合于3D食品打印的研究。
[1] KOTESWARA R C, VIDYA P V, HARIPRIYA S. Effect of chemical modification on molecular structure and functional properties of Musa AAB starch[J]. International Journal of Biological Macromolecule, 2015,81:1 039-1 045.
[2] LANARO M, FORRESTAL D P, SCHEURER S, et al. 3D printing complex chocolate objects: Platform design, optimization and evaluation[J]. Journal of Food Engineering, 2017,215:13-22.
[3] TOHIC C L, O′SULLIVAN J J, DRAPALA K P, et al. Effect of 3D printing on the structure and textural properties of processed cheese[J]. Journal of Food Engineering, 2017,220:56-64.
[4] FENG C X, WANG Q, LI H, et al. Effects of pea protein on the properties of potato starch-based 3D printing materials[J]. International Journal of Food Engineering, 2018,14(3).
[5] LIU Z, ZHANG M, BHANDARI B, et al. Impact of rheological properties of mashed potatoes on 3D printing[J]. Journal of Food Engineering. 2018, 220:76-82.
[6] HAZARIKA B J, SIT N. Effect of dual modification with hydroxypropylation and cross-linking on physicochemical properties of taro starch[J]. Carbohydrate Polymers,2016,140:269-278.
[7] CORREA Z, ZUNIGA A, GARFIAS C, et al. Isolation and characterization of Alstroemeria hookeri ssp. hookeri starch in comparison with potato starch[J]. Starch-Stärke. 2013, 65(11-12): 991-998.
[8] MOO-HUCHIN V M, CABRERA-SIERRA M J, ESTRADA-LE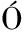 N R J, et al. Determination of some physicochemical and rheological characteristics of starch obtained from Brosimum alicastrum Swartz seeds[J]. Food Hydrocolloids, 2015,45:48-54.
N R J, et al. Determination of some physicochemical and rheological characteristics of starch obtained from Brosimum alicastrum Swartz seeds[J]. Food Hydrocolloids, 2015,45:48-54.
[9] KLUCINEC J D,THOMPSON D B. Fractionation of high-amylose maize starches by differential alcohol precipitation and chromatography of the fractions[J]. Cereal Chemistry, 1998,75(6):887-896.
[10] AACC method, (1999). Determination of the Pasting Properties of Rice with the Rapid Visco Analyser[S]. http://methods.aaccnet.org/summaries/61-02-01.aspx. (accessed 19 March, 2018).
[11] SAIBENE D, ZOBEL H F, THOMPSON D B, et al. Iodine-binding in granular starch: different effects of moisture content for corn and potato starch[J]. Starch-Störke, 2010,60(3-4):165-173.
[12] LIU J, FEI L, MICHELLE M, et al. Iodine binding property of a ternary complex consisting of starch, protein, and free fatty acids[J]. Carbohydrate.Polymers, 2009,75(2):351-355.
[13] YANG H, PARK J W. Effects of starch properties and thermal-processing conditions on surimi-starch gels[J]. LWT: Food Science and Technology, 1998,31(4):344-353.
[14] LUNDBERG B, PAN X, WHITE A, et al. Rheology and composition of citrus fiber[J]. Journal of Food Engineering, 2014,125(1):97-104.
[15] WU Y S, SEIB P A. Acetylated and hydroxypropylated distarch phosphates from waxy barley: paste properties and freeze-thaw stability[J]. Cereal Chemistry, 1990,67(2):202-208.
[16] FANG J M, FOWLER P A, TOMKINSON J, et al. The preparation and characterization of a series of chemically modified potato starches[J]. Carbohydrate Polymers, 2002,47:245-252.
[17] JIANG H, ZHENG L, ZOU Y, et al. 3D food printing: main components selection by considering rheological properties[J]. Critical Reviews in Food Technology, 2019,59(14):2 335-2 347.
[18] MANO J F, KONIAROVA D, REIS R L. Thermal properties of thermoplastic starch/synthetic polymer blends with potential biomedical applicability[J]. Journal of Materials Science. 2003,14(2):127-135.
[19] SIT N, MISRA S, DEKA S C. Characterization of physicochemical, functional, textural and color properties of starches from two different varieties of taro and their comparison to potato and rice starches[J]. Food Science and Technology Research, 2014,20(2):357-365.
[20] CHI H, XU K, XUE D, et al. Synthesis of dodecenyl succinic anhydride (DDSA) corn starch[J]. Food Research International, 2007,40:232-238.
[21] SOEST J J G V, TOURNOIS H, WIT D D, et al. Short-range structure in (partially) crystalline potato starch determined with attenuated total reflectance fourier-transform spectroscopy[J]. Carbohydrate Research, 1995,279(95):201-214.
[22] WILSON R H, KALICHEVSKY M T, RING S G, et al. Fourier-transform infrared study of the gelation and retrogradation of waxy-maize starch[J].Carbohydrate Research, 1987,166(1):162-165.
[23] KALSOOM U, NESTERENKO P N, PAULL B. Recent developments in 3D printable composite materials[J]. RSC Advances, 2016,6(65):60 355-60 371.
[24] SINGH N, SINGH J, SINGH S N. Morphological, thermal, rheological and noodle-making properties of potato and corn starch[J]. Journal of the Science of Food and Agriculture, 2002,82(12):1 376-1 383.
[25] LIAO L, ZHANG F L, LIN W J, et al. Gluten-starch interactions in wheat gluten during carboxylic acid deamidation upon hydrothermal treatment[J]. Food Chemistry, 2019:111-122.