白酒是将富含淀粉的原料经发酵后产生的酒精再通过蒸馏收集得到的高浓度蒸馏酒,是我国特有的酒精饮品。中国白酒与白兰地、威士忌、伏特加、金酒、朗姆酒为享有盛誉的六大蒸馏酒,具有悠久的历史和精湛的酿造技艺,是世界饮食文化的重要组成部分。白酒中的成分组成受原料种类和来源、酿造工艺以及贮存环境的影响存在很大差异,虽然白酒的整体质量由有机成分所确定[1-3],但其所含的多种无机元素不仅与白酒的品质密切相关,而且还会影响饮用者的身体健康[4-6]。有研究表明,白酒中的Cu具有催化氧化作用,含量过高会影响酒体的感官品质[7];Fe、Mn形成的配合物具有着色作用,会影响白酒的色泽[8];Mg、Fe、Ba超量或失衡均会引起酒体浑浊甚至沉淀,从而影响白酒的稳定性[9];As、Pb等重金属元素含量过高具有毒害作用,影响白酒的饮用安全[10]。因此,无机元素常用于白酒的质量控制和安全性研究。
白酒中无机元素的含量分布离散,且与白酒的种类密切相关,即使是相同元素在不同种类的白酒中仍然存在较大的差异[11]。白酒中大部分无机元素的含量处于微量和痕量水平级别,这就要求分析方法的灵敏度高、检出限低。在各种用于测定白酒中无机元素的原子光谱技术中,相比于传统的原子吸收光谱(atomic absorption spectroscopy, AAS)和电感耦合等离子发射光谱(inductively coupled plasma-atomic emission spectrum,ICP-OES),电感耦合等离子体质谱(inductively coupled plasma-mass spectrometry,ICP-MS)应用更广泛[12-13]。然而,采用ICP-MS测定未经消解的白酒中的痕量元素仍然具有挑战性,由于低含量痕量元素产生的信号强度弱,会受到来自基质元素产生的大量背景信号以及多原子离子的干扰,需要借助碰撞/反应池(collision/reaction cell,CRC)技术来消除这些干扰。尽管带CRC的ICP-MS减轻了分析挑战的压力,但依然不能消除一些棘手的质谱干扰[14]。电感耦合等离子体串联质谱(inductively coupled plasma tandem mass spectrometry,ICP-MS/MS)是在ICP-MS的ICP和CRC之间附加了一级四极杆质量过滤器(the first quadrupole,Q1),与位于CRC后端配置的二级四极杆质量过滤器(the second quadrupole,Q2)组成串联质谱(tandem mass spectrometry,MS/MS),通过Q1和Q2的双重过滤,可以将来自等离子体和样品基质的干扰离子阻止在检测器外,极大提高消除干扰性能和分析灵敏度[15-18]。本研究采用体积分数1%的硝酸稀释白酒样品,应用ICP-MS/MS法测定其中Mg、Al、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Se、Sr、Ba、Pb等14种无机元素,在MS/MS模式下分别选择O2和NH3/He为反应气消除质谱干扰,建立了白酒中多元素的ICP-MS/MS分析方法,采用SPSS主成分分析和聚类分析法探讨白酒特征元素和无机元素与白酒品种的关系,旨在为白酒中无机元素的分析提供科学方法,为白酒的品种识别提供理论依据。
1 材料与方法
1.1 材料与试剂
1 g/L的Mg、Al、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Se、Sr、Ba、Pb单元素标准溶液,中国计量科学研究院;10 mg/L的Li、Sc、Ge、Y、In、Tb、Bi混合内标元素标准溶液,美国Agilent公司;质量分数65%硝酸、无水乙醇,德国Merck公司;实验用水均为Milli超纯水。18种白酒(产地分别为四川9种、贵州3种、重庆3种、湖南3种),湖南长沙各大超市。
1.2 仪器及工作参数
Agilent 8800型电感耦合等离子体串联质谱仪,美国Agilent公司。Milli-Q超纯水机,美国Millipore公司。
ICP-MS/MS的工作参数:射频功率1 550 W;等离子模式低基质;等离子气流速15.0 L/min;载气流速1.09 L/min;辅助气流速1.8 L/min;补偿气流速0.2 L/min;采样深度8.0 mm;雾室温度2 ℃;质谱分析模式MS/MS;CRC气体O2、NH3/He(1∶9,V/V);反应气O2流速0.40 mL/min;反应气NH3/He流速3.0 mL/min;八极杆偏置电压-15 V(O2)、-20 V(NH3/He);KED偏置电压-10 V(O2)、-10 V(NH3/He)。
1.3 实验方法
采用体积分数1%的硝酸对白酒样品进行10倍稀释后直接进样,在选择的工作条件下利用ICP-MS/MS进行测定,通过内标混合T型接头在所有上机测试品中均在线加入1 mg/L的Li、Sc、Ge、Y、In、Tb、Bi混合内标元素标准溶液,所有空白溶液和标准溶液均加入5%vol的乙醇溶液以匹配样品基体消除黏度差别,校正基体效应。
1.4 数据处理
配制分析元素系列标准溶液,利用ICP-MS/MS的MassHunter工作站软件(美国Agilent公司)绘制校准曲线,通过校准曲线计算18个样品中14种无机元素的含量,组成18×14的原始数据分析矩阵,应用SPSS 25软件进行主成分分析和聚类分析。
2 结果与讨论
2.1 ICP-MS/MS分析
ICP-MS/MS在单四极杆(single quad, SQ)模式下,Q1仅具有离子导入或离子带通功能,类似于传统的ICP-MS,对于无干扰或受到轻微干扰元素的测定,在SQ标准模式(CRC中无反应气)下的灵敏度比MS/MS模式高,本实验样品中Sr、Ba、Pb受到的干扰比较轻微可忽略不计,采用SQ标准模式进行测定。在MS/MS模式下,Q1具有质量过滤功能,仅允许与分析离子具有相同质荷比(m/z)的离子进入CRC,在CRC内通过反应气的选择,确保CRC中反应过程和生成产物的一致性,利用分析离子或干扰离子与反应气反应产生的m/z差异,通过Q2对来自CRC的离子再次过滤消除干扰。本实验采用ICP-MS/MS分析白酒中无机元素的工作原理见图1。
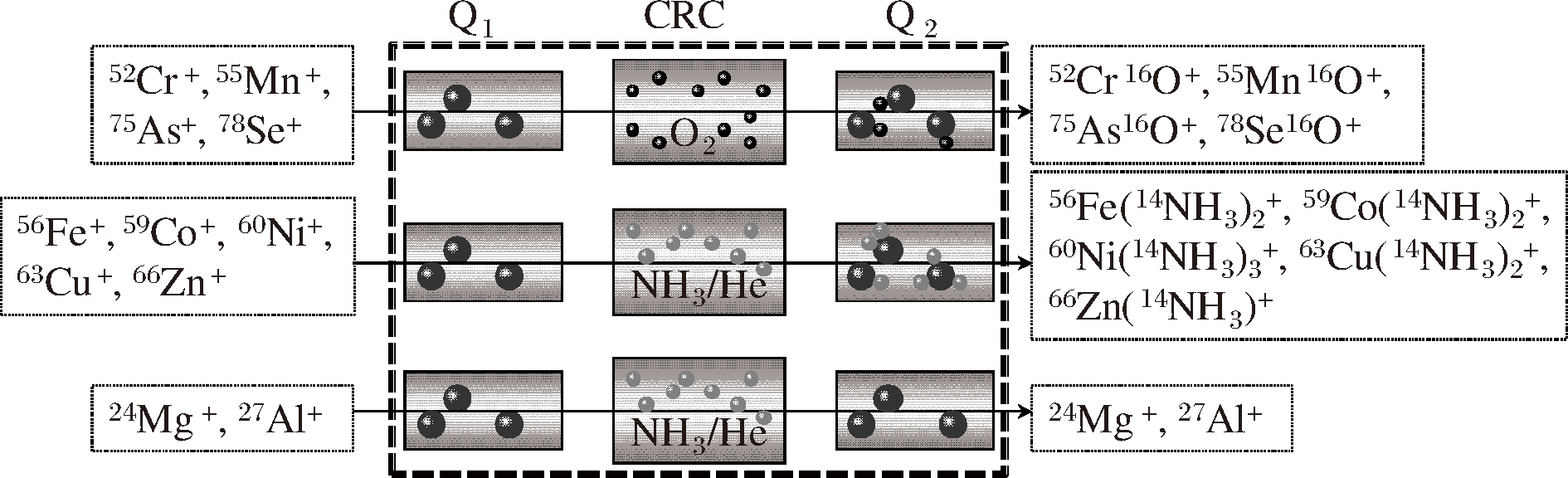
图1 在MS/MS模式下消除干扰的工作原理
Fig.1 The working mechanism of interferences eliminating
in the MS/MS mode
2.1.1 质谱干扰的消除
O2作为最强大和最有用的消除质谱干扰的反应气,在ICP-MS/MS分析中得到了广泛应用[19]。在MS/MS模式下,O2与52Cr+、55Mn+、78Se+的反应是吸热过程,利用八极杆偏置电压增加52Cr+、55Mn+、78Se+的动能,促使52Cr+、55Mn+、78Se+与O2反应生成相应的氧化物离子,O2与75As+的反应是放热过程,可以自发生成75As16O+,而与52Cr+、55Mn+、75As+、78Se+具有相同m/z的干扰离子不与O2反应,本实验设置Q1的m/z分别为52、55、75、78,52Cr+、55Mn+、75As+、78Se+进入CRC后与O2发生质量转移反应,设置Q2的m/z分别为68、71、91、97,使52Cr+、55Mn+、75As+、78Se+的氧化物离子52Cr16O+、55Mn16O+、75As16O+、78Se16O+进入Q2消除干扰。NH3含有一对孤对电子,作为消除质谱干扰的反应气,表现出高反应特性,其通用性仅次于![]() 在MS/MS模式下,通过对产物离子扫描发现,NH3与56Fe+、59Co+、60Ni+、63Cu+、66Zn+发生质量转移反应生成大量的团簇离子,其中团簇离
在MS/MS模式下,通过对产物离子扫描发现,NH3与56Fe+、59Co+、60Ni+、63Cu+、66Zn+发生质量转移反应生成大量的团簇离子,其中团簇离![]() 的丰度高且没有受到干扰,本实验设置Q1的m/z分别为56、59、60、63、66,Q2的m/z分别为90、93、111、97、83,采用NH3/He(He为缓冲气)质量转移法,将56Fe+、59Co+、60Ni+、63Cu+、66Zn+转移为团簇离子进行测定。NH3不与24Mg+和27Al+反应,但能与24Mg+和27Al+的干扰离子发生质量转移反应,基于24Mg+和27Al+在反应模式下m/z不变而干扰离子的m/z发生改变,本实验设置Q1和Q2的m/z均为24、27,利用NH3/He原位质量法进行Mg和Al的测定。元素Sr、Ba、Pb的高丰度同位素88Sr、137Ba、208Pb无需消除质谱干扰,在SQ标准模式下设置Q2的m/z分别为88、137、208进行测定。所有元素的质谱分析模式见表1。
的丰度高且没有受到干扰,本实验设置Q1的m/z分别为56、59、60、63、66,Q2的m/z分别为90、93、111、97、83,采用NH3/He(He为缓冲气)质量转移法,将56Fe+、59Co+、60Ni+、63Cu+、66Zn+转移为团簇离子进行测定。NH3不与24Mg+和27Al+反应,但能与24Mg+和27Al+的干扰离子发生质量转移反应,基于24Mg+和27Al+在反应模式下m/z不变而干扰离子的m/z发生改变,本实验设置Q1和Q2的m/z均为24、27,利用NH3/He原位质量法进行Mg和Al的测定。元素Sr、Ba、Pb的高丰度同位素88Sr、137Ba、208Pb无需消除质谱干扰,在SQ标准模式下设置Q2的m/z分别为88、137、208进行测定。所有元素的质谱分析模式见表1。
表1 待测元素的质谱分析模式
Table 1 Mass spectrometry analysis modes of analytes

同位素分析模式反应气质量对产物离子消除干扰方法24MgMS/MSNH3/HeQ1=Q2=2424Mg+原位质谱27AlMS/MSNH3/HeQ1=Q2=2727Al+原位质谱52CrMS/MSO2Q1=52, Q2=6852Cr16O+质量转移55MnMS/MSO2Q1=55, Q2=7155Mn16O+质量转移56FeMS/MSNH3/HeQ1=56, Q2=9056Fe(14NH3)+2质量转移59CoMS/MSNH3/HeQ1=59, Q2=9359Co(14NH3)+2质量转移60NiMS/MSNH3/HeQ1=60, Q2=11160Ni(14NH3)+3质量转移63CuMS/MSNH3/HeQ1=63, Q2=9763Cu(14NH3)+2质量转移66ZnMS/MSNH3/HeQ1=66, Q2=8366Zn(14NH3)+质量转移75AsMS/MSO2Q1=75, Q2=9175As16O+质量转移78SeMS/MSO2Q1=78, Q2=9478Se16O+质量转移88SrSQ无气体Q2=8888Sr+无需消除137BaSQ无气体Q2=137137Ba+无需消除208PbSQ无气体Q2=208208Pb+无需消除
2.1.2 内标元素的选择
样品溶液与标准溶液的基质组成差异表现为溶液的进样速率和雾化效率不同,形成基体效应,影响分析信号的稳定性,通常采用内标元素为参照物进行校正[21]。考察了Li、Sc、Ge、Y、In、Tb、Bi为内标元素,在待测样品中加入5 μg/L的混合标准溶液,通过测定各元素的加标回收率来选择内标元素。从图2可以看出,Sc作内标元素时,Mg、Al、Cr、Mn、Fe的加标回收率高于其他内标元素;Ge作内标元素时,Co、Ni、Cu、Zn的加标回收率最高;Y作内标元素时,As、Se、Sr的加标回收率最高;In和Bi作内标元素时,Ba和Pb的加标回收效果最高。因此,本实验Sc为Mg、Al、Cr、Mn、Fe的内标元素,Ge为Co、Ni、Cu、Zn的内标元素,Y为As、Se、Sr的内标元素,In为Ba的内标元素,Bi为Pb的内标元素。
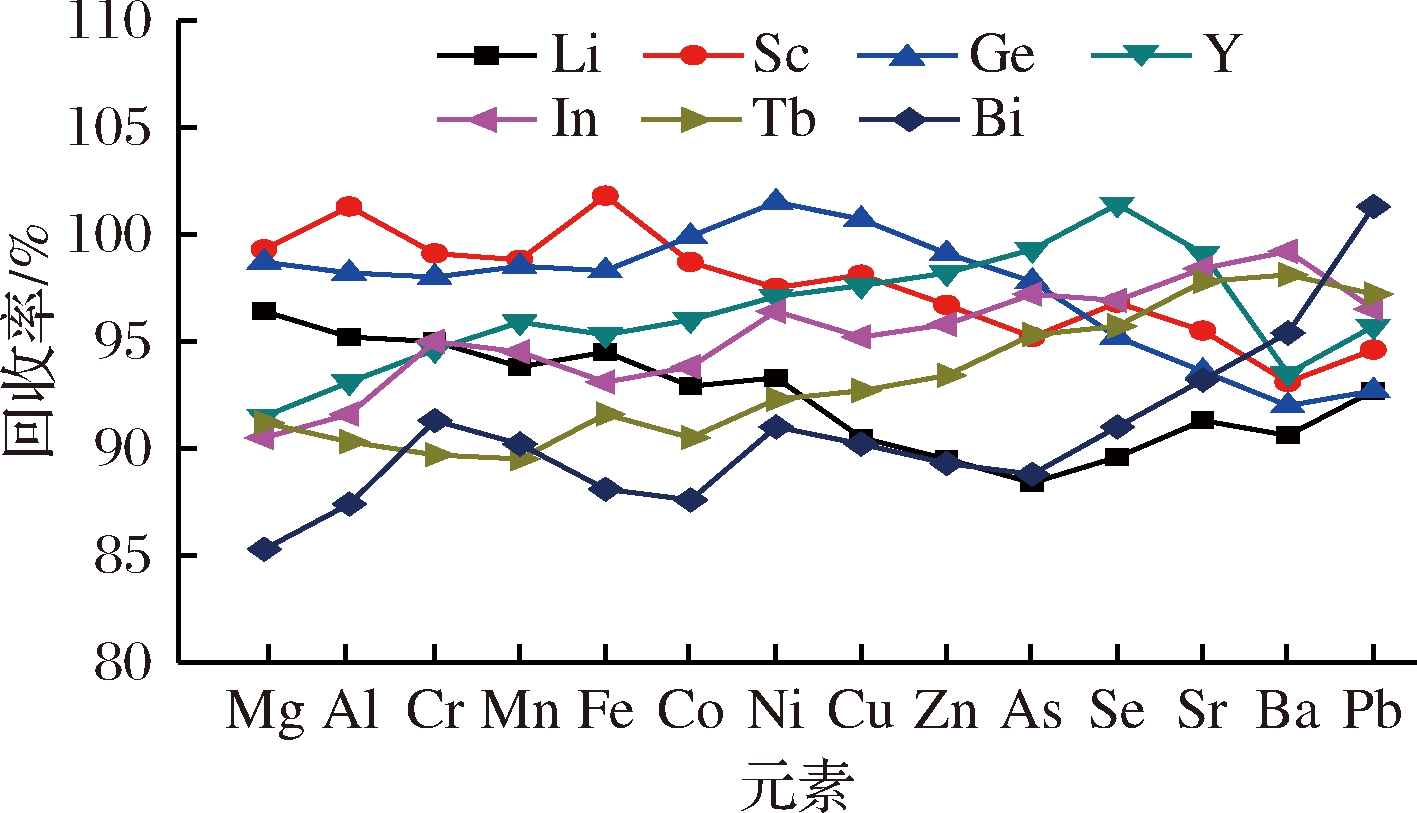
图2 内标元素的校正效果
Fig.2 Correction effect of internal standard elements
2.1.3 校准曲线与检出限
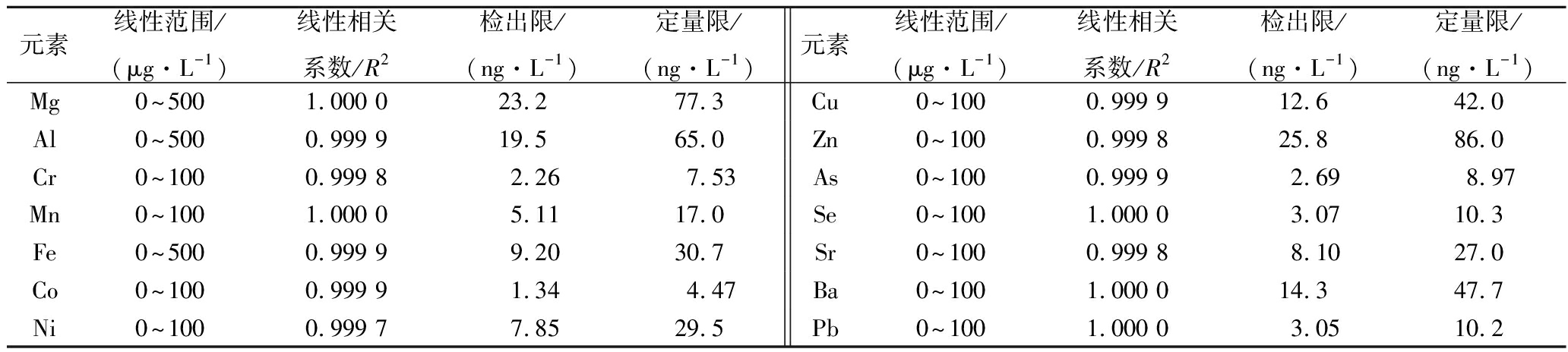
分别配制0、1.0、5.0、20.0、100 μg/L的Cr、Mn、Co、Ni、Cu、As、Se、Sr、Ba、Pb和0、5、20、100、500 μg/L的Mg、Al、Fe、Zn混合标准溶液,按所建立的分析方法上机测定后绘制校准曲线。连续测定空白溶液11次,以各元素测定结果的3倍标准偏差所对应的浓度为各元素的检出限,以测定结果的10倍标准偏差所对应的浓度为各元素的定量限。结果表明(表2),14个分析元素在各自范围内的线性相关系数≥0.999 7,检出限为1.34~25.8 ng/L,定量限为4.47~86.0 ng/L,说明方法的线性关系好,检出限低。
表2 分析元素的校准数据、检出限和定量限
Table 2 Calibration data, limits of detection (LODs), and limits of quantification (LOQs) of analytes
元素线性范围/(μg·L-1)线性相关系数/R2检出限/(ng·L-1)定量限/(ng·L-1)元素线性范围/(μg·L-1)线性相关系数/R2检出限/(ng·L-1)定量限/(ng·L-1)Mg0~5001.000 023.277.3Cu0~1000.999 912.642.0Al0~5000.999 919.565.0Zn0~1000.999 825.886.0Cr0~1000.999 82.267.53As0~1000.999 92.698.97Mn0~1001.000 05.1117.0Se0~1001.000 03.0710.3Fe0~5000.999 99.2030.7Sr0~1000.999 88.1027.0Co0~1000.999 91.344.47Ba0~1001.000 014.347.7Ni0~1000.999 77.8529.5Pb0~1001.000 03.0510.2
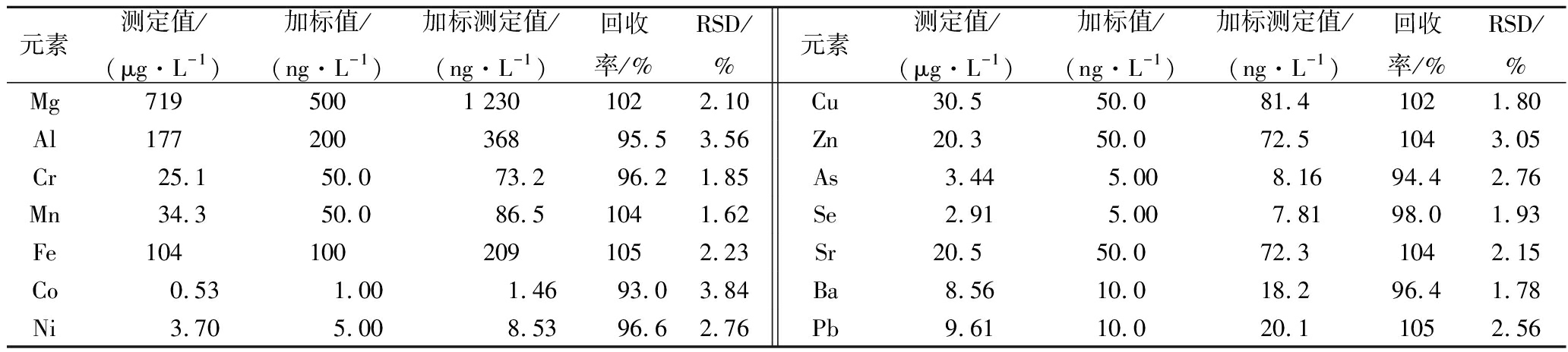
采用所建立的ICP-MS/MS法对实际白酒样品进行加标回收实验,每10 min测定1次,每个元素重复测定6次,通过计算加标回收率和相对标准偏差(relative standard deviation, RSD)来考察分析方法的准确性、稳定性和精密度。从表3可以看出,各元素的加标回收率为93.0%~105%,表明方法的准确度好;RSD≤3.84%,表明方法的稳定性好,精密度好。
表3 分析方法的准确度与精密度
Table 3 Accuracy and precision of analytical method
元素测定值/(μg·L-1)加标值/(ng·L-1)加标测定值/(ng·L-1)回收率/%RSD/%元素测定值/(μg·L-1)加标值/(ng·L-1)加标测定值/(ng·L-1)回收率/%RSD/%Mg7195001 2301022.10Cu30.550.081.41021.80Al17720036895.53.56Zn20.350.072.51043.05Cr25.150.073.296.21.85As3.445.008.1694.42.76Mn34.350.086.51041.62Se2.915.007.8198.01.93Fe1041002091052.23Sr20.550.072.31042.15Co0.531.001.4693.03.84Ba8.5610.018.296.41.78Ni3.705.008.5396.62.76Pb9.6110.020.11052.56
2.1.4 白酒中无机元素的含量
实验收集了国内18种白酒,其中来自四川9种(样品编号SC1-9)、贵州3种(样品编号GZ1-3)、重庆3种(样品编号CQ1-3)、湖南3种(样品编号HN1-3),测定各白酒中的14种无机元素,每个样品重复测定6次,结果见表4。18种白酒中Mg、Al、Fe的含量相对较高,而Co的含量最低,四川白酒中Mg的含量明显低于其他产地白酒,湖南白酒中的Al和Fe的含量明显高于其他产地白酒;对照我国白酒国家标准GB 2757—2012、GB 23545—2009GB 以及食品国家标准2762—2017所规定的限量值[10, 22-23],所有白酒中的重金属元素Mn、Ni、As、Pb的含量处于较低水平,远远低于国家标准中的限量值。表4结果显示不同产地白酒中无机元素的含量存在明显差异。
表4 不同白酒样品分析结果 单位:μg/L
Table 4 Analysis results of different Baijiu samples
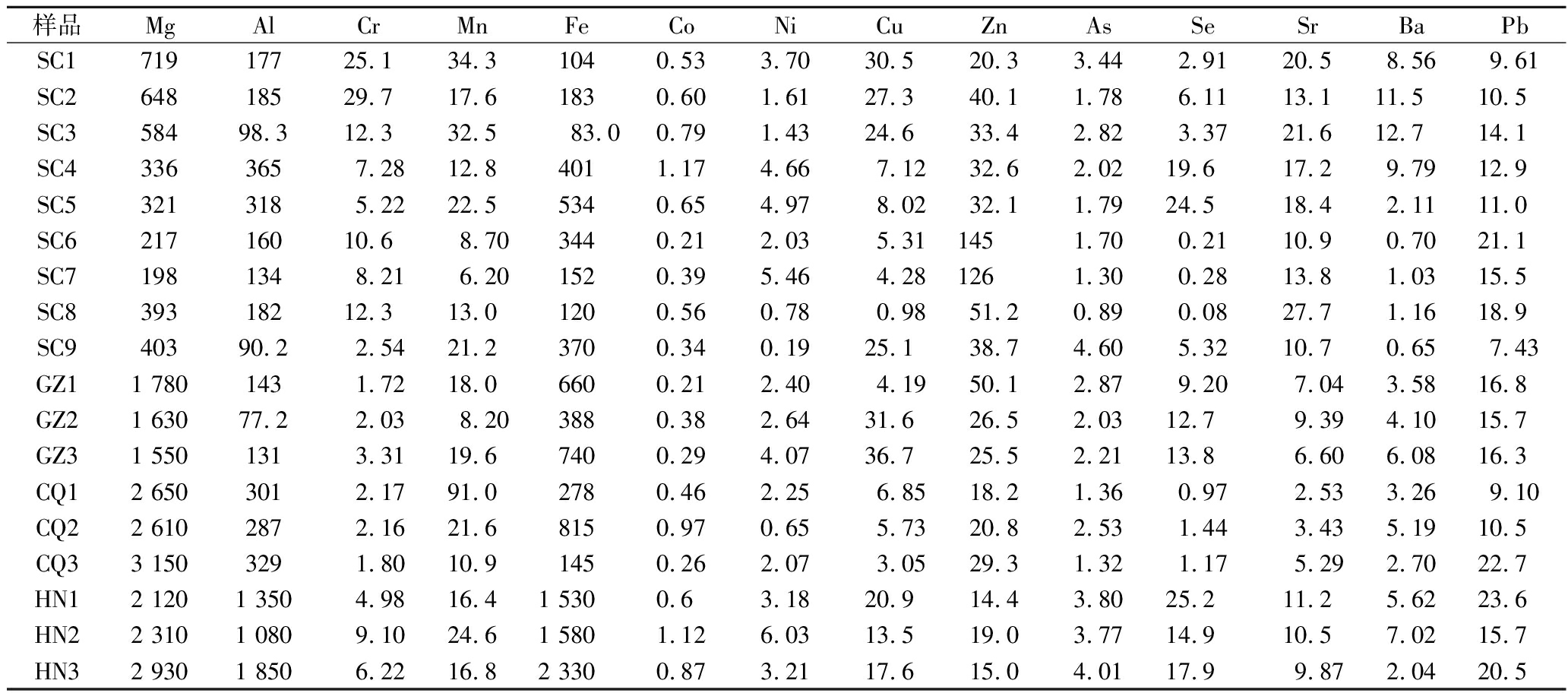
样品MgAlCrMnFeCoNiCuZnAsSeSrBaPbSC171917725.134.31040.533.7030.520.33.442.9120.58.569.61SC264818529.717.61830.601.6127.340.11.786.1113.111.510.5SC358498.312.332.583.00.791.4324.633.42.823.3721.612.714.1SC43363657.2812.84011.174.667.1232.62.0219.617.29.7912.9SC53213185.2222.55340.654.978.0232.11.7924.518.42.1111.0SC621716010.68.703440.212.035.311451.700.2110.90.7021.1SC71981348.216.201520.395.464.281261.300.2813.81.0315.5SC839318212.313.01200.560.780.9851.20.890.0827.71.1618.9SC940390.22.5421.23700.340.1925.138.74.605.3210.70.657.43GZ11 7801431.7218.06600.212.404.1950.12.879.207.043.5816.8GZ21 63077.22.038.203880.382.6431.626.52.0312.79.394.1015.7GZ31 5501313.3119.67400.294.0736.725.52.2113.86.606.0816.3CQ12 6503012.1791.02780.462.256.8518.21.360.972.533.269.10CQ22 6102872.1621.68150.970.655.7320.82.531.443.435.1910.5CQ33 1503291.8010.91450.262.073.0529.31.321.175.292.7022.7HN12 1201 3504.9816.41 5300.63.1820.914.43.8025.211.25.6223.6HN22 3101 0809.1024.61 5801.126.0313.519.03.7714.910.57.0215.7HN32 9301 8506.2216.82 3300.873.2117.615.04.0117.99.872.0420.5
2.2 主成分分析
主成分分析是将多个原始变量抽取和压缩成能代表原始变量大量信息的少数综合指标[24],本实验采用SPSS 25对国内18种白酒中的14种无机元素进行主成分分析。
2.2.1 无机元素的正态分布检验
采用SPSS 25的正态性检验对18种白酒中的14种无机元素进行K-S检验,Mg、Al、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Se、Sr、Ba、Pb的显著性(双侧)P值分别为0.230、0.364、0.208、0.278、0.236、0.137、0.105、0.231、0.288、0153、0.182、0.171、0.138、0.133,均大于显著水平(α=0.05),表明18种白酒中的14种无机元素的含量数据均服从正态分布。
2.2.2 无机元素的相关性分析
表5可以看出,14种元素两两之间大部分处于显著相关,少数处于极显著相关,因此,主成分分析可用于14种无机元素的相关性分析。
表5 白酒中无机元素的相关性矩阵
Table 5 Correlation matrix of inorganic elements in Baijiu
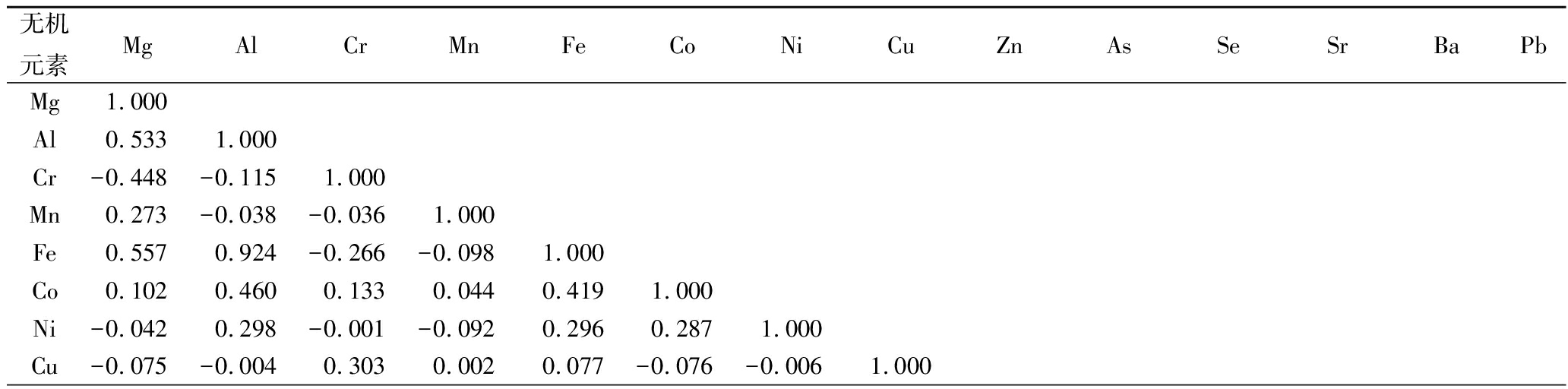
无机元素MgAlCrMnFeCoNiCuZnAsSeSrBaPbMg1.000Al0.5331.000Cr-0.448-0.1151.000Mn0.273-0.038-0.0361.000Fe0.5570.924-0.266-0.0981.000Co0.1020.4600.1330.0440.4191.000Ni-0.0420.298-0.001-0.0920.2960.2871.000Cu-0.075-0.0040.3030.0020.077-0.076-0.0061.000
续表5
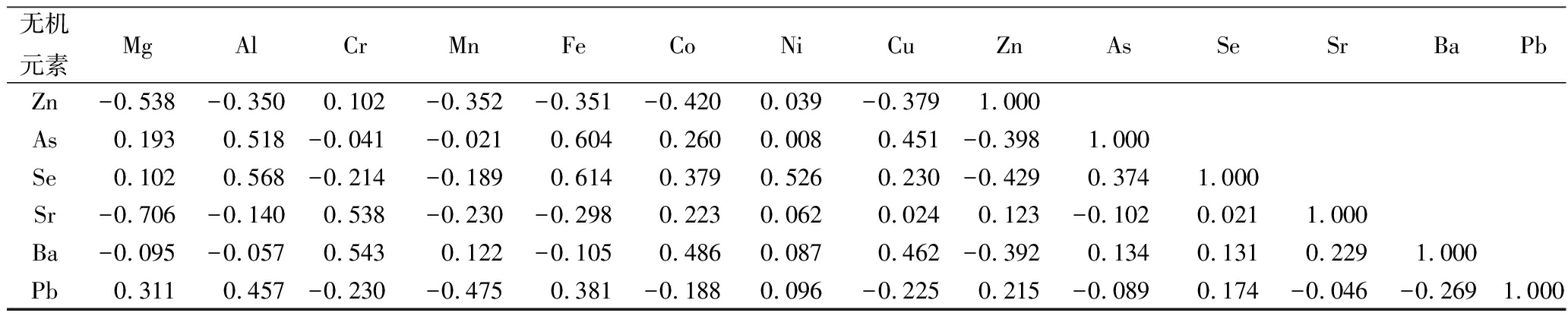
无机元素MgAlCrMnFeCoNiCuZnAsSeSrBaPbZn-0.538-0.3500.102-0.352-0.351-0.4200.039-0.3791.000As0.1930.518-0.041-0.0210.6040.2600.0080.451-0.3981.000Se0.1020.568-0.214-0.1890.6140.3790.5260.230-0.4290.3741.000Sr-0.706-0.1400.538-0.230-0.2980.2230.0620.0240.123-0.1020.0211.000Ba-0.095-0.0570.5430.122-0.1050.4860.0870.462-0.3920.1340.1310.2291.000Pb0.3110.457-0.230-0.4750.381-0.1880.096-0.2250.215-0.0890.174-0.046-0.2691.000
2.2.3 无机元素的因子分析
采用主成分分析法提取公因子,进行因子分析,结果见表6。基于累积方差贡献值大于80%且特征值大于1为原则,选择公因子数为5个时,累计方差贡献率为80.003%,包含了14种无机元素的大部分信息,因此,本实验提取5个主成分来评判18种白酒中无机元素的分布。
表6 主成分分析特征值和总体方差描述
Table 6 Principal component analysis characteristics
and total variance explained

主成分特征值方差/%累积方差/%主成分特征值方差/%累积方差/%14.03628.82628.82680.5463.90394.76822.77319.80748.63290.2651.89596.66332.10615.04163.674100.2391.70998.37241.2869.18472.858110.1691.20799.57951.0007.14580.003120.0380.26999.84860.8305.92685.928130.0150.10599.95370.6914.93690.864140.0070.047100.000
通过表7可以得到第一主成分F1、第二主成分F2、第三主成分F3、第四主成分F4、第五主成分F5的因子得分模型,分别为:
F1=0.661X1+0.884X2-0.321X3+0.026X4+0.927X5+0.494X6+0.335X7+0.171X8-0.611X9+0.624X10+0.709X11-0.339X12+0.075X13+0.282X14
F2=-0.410X1-0.070X2+0.689X3+0.117X4-0.124X5+0.501X6+0.132X7+0.573X8-0.378X9+0.279X10+0.201X11+0.538X12+0.814X13-0.534X14
F3=-0.470X1+0.232X2+0.194X3-0.741X4+0.169X5+0.127X6+0.467X7-0.191X8+0.489X9-0.085X10+0.344X11+0.545X12-0.117X13+0.519X14
F4=0.068X1+0.041X2-0.077X3+0.389X4-0.064X5+0.534X6+0.372X7-0.662X8-0.038X9-0.455X10+0.013X11+0.092X12+0.063X13-0.190X14
F5=0.243X1+0.254X2+0.361X3-0.068X4+0.086X5+0.213X6-0.533X7-0.226X8-0.036X9-0.021X10-0.413X11+0.180X12+0.174X13+0.345X14
可以看出,F1在X2、X5有较大荷载值,与对应的Al、Fe有高度正相关性,F2在X13有较大荷载值,与对应的Ba有高度正相关性,由于F1和F2对总方差的贡献达到了48.632%,因此,所对应的Al、Fe、Ba可作为本实验18种白酒的特征元素。
表7 白酒中无机元素的因子分析
Table 7 Factor analysis of inorganic elements in Baijiu
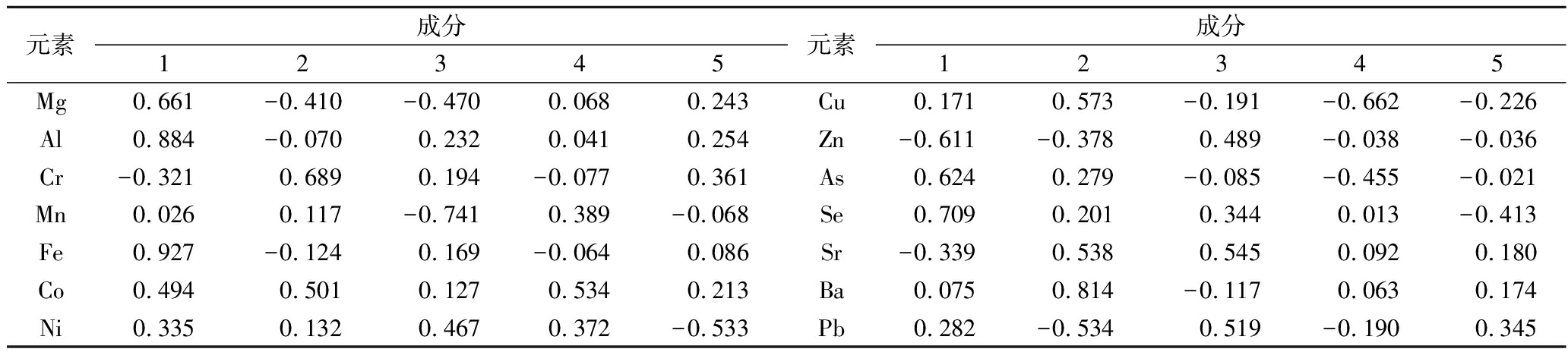
元素成分12345元素成分12345Mg0.661-0.410-0.4700.0680.243Cu0.1710.573-0.191-0.662-0.226Al0.884-0.0700.2320.0410.254Zn-0.611-0.3780.489-0.038-0.036Cr-0.3210.6890.194-0.0770.361As0.6240.279-0.085-0.455-0.021Mn0.0260.117-0.7410.389-0.068Se0.7090.2010.3440.013-0.413Fe0.927-0.1240.169-0.0640.086Sr-0.3390.5380.5450.0920.180Co0.4940.5010.1270.5340.213Ba0.0750.814-0.1170.0630.174Ni0.3350.1320.4670.372-0.533Pb0.282-0.5340.519-0.1900.345
2.3 聚类分析
采用SPSS 25对来自不同产地的18种白酒样品进行聚类分析,把性质相近的白酒归为一类。将14种原始变量经标准化处理后,采用系统聚类分析,选择组间连接聚类,以欧氏距离平方为测量准则,从图3可以看出,18种白酒样品分为了4类,表明不同产地白酒之间无机元素的含量存在较大差异,其中四川9种白酒很好地归为了一类,贵州的3种白酒归为一类,重庆的3种白酒归为一类,湖南3种白酒归为一类,表明以14种元素为原始变量可以将不同产地白酒进行正确归类。
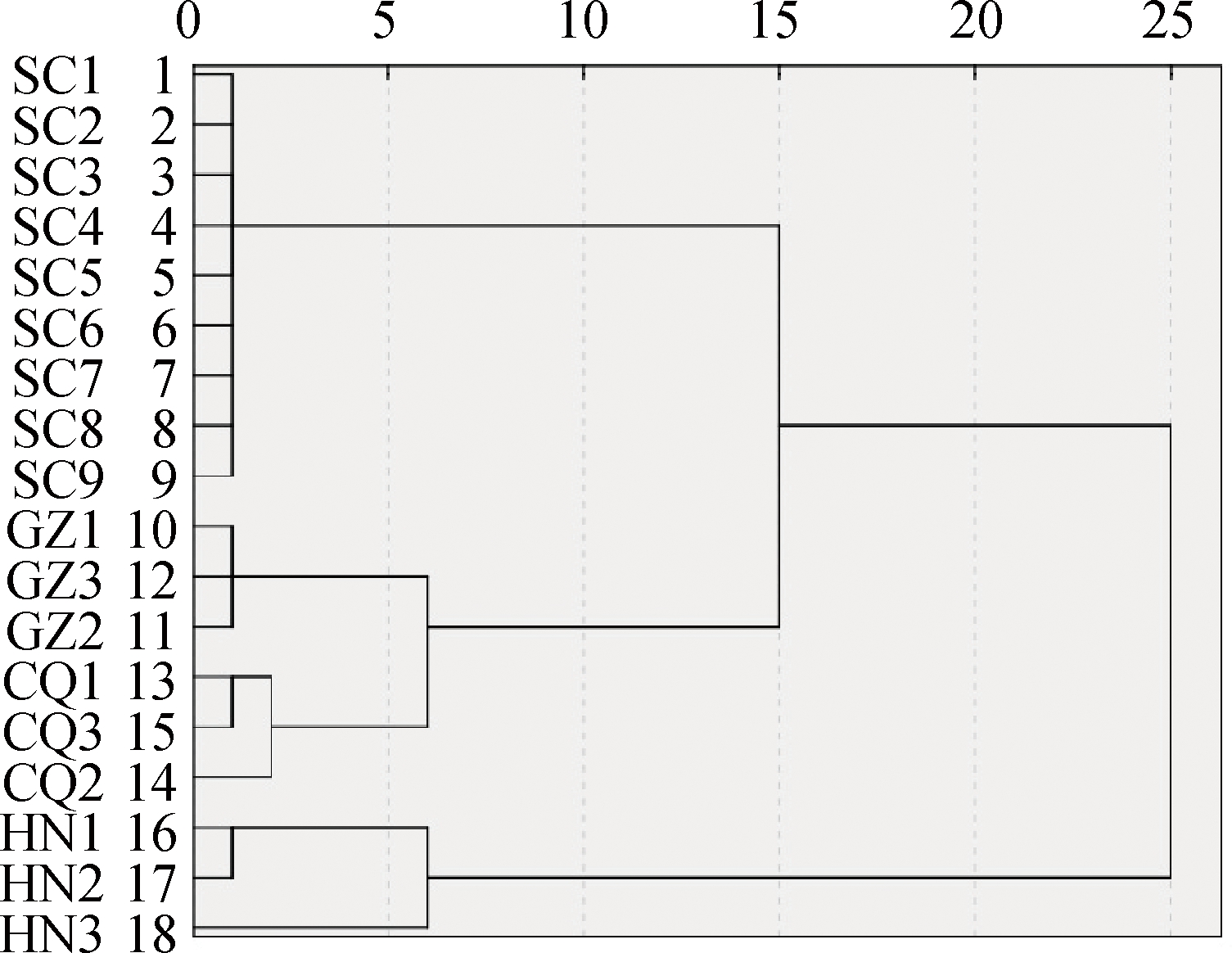
图3 白酒中无机元素含量系统聚类
Fig.3 Phylogenetic clustering of distilled Baijiu based
on inorganic elements
3 结论
该文研究了不同产地白酒中14种无机元素的组成。白酒样品经1%的硝酸简单稀释后直接采用ICP-MS/MS法进行测定,在MS/MS模式下,分别采用O2和NH3/He为反应气,利用质量转移法和原位质量法消除了质谱干扰。采用SPSS 25对18种白酒样品中的14种无机元素进行了主成分和聚类分析,提取了5个主成分来评判白酒中无机元素的分布,确定了Al、Fe、Ba为国内18种白酒的特征元素,聚类分析将国内18种白酒样品很好地按产地分为4类,白酒中无机元素的含量存在明显差异且具有典型的地理特征。
[1] 聂元皓, 徐岩, 吴群, 等. 芳香族化合物前体物质酪氨酸和苯丙氨酸在白酒中的来源解析[J].食品与发酵工业, 2018, 44(10): 1-6.
[2] DONG D, XHENG W, WANG W, et al. A new volatiles-based differentiation method of Chinese spirits using longpath gas-phase infrared spectroscopy [J]. Food Chemistry, 2014,155: 45-49.
[3] 范海燕, 范文来, 徐岩. 应用GC-O和GC-MS研究豉香型白酒挥发性香气成分[J].食品与发酵工业, 2015, 41(4): 147-152.
[4] SZYMCZYCHA-MADEJA A, WELNA M, JAMROZ P, et al. Advances in assessing the elemental composition of distilled spirits using atomic spectrometry[J]. TrAC Trends in Analytical Chemistry, 2015, 64: 127-135.
[5] 李永娇, 宋川, 张宿义, 等. ICP-MS 研究浓香型白酒发酵过程中多种金属元素的变化规律[J].食品工业科技, 2016, 37(17): 267-271.
[6] MOUTSATSOU A, CHALARAKIS E, ZARANGAS G. Influence of raw materials and distillation equipment on the heavy metal content of waste from an alcoholic anis-type beverage[J]. Journal of Hazardous Materials, 2003, 96(1): 53-64.
[7] NEVES E A, OLIVEIRA A, FERNANDES A P, et al. Simple and efficient elimination of copper(II) in sugar-cane spirits[J]. Food Chemistry, 2007, 101(1): 33-36.
[8] IBANEZ J G, CARREON-ALVAREZ A, BARCENA-SOTO M, et al. Metals in alcoholic beverages: A review of sources, effects, concentrations, removal, speciation, and analysis[J]. Journal of Food Composition and Analysis, 2008, 21(8): 672-683.
[9] MIKKELSEN Ø, SCHRØDER K H. Voltammetry using a dental amalgam electrode for heavy metal monitoring of wines and spirits[J]. Analytica Chimica Acta, 2002, 458(1): 249-256.
[10] 中华人民共和国国家卫生和计划生育委员会, 国家食品药品监督管理总局.GB 2762-2017, 食品安全国家标准食品中污染物限量[S].北京: 中国标准出版社, 2017.
[11] 万益群, 潘凤琴, 柳英霞, 等. 电感耦合等离子体原子发射光谱法测定白酒中23种微量元素[J].光谱学与光谱分析, 2009, 29(2): 499-503.
[12] 张建, 田志强, 卢垣宇, 等. 电感耦合等离子体质谱法检测白酒中28种元素[J]. 食品科学, 2013, 34(22): 257-260.
[13] 侯敏, 李志, 孙啸涛, 等. ICP-MS 直接进样法测定白酒中24 种金属元素[J].中国食品学报, 2017, 17(5): 239-246.
[14] AMAIS R S, VIRGILIO A, SCHIAVO D, et al. Tandem mass spectrometry (ICP-MS/MS) for overcoming molybdenum oxide interferences on Cd determination in milk[J]. Microchemical Journal, 2015, 120: 64-68.
[15] VETERE A, PRCFROCK D, SCHRADER W, et al. Quantitative and qualitative analysis of three classes of sulfur compounds in crude oil [J]. Angewandte Chemie International Edition, 2017, 56(36): 10 933-10 937.
[16] WHITTY-LEVEILLE L, DROUIN E, CONSTANTIN M, et al. Scandium analysis in silicon-containing minerals by inductively coupled plasma tandem mass spectrometry[J]. Spectrochimica Acta Part B, 2016, 118: 112-118.
[17] NELSON J, HOPFER H, SILVA F, et al. Evaluation of GC-ICP-MS/MS as a new strategy for specific heteroatom detection of phosphorus, sulfur, and chlorine determination in foods[J]. Journal of Agricultural and Food Chemistry, 2015, 63(18): 4 478-4 483.
[18] GUO W, JIN L, HU S, et al. Method development for the determination of total fluorine in foods by tandem inductively coupled plasma mass spectrometry with a mass-shift strategy[J]. Journal of Agricultural and Food Chemistry, 2017, 65: 3 406-3 412.
[19] BOTING K, TREU S, LEONHARD P, et al. First experimental proof of asymmetric charge transfer in ICP-MS/MS (ICP-QQQ-MS) through isotopically enriched oxygen as cell gas[J]. Journal of Analytical Atomic Spectrometry, 2014, 29(3): 578-582.
[20] OGRA Y, HIRATA T. Metallomics[M]. Germany: Springer, 2017: 183-194.
[21] VANHAECKEL F, VANHOE H, DAMS R, et al. The use of internal standards in ICP-MS[J]. Talanta, 1992, 39(7): 737-742.
[22] 中华人民共和国国家卫生部. GB 2757—2012, 食品安全国家标准蒸馏酒及其配制酒[S].北京: 中国标准出版社, 2012.
[23] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会.GB 2762—2017, 白酒中锰的测定电感耦合等离子体原子发射光谱法[S].北京: 中国标准出版社, 2009.
[24] 周志华. 机器学习[M]. 北京: 清华大学出版社, 2016: 229-231.