大曲是以小麦(或配有大麦、豌豆)为主要原料,自然接种网罗环境微生物,在人工控制的温度和湿度下培育而成[1]。大曲富含多种微生物、酶类、复合香气成分,对白酒品质有重要贡献[2]。随着大曲生产规模不断扩大,传统单层曲坯制曲模式满足不了生产需求,已逐步发展成多层曲坯立体制曲模式[3]。这种制曲模式虽满足了生产需求,但不同坯层间存在微环境(温度、氧气含量、湿度等)的差异,导致大曲质量有一定差异,不利于实现标准化制曲。目前,立体制曲的研究主要针对不同楼层大曲、曲块部位的相关指标差异性分析。明红梅等[4]对低温季节楼盘式制曲研究发现,大曲微生物分布受到立体空间、大曲品温、室温等环境因素的影响;杨勇等[5]研究表明,中高温成品曲曲心的酯化力、酸性蛋白酶活力最高,曲皮微生物数量、糖化力、发酵力最高;李登勇等[6]研究表明,高温大曲曲表酸度、酯化力比曲心高,但曲心水分、总挥发性物质含量及种类多于曲表。综上所述,目前针对不同曲层大曲质量的差异及其与微环境的相关性研究报道较少。
大曲的制作经过发酵和贮存两个时期[7]。研究以秋季安曲的中高温成品大曲为研究对象,对不同曲层大曲的理化生化指标、感官评分、微生物数量、特征风味物质进行对比分析,探究不同曲层中高温成品大曲质量的差异性,以及贮存期的微环境对大曲质量的影响,为今后改进制曲工艺,提升大曲品质奠定基础,进一步推动制曲生产的规范化、标准化。
1 材料与方法
1.1 实验材料
1.1.1 样品
中高温成品大曲,从安曲到出库时间总计90 d,其中贮存期为60 d,由四川某著名白酒生产企业提供。
1.1.2 主要仪器与设备
DHG-9023A电热干燥箱,上海琅玕实验设备有限公司;LRH-250生化培养箱,上海合恒仪器设备有限公司;固相微萃取装置,美国Supelco公司;TRACE 1300气相色谱-质谱联用仪,美国Thermo公司;固相微萃取头(2cm 50/30 μm DVB/CAR/PDMS),美国Supelco公司。
1.2 实验方法
1.2.1 取样方法及样品前处理
随机选3个不同曲库,每个库房各选不同曲层的大曲,根据曲块在贮存期贮存位置的不同,分为底层、中下层、中层、中上层、顶层样本。采用五点取样法在每个曲层的四角和中心位置各选取1块大曲。将整块大曲粉碎过20目筛,各曲粉混匀后采用四分法浓缩至200 g作为1个样本,共30个样本,4 ℃冰箱保藏备用。
1.2.2 大曲感官评定方法
10位制曲生产经验丰富的工作人员,参考文献[8]通过外表、断面、皮张、香味进行评价打分,详见表1。
表1 大曲感官评分标准表
Table 1 Sensory scoring standard of Daqu

等级外表断面皮张香味一级棕黄色、灰白色,穿衣好,表面光滑。6~8分整齐、泡气、呈灰白色或有黄、红菌斑,菌丝生长丰满,有轻微水圈。21~25分L≤0.5 cm。10~12分曲香味浓厚纯正或有酱香味, 无异味。13~15分二级多为灰白色,有棕黄色,穿衣略差,表面欠光滑。3~5分整齐,较泡气,呈灰白色或有少量黄、红菌斑,有轻微水圈。15~20分0.5 cm
注:总分为60分
1.2.3 大曲理化生化指标检测及微生物计数
水分、酸度、酯化力、氨基酸态氮、酒化力检测方法参考文献[9];微生物(霉菌、酵母、芽孢杆菌)计数参考文献[4]。
1.2.4 大曲挥发性物质的检测方法
取1.2.1样品研磨后过40目筛,将3 g样品加入20 mL顶空瓶,加内标2-辛醇30 μL,60 ℃平衡20 min, 萃取吸附30 min[10],升温程序参考文献[10]。
1.2.5 挥发性风味物质的定性与半定量
定性:检出挥发性风味物质的质谱图,通过与标准谱库对比鉴定,选取匹配度大于90%[11]的挥发性物质。
半定量:采用顶空固相微萃取结合气质联用方法,内标2-辛醇半定量,化合物质量浓度为内标物质量浓度与化合物、内标物峰面积比值的乘积[7]。
1.2.6 气味活度值法分析大曲风味物质
气味活度值(odor activity value,OAV)即物质质量浓度与香气阈值之比,表示大曲中各香气化合物对整体香气成分的贡献,当 OAV>1时,认为该风味物质对样品香气有贡献,且OAV 越大,表明该风味物质贡献越大[12-13]。
1.2.7 数据处理
采用Spss 20软件单因素方差和主成分分析,Origin 8.5作图。
2 结果与分析
2.1 大曲的理化生化指标值及感官评分差异性分析
大曲理化生化指标及大曲的外观、香味等反映大曲质量,检测样品的理化生化指标并进行感官评价后,做单因素方差分析,结果见表2。大曲微生物总数及各类微生物相对百分比见图1。
表2 不同曲层大曲理化生化指标值及感官评分
Table 2 Biochemical index values and sensory scores of different curved layers

曲层水分/%酸度/[mmol·(10 g)-1]酒化力/%vol酯化力 /[mg·(50 g样品·7 d)-1]氨基酸态氮/(g·kg-1)感官评分/分底层13.29±0.07b0.61±0.08a12.58±0.15a746.68±2.91a2.60±0.11a80.28±2.5a中下层13.05±0.15ab0.70±0.07a12.21±0.32a745.40±0.85a2.79±0.06ab81.95±1.39a中层12.87±0.18ab0.68±0.07a12.80±0.30a753.99±1.03b3.03±.014bc81.39±1.39a中上层12.69±0.19a0.70±0.15a13.06±0.14a752.68±0.88b3.13±0.11bc83.34±1.67a顶层12.88±0.02ab0.73±0.16a12.92±0.26a754.00±1.61b3.22±0.03c80.42±2.92a
注:所有理化生化指标以绝干计。感官评分换算成100分制。同列标注的不同字母表示差异性显著(P<0.05),相同字母表示差异不显著(P>0.05)
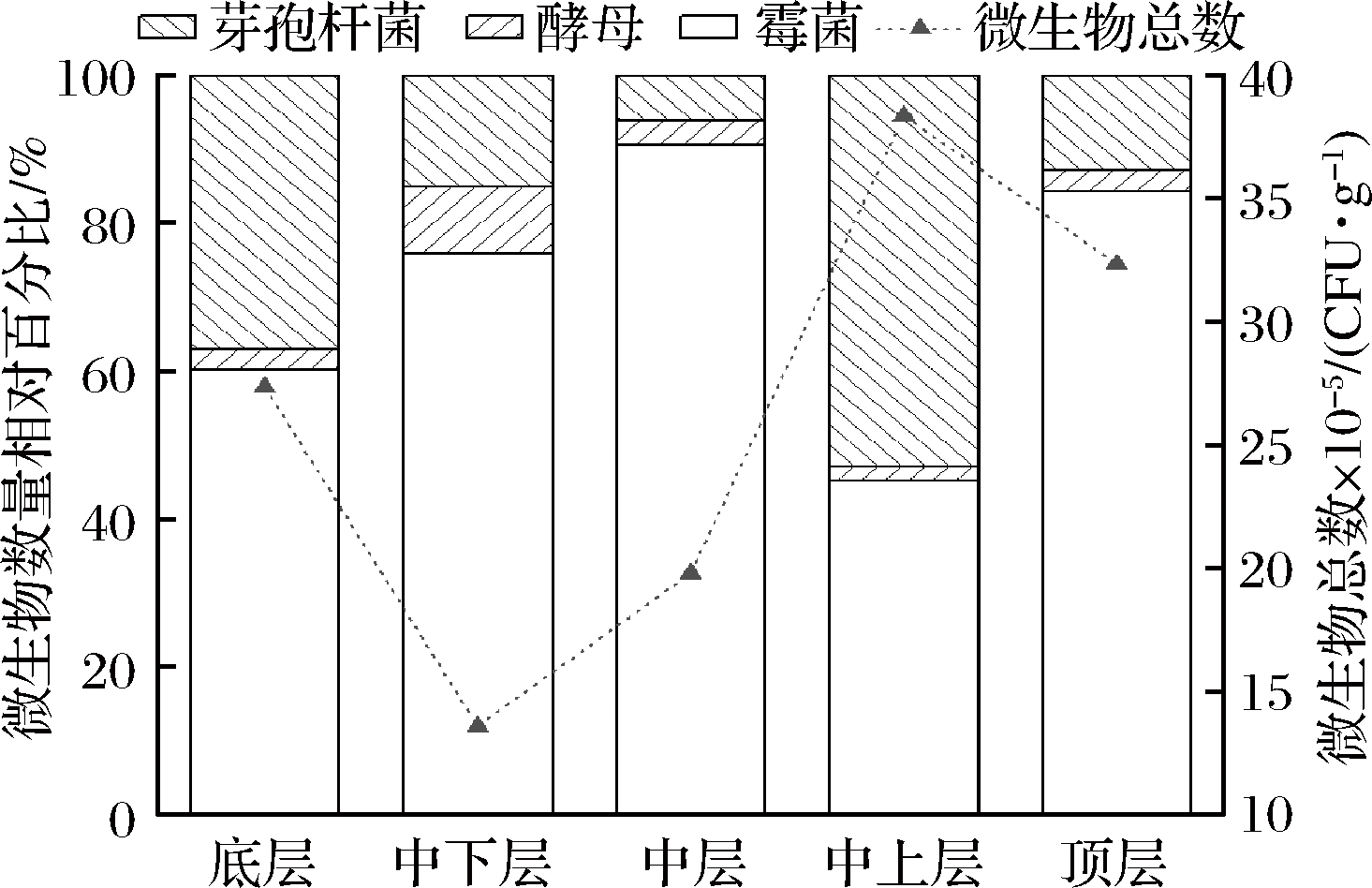
图1 大曲微生物总数及各类微生物相对百分比
Fig.1 The total number of microorganisms in Daqu
and the relative percentage of various microorganisms
大曲酸度主要是产酸菌的有机酸代谢,脂肪、淀粉等的降解[14],酒化力是大曲液化力、糖化力和微生物产酒能力的综合评价[8]。由表2可知,酸度、酒化力值,感官评分在各曲层间均差异不显著,可能是各曲层微环境的差异对于产酸和产酒等微生物的繁殖与代谢及感官评分没有明显影响。
由表2可知,酯化力,水分、氨基酸态氮含量在部分曲层差异显著。底层水分与中上层差异显著,底层水分最高(13.29%),可能是大曲在贮存过程中,水分受重力影响向下沉积,且底层温度相对较低,水分不易挥发。顶层氨基酸态氮含量与中下层、底层差异显著。大曲中游离氨基酸主要是原料中蛋白质的降解转化[15],与产蛋白酶微生物有关。顶层氧气充足,可能有利于产蛋白酶的芽孢杆菌与霉菌繁殖代谢。由图1知,顶层霉菌数比其余各曲层高[数量级约106 CFU/g(曲)],顶层霉菌和芽孢杆菌数量总和比中下层、底层霉菌和芽孢杆菌数量总和均值高60.82%。中层及以上曲层的酯化力值与中下层、底层差异显著。大曲酯化力是评价微生物代谢己酸乙酯酯酶的活力,其优势微生物是霉菌和酵母[16-17],中层及以上曲层温度较高、氧气较充足,有利于酵母和霉菌富集。顶层酵母数(数量级约104 CFU/g·曲)比底层酵母数高22.80%。且各曲层的酵母、霉菌总数均值比较,中层及以上曲层微生物总数比中下层、底层微生物总数高50.19%,从而导致大曲酯化力值差异。
2.2 不同曲层大曲的特征风味物质含量差异性分析
大曲风味物质是白酒香气的重要来源[18]。对样本进行挥发性物质检测,结合文献[7,10,19-22]中报道的风味物质,共确定42种大曲风味物质。其中酯类18种、醛酮类5种、醇类1种、芳香类6种、烷烯类9种、吡嗪类3种。酯类占总风味物质的质量百分比最大,为74.50%。经分析,中上层大曲风味物质种类数和总含量均较多,其挥发性成分总离子流图见图2。
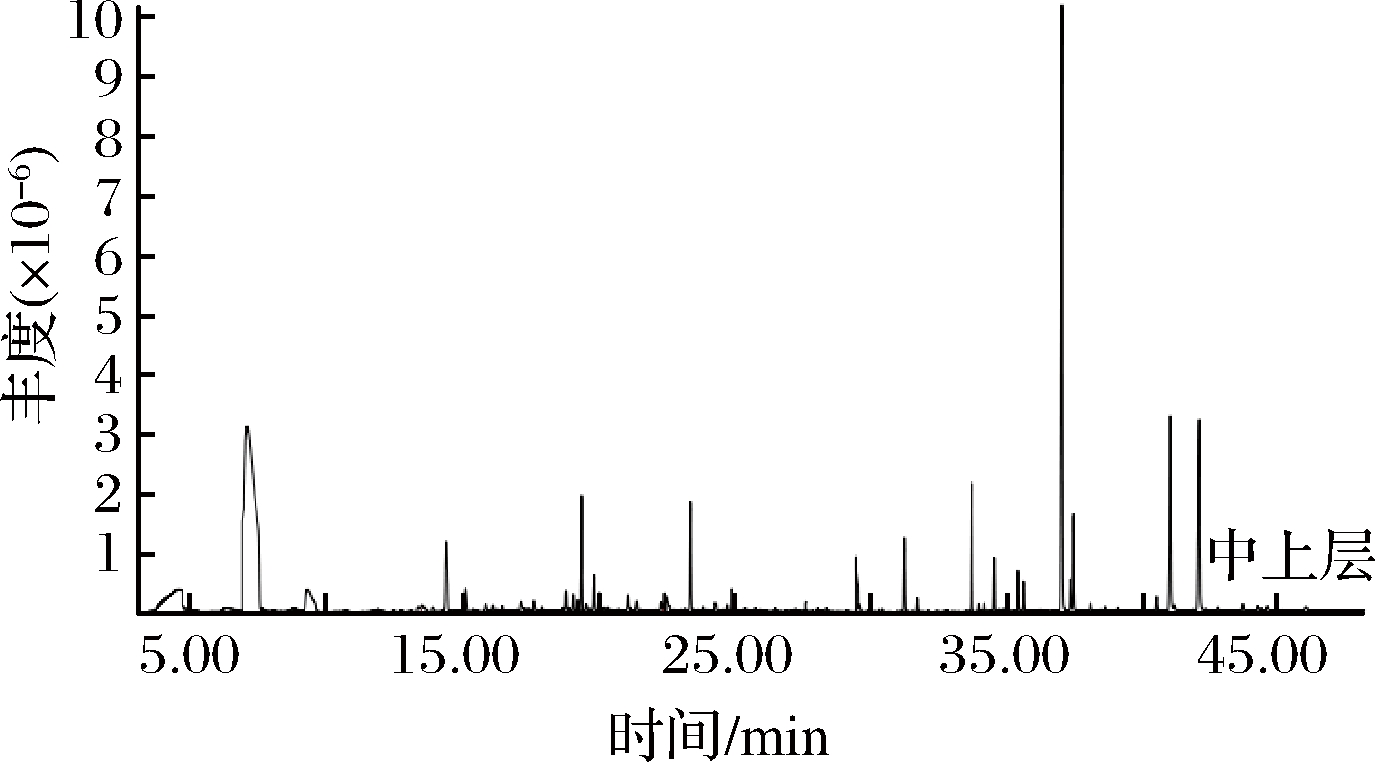
图2 中上层大曲挥发性成分总离子流图
Fig.2 Middle-upper Daqu volatile component
total ion current map
大曲中特征风味物质是大曲的关键性香气成分。OAV值越大,对整体香气贡献越大[13],以各曲层风味物质平均含量计算OAV值,得OAV值>1有辛酸乙酯、正己酸乙酯、十六酸乙酯、β-石竹烯,并结合文献[7,10,19-24]中报道的大曲主要风味物质:9-十六碳烯
酸乙酯、十二酸乙酯、十八酸乙酯、油酸乙酯、十四酸乙酯、亚油酸乙酯、壬酸乙酯、十五酸乙酯、苯乙醇、2,3,5,6-四甲基吡嗪、2,3,5-三甲基吡嗪,共选择出15种特征风味物质。
为比较各曲层15种特征风味物质含量的差异,进行单因素方差分析,结果见表3。
由表3可知,中上层大曲亚油酸乙酯含量与顶层差异显著,中上层亚油酸乙酯含量最高,为1 567.25 μg/kg。有研究表明,温度能促进长链酯类化合物的形成[24],中上层温度较高,可能有利于亚油酸乙酯的生成。其次,长链酯类的合成还与某些酵母有关[27],还待进一步研究。顶层亚油酸乙酯含量最低为79.25 μg/kg。亚油酸乙酯活泼不稳定,顶层氧气较充足,可能促进亚油酸乙酯氧化分解为醛、羧酸等复杂混合物[28]。除亚油酸乙酯以外的14种特征风味物质含量在各曲层间均不显著差异。张春林等[7]报道,中高温大曲在培菌阶段的总体风味物质含量已达到较高值。结合生产实践,随机翻曲后,可能对大曲的质量起到均质作用。贮存期各曲层间的湿度、温度、氧气等微环境及微生物分布的不同,并没有导致各曲层特征风味物质含量明显的差异。
表3 不同曲层大曲特征风味物质的含量
Table 3 Content of flavor substances in different curved layers

特征风味物质阈值[12,18-19,25-26]/(μg·kg-1)含量/(μg·kg-1)底层中下层中层中上层顶层9-十六碳烯酸乙酯-159.85±61.81a118.58±20.18a341.68±40.37a147.54±48.52a107.32±1.18a辛酸乙酯40.00161.92±4.38a45.56±26.98a154.80±32.68a153.69±10.10a74.37±6.74a十二酸乙酯400.00175.47±14.20a74.34±19.00a171.73±23.84a112.33±5.29a106.42±54.92a十八酸乙酯-40.19±5.33a34.10±16.82a53.78±5.30a61.49±4.23a46.50±30.36a油酸乙酯-606.72±260.78a552.78±20.14a824.48±106.91a564.85±283.57a638.03±352.33a壬酸乙酯-144.65±32.26a56.93±25.81a99.20±12.86a98.80±22.86a103.15±11.42a正己酸乙酯1.00438.45±22.32a318.46±84.83a749.30±12.89a614.85±239.77a333.96±45.28a十四酸乙酯-175.72±29.31a164.71±16.42a257.80±41.02a276.01±6.44a172.10±91.13a亚油酸乙酯-806.54±87.14ab672.08±24.72ab804.73±70.93ab1 567.25±32.35b79.25±13.86a十六酸乙酯2 000.001 936.29±342.45a1 780.06±176.43a2 323.20±202.83a2 722.75±336.48a1 771.99±36.69a十五酸乙酯-62.41±33.47a59.19±8.40a100.50±7.67a97.61±11.16a54.42±2.73a苯乙醇1 000.00483.74±72.30a254.72±19.37a245.210±41.89a376.81±77.45a268.13±36.34aβ-石竹烯64.00103.69±17.76a25.55±2.38a66.45±14.83a89.88±26.22a105.84±7.55a2,3,5,6-四甲基吡嗪10 000.00162.78±20.71a24.34±8.69a81.49±14.19a79.22±7.95a49.28±0.37a2,3,5-三甲基吡嗪56.0062.22±7.54a12.44±7.40a25.78±7.35a43.29±18.64a18.80±0.27a
注:表中化合物的阈值为在水中的阈值,“-”表示无法查到该化合物在水中的阈值。同行标注的不同字母表示差异性显著(P<0.05),同行标注的相同字母表示差异不显著(P>0.05)
2.2.1 酯类物质比较分析
由表3可知,中上层与中下层大曲比较,酯类物质中十六酸乙酯含量差值最大(942.69 μg/kg)。酯类物质的合成与有些芽孢杆菌相关[29]。
底层与顶层大曲比较,酯类物质中亚油酸乙酯含量差值最大(727.29 μg/kg)。底层芽孢杆菌较为丰富略低于中上层(数量级约106 CFU/g·曲),底层芽孢杆菌数比顶层高146.34%,可能是底层水分含量较多,有利于某些芽孢杆菌繁殖,从而促进酯类物质生成[29]。
2.2.2 芳香类物质及萜烯物质比较分析
由表3知,中上层与中下层比较,苯乙醇含量差值为122.09 μg/kg。苯乙醇的生成代谢主要与苯丙氨酸代谢相关[12,30]。中上层温度较高、氧气较充足,可能有利于一些酵母及芽孢杆菌繁殖代谢[30-31],促进苯乙醇生成。
底层与顶层比较,苯乙醇含量差值为215.62 μg/kg。底层芽孢杆菌数量较多,一些芽孢杆菌具有产蛋白酶的能力[31],从而促进苯乙醇生成。
中上层β-石竹烯含量比中下层更高,其差值为64.33 μg/kg;顶层β-石竹烯含量比底层略高。研究发现,萜烯类物质生成与某些酵母[32]和霉菌[33-34]有关。顶层、中上层氧气较充足,有利于富集好气性酵母和霉菌,可能有利于β-石竹烯生成,还待进一步研究。
2.2.3 吡嗪类物质比较分析
吡嗪类物质的形成与微生物酶和美拉德反应有关[35]。由表3知,中上层与中下层比较,2,3,5,6-四甲基吡嗪含量差值为54.89 μg/kg。中上层芽孢杆菌数最高,一些产蛋白酶的芽孢杆菌代谢产生氨基酸等物质,促进吡嗪类产生。
底层与顶层比较,2,3,5,6-四甲基吡嗪含量差值为113.50 μg/kg。底层芽孢杆菌数较多,经芽孢杆菌蛋白酶作用,产生大量氨基酸等物质,有利于吡嗪类物质的生成。除此以外,顶层大曲特征风味物质含量较少,可能还与自然挥发有关。
2.3 不同曲层大曲质量比较
2.3.1 不同曲层大曲理化生化指标、感官评分主成分及聚类分析
沈才洪等[8]在大曲传统评体系基础上,引入了生香力、酒化力,将理化指标和感官评分作为静态因子,生化指标作为动态因子。因此将各曲层理化生化指标值、感官评分进行主成分分析,提取2个主成分,累计贡献率达到87.14%,说明这2个主成分能够反映样本信息量。建立大曲综合得分F的数学模型:F=0.79F1+0.21F2,分析结果见表4。绘制不同曲层大曲质量评价指标主成分散点图,见图3。
由表4、图3可知,中上层综合得分最高,底层和中下层综合得分较低。中层和顶层聚为一簇,中上层、底层、中下层分别单独一簇。因此,大曲质量可分为4个不同的类别。
表4 不同曲层大曲质量的主成分分析
Table 4 Principal component analysis of Daqu
quality of different curved layers
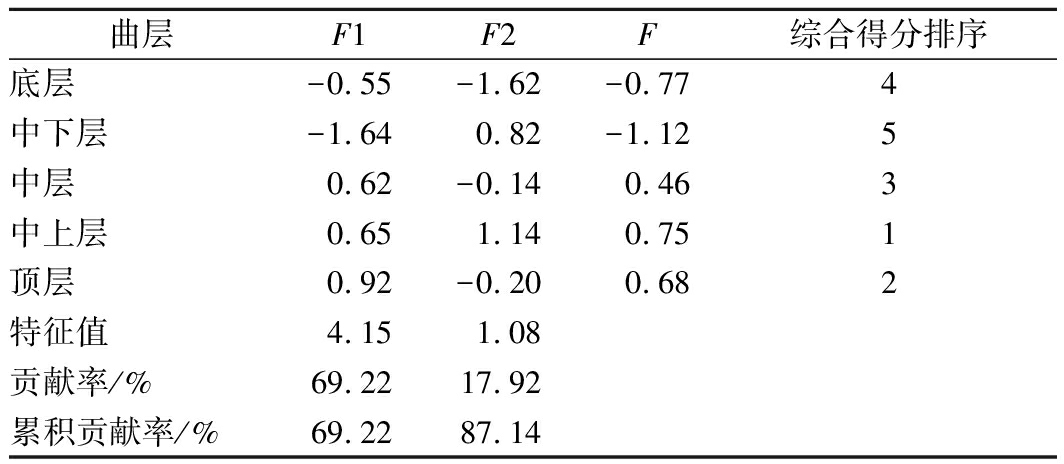
曲层F1F2F综合得分排序底层-0.55-1.62-0.77 4中下层-1.64 0.82-1.12 5中层0.62 -0.140.46 3中上层0.65 1.14 0.751顶层0.92 -0.200.68 2特征值4.151.08贡献率/%69.2217.92累积贡献率/%69.2287.14

图3 不同曲层大曲的质量主成分散点图
Fig.3 The main quality of the different curved layers of Daqu
2.3.2 不同曲层大曲特征风味物质主成分及聚类分析
随着分析技术的进步,大曲香气评价逐步进入大曲质量体系[10]。将各曲层的15种特征风味物质含量数据进行主成分分析,提取3个主成分,累计贡献率达到93.16%,说明这3个主成分能够反映样本信息量。建立大曲特征风味含量综合得分F的数学模型:F=0.53F1+0.31F2+0.16F3,分析结果见表5。绘制不同曲层特征风味物质主成分散点图,见图4。
表5 特征风味物质主成分得分及综合得分
Table 5 Main component score and comprehensive
score of characteristic flavor substances

曲层F1F2F3F综合得分排序底层-0.60 1.70 -0.15 0.18 3中下层-0.60 -1.26 -0.73 -0.82 5中层0.54 -0.31 1.81 0.48 2中上层1.640.12 -0.92 0.76 1顶层-0.98 -0.25 -0.01 -0.60 4特征值7.414.272.29贡献率/%49.3828.4915.29累积贡献率/%49.3877.8793.16
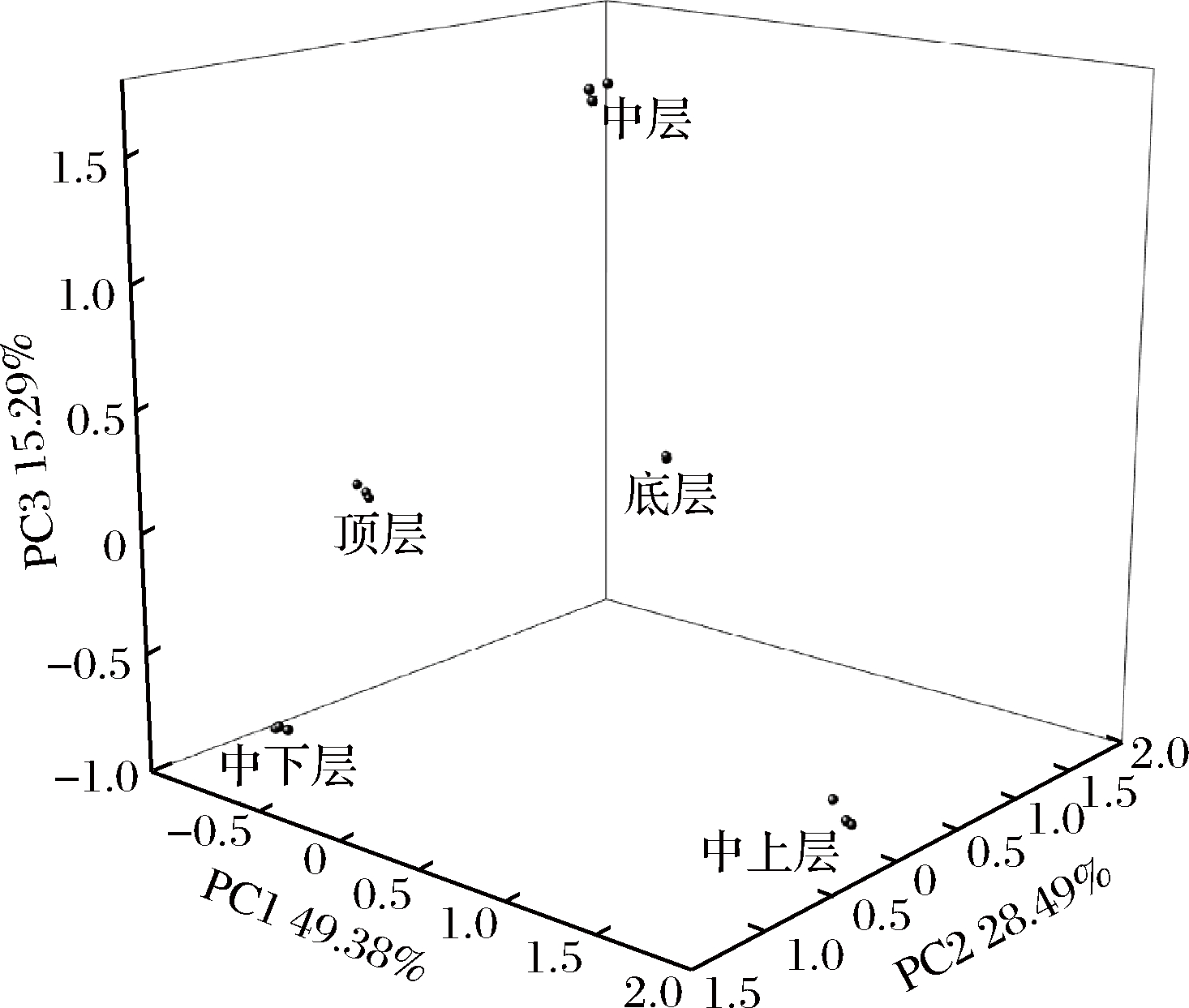
图4 不同曲层大曲特征风味物质主成分散点图
Fig.4 Dispersion point map of flavor material in different
curved layers
由表5、图4可知,中上层综合得分最高,中下层和顶层综合得分较低。中上层、中层分别单独聚为一簇,顶层、中下层、底层因距离较近,则聚为一簇。因此,大曲品质可分为3个不同类别。
结合2.3分析,中上层大曲质量最优。从理化生化指标、感官评分来评价,底层和中下层大曲品质较差;从特征风味物质含量来评价,中下层和顶层大曲品质较差。基于各曲层的理化生化指标值、感官评分的差异更为显著。因此,大曲质量评价应以理化生化指标、感官评分为主要,特征风味物质含量为辅助。
3 结论
经过对各曲层理化生化指标、感官评分的分析,底层大曲水分含量与中上层差异显著;顶层大曲的氨态氮含量与中下层、底层差异显著;中层及以上曲层酯化力值与中下层、底层差异显著。对大曲的15种特征风味物质含量比较分析,中上层大曲亚油酸乙酯含量与顶层差异显著。
综合大曲的理化生化指标、感官评分和特征风味物质含量评价,中上层大曲质量为最优。从理化生化指标、感官评分来分析,底层和中下层大曲品质较差;从特征风味物质含量来分析,中下层和顶层大曲品质较差。因此,建议不同曲层配合使用,并对制曲工艺进行改进,如顶层大曲根据温度变化适当加强草帘覆盖,防止风味物质挥发;底层大曲可加强保温,防止曲虫的破坏等。
大曲风味物质的变化与微环境差异和微生物分布不同的关联,以及结合高通量测序技术分析大曲中微生物群落结构,更深入地揭示大曲风味物质与微生物之间的关系,还有待后续研究。本研究受到样品季节和数量的局限、已定性风味物质的数据库的限制等因素的影响,以及大曲特征风味物质的确定,还有待深入研究。本研究结果为大曲质量的优化和制曲工艺的改进提供了依据,从而促进制曲生产标准化、规模化发展,有利于白酒生产企业的可持续健康发展。
[1] 张春林,敖宗华,炊伟强,等.顶空固相微萃取-气质联用快速测定大曲中的挥发性风味成分[J].食品科学,2011,32(10):137-140.
[2] JIN Y,LI D,AI M,et al. Correlation between volatile profiles and microbial communities:A metabonomic approach to study Jiang-flavor liquor Daqu [J].Food Research International,2019,121:1-20.
[3] 尚英,许德富,张宿义,等.中高温大曲多层曲坯立体培菌发酵过程的温度演变趋势探讨[J].酿酒,2017,44(3):30-35.
[4] 明红梅,周健,许德富,等.低温季节楼盘式制曲中大曲微生物变化趋势的初步研究[J].酿酒科技,2014(5):39-42.
[5] 杨勇,李燕荣,姜雷,等.中高温大曲曲块部位间生化指标的差异及变化规律研究[J].食品与发酵工业,2019,45(19):73-78.
[6] 李登勇,黄钧,丁晓菲,等.酱香型大曲的挥发性组分时空性特征的分析[J].食品与发酵工业,2018,44(7):243-249.
[7] 张春林,敖宗华,炊伟强,等.固相微萃取-气相色谱-质谱法分析中高温大曲发酵、贮存过程中挥发性风味成分的变化[J].食品与发酵工业,2011,37(4):198-203.
[8] 沈才洪,张良,应鸿,等.大曲质量标准体系设置的探讨[J].酿酒科技,2005(11):19-24.
[9] QB/T 4257—2011,酿酒大曲通用分析方法[S]. 北京:中国轻工业出版社,2012.
[10] 明红梅,姚霞,周健,等.中高温浓香型大曲中挥发性香味物质分析[J].酿酒科技,2015(6):73-79.
[11] 田力.《气相色谱-质谱联用仪》校准规范实际应用经验[J].中国计量,2010(12):93.
[12] 孟维一,黄明泉,孙宝国,等.HS-SPME结合GC-O-MS技术分析不同大曲中的香气活性化合物[J].食品工业科技,2017,38(6):54-61;78.
[13] 宋诗清,童彦尊,冯涛,等.金佛手香气物质的多维分析及其特征香气物质的确定[J].食品科学,2017,38(24):94-100.
[14] 周斐成,吴生文,朱庆圣,等.特香型大曲发酵过程中曲块不同部位理化指标及主要酶系动态分析[J].中国酿造,2019,38(4):58-64.
[15] 曹振华,沈才洪,秦辉,等.泸型大曲中曲香与微生物和生理生化指标间的关系[J].酿酒科技,2016(3):42-44;48.
[16] 何培新,胡晓龙,郑燕,等.中国浓香型白酒“增己降乳”研究与应用进展[J].轻工学报,2018,33(4):1-12.
[17] 郭通航,王沙莉,夏海锋,等.伯克霍尔德氏菌胞外酯酶催化己酸乙酯合成的研究[J].酿酒科技,2015(7):51-55.
[18] ZHANG W X,WU Z Y,ZHANG Q S,et al.Combination of newly developed high quality Fuqu with traditional Daqu for Luzhou -flavor liquor brewing[J]. World Journal of Microbiology & Biotechnology,2009,25(10):1 721-1 726.
[19] 周健,郭志,明红梅,等.优质中高温浓香型大曲主要香味成分的初步研究[J].酿酒科技,2014(4):11-14.
[20] 范文来,徐岩.酒类风味化学[M].北京:中国轻工业出版社.2014.
[21] 郑佳,彭智辅,赵东.中国传统酿酒大曲的风味化学研究进展[J].酿酒科技,2017(3):89-94.
[22] 陈勇,陈泽军,周瑞平,等.顶空固相微萃取-气相色谱-质谱法测定大曲中的挥发性组分[J].中国调味品,2013,38(2):70-75.
[23] ZHANG C,AO Z,CHUI W Q,et al.Characterization of the aroma-active compounds in Daqu:a tradition Chinese liquor starter[J].European Food Research and Technology,2012,234(1):69-76.
[24] 夏玙,罗惠波,周平,等.热风干燥工艺对贮存期大曲挥发性物质的影响[J].食品与发酵工业,2018,44(6):126-132.
[25] 里奥·范海默特,刘强.化合物香味阈值汇编[M].北京:科学出版社, 2015.
[26] 孙宝国,陈海涛.食用调香术[M].北京:化学工业出版社.2017.
[27] 丘梓俊.影响豉香型白酒中高级脂肪酸乙酯生成的因素及其形成机理[J].轻工标准与质量,2019(1):76-78.
[28] 徐寿昌.有机化学[M].北京:高等教育出版社,1993.
[29] 罗莉,李欣,常煦.等.芽孢杆菌在中国白酒酿造中的应用机理研究进展[J].酿酒科技,2019(1):99-104.
[30] 杜闪,王雪花,杨政茂,等.生物转化合成β-苯乙醇代谢途径及其调控的研究[J].食品与发酵工业,2014,40(1):168-173.
[31] 罗建超,谢和.大曲中产酱香芽孢杆菌的筛选及其代谢产香探析[J].酿酒科技,2012(5):35-40.
[32] 卜光明,周化斌,周茂洪,等.酿造酒中非酿酒酵母的研究进展[J].食品工业科技,2019,40(14):346-352.
[33] 张璐璐,范刚,何进,等.柠檬烯微生物转化及其相关酶的研究进展[J].食品工业科技,2019,40(12):317-325;330.
[34] 李纪顺,陈凯,杨合同,等.木霉抗生性代谢产物研究进展[J].农药,2010,49(10):713-716;719.
[35] ZHENG J,ZHAO D PENG Z,et al.Variation of aroma profile in fermentation process of Wuliangye baobaoqu starter[J]. Food Research International,2018,114:64-71.