食品中的蛋白质和多糖通过氢键、疏水相互作用、范德华力、离子桥联或共价键等形成具有一定三维网络凝胶结构的连结,形成具有独特的质地结构和感官特性的凝胶,如豆腐、肉皮冻、果冻[1-4]。蛋白-多糖凝胶的研究扩大了蛋白与胶的使用范围,为食品的研究和发展开辟了一条新的渠道。蛋白通过受热变性后结构展开,分子凝聚形成具有三维空间网络结构的凝胶,蛋白质的两性结构及凝胶形成的网络空间也为包载花青素、姜黄素等生物活性物质提供了空间[5-8]。乳清分离蛋白(whey protein isolate,WPI)是是乳清经过浓缩精制得到的蛋白质,具有一定营养价值和生物活性,常作为一种食品添加剂来提高食品的凝胶、乳化等功能特性[9]。高酰基结冷胶(high acyl gellan gum,HG)是一种微生物多糖,其形成的凝胶黏弹且柔软,且受Ca2+等离子影响较小,在乳品及果汁饮料中作为增稠剂和稳定剂使用[10-12]。
乳清蛋白与蓝莓果胶通过静电作用形成的复合物,能够提高复合物的黏度,并促进蛋白质-蓝莓果泥的稳定性[13]。酸化牛奶中酪蛋白与结冷胶结合可以形成连续的凝胶网络,增强了复合物的质地特性[14]。结冷胶作为复配胶的材料成为食品领域研究的热点,它可溶解在热牛奶中,冷却时形成的网络结构可以悬浮巧克力牛奶饮料中的可可粉微粒,并能够稳定奶昔、冰淇凌;在生物医学方面,通过封装活性原料用于药物控制释放[15-16]。
目前改进凝胶形成方式,开发新型的凝胶产品,受到极大关注。本论文采用乳清分离蛋白(whey protein isolate,WPI)、高酰基结冷胶为材料,制备乳清分离蛋白-高酰基结冷胶混合凝胶(WPI-HG),分析乳清分离蛋白和高酰基结冷胶的相互作用,为拓展乳清分离蛋白和多糖的新型凝胶食品,提高传统食品的质量,改善食品的加工工艺提供基础理论数据。
1 材料与方法
1.1 材料与试剂
高酰基结冷胶(食品级),美国唐瑞斯食品物料公司;乳清分离蛋白(WPI9410),美国希里玛公司,其他试剂均为分析纯。
1.2 仪器与设备
722S型可见分光光度计,上海菁华科技仪器有限公司;数显恒温水浴锅,HH-2,金坛市瑞尔电器有限公司;HC-3018R冷冻离心机,安徽中科中佳科学仪器有限公司;LGJ-10真空冷冻干燥机,北京松源华兴科技发展有限公司;TA-XT plus质构仪,英国Stable Micro Systems公司;Nicolet 6700傅里叶红外光谱仪,美国Thermo Nicolet公司;钨灯丝扫描电子显微镜EVO MA15,德国卡尔蔡司股份公司;HAAKE RS6000型流变仪,赛默飞世尔科技公司;UV1800紫外分光光度计,日本岛津公司。
1.3 实验方法
1.3.1 混合凝胶配制
分别配制200 g/L的乳清分离蛋白溶液和10 g/L的高酰基结冷胶溶液,放置4 ℃条件下过夜备用。按照不同比例配制乳清分离蛋白-高酰基结冷胶溶液(WPI-HG),使混合液中乳清分离蛋白含量为100 g/L,高酰基结冷胶质量浓度分别为1、1.5、2、2.5、3和4 g/L[分别为WPI+HG(1 g/L)、WPI+HG(1.5 g/L)、WPI+HG(2 g/L)、WPI+HG(2.5 g/L)、WPI+HG(3 g/L)、WPI+HG(4 g/L)],并在95 ℃加热0.5 h,冷却后4 ℃下稳定20 h,形成凝胶。
1.3.2 凝胶强度(gel strength)
采用质构仪分析凝胶强度。使用P 0.5探头,测前、中、后速度为1 mm/s,感应力为3 g。平行测量3次。
1.3.3 凝胶保水性(water holding capacity)
将样品在10 000 r/min的离心机中离心15 min,用定性滤纸吸去水分。测定样品离心前后质量,按公式(1)计算保水率:
(1)
式中:w,凝胶保水率,%; m0,离心前凝胶质量,g; m1,离心后凝胶质量,g。
1.3.4 凝胶透光率(transmittance)
将凝胶放置于1 cm比色管中,测其在620 nm处的透光率。
1.3.5 游离巯基分析
使用Tris-Gly将样品稀释至蛋白含量1 mg/mL,8 000 r/min离心15min,取3 mL上清液并加入30 μL DTNB溶液,混匀后反应15 min,测定412nm处吸光度,采用公式(2)计算游离巯基含量:
(2)
式中: δ,游离巯基含量,μmol/g 蛋白;A412,412 nm处的吸光度值;D,稀释倍数; ρ,蛋白质质量浓度,mg/mL。
1.3.6 流变学性质测定
动态温度扫描参数设定:温度变化范围25~95 ℃,升温速度为2 ℃/min,保持10 min,降温速率4 ℃/min,扫描应变为0.01%,扫描频率为1 Hz,每个样品做3次平行,使用甲基硅油密封。
1.3.7 傅里叶红外光谱分析
样品冷冻干燥后,采用KBr压片后使用傅里叶红外光谱仪进行扫描检测,扫描范围4 000~400 cm-1,分辨率为4 cm-1。
1.3.8 扫描电子显微镜分析
样品冷冻干燥后,喷金后采用钨灯丝电子扫描电镜观察。
1.3.9 数据统计与分析
采用软件Origin 9和SPSS 24对试验数据进行分析和作图,数据结果用平均值±标准差来表示,显著性差异分析采用单因素方差分析(One-way ANOVA)进行,显著水平α=0.05。
2 结果与分析
2.1 高酰基结冷胶浓度对混合凝胶形成的影响
制备的乳清分离蛋白-高酰基结冷胶混合凝胶图片如图1所示。由图1可知,高酰基结冷胶对混合凝胶的形成具有显著作用,随着高酰基结冷胶浓度增大,混合凝胶的外观结构逐步稳定,在高酰基结冷胶质量浓度3 g/L时,能够形成稳定的凝胶。

a-WPI+HG(1 g/L);b-WPI+HG(1.5 g/L);c-WPI+HG(2 g/L);
d-WPI+HG(2.5 g/L);e-WPI+HG(3 g/L);f-WPI+HG(4 g/L)
图1 乳清分离蛋白-高酰基结冷胶混合凝胶图片
Fig.1 Visual observation of WPI-HG gels
2.2 高酰基结冷胶质量浓度对混合凝胶硬度的影响
高酰基结冷胶质量浓度对乳清分离蛋白-高酰基结冷胶混合凝胶的凝胶强度影响如图2所示。从图2可以看出,高酰基结冷胶浓度对凝胶强度的影响显著。随着高酰基结冷胶浓度的增加,混合凝胶的强度不断增强,在4 g/L时,凝胶强度最大,为26.97 g,表明高酰基结冷胶可以提高乳清分离蛋白-高酰基结冷胶混合凝胶的凝胶强度。
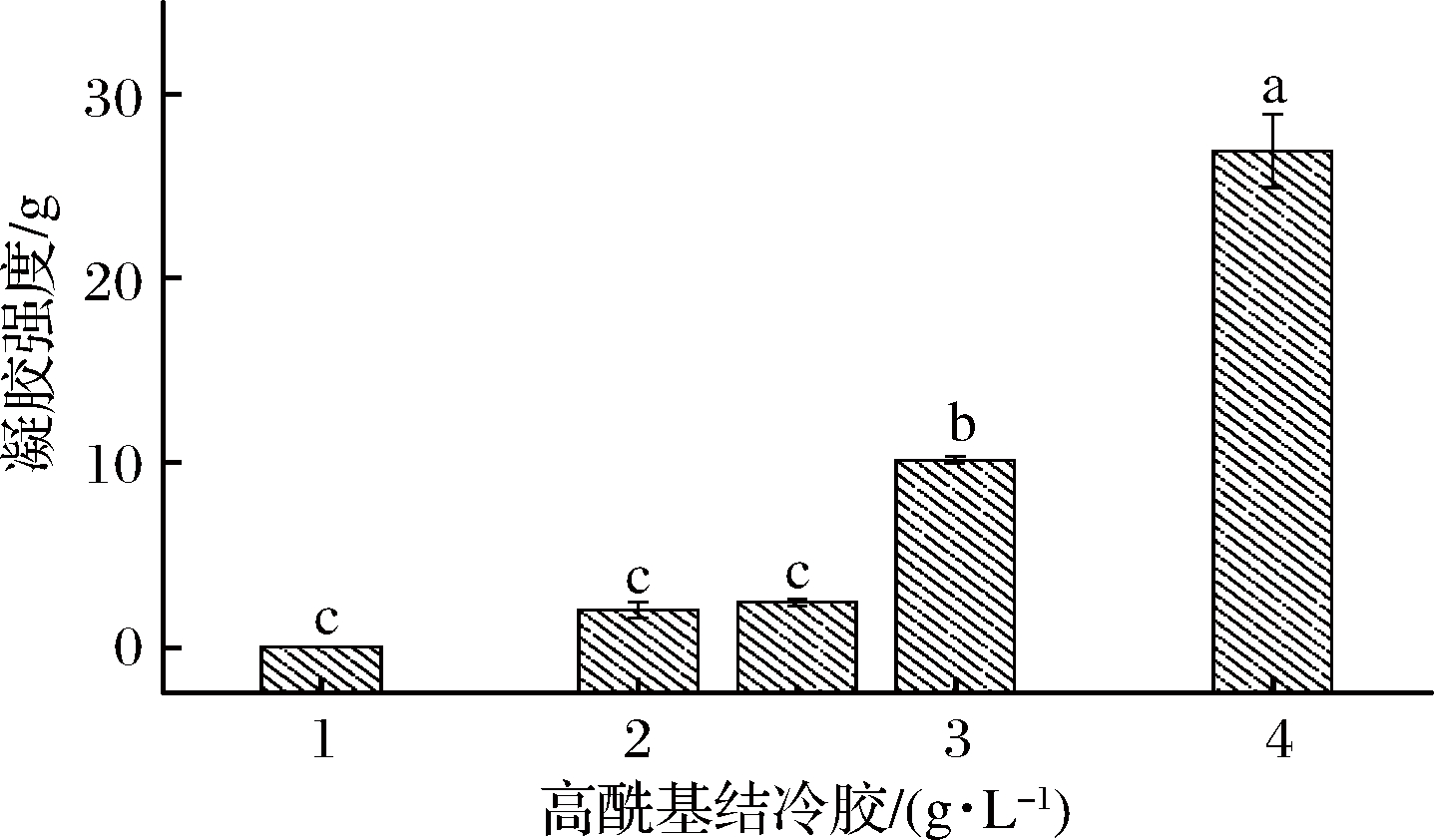
图2 乳清分离蛋白-高酰基结冷胶混合凝胶的强度
Fig.2 The gel strength of WPI-HG gels
2.3 高酰基结冷胶浓度对混合凝胶保水性的影响
高酰基结冷胶对混合凝胶的保水性影响如图3所示。随着高酰基结冷胶添加量的增加,混合凝胶的保水性明显上升,其中高酰基结冷胶为2.5 g/L时,保水性最大,为97.41%,这可能是高酰基结冷胶富含大量亲水基团,能够结合大量水分子,且形成的乳清分离蛋白-高酰基结冷胶混合凝胶具有一定的网络,也增加了对水分的束缚作用。这一结果与魔芋葡甘聚糖-咸蛋清蛋白混合凝胶等的凝胶特性一致[17-19]。
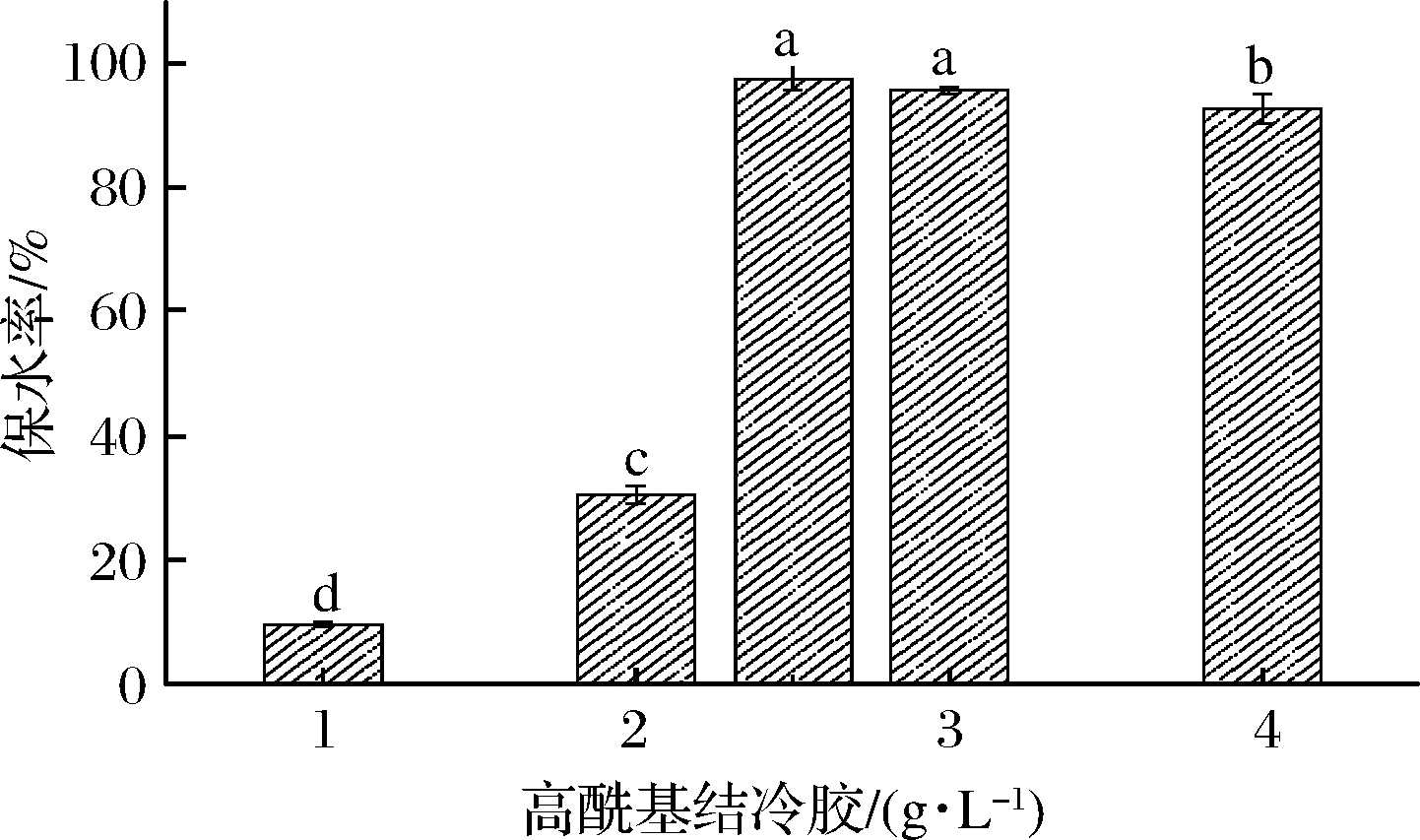
图3 乳清分离蛋白-高酰基结冷胶混合凝胶的保水性
Fig.3 The water holding capacity of WPI-HG gels
2.4 高酰基结冷胶浓度对混合凝胶透光率的影响
高酰基结冷胶对混合凝胶的透过光率影响如图4所示。
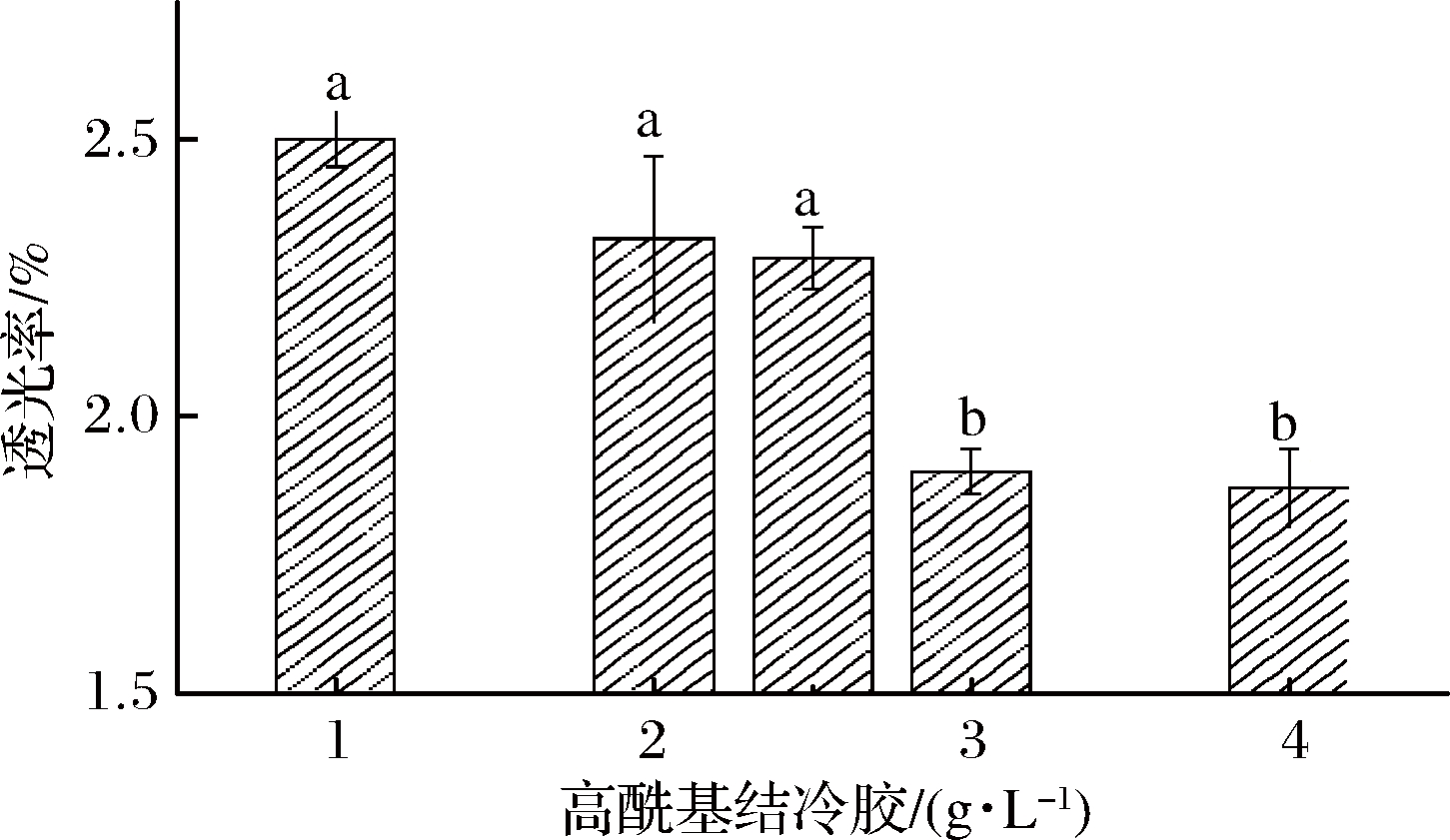
图4 乳清分离蛋白-高酰基结冷胶混合凝胶的透光率
Fig.4 The transittance of WPI-HG gels
由图4可以看出,随着高酰基结冷胶质量浓度的增大,混合凝胶的透光率逐渐降低,这可能是随着高酰基结冷胶浓度增加,形成的混合凝胶结构更加精密所致。
2.5 游离巯基分析
游离巯基形成的二硫键能够有效增强蛋白质分子间作用力,对凝胶的形成具有重要作用[19],如图5所示。
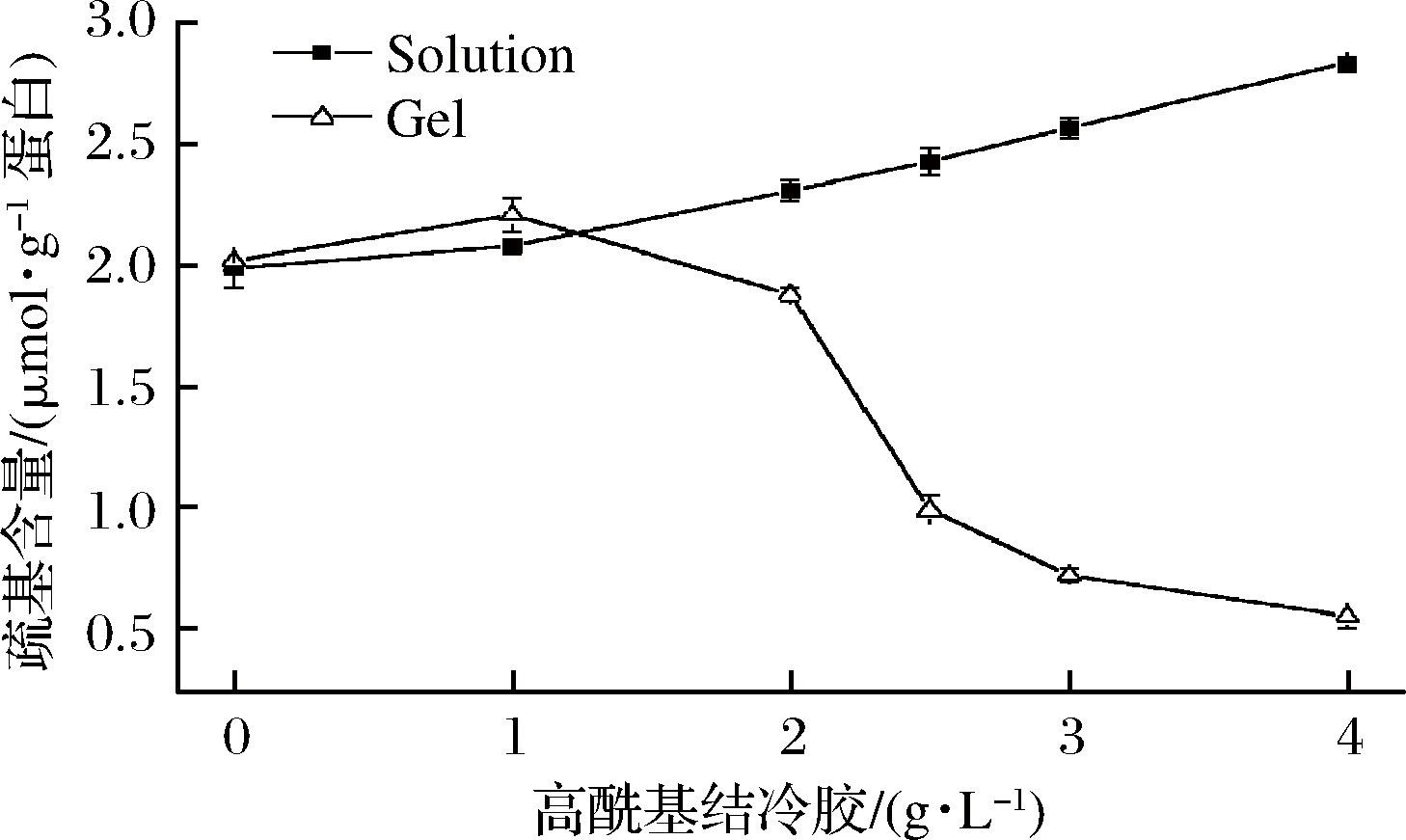
图5 乳清分离蛋白-高酰基结冷胶溶液和凝胶的
巯基含量
Fig.5 Free SH contents of solution and gel
未加热的混合溶液中巯基含量随着高酰基结冷胶含量增大而显著增加(P<0.05),加热后的凝胶中巯基含量显著降低。说明乳清分离蛋白与高酰基结冷胶的结合,阻碍了蛋白质游离巯基间的结合,从而提高了溶液中游离巯基含量;加热凝胶化过程中游离巯基相结合形成二硫键,且随着高酰基结冷胶含量增加,游离巯基减少,形成的二硫键增多,这也与凝胶强度增大结果一致。
2.6 混合凝胶溶液的流变学特性
温度扫描能够反应凝胶形成过程中的动态黏弹性变化,储能模量G′值能够反应样品的弹性特性或材料的固体样性质,耗损模量G″反应样品的黏性特性[20]。乳清分离蛋白-高酰基结冷胶溶液的温度扫描结果如图6所示。
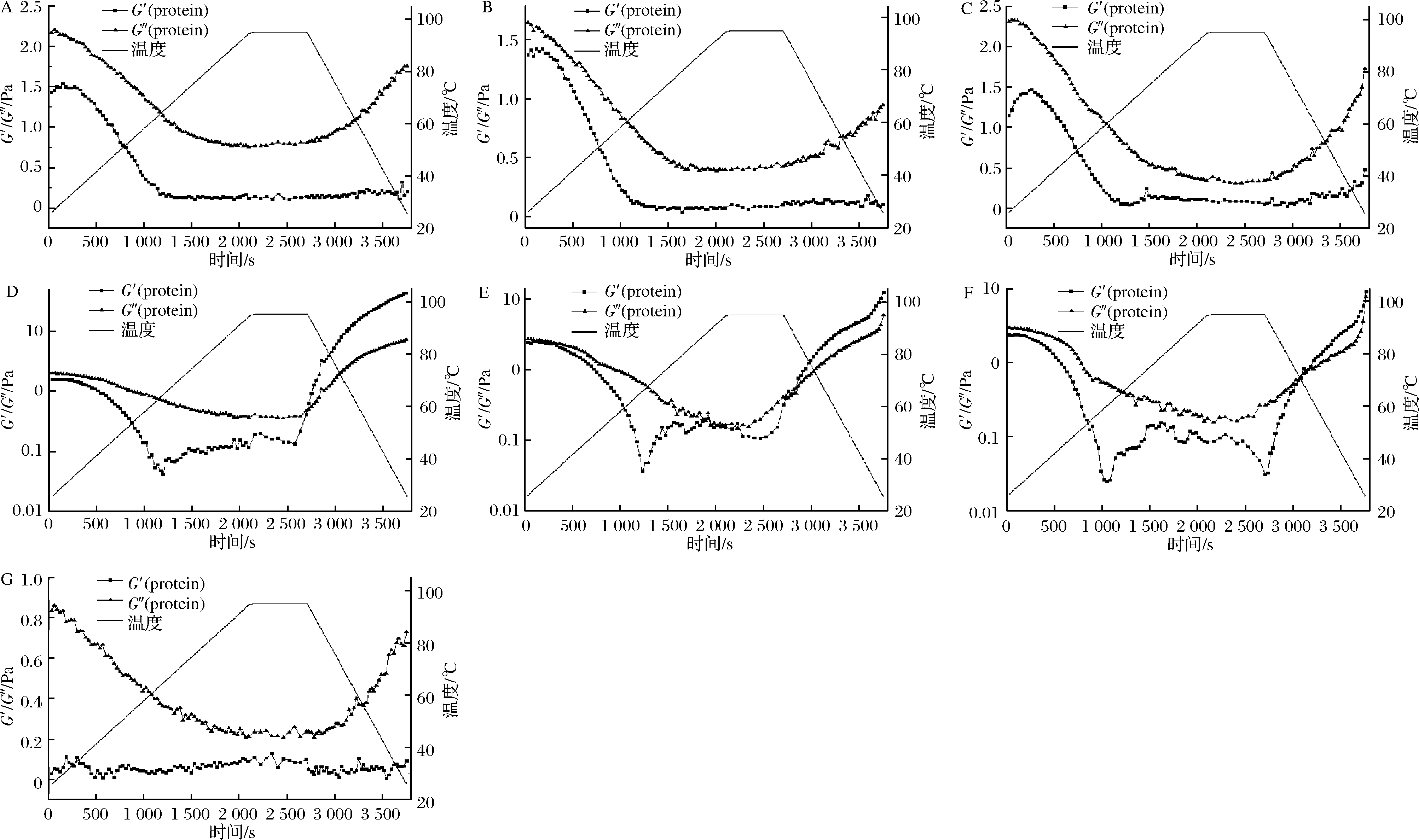
A-WPI溶液;B-WPI+HG(1 g/L)溶液;C-WPI+HG(2 g/L)溶液;D-WPI+HG(2.5 g/L)溶液;E-WPI+HG(3 g/L)溶液;
F- WPI+HG(4 g/L)溶液;G- HG(4 g/L)溶液
图6 乳清分离蛋白-高酰基结冷胶溶液的流变性质
Fig.6 Temperature scan of composites during thermal gelation
由图6-A、图6-B、图6-C和图6-G可以看出,溶液的G″均大于G′,说明这几种溶液主要表现为液体的粘性特性。从图6-D、图6-E、图6-F可以看出,随着高酰基结冷胶添加量增加,其黏弹性发生明显变化,在1 000 s后,G′均明显增大,说明开始形成蛋白凝胶网络,在2 600 s后,G′显著上升,且大于G″值,说明此时体系发生相变,表现为固体的弹性特性;添加2.5 g/L高酰基结冷胶发生相变的时间约2 700 s,添加3.0 g/L高酰基结冷胶的体系需要2 830 s,添加4 g/L高酰基结冷胶的体系需要约3 060 s,这说明了高酰基结冷胶能够促使乳清分离蛋白形成热凝胶,且随着含量增加其形成稳定凝胶所需时间增加,也说明提高高酰基结冷胶含量可以提高乳清分离蛋白相转变温度。
2.7 混合凝胶微观结构分析
混合凝胶的显微结构电镜图如图7所示。可以看出,高酰基结冷胶呈现孔径较大的网络结构,且空隙不规则;乳清分离蛋白呈不规则片状,且有非常明显的蛋白质颗粒[21]。乳清蛋白-高酰基结冷胶混合凝胶呈现紧密堆叠结构,且随着高酰基结冷胶浓度的增大,形成孔径较小的立体网络结构,这也为负载生物活性物质提供了空间。

a-HG;b-WPI;c-WPI+HG(2 g/L);
d-WPI+HG(3 g/L);e-WPI+HG(4 g/L)
图7 显微结构观察
Fig.7 SEM of the microstructure
2.8 混合凝胶的FTIR分析
乳清分离蛋白-高酰基结冷胶混合凝胶的傅里叶红外光谱扫描结果如图8所示。乳清分离蛋白和乳清分离蛋白-高酰基结冷胶混合凝胶的红外光谱图趋势整体一致,说明没有形成新的共价键。乳清分离蛋白在1 500~1 600 cm-1之间的吸收代表了蛋白质分子的C—N拉伸振动峰或N—H弯曲振动峰,属于酰胺II带,是蛋白质的特征峰[19],1 531 cm-1和1 631 cm-1处的吸收分别代表了蛋白质分子中Lys的NH3+的弯曲振动和His的C![]() C伸缩振动[22]。这些特征峰在乳清蛋白-高酰基结冷胶凝胶中也有体现,其中1 531 cm-1处吸收峰向短波数1 523 cm-1偏移,1 631 cm-1处偏移至1 627 cm-1,说明乳清蛋白与高酰基结冷胶分子间存在氢键和静电相互作用[17]。氢键与静电作用也可能是高酰基结冷胶与乳清分离蛋白能够形成稳定的凝胶结构的重要原因。
C伸缩振动[22]。这些特征峰在乳清蛋白-高酰基结冷胶凝胶中也有体现,其中1 531 cm-1处吸收峰向短波数1 523 cm-1偏移,1 631 cm-1处偏移至1 627 cm-1,说明乳清蛋白与高酰基结冷胶分子间存在氢键和静电相互作用[17]。氢键与静电作用也可能是高酰基结冷胶与乳清分离蛋白能够形成稳定的凝胶结构的重要原因。
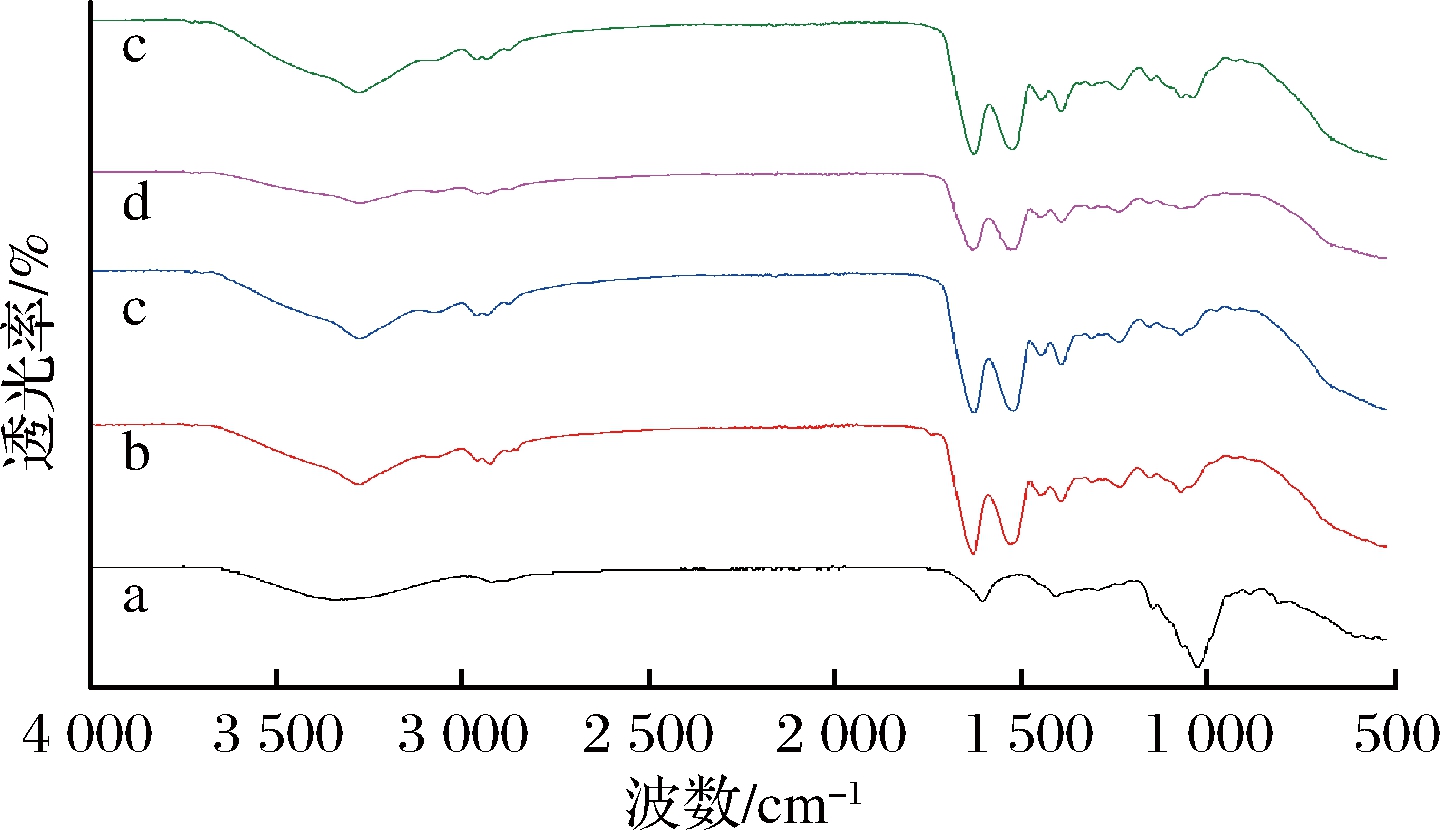
a-HG;b-WPI;c-WPI+HG(2 g/L);d-WPI+HG(3 g/L);
e-WPI+HG(4 g/L)
图8 红外光谱分析
Fig.8 FTIR spectra
3 结论
本文研究了高酰基结冷胶浓度对乳清分离蛋白-高酰基结冷胶复合凝胶的影响,结果表明混合凝胶的凝胶强度和保水性均优于乳清分离蛋白凝胶,且随着高酰基结冷胶浓度增大而增大,高酰基结冷胶的浓度为3 g/L时,可形成形态稳定的混合凝胶;浓度为4 g/L时,复合凝胶的凝胶强度最大为26.97 g,保水性最好为97.41%,透光率最低为1.87%。高酰基结冷胶增加了乳清分离蛋白溶液的游离巯基含量,有利于加热形成二硫键,增强凝胶结构,且高酰基结冷胶含量增加可以提高混合凝胶相转变温度。红外光谱结果表明乳清分离蛋白与高酰基结冷胶之间存在分子间作用力,微观结构表明复合凝胶形成结构均匀的立体网络结构。
[1] WEI G, SU Z, REYNOLDS N P, et al. Self-assembling peptide and protein amyloids: from structure to tailored function in nanotechnology[J]. Chemical Society Reviews, 2017, 46(15): 4 661-4 708.
[2] YU Z, XU Q, DONG C, et al. Self-assembling peptide nanofibrous hydrogel as a versatile drug delivery platform[J]. Current Pharmaceutical Design, 2015, 21(29): 4 342-4 354.
[3] 金星, 迟涛, 于鑫欣, 等. 热处理乳清蛋白对凝固型酸乳凝胶品质的影响[J]. 食品工业科技, 2018, 39(16):8.
[4] 王岩, 王存堂, 蒋继丰, 等. 离子强度和温度对乳清蛋白凝胶的影响[J]. 食品科学, 2010,31(1): 123-126.
[5] 卢晓明, 王静波, 任发政, 等. 乳清蛋白在食品工业中的应用[J]. 食品科学, 2010,31(1): 262-267.
[6] FU W, NAKAMURA T. Explaining the texture properties of whey protein isolate/starch co-gels from fracture structures [J]. Bioscience, Biotechnology, and Biochemistry, 2017, 81(4): 839-847.
[7] ÇAKIR E, DAUBERT C R, DRAKE M A, et al. The effect of microstructure on the sensory perception and textural characteristics of whey protein/κ-carrageenan mixed gels [J]. Food Hydrocolloids, 2012, 26(1): 33-43.
[8] BETZ M, KULOZIK U. Whey protein gels for the entrapment of bioactive anthocyanins from bilberry extract [J]. International Dairy Journal, 2011, 21(9): 703-710.
[9] LIU K, LI Q M, ZHA X Q, et al. Effects of calcium or sodium ions on the properties of whey protein isolate-lotus root amylopectin composite gel[J]. Food Hydrocolloids, 2019, 87: 629-636.
[10] 张帆. 高酰基结冷胶的乳化特性及其对β-胡萝卜素乳液稳定性、消化特性的影响[D].杭州:浙江工商大学,2018.
[11] YANG X, HOU Y, GONG T, et al. Concentration-dependent rheological behavior and gelation mechanism of high acyl gellan aqueous solutions[J]. International Journal of Biological Macromolecules, 2019, 131: 959-970.
[12] MORRIS E R, NISHINARI K, RINAUDO M. Gelation of gellan-a review[J]. Food Hydrocolloids, 2012, 28(2): 373-411.
[13] CHEVALIER L M, RIOUX L E, ANGERS P, et al. Study of the interactions between pectin in a blueberry puree and whey proteins: Functionality and application[J]. Food Hydrocolloids, 2019, 87: 61-70.
[14] BULDO P, BENFELDT C, CAREY J P, et al. Interactions of milk proteins with low and high acyl gellan: Effect on microstructure and textural properties of acidified milk[J]. Food Hydrocolloids, 2016, 60: 225-231.
[15] YUAN C R, MORRISON N A, CLARK R. Calcium stable high acyl gellan gum for enhanced colloidal stability in beverages: U.S. Patent Application 14/507,497[P]. 2015-2-12.
[16] OLIVEIRA CARDOSO V M, CURY B S F, EVANGELISTA R C, et al. Development and characterization of ross-linked gellan gum and retrograded starch blend hydrogels for drug delivery applications[J]. Journal of the Mechanical Behavior of Biomedical Materials, 2017, 65: 317-333.
[17] 谭芦兰,唐宏刚,杨慧娟,等.魔芋胶对咸蛋清蛋白热诱导凝胶特性的影响[J/OL].中国食品学报:1-10[2019-08-28].http://kns.cnki.net/kcms/detail/11.4528. TS.20190613.1029.002.html.
[18] 李荣,马慧婷,姚兰英,等.低酰基结冷胶-乳清蛋白混合凝胶的凝胶特性[J].现代食品科技,2018, 34(1):31-37.
[19] LIU Kang, LI Qiangming, ZHA Xueqiang, et al. Effects of calcium or sodium ions on the properties of whey protein isolate-lotus root amylopectin composite gel[J]. Food Hydrocolloids, 2019,87:629-636.
[20] 朱桂兰, 叶银杉, 葛洁, 等.低酰基结冷胶-果胶复配体系的性能[J].食品科学,2017,38(13):66-70.
[21] 张予心,蔡丹,宋秋梅,等.乳清蛋白与海藻酸钠复合物凝胶特性的影响因素[J].中国食品学报,2017,17(5):40-48.
[22] BARTH A, ZSCHERP C. What vibrations tell about proteins[J]. Quarterly Reviews of Biophysics, 2002, 35(4): 369-430.