我国是黄瓜的生产大国,约占世界黄瓜栽培面积的60%,规模和产量都位居世界第一。鲜切黄瓜食用方便,营养价值高,受到广大消费者的喜爱。但鲜切黄瓜货架期短,在低温储藏期间极易受微生物污染而引起腐败变质,这极大地限制了鲜切黄瓜的销售范围和销售量。赵磊等[1]和MENG等[2]研究发现,鲜切黄瓜在4 ℃下最多可以贮藏6 d,6 d后微生物总数超标。目前,关于鲜切黄瓜的研究在国内外已有较多报道,包括两大方面:病原菌的检测及防控和营养品质的保持。SUN等[3]研究了常压低温等离子体对鲜切黄瓜中大肠杆菌的杀菌机理,SHARMA等[4]研究了噬菌体混合物对鲜切黄瓜中纽波特沙门菌存活率的影响,JOSHI等[5]和朱莉等[6]分别研究了电子束辐照和不同包装材料对鲜切黄瓜品质的影响。但关于腐败微生物对鲜切黄瓜品质的研究较少。
气调保鲜包括气调包装(modified atmosphere packaging, MAP)和气调贮藏(controlled atmosphere storage, CAS)。MAP是一种天然且非添加性的食品保鲜技术,广泛用于鲜切产品贮藏保鲜,保持产品外观,质地,颜色,延长货架期并抑制微生物的生长[7-8]。但是,由于采后果蔬仍存在呼吸和代谢活动,MAP中的气体成分随着贮藏期的延长而逐渐变化,O2浓度降低和CO2浓度增加,高浓度的CO2会导致醇、醛的积累,电解质渗漏增加,从而对果蔬造成损害[9-10]。气调贮藏能保持稳定的低O2、高CO2和温度、湿度的环境,抑制果蔬代谢活动,保持果蔬的营养和感官品质,延缓果蔬腐烂。WAGHMARE等[11]研究表明,5%O2、10%CO2气调包装抑制了香菜中微生物的生长,维持了硬度和色泽,保持了感官品质。SERRADILLA等[12]发现5% O2、10% CO2气调包装抑制了甜樱桃中嗜冷菌、假单胞菌、酵母菌和霉菌等微生物的生长,延缓了由微生物引起的腐败。HENRIQUE等[13]发现5% O2、20% CO2气调箱贮藏可以保持芒果品质超过30 d而不产生负面影响。但关于气调箱贮藏对腐败菌引起的品质变化的研究较少。
变形假单胞菌(Pseudomonas plecoglossicida)在引起鲜切黄瓜腐败变质的微生物中占主导地位。关于变形假单胞菌对鲜切黄瓜品质影响少有报道。本实验采用3%O2、7%CO2气调贮藏(先前实验研究了不同气调条件对鲜切黄瓜品质的影响确定了最佳气调贮藏条件,该气调条件下鲜切黄瓜可贮藏至12 d),研究其对变形假单胞菌增殖以及由变形假单胞菌导致的鲜切黄瓜细胞壁组成和结构变化的影响。研究可为鲜切果蔬企业的产品保鲜技术提供参考,为气调贮藏在鲜切果蔬中的应用推广提供理论支持。
变形假单胞菌(Pseudomonas plecoglossicida),本实验室保存。菌株分离自冷藏条件下腐烂的鲜切黄瓜。
黄瓜,购于北京当地市场。挑选具有相同的成熟度并去除畸形、腐烂、机械损伤的黄瓜。
三氯乙酸、硫代巴比妥酸等试剂,均为分析纯;假单胞菌CFC(cephalothin-sodium fusidate cetrimide, CFC)选择性培养基,青岛海博生物技术有限公司;β-半乳糖苷酶(β-galactosidase, β-GAL)活性检测试剂盒、纤维素酶(cellulase, CL)活性检测试剂盒、原果胶含量检测试剂盒、可溶性果胶含量检测试剂盒,均购于北京索莱宝生物科技有限公司。
A11基本型分析研磨机、T10基本型分散机,艾卡(广州)仪器设备有限公司,IKA中国;GXH-3051便携式CO2红外线分析器,上海精密仪器仪表有限公司;UV-1800紫外分光光度仪,日本岛津公司;CM-3700D台式分光测色仪,日本柯尼卡-美能达公司;TA-XT Plus质构仪,英国SMS公司;YS-XCAB/D602气调保鲜试验箱,杭州屺石科技有限公司;HITACHI SU-8010高分辨场发射扫描电镜,日本日立高新技术公司。
1.3.1 Pseudomonas plecoglossicida菌悬液制备
取冻存菌液100 μL,加至100 mL LB(luria-bertani)液体培养基中,220 r/min、28℃下培养24 h复活菌株,再取复活后的菌液100 μL加至100 mL LB液体培养基中,220 r/min、28℃下培养8 h,并调整浓度至10-8 CFU/mL。
1.3.2 样品及接种菌处理
黄瓜用流动水清洗干净后,参考GB28233—2011次氯酸钠发生器安全与卫生标准,用含200 mg/L有效氯的次氯酸钠溶液消毒2 min,减少黄瓜自身的微生物量,消毒后再用去离子水将残余的消毒剂冲净,晾干,在无菌台上切成0.9 cm厚的薄片,放在保鲜盒中待接菌。
吸取100 μL、10-8 CFU/mL菌悬液均匀接种至鲜切黄瓜片的一面。整个接种过程在无菌操作台上进行。接种后的黄瓜片晾干15 min后贮藏。本实验目的是研究气调贮藏对变形假单胞菌及其导致的鲜切黄瓜细胞壁降解以及细胞壁降解引起的生理生化指标变化,因此处理组都接种了变形假单胞菌,处理分两组,接菌空气对照组(control, CK);接菌气调贮藏组(control atmosphere storage, CAS), 3% O2, 7%CO2, 90%N2。在4℃,90%相对湿度下贮藏12 d,每2 d检测相关指标。
1.4.1 变形假单胞菌计数
取20 g样品于30 mL 0.9%(质量分数)无菌盐水溶液中,使用手持式打浆机打匀,然后9倍梯度稀释到合适浓度,取最后2个稀释梯度中100 μL液体进行平板涂布。用CFC选择性琼脂对变形假单胞菌计数。变形假单胞菌菌落总数以相对于接种时(0 d)的增加量表示。
1.4.2 扫描电镜
在鲜切黄瓜接种面取样,取出长、宽、厚度为0.5 cm × 0.2 cm × 0.1 cm的果肉,按1∶20完全浸入2.5%(质量分数)戊二醛中固定24 h,送至中国农业科学院农产品加工所进行样品后续处理和扫描电镜观察。
1.4.3 细胞壁降解酶和细胞壁成分测定
β-半乳糖苷酶活性、纤维素酶活性、原果胶含量和可溶性果胶含量,均采用试剂盒检测。
1.4.4 色度
鲜切黄瓜片色度使用台式色差仪测量,结果表示为L*(亮度)、a*(红、绿色)、b*(黄、蓝色)和ΔE值。
1.4.5 理化指标测定
鲜切黄瓜片硬度采用装有5 mm探头的质构仪测定。硬度表示为探头以10 mm/s的速度刺穿至5 mm深度所需的最大力。
相对电导率的测定参考NASEF[14]的方法,使用无菌不锈钢穿孔器(直径1.0 cm)从黄瓜片上切下1 g样品,置于装有50 mL去离子水的100 mL锥形烧瓶中,封口后在30℃下振荡2 h,然后用电导率仪测量电导率值(R1);将样品加热煮沸10 min,冷却至室温后测量电导率值(R2)。相对电导率按公式(11)计算:
(1)
丙二醛(malondialdehyde, MDA)测定采用钱磊等[15]方法,略作改动。称取3 g样品,加3 mL磷酸盐缓冲液冰浴研磨,研磨后转入10 mL离心管中,并用1 mL磷酸盐缓冲液冲洗研钵,一并转入离心管中,用分散机充分匀浆,再加入2 mL磷酸盐缓冲液,4℃,13 000×g离心20 min。取1.5 mL上清液加入2.5 mL 0.5%(质量分数)硫代巴比妥酸溶液,沸水浴15 min,取出冷却至室温后,4℃,8 000×g离心10 min,取上清液,在450、532和600 nm波长下测定吸光值MDA计算如公式(2)所示:
(2)
式中:A450、A532和A600分别是450、532和600 nm处上清液的吸光度;V反是反应液体积;M是所测样品质量;V提是提取液体积;MDA含量,nmol/g。
实验设计为完全随机设计。采用SPSS 19.0统计软件进行数据分析,组间均值比较使用单因素方差分析(one-way ANOVA),数据表示为平均值±标准差,实验重复3次,P<0.05表示差异具有显著性。
如图1所示,气调贮藏抑制了鲜切黄瓜中变形假单胞菌的生长。在2和4 d时,CAS处理组中变形假单胞菌出现了负增长,说明气调贮藏对腐败菌有抑制作用;而对照组中变形假单胞菌的增长显著高于CAS处理组。随着贮藏时间的延长,两个处理组中的变形假单胞菌都出现了不同程度的增加,对照组在第6天比第2天增加了1.46 lg CFU/g,而CAS处理组仅增加了0.48 lg CFU/g。在贮藏至第12天时,对照组和CAS处理组分别增加了2.77 lgCFU/g和2.29 lgCFU/g。在贮藏期间由于变形假单胞菌的生长,导致对照组鲜切黄瓜在贮藏至第6天时,表面明显出现了变形假单胞菌菌落,但主要分布在鲜切黄瓜片的中心位置,在贮藏结束时(第12天),鲜切黄瓜表面长满了变形假单胞菌,并且产生了异味;而CAS处理组在整个贮藏期间都没有出现明显的菌落生长,有效地保持了鲜切黄瓜的外观,仅在第12天时表面变暗。总体来说,在整个贮藏期间CAS处理对鲜切黄瓜中的变形假单胞菌的生长都有抑制作用。

图1 CAS对变形假单胞菌生长的影响
Fig.1 Effect of CAS on the growth of Pseudomonas
plecoglossicida
如图2-a所示,在第0天接种变形假单胞菌时,变形假单胞菌并没有立即进入到鲜切黄瓜的组织细胞中,并且此时的细胞结构完整。在气调贮藏至12 d时(图2-b),在鲜切黄瓜细胞内部发现了少量变形假单胞菌,细胞的结构仍较为完整,没有明显的损伤。但对照组贮藏至12 d时(图2-c),鲜切黄瓜组织细胞内长满变形假单胞菌,细胞壁损害严重,无法分清相邻的细胞,组织完全塌陷。

a-0 d接种;b-12 d气调组;c-12 d CK组
图2 CAS对接种变形假单胞菌的鲜切黄瓜细胞微观
结构的影响
Fig.2 Effect of CAS on the microstructure of fresh-cut cucumber
cells inoculated with Pseudomonas plecoglossicida
如图3-a所示,β-半乳糖苷酶活性在贮藏期间不断增加。与对照组相比,CAS处理显著地抑制了鲜切黄瓜中β-半乳糖苷酶活性的增加。第6天和等12天时,CAS处理组中的β-半乳糖苷酶活性仅为对照组的72.69%和65.57%。
纤维素酶活性在贮藏期前4 d快速降低,随后稍有增加,但均低于第0天(图3-b)。在贮藏期内,对照组的纤维素酶活性显著高于CAS处理组,10 d和12 d时,对照组纤维素酶活是CAS处理组的1.95和3.18倍。
如图3-c所示,随着贮藏天数的增加,2个处理组中的原果胶含量都不断下降,CAS处理延缓了原果胶含量的下降。贮藏结束时,与0 d相比,对照组和CAS处理组中原果胶含量分别下降了78.5%和67.87%。
鲜切黄瓜中可溶性果胶含量与原果胶含量的变化趋势相反,在贮藏期内不断上升(图3-d)。对照组在贮藏期间可溶性果胶含量始终高于CAS处理组。对照组在0~6 d增加较为缓慢,6 d后,对照组中可溶性果胶含量迅速增加,到贮藏结束时比0 d增加了0.74 μmol/g FW;CAS处理组可溶性果胶含量在前10 d都缓慢增加,在第12天时增加稍快,贮藏结束时与0 d相比,仅增加了0.36 μmol/g FW。
如图4-a所示,贮藏期间鲜切黄瓜的亮度不断下降。对照组在贮藏后期快速下降,在贮藏前期的变化较为平稳,与0 d相比,12 d时对照组亮度降低了10.3%。而CAS处理组在12 d内的下降趋势都较为缓慢,在贮藏结束时,CAS处理组仅比0 d时的亮度值下降了3.1%。
由图4-b可知,贮藏期内2个处理条件下的a*值呈增加趋势。CAS处理组a*值缓慢增加,保持了鲜切黄瓜的绿度。对照组中的a*值在0~4 d和6~10 d增加缓慢,在4~6 d和10~12 d增加较快。在贮藏结束时与0 d相比,CAS处理组和对照组a*值分别下降了36.08%、117.19%。
由图4-c可知对照组b*值呈波动式增加。从4~6 d增加最快,增加了11.56%。CAS处理组在10~12 d增加较快,增加了5.49%。贮藏期内,CAS处理组b值均低于对照组。
如图4-d所示,鲜切黄瓜的总色差值随贮藏时间的增加而上升。贮藏期间对照组中总色差迅速增加,第12天时的总色差值比第0天增加了13.25;CAS处理组总色差值的增加较为缓慢,第12天时的总色差值比第0天增加了4.48。
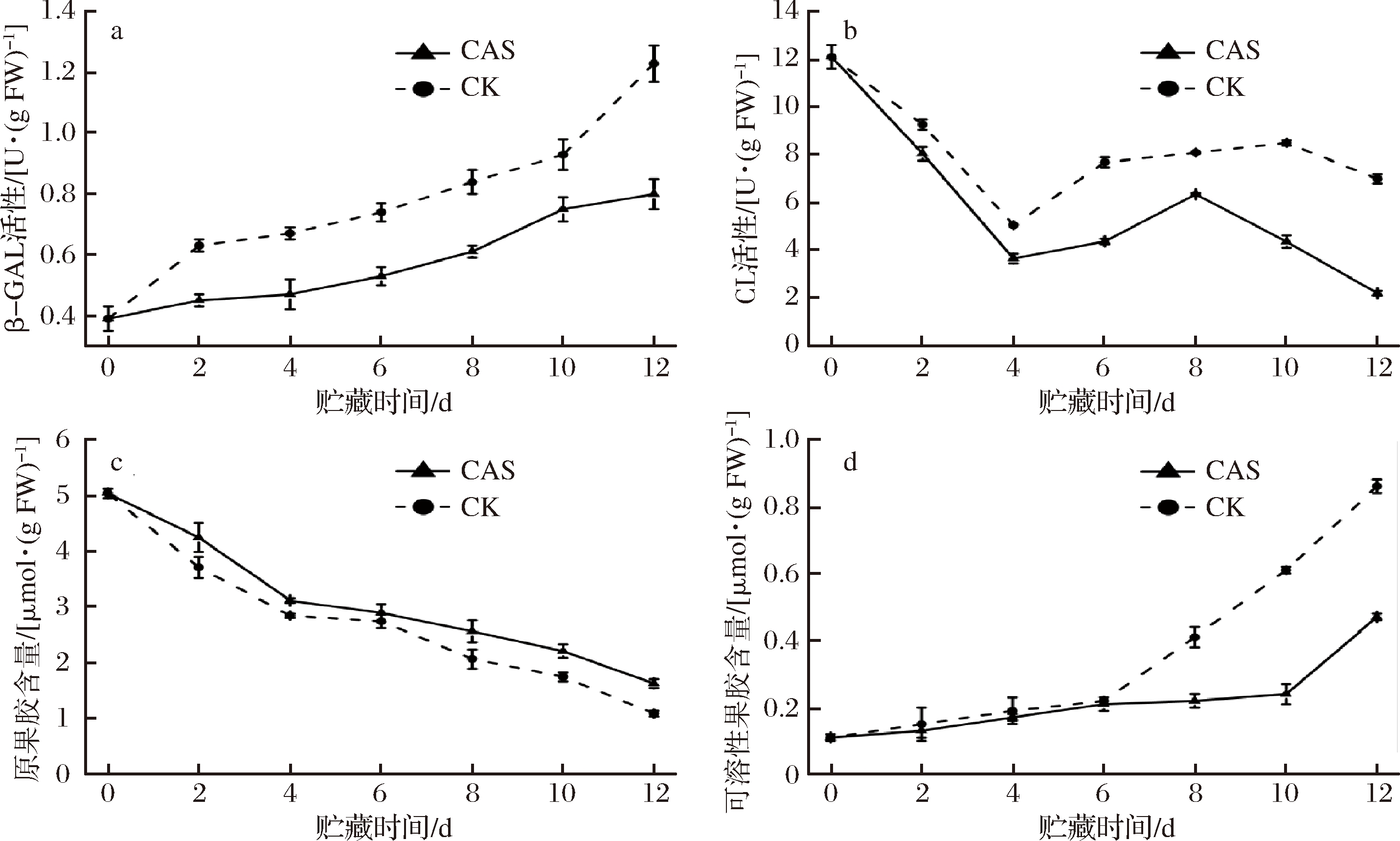
a-β-GAL;b-CL活性;c-原果胶含量;d-可溶性果胶含量
图3 CAS对接种变形假单胞菌的鲜切黄瓜细胞壁降解酶和细胞壁成分的影响
Fig.3 Effect of CAS on cell wall degrading enzyme and cell wall components of fresh-cut cucumber inoculated with
Pseudomonas plecoglossicida
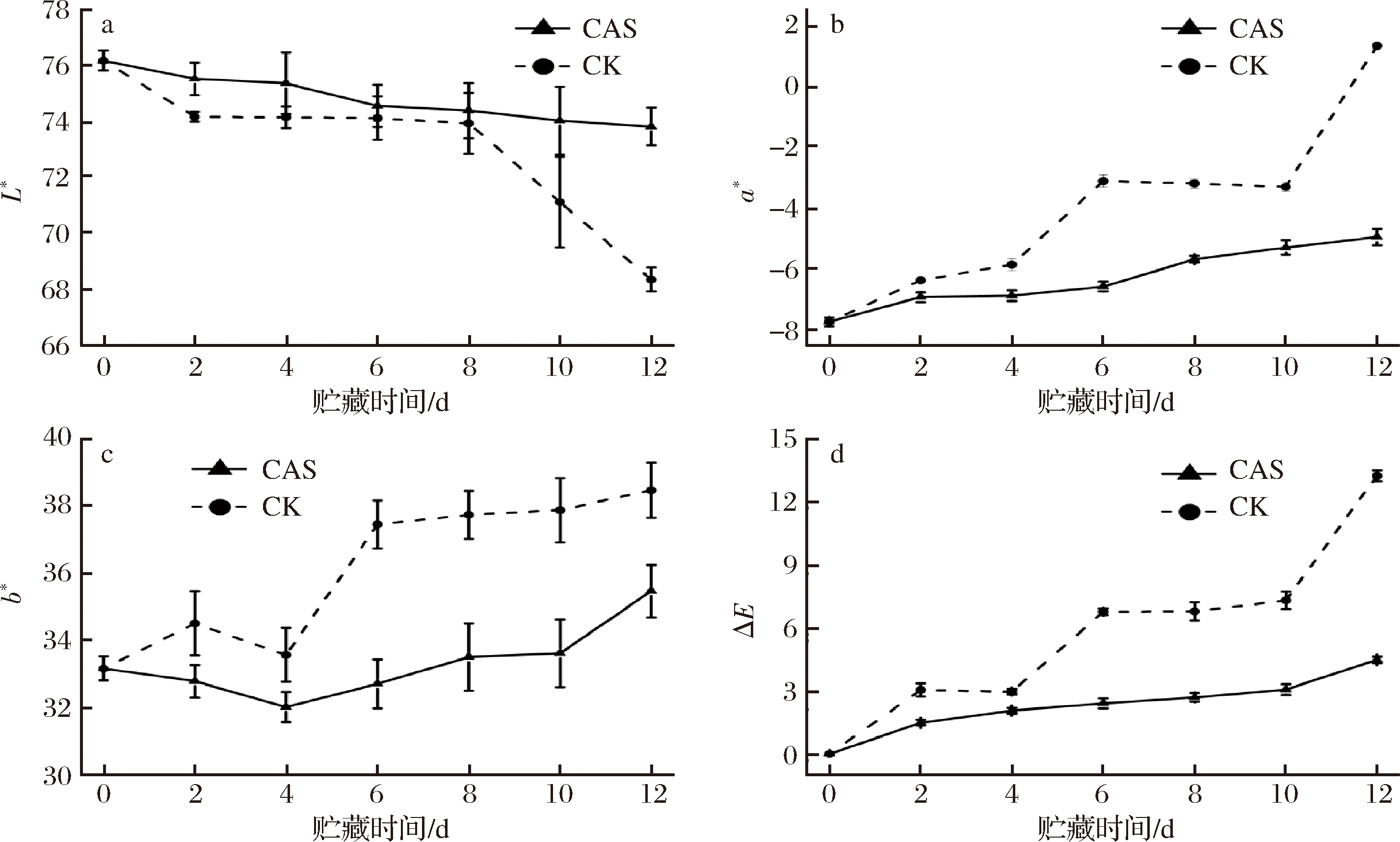
a-L*;b-a*;c-b*;d-ΔE
图4 CAS对接种变形假单胞菌的鲜切黄瓜色泽的影响
Fig.4 Effect of CAS on the color of fresh-cut cucumber inoculated with Pseudomonas plecoglossicida
由图5-a可知鲜切黄瓜的硬度不断降低。在整个贮藏期内,CAS处理组硬度均高于对照组。贮藏后期对照组硬度下降较快。贮藏结束时,CAS处理组硬度是对照组的1.06倍。
贮藏期间,鲜切黄瓜的相对电导率和MDA含量的变化趋势相似,均不断增加(图5-b和图5-c)。与对照组相比,CAS处理显著抑制了相对电导率的增加。对照组相对电导率在前6 d增加相对较慢,6 d后迅速增加;CAS处理组中相对电导率在前8 d缓慢增加,在8~12 d增加较快。贮藏结束时,对照组相对电导率是CAS处理组的1.08倍。在整个贮藏期间,对照组MDA含量迅速增加,而CAS处理组中MDA含量缓慢增加;在贮藏结束时,对照组MDA含量从0 d的0.12 nmol/g增加到了0.26 nmol/g,增加了116.67%,CAS处理组MDA含量从0 d的0.12 nmol/g增加到了0.19 nmol/g,仅增加了58.33%。
鲜切黄瓜由于机械损伤导致自身的防卫能力下降,易受微生物侵染而引起腐败变质。研究鲜切黄瓜冷藏期间腐败菌的气调防控具有重要意义。CAS处理显著抑制了变形假单胞菌的生长速率以及变形杆
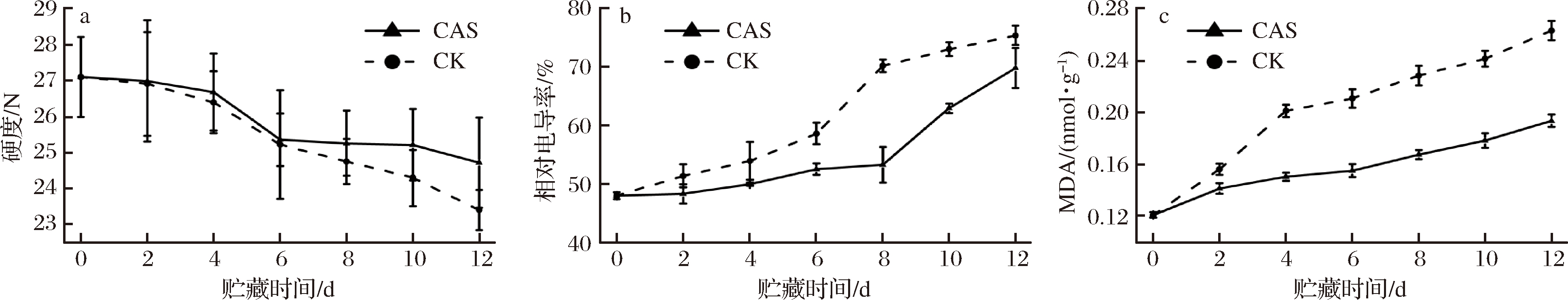
a-硬度;b-相对电导率;c-MDA
图5 CAS对接种变形假单胞菌的鲜切黄瓜硬度、相对电导率和MDA的影响
Fig.5 Effect of CAS on firmness, relative conductivity and MDA of fresh-cut cucumber inoculated with Pseudomonas plecoglossicida
菌导致的黄瓜细胞结构的降解。扫描电镜结果显示,12 d时,对照组的组织细胞中长满变形假单胞菌,组织结构受损严重,完全塌陷,而CAS处理组细胞壁较为完整,只是略有松散。ANASTASIA等[16]发现5% O2和15%CO2的气调包装可以有效地抑制鲜切沙拉中乳酸菌和假单胞菌的生长。PAN等[17]研究发现4%O2和5%CO2的气调包装下鲜切菠萝中好氧菌比对照组低2 lg CFU/g。刘程慧[18]用扫描电镜观察腐败霉菌侵染鲜切苹果的过程发现侵入后苹果组织细胞结构完全瓦解、腐烂。由此可见,气调处理可抑制微生物生长及微生物导致的组织结构的破坏。
色泽和外观直接影响鲜切果蔬产品的接受度和商品价值[19]。贮藏至6 d时,对照组表面由于变形假单胞菌的生长色泽明显发生变化,12 d时表面变黄且失去光泽。气调贮藏延缓了鲜切黄瓜中L*值的下降、以及a*、b*和ΔE值的增加,维持了鲜切黄瓜的色泽和外观。SHEN等[20]在鲜切土豆中的研究发现,4%O2和10%CO2的气调包装抑制了微生物生长,从而维持了色泽。WAGHMARE等[21]研究表明,4%O2和10%CO2的气调包装对鲜切瓜儿豆的色泽影响最小。MASHABELA等[22]研究表明,0.38%O2和28.53%CO2的气调包装可以减少贮藏期间鲜切花椰菜的颜色变化,保持较低的ΔE值,具有较高的商品接受度。
细胞壁的完整性与果蔬品质密切相关。微生物会产生胞外纤维素酶、β-半乳糖苷酶等细胞壁降解酶,降解纤维素、含半乳糖苷的胞壁多糖,还会促使原果胶转变为可溶性果胶,从而使组织软化、塌陷,进一步促进微生物侵入细胞内并利用细胞内营养物质快速增殖,最终导致果蔬腐烂[23-25]。CAS处理抑制了纤维素酶和β-半乳糖苷酶活性的增加,延缓了原果胶的降解和可溶性果胶含量的增加,这可能是因为气调贮藏抑制了微生物的生长,减少了细胞壁降解酶的产生,保持了细胞壁的完整性。由于气调贮藏保持了细胞壁成分,从而延缓了硬度的下降,抑制了相对电导率和MDA含量的增加速率。FAN等[26]发现气调包装抑制了鲜切黄瓜中微生物的生长并保持了细胞壁的完整。LI等[27]研究发现气调贮藏抑制了梨中细胞壁降解酶酶活,维持了硬度。
综上,CAS处理显著抑制了变形假单胞菌的生长,维持了细胞壁完整性,降低了纤维素酶活性、抑制了β-半乳糖苷酶活性的增加和可溶性果胶的产生,并延缓了原果胶的降解,从而保持了鲜切黄瓜的硬度,抑制了MDA的产生和相对电导率的增加,同时维持了鲜切黄瓜的外观和色泽。可见,CAS处理通过抑制腐败微生物的生长以及微生物导致的细胞壁降解从而保持鲜切黄瓜的品质。实验结果可以为鲜切黄瓜的贮藏保鲜提供参考。
[1] 赵磊,王丹,马越,等.短波紫外线照射对鲜切黄瓜片品质的影响[J].食品工业, 2019, 40(5): 205-209.
[2] MENG X, ZHANG M, ZHAN Z, et al. Changes in quality characteristics of fresh-cut cucumbers as affected by pressurized argon treatment[J]. Food&Bioprocess Technology, 2014, 7(3): 693-701.
[3] SUN Y, ZHANG Z W, WANG S Q. Study on the bactericidal mechanism of atmospheric-pressure low-temperature plasma against Escherichia coli and its application in fresh-cut cucumbers[J]. Molecules, 2018, 23(4): 975.
[4] SHARMA M, DASHIELL G, HANDY E T, et al. Survival of Salmonella newport on whole and fresh-cut cucumbers treated with lytic bacteriophages[J]. Journal of Food Protection, 2017, 80(4): 668-673.
[5] JOSHI B, MOREIRA R G, OMAC B, et al. A process to decontaminate sliced fresh cucumber(Cucumis sativus) using electron beam irradiation[J]. LWT-Food Science and Technology, 2018, 91: 95-101.
[6] 朱莉,王丹,马越,等.不同包装材料对鲜切黄瓜品质的影响[J].食品工业, 2017, 38(6): 32-36.
[7] WILSON M D, STANLEY R A, EYLES A, et al. Innovative processes and technologies for modified atmosphere packaging of fresh and fresh-cut fruits and vegetables: A review[J]. Critical Reviews in Food Science and Nutrition, 2017, 59(3): 411-422.
[8] OLIVEIRA M, ABADIAS M, USALL J, et al. Application of modified atmosphere packaging as a safety approach to fresh-cut fruits and vegetables-a review[J]. Trends in Food Science & Technology, 2015, 46(1): 13-26.
[9] BOVI G G, CALEB O J, ILTE K, et al. Impact of modified atmosphere and humidity packaging on the quality, off-odour development and volatiles of ′Elsanta′ strawberries[J]. Food Packaging and Shelf Life, 2018, 16: 204-210.
[10] LI Y, ISHIKAWA Y, SATAKE T, et al. Effect of active modified atmosphere packaging with different initial gas compositions on nutritional compounds of shiitake mushrooms(Lentinus edodes)[J]. Postharvest Biology and Technology, 2014, 92: 107-113.
[11] WAGHMARE R B, ANNAPURE U S. Integrated effect of sodium hypochlorite and modified atmosphere packaging on quality and shelf life of fresh-cut cilantro[J]. Food Packaging and Shelf Life, 2015, 3: 62-69.
[12] SERRADILLA, MANUEL JOAQU N, VILLALOBOS, et al. Study of microbiological quality of controlled atmosphere packaged ′Ambrunés′ sweet cherries and subsequent shelf-life[J]. International Journal of Food Microbiology, 2013, 166(1): 85-92.
N, VILLALOBOS, et al. Study of microbiological quality of controlled atmosphere packaged ′Ambrunés′ sweet cherries and subsequent shelf-life[J]. International Journal of Food Microbiology, 2013, 166(1): 85-92.
[13] HENRIQUE D A T G, SANTOS L O, CUNHA ![]() et al. Effect of carbon dioxide(CO2) and oxygen(O2) levels on quality of ‘Palmer’ mangoes under controlled atmosphere storage[J]. Journal of Food Science and Technology, 2017, 55(1): 145-156.
et al. Effect of carbon dioxide(CO2) and oxygen(O2) levels on quality of ‘Palmer’ mangoes under controlled atmosphere storage[J]. Journal of Food Science and Technology, 2017, 55(1): 145-156.
[14] NASEF I N. Short hot water as safe treatment induces chilling tolerance and antioxidant enzymes, prevents decay and maintains quality of cold-stored cucumbers[J]. Postharvest Biology and Technology, 2018, 138: 1-10.
[15] 钱磊,张业尼,李涛,等.羧甲基壳聚糖与滑菇肽对杏鲍菇保鲜效果研究[J].食品与发酵工业, 2019, 45(18): 168-175.
[16] KAPETANAKOU A E, TAOVKIS P,SKANDAMIS P N. Model development for microbial spoilage of packaged fresh-cut salad products using temperature and in-package CO2 levels as predictor variables[J]. LWT-Food Science and Technology, 2019, 113: 108 285.
[17] PAN Y G, ZHU J, LI S Y. Effects of pure oxygen and reduced oxygen modified atmosphere packaging on the quality and microbial characteristics of fresh-cut pineapple[J]. Fruits, 2015, 70(2): 101-108.
[18] 刘程惠.鲜切苹果腐败霉菌侵染生物学机理及其臭氧防控研究[D].沈阳:沈阳农业大学, 2016.
[19] 范新光,梁畅畅,郭风军,等.近冰温冷藏过程中果蔬采后生理品质变化的研究现状[J].食品与发酵工业, 2019, 45(18): 270-276.
[20] SHEN X, ZHANG M, DEVAHASTIN S, et al. Effects of pressurized argon and nitrogen treatments in combination with modified atmosphere on quality characteristics of fresh-cut potatoes[J]. Postharvest Biology and Technology, 2019, 149: 159-165.
[21] WAGHMARE R B, ANNAPURE U S. Effects of hydrogen peroxide, modified atmosphere and their combination on quality of minimally processed cluster beans[J]. Journal of Food Science & Technology, 2017, 54(11): 3 658-3 665.
[22] MASHABELA M, MAHAJAN P V, SIVAKUMAR D. Influence of different types of modified atmosphere packaging films and storage time on quality and bioactive compounds in fresh-cut cauliflower[J]. Food Packaging and Shelf Life, 2019, 22: 100 374.
[23] LEE D H, KIM J B, KIM M, et al. Microbiota on spoiled vegetables and their characterization[J]. Journal of Food Protection, 2013, 76(8): 1 350-1 358.
[24] DUKARE A S, PAUL S, NAMBI V E, et al. Exploitation of microbial antagonists for the control of postharvest diseases of fruits: A review[J]. Critical Reviews in Food Science and Nutrition, 2018, 59(2): 1-16.
[25] 宋丹丹,孔庆军,李鸿彬,等.蟠桃褐腐病原菌生物学特性及细胞壁降解酶活性[J].食品科学, 2017, 38(10): 42-48.
[26] FAN K, ZHANG M, JIANG F. Ultrasound treatment to modified atmospheric packaged fresh-cut cucumber: Influence on microbial inhibition and storage quality[J]. Ultrasonics Sonochemistry, 2019, 54: 162-170.
[27] LI M, ZHI H, DONG Y. Textural property and cell wall metabolism of ′Golden Bosc′ and ′d′Anjou’ pears as influenced by oxygen regimes after long-term controlled atmosphere storage[J]. Postharvest Biology and Technology, 2019, 151: 26-35.