食物蛋白源降尿酸活性肽的研究进展
胡晓1*,周雅1,2,杨贤庆1,吴燕燕1,陈胜军1,李来好1,马海霞1
1(中国水产科学研究院南海水产研究所,农业农村部水产品加工重点实验室,广东 广州,510300)2(上海海洋大学 食品学院,上海,201306)
摘 要 高尿酸血症是一种由嘌呤代谢紊乱引起的慢性疾病,已严重威胁到人类的健康。长期的高尿酸血症会导致痛风的发生。目前临床用于治疗高尿酸血症的药物如别嘌呤醇、秋水仙碱等存在毒副作用大等问题,因此开发高效、安全的天然降尿酸活性物质成为国内外学者研究的热点。食物蛋白源降尿酸活性肽是指利用食源性动、植物蛋白制得的具有降低生物体内血尿酸水平功效的生物活性肽。该文对目前国内外食物蛋白来源的降尿酸活性肽的制备、分离纯化、功能活性评价、结构鉴定予以综述,并对此研究领域的发展趋势予以展望,旨在为降尿酸功能性食品的研究及开发提供参考。
关键词 降尿酸活性肽;制备;分离纯化;活性评价;结构鉴定
第一作者:博士,副研究员(本文通讯作者,E-mail:hnhuxiao@163.com)
基金项目:现代农业产业技术体系建设专项(CARS-47);广东省自然科学基金项目(2019A1515011588,2017A030313164);广东省科技创新战略专项资金(纵向协同管理方向)计划项目(2018S0044);国家重点研发计划(2018YFD0901102);“扬帆计划”引进创新创业团队专项(2015YT02H109)
收稿日期:2019-09-05,改回日期:2019-10-31
DOI:10.13995/j.cnki.11-1802/ts.022183
引用格式:胡晓,周雅,杨贤庆,等.食物蛋白源降尿酸活性肽的研究进展[J].食品与发酵工业,2020,46(4):287-293.HU Xiao,ZHOU Ya,YANG Xianqing, et al. Research progress on anti-hyperuricemic peptides obtained from food proteins[J].Food and Fermentation Industries,2020,46(4):287-293.
Research progress on anti-hyperuricemic peptides obtained from food proteins
HU Xiao1*, ZHOU Ya1,2, YANG Xianqing1, WU Yanyan1,CHEN Shengjun1, LI Laihao1, MA Haixia1
1(Key Laboratory of Aquatic Product Processing, Ministry of Agriculture and Rural Affairs, South China Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Guangzhou 510300, China)2 (College of Food Science and Technology, Shanghai Ocean University, Shanghai 201306, China)
ABSTRACT Hyperuricemia is a chronic disease caused by disorders of purine metabolism, which can seriously threaten human health. Prolonged hyperuricemia may lead to gout. Drugs such as allopurinol and colchicine, which are currently used in the treatment of hyperuricemia, have strong side effects. Therefore, researchers in China and other countries are focused on seeking effective and safe natural anti-hyperuricemic bioactive compounds. Food-derived anti-hyperuricemic peptides refer to bioactive peptides prepared from animal or plant proteins and have the effect of lowering uric acid in vivo. This paper contains a review of the preparation, purification, functional activity evaluation, and structure identification of food-derived anti-hyperuricemic peptides. The development trend of the research field has been prospected, with an aim to provide a reference for the research and development of uric anti-hyperuricemic functional foods.
Key words anti-hyperuricemic peptides; preparation; purification; activity evaluation; structure identification
近年来,随着人们的生活水平的提高和饮食习惯的变化,高尿酸血症的患病率在全球范围内呈现逐年增高的趋势。高尿酸血症是人体内尿酸分泌增多或尿酸排泄障碍引起的血液中的尿酸浓度超出正常范围的疾病。长期高尿酸血症容易导致钠尿酸盐在关节及周围软组织处沉积,导致痛风[1],并可引发高血压[2-3]、代谢类疾病[4]、心血管疾病[5]等多种并发症。尿酸(C5H4N4O3)是生物体内细胞代谢和食物中的嘌呤的代谢最终产物。在正常嘌呤饮食状态下,非同日2次空腹血尿酸水平男性>416 μmol/L,女性>357 μmol/L即被诊断为高尿酸血症[6]。目前为止尚未发现可根治痛风的药物,临床上一般使用别嘌呤醇、非布索坦、苯溴马隆、拉布立酶等药物来治疗高尿酸血症或痛风[7]。虽然这些药物疗效较好,但存在一定的副作用,如引起腹痛、恶心、呕吐、发热、皮疹、肾脏疾病等不良反应[8-9]。
生物活性肽是一种安全性高、加工性能良好且易被人体吸收的功能性化合物,其已被证明具有抗衰老、抗病毒、抗肿瘤、抗氧化、降血压、降血糖等多种活性,已被广泛应用于化妆品、医药和功能性食品等多个领域[10-11]。食物蛋白源降尿酸活性肽是指以食源性动、植物蛋白为原料制得的具有降低生物体内血尿酸水平功效的生物活性肽。目前国内外关于食物蛋白源降尿酸活性肽的研究较少,仍处于起步阶段。本文对目前国内外食物蛋白源降尿酸活性肽的制备、分离纯化、功能活性评价及结构鉴定进行综述,并介绍其发展前景,以期为降尿酸功能性食品的研究及开发应用提供参考。
1 降尿酸活性肽作用机理
黄嘌呤氧化酶(XOD,EC 1.17.3.2)是一种其催化中心包含2个铁硫中心(2Fe-2S)、1个钼蝶呤辅因子(Mo-pt)和1个黄素腺嘌呤二核苷酸(FAD)的氧化还原酶类[12]。XOD可以将次黄嘌呤氧化为黄嘌呤,再将黄嘌呤氧化为尿酸[13]。其中钼辅因子Mo-pt是维持XOD酶活的关键部位。Mo-pt结构中的Mo-OH对底物碳原子进行亲核攻击,使Mo6+还原为Mo4+,形成中间体。当体系释放出产物黄嘌呤或尿酸后,Mo4+再次氧化成Mo6+[14]。
XOD活性位点附近氨基酸残基能形成疏水空腔,食物蛋白源降尿酸活性肽中的某些氨基酸能结合到这些疏水空腔中,与XOD中的氨基酸残基间以疏水相互作用、氢键、静电相互作用、范德华力等作用力发生竞争性/非竞争性结合,从而改变其空间结构,进而抑制XOD活性,达到减少尿酸生成的效果。此外,食物蛋白源降尿酸活性肽能够降低XOD的mRNA表达量,从而使细胞内XOD的含量减少。黎青勇[15]研究发现,多肽Pro-Pro-Lys-Asn-Trp对XOD的作用是非竞争性抑制,而Trp及多肽Trp-Asp-Gln-Trp对XOD的作用是一种混合型抑制作用。NONGONIERMA等[16-17]研究发现,Trp及含Trp的二肽(Arg-Trp,Trp-Val,Val-Trp,Lys-Trp和Ile-Trp)具有XOD抑制活性,且属于非竞争性抑制,这是由于它们与XOD抑制类药物(如别嘌呤醇)具有相似的结构。刘洋[18]研究发现海洋鱼降尿酸活性肽能够减少高尿酸血症小鼠体内XOD的mRNA表达量,从而减少细胞内XOD的含量,起到减少尿酸生成的作用。
2 降尿酸活性肽的制备
生物活性肽可通过酶解法、微生物发酵法、化学水解法、化学合成法、基因工程等方法制备[19]。目前用于制备食物蛋白源降尿酸活性肽的方法主要有酶解法和微生物发酵法,此外还有不以食物蛋白为原料,直接化学合成目标肽的固相合成法。
2.1 酶解法
酶解法就是利用蛋白酶对底物蛋白质肽链的剪切作用,使得具有降尿酸活性的肽段得以释放的方法[20]。酶解法制备降尿酸活性肽具有生产成本低廉、产品安全性高、制备条件温和、酶解过程易于控制等特点[21],故酶解法是制备降尿酸活性肽最为常用的方法。酶解法中酶的筛选非常重要,常见的蛋白酶有:中性蛋白酶、碱性蛋白酶、酸性蛋白酶、复合蛋白酶、木瓜蛋白酶、胰蛋白酶等。蛋白酶催化水解蛋白质时,肽链的长度、氨基酸的种类和数量都会受到诸多作用条件(加酶量、酶解温度、酶解pH、酶解时间等)的影响,从而影响酶解效果和肽的生物活性[22]。实际操作中需优化获得最佳酶解工艺条件,从而提高降尿酸活性肽的制备效率。表1列出了利用动植物原料制备降尿酸活性肽的主要方法和结果。LI等[23]以脱脂核桃粉、脱酚脱脂核桃粉为原料,用Alcalase2.4L蛋白酶酶解得到具有降尿酸的生物活性肽Ala-Asp-Ile-(Tyr)2-Glu、Trp-(Pro)2-Lys-Asn。邹琳[27]以鲣鱼为原料,采用酶解法制备降尿酸活性肽,研究发现中性蛋白酶的水解度、氮回收率和黄嘌呤氧化酶(XOD)抑制活性均为最高。MUROTA等[29]用碱性蛋白酶,从鲨鱼软骨水提取物中分离鉴定出具有降尿酸活性的肽Tyr-Leu-Asp-Asn-Tyr和Ser-(Pro)2-Tyr-Trp-Pro-Tyr。刘洋等[18]以海洋鱼为原料制备降尿酸活性肽,验证了中性蛋白酶为最佳酶解用酶。赵谋明等[31]通过单因素试验确定中性蛋白酶和胰酶复合为水解秋刀鱼制备降尿酸活性肽的最佳蛋白酶。在实际应用中,由于酶制剂价格较为昂贵,会增加工业化生产时的成本,因此未来可将固定化酶技术应用于降尿酸活性肽的制备中,不仅能实现连续生产,而且固定化酶具有良好的化学稳定性和热稳定性,可重复使用。
2.2 微生物发酵法
微生物发酵法是通过选育优良的发酵菌种,利用菌种产生的蛋白酶水解底物蛋白,再进行分离纯化,得到生物活性肽。微生物发酵法多采用蛋白酶活力较高的细菌、霉菌和酵母菌作为发酵菌种。微生物发酵法具有诸多优点,如反应条件温和、菌种繁殖迅速、发酵工艺简单、生产成本低、易于工业化生产,且得到的生物活性肽分子质量较小,具备较好的生物活性等[32]。MUROTA等[33]用食品级地衣芽孢杆菌蛋白酶酶解鲨鱼软骨制备得到水解物,并分离纯化出具有降尿酸生物活性的多肽。微生物发酵法也有一些缺点,如可用于制备降尿酸活性肽的产酶菌种较少,部分产酶菌及其代谢产物具有一定的毒性,同时发酵过程较难控制等问题。
2.3 固相合成法
固相合成法是一种化学合成生物活性肽的方法。固相多肽合成首先要确定出目标肽段中氨基酸的组成及排列顺序,一般是从C端(羧基端)向N端(氨基端)延伸添加氨基酸的过程[34]。多肽的固相合成法主要包括叔丁氧碳基合成法(Boc合成法)和9-甲氧羟基合成法(Fmoc合成法)两种常用方法。其中Fmoc合成法较多应用在降尿酸活性肽的制备中。LI等[35]采用Fmoc合成法合成含有Trp的核桃蛋白衍生肽,并验证了其能够有效抑制XOD活性,且随着Trp含量的增加.其抑制活性增强。LI等[28]从鲣鱼酶解产物中鉴定出2种XOD抑制肽,其分别为Trp-Met-Leu和Pro-Gly-Ala-Cys-Ser-Asn,并用Fmoc合成法对其进行了化学合成,评价了其XOD抑制活性。MUROTA等[29]从鲨鱼软骨水提取物中分离鉴定出降尿酸活性肽,并通过Fmoc合成法获得相关肽段,同时对人工合成肽段的降尿酸活性予以了评价。任娇艳等[36]采用标准Fmoc方案,选用wang树脂进行固相合成了一种具有降尿酸功效的三肽Tyr-Glu-Gly。虽然固相合成法可直接合成目标肽段,但此法成本较高,残留化合物较多,限制了其大规模生产及工业化应用。
3 降尿酸活性肽的分离与纯化
为获得具有较高活性的降尿酸活性肽组分,需要进一步对酶解产物进行分离富集处理。常用的分离纯化技术包括:超滤、离子交换色谱法(ion exchange chromatograhy,IEC)、凝胶色谱法(size exclusion chromatography,SEC)以及反向高效液相色谱(reverse phase-high perfomance liquid chromatography,RP-HPLC)。
3.1 膜分离
膜分离是利用半透膜表面不同大小微孔的筛分作用,可实现不同大小的混合物分离的技术[37]。对降尿酸活性肽进行膜分离的方法主要是超滤。
超滤是一种加压膜分离技术,是利用物理筛分的原理实现对降尿酸活性肽的初步分离。将酶解液通过不同截留分子质量的多孔膜进行超滤,其操作简单,过滤效果较好[38]。盛周煌[26]在对罗非鱼皮胶原蛋白降尿酸活性肽分离纯化中,将罗非鱼皮胶原蛋白酶解液依次通过截留分子质量为5 000 Da、3 000 Da的超滤膜以后,获得对XOD抑制活性最好的组分。邹琳[27]在鲣鱼降尿酸活性肽的分离纯化中,将鲣鱼酶解产物依次通过截留分子质量为1 000 Da、600 Da和300 Da的超/纳滤膜,从鲣鱼酶解物中分离纯化出降尿酸活性肽。但超滤往往只能实现降尿酸活性肽的粗分离,要进行降尿酸活性肽的精细分离,还需与其他技术联用。
3.2 色谱分离
目前用于纯化降尿酸活性肽的色谱分离法主要有3种:离子交换色谱法(IEC)、凝胶色谱法(SEC)以及反向高效液相色谱(RP-HPLC)。IEC以离子交换剂为固定相,依据流动相中的带电的溶质分子与交换剂中离子作用力大小不同实现分离。SEC又称体积排阻色谱法,根据流动相是水溶性溶剂或有机溶剂又可分为凝胶过滤色谱(gel filtration chromatography,GFC)和凝胶渗透色谱(gel permaeation chromatography,GPC),其分离原理是根据多肽的分子质量大小、形状不同,其在凝胶上受阻滞的程度不同,故其通过凝胶孔径的速度不同,常以Sephadex G-15、Sephadex G-25和Sephadex G-50作为固定相。RP-HPLC是根据蛋白质分子在固定相和流动相中的分配不同从而达到分离的目的。通常以C8、C18作为固定相,用乙腈或甲醇作为流动相,常用于分离分子质量低于5 000 Da的肽类物质。
在实际操作中,单一的分离方法很难实现降尿酸活性肽的多级分离,通常需要多种方法联合使用。一般先经过离子交换柱或凝胶色谱柱分离,然后再经高效液相色谱进行纯化。LIU等[24]通过Sephadex G-50凝胶过滤与高效液相色谱法从水稻的提取物中鉴定出结构为(Ala)4-Gly-Ala-Lys-Ala-Arg (785.91 Da)的新型降尿酸活性肽。盛周煌等[26]将罗非鱼皮胶原蛋白酶解液依次经过超滤膜、DEAE-52 Cellulose 离子交换柱层析、Sephadex G-25 凝胶过滤和RP-HPLC制备柱分离,获取了具有高效降尿酸潜力的短肽。LI等[28]用离子交换层析和凝胶过滤色谱对鲣鱼水解产物、核桃水解产物以及大豆水解产物进行了分离纯化,获得具有体外XOD抑制活性的六肽和三肽。HE等[30]通过Sephadex G-15凝胶过滤柱分离金枪鱼蛋白水解物,分离出13个具有降尿酸活性的二肽与三肽。NONGONIERMA等[16]将乳铁蛋白水解产物中的多肽吸附到活性炭上,使用乙腈逐步洗脱,然后使用RP-HPLC实现不同亲疏水性肽的分离,并检测了其XOD抑制活性。
表1 食物蛋白源降尿酸活性肽的制备、分离纯化及结构鉴定列表
Table 1 Preparation, purification and identification of food-derived anti-hyperuricemic peptides

原料蛋白酶酶解条件纯化鉴定氨基酸序列活性评价参考文献核桃粉Alcalase2.4L蛋白酶E/S=1%(质量分数),pH 7.0, 55 ℃,9 h纯化:GFC、RP-HPLC鉴定:LC-ESI-MS/MSAla-Asp-Ile-Tyr-Thr-Glu、Trp-Pro-Pro-Lys-AsnXOD抑制率IC50值:19.01 mg/mL(Ala-Asp-Ile-Tyr-Thr-Glu)、17.75 mg/mL(Trp-Pro-Pro-Lys-Asn)[23]水稻--纯化:GFC、RP-HPLC、HPLC鉴定:MS(Ala)4-Gly-Ala-Lys-Ala-Arg血尿酸浓度:32.99 mg/kg、血清肌酐浓度:83.02 μM((Ala)4-Gly-Ala-Lys-Ala-Arg, 10 μg/kg)[24]平菇--纯化:GFC、UF、SPE、RP-HPLC鉴定:LC-MS/MSPhe-Cys-HisXOD抑制率IC50值:0.9 mg/mL(Phe-Cys-His)[25]罗非鱼皮复合蛋白酶E/S=3.2%(质量分数),pH 8.0,48 ℃,6 h纯化:UF、IEC、GFC、HPLC鉴定:LC-MS/MSThr-Ser-Pro-TrpXOD抑制率IC50值:3.51 mg/mL(Thr-Ser-Pro-Trp)[26]鲣鱼中性蛋白酶加酶量:489.86 U/g,pH 7.08, 49.5 ℃,5 h纯化:UF鉴定:MALDI-TOF/TOF-MSAla-Cys-Glu-Cys-AspXOD抑制率IC50值:7.23 mg/mL(Ala-Cys-Glu-Cys-Asp)[27]木瓜蛋白酶E/S=0.35%(质量分数),pH7.0,55 ℃,4 h纯化:IEC、GFC鉴定:LC-ESI-MS/MSTrp-Met-Leu、Pro-Gly-Ala-Cys-Ser-AsnXOD抑制率:65.5% (酶解物, 25 mg/mL)[28]鲨鱼软骨碱性蛋白酶加酶量:0.04%(体积分数),pH 8.0,60 ℃,4 h纯化:SEC鉴定:RP-HPLCTyr-Leu-Asp-Asn-Tyr、Ser-Pro-Pro-Tyr-Trp-Pro-Tyr5 mg/kg体重静脉注射可显著降低血尿酸水平(Tyr-Leu-Asp-Asn-Tyr、Ser-Pro-Pro-Tyr-Trp-Pro-Tyr)[29]金枪鱼Alcalase2.4L蛋白酶E/S=0.25%(质量分数),pH 7.0,55 ℃,6 h纯化:GFC鉴定:UPLC/MS/MSPhe-His、Phe-Lys、Phe-Arg、Phe-Trp、Leu-Arg、Leu-Trp、Val-Trp、Tyr-His、Ala-Leu-Trp、Phe-Val-Arg、Gly-Val-Trp、Leu-Phe-Trp、Leu-Gly-TrpXOD抑制率IC50值:25.7 mmol/L(Phe-His)[30]
注:-表示无
4 降尿酸活性肽体内外活性评价
4.1 体外降尿酸活性评价
XOD抑制活性的测定方法包括紫外分光光度法、双酶偶联法、荧光分析法、MTS/PMS还原法、NBT/PMS显色法、细胞色素法、邻二氮菲法、高效液相色谱法等。对于肽类,大多是测定产物在XOD的催化的下产生尿酸的含量。紫外分光光度法和高效液相色谱法是目前研究XOD活性最常用的方法。JANG等[25]采用紫外分光光度法测定平菇提取物的XOD抑制活性,并从其中分离纯化出具有降尿酸作用的三肽Phe-Cys-His。LI等[23]用高效液相色谱法定量测定脱脂核桃蛋白酶解物和脂脱酚核桃蛋白酶解物在XOD作用下产生尿酸的速率,来评价降尿酸活性肽的XOD抑制活性。苏国万等[39]发明一种以核桃粕为原料制备具有降尿酸功效的生物活性肽的方法,并采用反向高效液相色谱法评价降尿酸活性肽的XOD抑制活性。刘丹等[40]通过孵育人肝细胞LO2建立了一种高尿酸血症肝细胞模型,通过高效液相色谱检测尿酸生成量来评价乳清蛋白肽对XOD的抑制活性,发现乳清蛋白肽具有较好的XOD抑制活性。杨柳[41]建立了筛选降尿酸多肽类物质的体外测定方法,采用双酶偶联法联合高效液相色谱法(HPLC法)测定多肽类物质的体外XOD抑制活性。康小燕等[42]建立了适应于筛选降尿酸多肽类物质的体外测定方法,在优化后的酶反应条件下对比了双酶偶联法和高效液相色谱法的精密度和准确度等,验证了双酶偶联法联合高效液相色谱法筛选具有降尿酸功效的多肽类物质的可行性。
4.2 体内降尿酸活性评价
体内降尿酸活性评价要建立高尿酸血症动物模型,对动物进行给药处理,根据给药前后高尿酸血症动物模型血清尿酸水平的变化判断肽的降尿酸活性。高尿酸血症的模型动物主要包括啮齿类及禽类[43-44]。啮齿类动物常用Sprague-Dawley大鼠(SD大鼠)、Wister大鼠、KM小鼠、昆明小鼠、C57BL/6小鼠、ICR小鼠等;禽类动物常用罗曼蛋鸡、迪法克鹌鹑[45-46]。诱导痛风和高尿酸血症动物模型的方法主要有:补充尿酸或尿酸前体法诱导模型[47-49]、抑制尿酸排泄或分解模型、真菌产物诱导模型[50]、基因敲除模型。
费洪新等[49]在昆明小鼠后足右侧足底皮下及小鼠后足右侧背侧足趾部注射等量尿酸钠溶液,成功构造高尿酸小鼠模型。黎青勇[15]用氧嗪酸钾灌胃SD大鼠,建立高尿酸血症的动物模型,验证了脱脂核桃蛋白酶解物和脱酚脱脂核桃蛋白酶解物具有降尿酸作用。孙婷婷等[51]对SD大鼠灌胃酵母膏淀粉混合液,同时喂以氧嗪酸钾,构建高尿酸血症动物模型,验证了仿刺参酶解液具有XOD抑制活性的功效。石拓等[52]通过腺嘌呤和氧嗪酸钾灌胃Wistar雄性大鼠3周,同时让其自由进食含10%酵母膏饲料,建立了高尿酸血症大鼠模型。孙敏[53]采用黄嘌呤和盐酸乙胺丁醇混悬液灌胃昆明小鼠建立痛风动物模型,证明了蜂毒物质中起到降尿酸作用的主要物质为蜂毒肽。张锐等[54]用腺嘌呤和乙胺丁醇对SD大鼠灌胃3周,构造高尿酸血症模型,证明Ca+酪蛋白磷酸肽(CPPs)饮食可以降低高尿酸血症模型大鼠肝脏中XOD活性,降低血清尿酸水平。由于大、小鼠饲养方便、操作简单且为哺乳动物,与人类种属接近,故目前应用在肽的降尿酸活性评价中的高尿酸血症模型动物主要是大、小鼠。
5 降尿酸活性肽的结构鉴定
降尿酸活性肽的生物活性主要受其分子质量大小以及氨基酸组成与序列的影响,因此鉴定肽的序列组成具有十分重要的意义。鉴定降尿酸活性肽的序列和分子质量常用液相色谱-质谱联用技术(LC-MS/MS),为提高测定结果的准确性,此技术常与电喷雾电离源(ESI)、联用混合四级杆飞行时间质谱仪(Q-TOF mass)等联合使用[55]。黎青勇[15]采用超高压液相色谱-高分辨质谱联用仪,对经过分离纯化后的脱脂脱酚核桃蛋白肽F1进行结构解析,分析出7种蛋白多肽片段,分别为Trp-Asp-Asp、His-Cys-Pro-Phe、Trp-Asp-Gln-Trp、(Pro)2-Lys-Asn-Trp、Trp-(Pro)2-Lys-Asn、Ala-Asp-Ile-Tyr-Thr-Glu和Trp-Ser-Arg-(Glu)2-Gln-Glu。盛周煌[26]用LC-MS/MS鉴定降尿酸活性肽序列,经过LC-MS/MS对氨基酸序列分析得到具有降尿酸活性的罗非鱼皮胶原蛋白肽的序列为Thr-Ser-Pro-Trp。邹琳[27]通过亲和超滤-液质技术(MALDI-TOF/TOF-MS),分离鉴定出鲣鱼酶解物中发挥降尿酸活性的肽段,其氨基酸序列为Ala-Cys-Glu-Cys-Asp,并通过分子对接技术研究了其构效关系。HE等[30]用超高压液相色谱-质谱联用技术从金枪鱼蛋白酶解物中鉴定出13个具有降尿酸活性的二肽/三肽。
从目前已鉴定一级结构的食物蛋白源降尿酸活性肽来看,其通常为由10个以下的氨基酸组成的寡肽,分子质量一般都小于1 000 Da。鉴定降尿酸活性肽的序列结构,对深入研究降尿酸活性肽的构效关系,实现降尿酸活性肽的高效制备及产品开发等方面具有十分重要的意义,可为降尿酸活性肽作用机制等方面的研究提供重要依据。
6 降尿酸活性肽构效关系
食物蛋白源降尿酸活性肽的一级结构中氨基酸的种类、数目及基团所处的位置等都会影响其生物活性。对降尿酸活性肽的构效关系进行研究,有利于其生产应用与产品开发。
6.1 氨基酸种类影响
氨基酸种类、数目是影响肽降尿酸活性的重要因素。降尿酸活性肽中的Trp、Phe残基能够阻断XOD与底物黄嘌呤的结合,从而减少尿酸的产生,所以含芳香族氨基酸尤其是含Trp残基、Phe残基的降尿酸活性肽具有更高的XOD抑制活性[15,30,35]。HE等[30]研究发现含有Phe的二肽/三肽具有很好的XOD抑制活性,其中活性最高的Phe-His主要通过与XOD形成2个氢键和1个π-π堆积来进行结合。此外,肽中氨基酸的疏水性与肽的降尿酸活性存在一定的关联。亲水性肽与XOD的氨基酸残基之间主要涉及氢键和静电相互作用,而疏水性肽与XOD的氨基酸残基之间主要涉及疏水相互作用。疏水性肽比亲水性肽更容易进入XOD的活性位点,形成与XOD催化底物竞争的机制,故含疏水性氨基酸的降尿酸活性肽具有更强的XOD抑制活性[28]。
6.2 氨基酸位置影响
多肽中氨基酸残基的位置也会影响其XOD抑制活性。不同种类的氨基酸在多肽上的不同位置对XOD抑制活性的影响也不同。研究表明,芳香族氨基酸(如Trp、Tyr、Phe 和 His)及亲水性氨基酸位于N端比C端能使二肽、三肽发挥更高XOD抑制活性,芳香族氨基酸位于中间位置不利于多肽发挥XOD抑制活性。对于疏水性氨基酸来说,疏水氨基酸位于C端促使多肽具有更高的XOD抑制活性[15]。
7 展望
近年来,随着人们生活水平的提高,越来越多人受到高尿酸血症及痛风的困扰,其发病率高、危害性大。但目前临床治疗使用的药物都对人体具有明显的毒性及副作用,因此开发高效、经济、安全的降尿酸活性肽具有十分重要的意义。本文综述了目前关于国内外食物蛋白源降尿酸活性肽的制备、分离纯化、功能活性评价及结构鉴定方面的研究。现国内外研究多采用酶解法、微生物发酵法和固相合成法进行降尿酸活性肽的制备;采用超滤、离子交换色谱法、凝胶色谱法以及反向高效液相色谱实现降尿酸活性肽的多级分离纯化;采用液相色谱-质谱联用技术鉴定降尿酸活性肽的氨基酸序列。由于食物蛋白源降尿酸活性肽制备原料来源广泛,制备工艺较为成熟,且其安全性高,分子质量小,易被人体吸收,作用效果较好,故其在食品、医药及化妆品等领域有极大的利用价值。但目前对食物蛋白源降尿酸活性肽的研究大多集中在制备、分离与结构鉴定方面,其活性评价大多停留在细胞模型与动物模型水平,相关的人体实验开展较少,仍处于试验阶段,尚未进行大规模工业化生产及临床应用。此外,食物蛋白源降尿酸活性肽的构效关系及作用机理有待进一步深入研究。随着国内外相关研究的不断开展,从食物蛋白源开发降尿酸活性肽将在预防与治疗高尿酸血症及痛风症方面具有广阔的应用前景。
参考文献
[1] 邹筱芳,巫冠中.尿酸肾损伤的分子机制研究进展[J].安徽医药,2015,19(1):5-9.
[2] WANG J, CHEN R P, LEI L, et al. Prevalence and determinants of hyperuricemia in type 2 diabetes mellitus patients with central obesity in Guangdong Province in China[J].Asia Pacific Journal of Clinical Nutrition,2013,22(4):590-598.
[3] KRISHNAN E. Interaction of inflammation, hyperuricemia, and the prevalence of hypertension among adults free of metabolic syndrome: nhanes 2009-2010[J].Journal of the American Heart Association,2014,3(2):e000 157-e000 157.
[4] YOU L L, LIU A P, WUYUN G W, et al. Prevalence of hyperuricemia and the relationship between serum uric acid and metabolic syndrome in the Asian Mongolian area[J]. Journal of Atherosclerosis and Thrombosis,2014,21(4):355-365.
[5] GUSTAFSSON D, UNWIN R. The pathophysiology of hyperuricaemia and its possible relationship to cardiovascular disease, morbidity and mortality[J]. BMC Nephrology,2013,14(1):164.
[6] CHEN S, GUO X, DONG S, et al. Association between the hypertriglyceridemic waist phenotype and hyperuricemia:A cross-sectional study[J].Clinical Rheumatology,2017,36(5):1 111-1 119.
[7] 马金魁,张宏斌.高尿酸血症及治疗药物的研究进展[J].广东医学,2018,39(s2):262-267.
[8] 王朝晖,苏冠华.临床用药速查手册[M].北京:中国协和医科大学出版社,2009.
[9] 曹启江,宋庆凤,姚满,等.治疗痛风新型药物研究进展[J].广东医学,2019,40(10):1 497-1 500.
[10] 艾国,杜丽娜,梅兴国.蛋白质、多肽类药物新剂型与新技术发展动态[J].中国生化药物杂志,2004,25(6):366-369.
[11] 吴建中,赵谋明,宁正祥.食品中的生物活性多肽[J].食品与发酵工业,2002,28(11):46-50.
[12] 王成华,邢新会.黄嘌呤氧化酶的研究进展及其发展前景[J].广西科学,2017,24(1):15-24.
[13] 刘晓然,李泰明.黄嘌呤氧化酶抑制剂在高尿酸血症治疗中的研究进展[J].轻工科技,2017,33(9):20-21.
[14] 赵莹, 张启虹, 冯明声, 等. 降尿酸药物黄嘌呤氧化酶抑制剂的研究进展[J]. 药学进展, 2009, 33(2):55-61.
[15] 黎青勇.核桃源降尿酸肽靶向抑制黄嘌呤氧化酶活性的构效机制研究[D].广州:华南理工大学,2018.
[16] NONGONIERMA A B, FITZGERLD R J. Tryptophan-containing milk protein-derived dipeptides inhibit xanthine oxidase[J]. Peptides, 2012, 37(2):263-272.
[17] NONGONIERMA A B, MOONEY C, SHIELDS D C, et al. Inhibition of dipeptidyl peptidase IV and xanthine oxidase by amino acids and dipeptides[J]. Food Chemistry, 2013, 141(1):644-653.
[18] 刘洋.海洋鱼抗痛风肽的制备及其作用机理研究[D].广州:华南理工大学,2014.
[19] 张开平,苏仕林,刘燕丽,等.生物活性肽功能及制备方法的研究进展[J].农产品加工,2015(12):61-64.
[20] SU X, DONG C, ZHANG J, et al. Combination therapy of anti-cancer bioactive peptide with Cisplatin decreases chemotherapy dosing and toxicity to improve the quality of life in xenograft nude mice bearing human gastric cancer[J].Cell and Bioscience, 2014,4(1):1-13.
[21] 阮晓慧,韩军岐,张润光,等.食源性生物活性肽制备工艺、功能特性及应用研究进展[J].食品与发酵工业,2016,42(6):248-253.
[22] 刘铭,刘玉环,王允圃,等.制备、纯化和鉴定生物活性肽的研究进展及应用[J].食品与发酵工业,2016,42(4):244-251.
[23] LI Q Y, KANG X Y, SHI C C, et al. Moderation of hyperuricemic rats via consuming walnut protein hydrolysates diet and identification of new antihyperuricemic peptides[J].Food and Function.2018, 9(1):107-116.
[24] LIU N X, WANG Y, YANG M F, et al. New rice-derived short peptide potently alleviated hyperuricemia induced by potassium oxonate in rats [J]. Journal of Agricultural and Food Chemistry,2019,67(1):220-228.
[25] JANG I T, HYUN S H, SHIN J W, et al. Characterization of an anti-gout xanthine oxidase inhibitor from Pleurotus ostreatus[J]. Mycobiology,2014,42(3):296-300.
[26] 盛周煌.罗非鱼皮胶原蛋白降尿酸活性肽的研究[D].广州:华南理工大学,2018.
[27] 邹琳.鲣鱼黄嘌呤氧化酶抑制肽的酶解制备及功能活性评价[D].杭州:浙江大学,2019.
[28] LI Y J, KANG X Y, LI Q Y, et al. Anti-hyperuricemic peptides derived from bonito hydrolysates based on in vivo hyperuricemic model and in vitro xanthine oxidase inhibitory activity[J].Peptides,2018,107:45-53.
[29] MUROTA I, TAGUCHI S, SATO N, et al. Identification of antihyperuricemic peptides in the proteolytic digest of shark cartilage water extract using in vivo activity-guided fractionation[J].Journal of Agricultural and Food Chemistry,2014, 62(11):2 392-2 397.
[30] HE W W, SU G W, SUN D X, et al. In vivo anti-hyperuricemic and xanthine oxidase inhibitory properties of tuna protein hydrolysates and its isolated fractions[J].Food Chemistry,2019,272:453-461.
[31] 赵谋明,徐巨才,刘洋,等.秋刀鱼制备黄嘌呤氧化酶抑制肽的工艺优化[J].农业工程学报,2015,31(14):291-297.
[32] 白雪,李丹凤,王婷婷,等.发酵法制备生物活性肽及其产物的初步分析[J].食品工业科技,2013,34(23):201-205.
[33] MUROTA I, TAMAI T, BABA T, et al. Uric acid lowering effect by ingestion of proteolytic digest of shark cartilage and its basic fraction[J].Journal of Food Biochemistry,2010,34(1):182-194.
[34] YU L, YANG L, AN W, et al. Anticancer bioactive peptide-3 inhibits human gastric cancer growth by suppressing gastric cancer stem cells[J].Journal of Cellular Biochemistry,2014,115(4):697-711.
[35] LI Q Y, SHI C C, WANG M, et al. Tryptophan residue enhances in vitro walnut protein-derived peptides exerting xanthine oxidase inhibition and antioxidant activities[J].Journal of Functional Foods,2019,53(53):276-285.
[36] 任娇艳,康小燕.一种具有降尿酸活性的多肽及其应用:中国,106317178A[P].2017-01-11.
[37] 杨方威,冯叙桥,曹雪慧, 等.膜分离技术在食品工业中的应用及研究进展[J].食品科学,2014,35(11):330-338.
[38] 王志斌,杨宗伟,邢晓林,等.膜分离技术应用的研究进展[J].过滤与分离,2008,18(2):19-23.
[39] 苏国万,赵谋明,赵强忠,等.一种用核桃粕制备具有降尿酸功效的生物活性肽的方法:中国,103627760A[P].2014-03-12.
[40] 刘丹,任娇艳,梁明.高尿酸血症细胞模型的构建及其在降尿酸肽筛选中的应用[J].现代食品科技,2017,33(8):72-79.
[41] 杨柳,康小燕,梁明,等.筛选降尿酸肽的体外测定方法的建立与优化[J].现代食品科技,2018,34(4):249-257.
[42] 康小燕. 磁性微球固定化黄嘌呤氧化酶的制备及其分离降尿酸肽的研究[D].广州:华南理工大学,2017.
[43] 王晗,张敏,路腾飞,等.高尿酸血症动物模型研究进展[J].天津中医药大学学报,2014,33(4):253-256.
[44] 刘静,徐玲玲.常用痛风模型的作用机制及评价[J].中国药师,2012,15(8):1 193-1 194.
[45] 杨会军,李兆福,彭江云.高尿酸血症动物模型研究概况[J].中医学报,2013,28(1):60-62.
[46] 马思佳,霍娇,张立实.高尿酸血症动物模型研究进展[J].卫生研究,2015,44(1):158-162.
[47] PINEDA C, FUENTES-G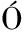 MEZ, ARTURO J, et al. Animal model of acute gout reproduces the inflammatory and ultrasonographic joint changes of human gout[J]. Arthritis Research and Therapy,2015,17(1):37.
MEZ, ARTURO J, et al. Animal model of acute gout reproduces the inflammatory and ultrasonographic joint changes of human gout[J]. Arthritis Research and Therapy,2015,17(1):37.
[48] SANTOS R M S, OLIVEIRA S M, SILVA C R, et al. Anti-nociceptive and anti-edematogenic effects of glibenclamide in a model of acute gouty attack in rats[J].Inflammation Research,2013,62(6):617-625.
[49] 费洪新,韩玉生,廖婷,等.车前子对小鼠急性痛风性关节炎的影响[J].黑龙江科学,2014,5(5):9-11.
[50] KUBENA L F, PHILLIPS T D, CREGER C R, et al. Toxicity of ochratoxin A and tannic acid to growing chicks[J]. Poultry Science,1983,62(9):1 786-1 793.
[51] 孙婷婷,李妍妍,周君,等.仿刺参酶解液抑制黄嘌呤氧化酶活性的研究[J].中国食品学报,2019,19(7):128-137.
[52] 石拓,卢存龙,李龙,等.液相色谱-质谱研究高尿酸血症大鼠血清代谢组学[J].基础医学与临床,2019,39(3):337-342.
[53] 孙敏.蜂毒活性肽的分离纯化及生理功能研究[D].济南:济南大学,2017.
[54] 张锐,姚芳芳,何伟.酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠的影响[J].食品科学, 2010, 31(21):332-334.
[55] ASHA K K, REMYA-KUMARI K R, ASHOK-KUMAR K, et al. Sequence determination of an antioxidant peptide obtained by enzymatic hydrolysis of oyster Crassostrea madrasensis (Preston)[J].International Journal of Peptide Research and Therapeutics, 2016, 22(3):421-433.

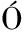 MEZ, ARTURO J, et al. Animal model of acute gout reproduces the inflammatory and ultrasonographic joint changes of human gout[J]. Arthritis Research and Therapy,2015,17(1):37.
MEZ, ARTURO J, et al. Animal model of acute gout reproduces the inflammatory and ultrasonographic joint changes of human gout[J]. Arthritis Research and Therapy,2015,17(1):37.