表1 直链淀粉晶种的粒度参数
Table 1 The particle size parameters of amylose crystal seeds
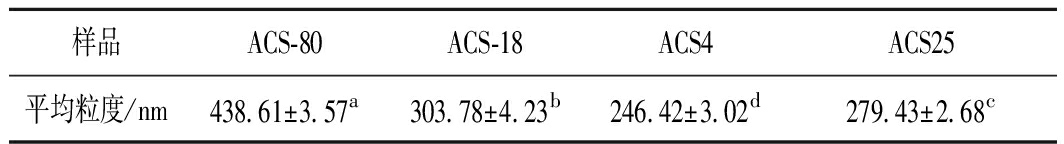
样品ACS-80ACS-18ACS4ACS25平均粒度/nm438.61±3.57a303.78±4.23b246.42±3.02d279.43±2.68c
糊化淀粉在冷却和贮藏中,直链淀粉和支链淀粉通过氢键重新排列成有序微晶的过程,称为淀粉回生(老化),其实质是淀粉分子链在氢键等分子间作用力的驱动下从无序到有序的排列[1-2]。淀粉老化是导致市场上面包、蛋糕、米糕等米面制品风味劣变,口感变差,货架期缩短的主要原因[3]。目前对于回生的研究多集中于外源调控方面,缺乏回生不同阶段间关系的解析[4-5]。直链淀粉主导的短期回生和支链淀粉主导的长期回生阶段之间的关系问题,是米面制品抗回生技术调控的共性理论基础。研究认为短期回生为长期回生提供了“启动子”,但是由于回生体系复杂及研究手段局限,该理论尚未得到系统阐述。聚合物结晶的经典动力学模型指出,结晶包括成核、生长和形成完美晶体3个过程。在淀粉的重结晶体系中,回生的本质也是成核和晶体生长的过程。因此,晶核是淀粉回生研究的切入点与重要因子,是回生共性理论突破的关键。
基于此,本文在大米淀粉回生过程中,添加短期回生阶段形成的晶种,简化回生研究体系,诱导淀粉长期回生。通过FTIR和13C CP/MAS NMR来探究其对淀粉长期回生的影响,以期揭示淀粉短期回生与长期回生阶段之间的关联性,丰富淀粉回生共性理论。
大米淀粉,江西金农发展有限公司;正丁醇(分析纯),国药集团化学试剂有限公司;异戊醇(分析纯),国药集团化学试剂有限公司;浓H2SO4(分析纯),国药集团化学试剂有限公司;KBr(分析纯),国药集团化学试剂有限公司。
Nano Brook Omni型多角度粒度与高灵敏度Zeta电位分析仪,美国布鲁克海文仪器公司;IS10傅里叶红外光谱仪,美国Nicolet公司;AVIII 400 MHZ WB光谱仪,德国Bruker公司。
1.3.1 直链淀粉晶种的制备及粒度测定
参考程科等[6]的方法并加以优化,从大米淀粉(直链淀粉含量为12.2%)中提取直链淀粉。用去离子水配制200 g/L的淀粉乳,搅拌均匀后置于沸水浴中预糊化30 min,然后于121 ℃的高压灭菌锅中继续糊化20 min。糊化完成后立即取出,分别在-80、-18、4和25 ℃环境中以不同的平均降温速率(依次为6.71、3.00、1.78和0.75 ℃ /min)冷却,降温至25 ℃之后,转移至25 ℃下保温回生,冷却和保温回生过程持续12 h,制备获得的样品依次命名为RA-80、RA-18、RA4和RA25。上述4种样品回生完成后干燥,研磨后过筛,用3.16 mol/L浓H2SO4配制固形物含量为10%的晶种酸解液,在45 ℃下搅拌水解7 d,离心洗涤至中性,将产物配成30 g/L的悬浊液保存得到直链淀粉晶种,依次命名为ACS-80、ACS-18、ACS4和ACS25。
将30 g/L直链淀粉晶种悬浊液稀释至1 g/L,超声10 min以破除颗粒团聚。超声完成后,立即转到电位仪的样品池中,进行粒度测定。
1.3.2 无定形淀粉、回生淀粉的制备
将原淀粉配成100 g/L的淀粉乳,在沸水浴中加热糊化30 min,然后立即转移至60 ℃烘箱中烘干,研磨,过筛,得到无定形淀粉(AS)。
配制100 g/L的淀粉乳,置于沸水浴中糊化30 min,然后冷却至60 ℃时,按7%的晶种添加量加入直链淀粉晶种并搅拌均匀。未添加晶种的原淀粉体系为空白对照组(kb)。所有的样品贮藏在4 ℃下回生21 d后取出,烘箱烘干,研磨,过筛,置于密封袋中备用。空白对照组样品命名为kb-21,添加ACS-80, ACS-18, ACS4和ACS25的回生淀粉依次命名为ACS-80-21, ACS-18-21, ACS4-21和ACS25-21。
1.3.3 直链淀粉干预下的回生淀粉的短程有序度及双螺旋含量测定
采用FTIR测定回生淀粉的短程有序度。在红外灯照射环境下,将回生淀粉样品和预先磨细的溴化钾以1∶20(质量比)混合,用玛瑙研钵研磨至合适粒度后,压成厚薄适中的压片。实验参数如下:扫描波长为4 000~ 400 cm-1,分辨率为4 cm-1,扫描次数为16,纯KBr压片为空白背景。使用OMNIC软件对红外光谱进行去卷积处理。
利用13C CP/MAS NMR测定回生淀粉中双螺旋含量。实验参数如下所示:仪器工作频率为100.62 MHz,配有4 mm的双共振探头,以六甲基苯作校准液,样品采集时间为0.016 s,接触时间1.6 ms,扫描次数1 600次。延迟时间2 s,转速6 kHz。使用Excel、Origin和Peakfit软件对数据进行分析。
动态光散射(dynamiclight scattering,DLS)法根据激光照射溶液体系中做布朗运动的颗粒产生的动态散射光来获取粒径信息。当激光照射悬浮液时,其中的颗粒会使激光发生散射,颗粒受周围分子的碰撞而发生布朗运动[7]。根据多普勒效应,散射光频率受入射光频率影响,以其为中心随机波动,从而影响散射光强。一般来说,颗粒粒径小,布朗运动速度快,散射光频率变化快,散射光强波动也快;反之,则慢。进行相关函数运算可得粒径信息。
由DLS法得到的直链淀粉晶种的粒度结果如表1所示,ACS-80、ACS-18、ACS4及ACS25的平均粒度分别为438.61、303.78、246.42及279.43 nm,粒径均为纳米级。大米淀粉在已知谷物里颗粒最小,粒径为4~9 μm,形状为不规则多边形。在加热糊化过程中,淀粉分子链吸热膨胀,变成无规则团状。在回生前加入的纳米级的直链淀粉晶种,可以顺利进入其内部,与淀粉分子链充分接触,起到诱导作用。
表1 直链淀粉晶种的粒度参数
Table 1 The particle size parameters of amylose crystal seeds

样品ACS-80ACS-18ACS4ACS25平均粒度/nm438.61±3.57a303.78±4.23b246.42±3.02d279.43±2.68c
注:ACS-80、ACS-18、ACS4、ACS25:依次为在前期降温环境温度-80、-18、4、25 ℃下冷却后经处理制备得的直链淀粉晶种。同一行中具有不同小写字母之间存在显著差异(P<0.05)
淀粉回生过程中形成的双螺旋结构构成回生淀粉的短程有序结构。本实验通过FTIR研究回生淀粉的短程有序结构。由图1-a可以看出,加入晶种后回生淀粉特征吸收峰没有发生变化,说明在原淀粉中加入直链淀粉晶种不会改变回生淀粉的官能团。
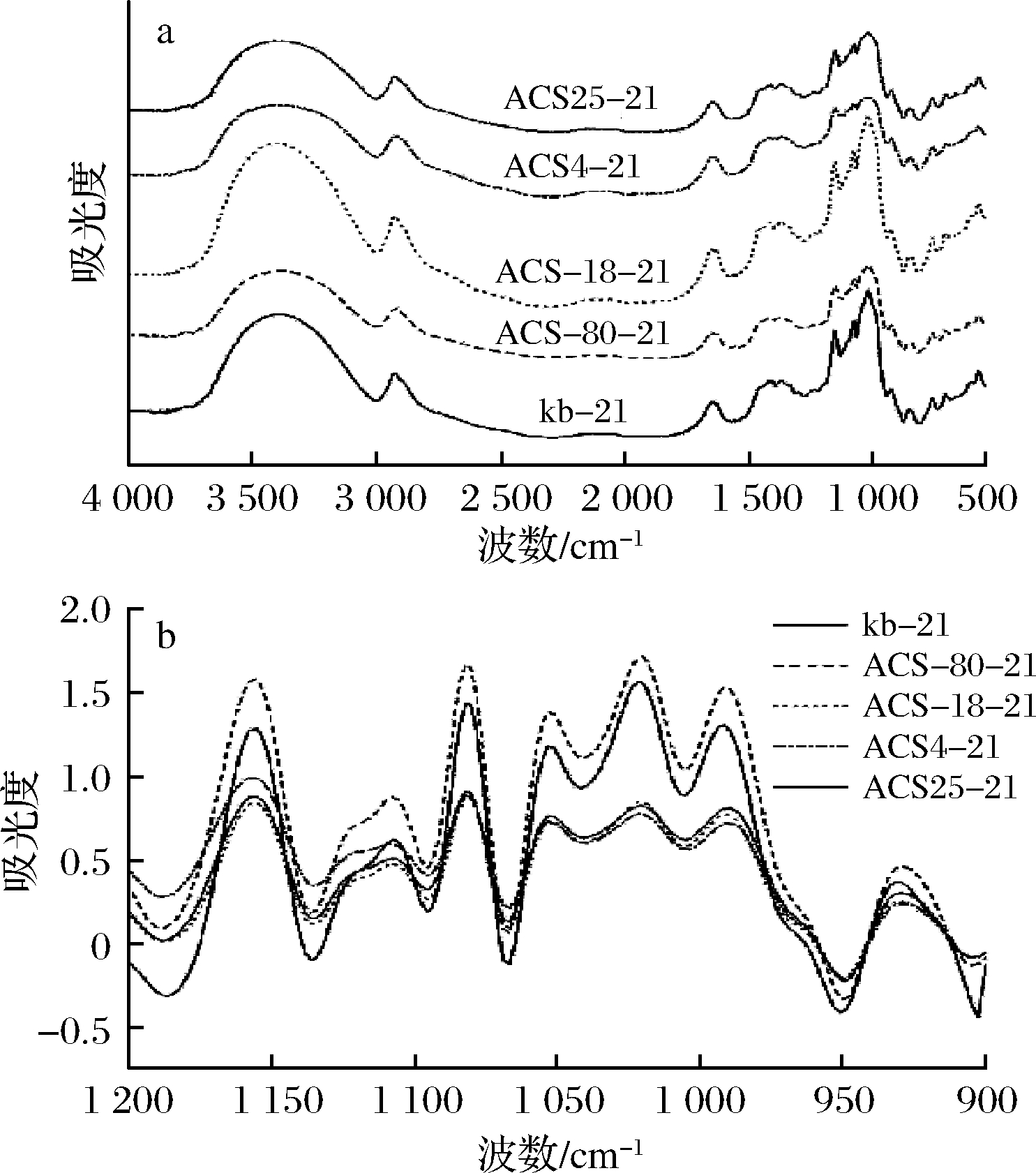
a-红外光谱图;b-去卷积图;
kb-21-未添加直链淀粉晶种的回生21d淀粉;ACS-80-21、ACS-18-21、
ACS4-21、ACS25-21-依次为添加ACS-80、ACS-18、ACS4、ACS25的
回生21d淀粉,下同
图1 直链淀粉晶种干预下的回生淀粉的傅里叶红外光谱图
及去卷积图
Fig.1 The Fourier transform infrared spectroscopy and
deconvolution graph of retrograded starch under the
intervention of amylose crystal seeds
对回生淀粉的红外光谱图进行去卷积处理,得到结果如图1-b所示。1 047和1 022 cm-1分别代表淀粉的结晶区和无定形区,995 cm-1处的吸收峰则对应羟基的弯曲振动[8-9]。淀粉研究中常用1 047和1 022 cm-1的吸光度之比(1 047 cm-1/1 022 cm-1)及1 022 cm-1和995 cm-1的吸光度之比(1 022 cm-1/995 cm-1)表征淀粉的短程有序度。样品红外光谱去卷积之后的比值结果如表2所示。直链淀粉晶种干预下回生淀粉1 047/1 022 cm-1升高,1 022/995 cm-1降低。表明在回生过程中,直链淀粉晶种的添加提高了回生淀粉的短程有序度,促进了淀粉的长期回生。此外,ACS4干预下的回生淀粉的短程有序度最高,促进长期回生效果最显著。原因可能是降温速率快时,分子链迁移受阻碍,影响直链淀粉有序重排进而影响晶种的结晶效果。但在单一贮藏温度环境中,B-型淀粉的重结晶过程受到成核的强烈限制,在最适合成核温度附近大米淀粉重结晶程度最高[10],而其最适成核温度为4℃,所以ACS4的结晶效果最好,其后依次为ACS25、ACS-18和ACS-80。结晶效果好的晶种在干预淀粉回生时可以起到更好的诱导作用,促进淀粉长期回生。
表2 直链淀粉晶种干预下的回生淀粉的短程有序参数
Table 2 The short-range ordered parameters of retrograded
starch under the intervention of amylose crystal seeds

样品1 047/1 022 cm-11 022/995 cm-1kb-21#0.670±0.005e1.246±0.004aACS-80-210.731±0.003d1.220±0.006bACS-18-210.800±0.002c1.149±0.002cACS4-210.887±0.003a1.029±0.003eACS25-210.853±0.012b1.043±0.004d
注:kb-21: 未添加直链淀粉晶种的回生21d淀粉;ACS-80-21、ACS-18-21、ACS4-21、ACS25-21:依次为加入ACS-80、ACS-18、ACS4、ACS25的回生21d淀粉;同一列中具有不同小写字母之间表示存在显著差异(P <0.05)
相较于X射线衍射所得的具有较大范围(结晶度)的结构信息,固态13C-核磁共振技术(13C-NMR)是对淀粉分子序列短距离范围的探测,检测范围较窄。各种淀粉的核磁共振光谱图相似,按化学位移分主要分为C1、C4、C2,C3,C5和C6四个区域。B-型淀粉双螺旋结构中具有两个葡萄糖残基,在C1区域中为双重峰,如图2所示。由于C1~C5信号的相对强度对施加的交叉极化接触时间的持续时间不敏感,因此可以通过计算结晶区的峰面积与回生淀粉的峰面积之比得出样品中结晶结构的相对含量。
C4-PPA法中淀粉的核磁图谱分成由双螺旋结构组成的结晶区和无定形区两部分,而忽略了其中单螺旋结构的存在,具有局限性。因此在本实验中,运用差减法去除由于C1共振而在有序环境中产生的重叠的非晶信号,将回生淀粉的核磁共振光谱图分解为无定形亚谱和结晶亚谱。由于C4区的峰较独立,与其他峰不重叠,故差减法中常选择其附近的点作为校准参考点[11]。分别选取82,83,84和85 ppm为参考点,差减法得到的结晶亚谱如图3所示。以85 ppm为参考点得到的结晶亚谱在一定区域中峰值强度比其他3个参考点得到的结晶亚谱强度高,所以选定85 ppm为参考点处理回生淀粉的核磁图谱。

AS-无定形淀粉;kb-21-未添加直链淀粉晶种的回生21d淀粉;
ACS-80-21、ACS-18-21、ACS4-21、ACS25-21-依次为添加ACS-80、
ACS-18、ACS4、ACS25的回生21d淀粉
图2 回生淀粉样品及无定形淀粉的原始13C CP/MAS图谱
Fig.2 Original 13C CP/MAS mapping of retrograded
starch samples and amorphous starch

a-添加ACS-80的回生21d淀粉;b-添加ACS-18的回生21d淀粉;c-添加ACS4的回生21d淀粉;d-添加ACS25的回生21d淀粉;
e-未添加直链淀粉晶种的回生21d淀粉
图3 分别以82、83、84和85 ppm为参考点用差减法得到的回生淀粉的结晶区亚谱
Fig.3 The crystalline sub-spectra of retrograded starch was obtained by using spectral subtraction using 82,83,84 and
85 ppm as reference point, respectively
C1区域(94~ 105 ppm)中没有来自其他碳位的重叠信号,链构象和糖苷扭转角之间关系更直观,所以选择C1区来计算淀粉样品中的双螺旋含量。C1区中结晶亚谱又分为单螺旋和双螺旋两部分,其中103 ppm处的峰为V-型结晶构象峰,通过峰面积之比来求出单螺旋和双螺旋相对比例。参考TAN等[11]的方法计算双螺旋含量,结果见表3。由表3可以看出,与空白对照组相比,实验组的双螺旋含量有所提高,表明直链淀粉晶种的干预可以促进回生淀粉双螺旋的形成。其原因是酸解法制备直链淀粉晶种过程中去除大部分无定形区,从而暴露出更多的结晶区,在加至原淀粉中干预回生的过程中,可以与原淀粉中支链淀粉外支链间快速重排,从而形成更多的双螺旋结构。其中添加ACS4的回生淀粉双螺旋含量最高,其次是添加ACS25和ACS-18,最低的则为添加ACS-80的回生淀粉。这也说明ACS4结晶效果更好,其与支链淀粉外支链间重排阻力小,促进双螺旋形成效果更好。
表3 13C CP/MAS-NMR中各样品C1峰面积及
双螺旋含量
Table 3 The C1 peak area and double-helix content of
samples in 13C CP/MAS-NMR
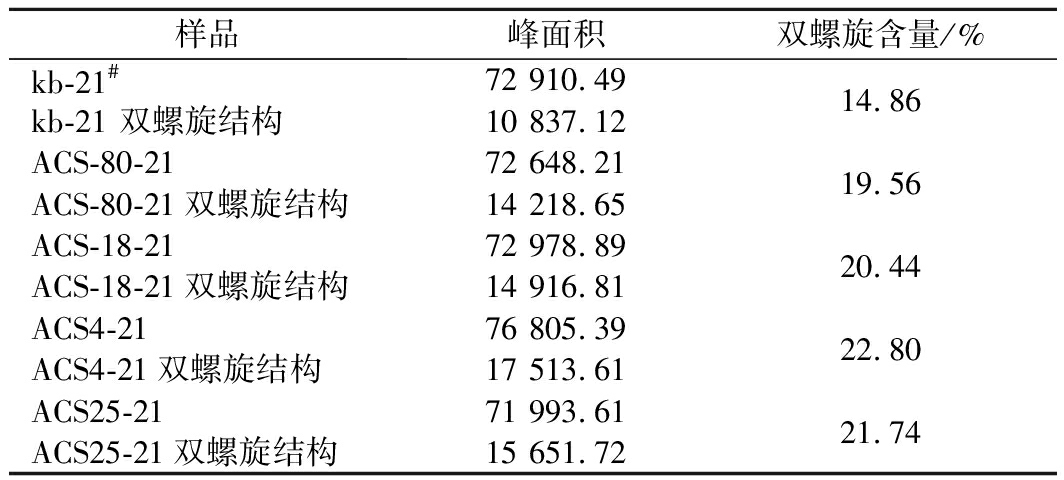
样品峰面积双螺旋含量/%kb-21#kb-21 双螺旋结构72 910.4910 837.1214.86ACS-80-21ACS-80-21双螺旋结构72 648.2114 218.6519.56ACS-18-21ACS-18-21双螺旋结构72 978.8914 916.8120.44ACS4-21ACS4-21双螺旋结构76 805.3917 513.6122.80ACS25-21ACS25-21双螺旋结构71 993.6115 651.7221.74
注:#kb-21未添加直链淀粉晶种的回生21d淀粉;ACS-80-21、ACS-18-21、ACS4-21、ACS25-21依次为加入ACS-80、ACS-18、ACS4、ACS25的回生21d淀粉
通过酸解法制备的直链淀粉晶种,粒径在200~450 nm。直链淀粉晶种导致大米淀粉长期回生过程中,回生淀粉的短程有序度提高、双螺旋含量增加,表明短期回生中形成的晶核对长期回生起促进作用。此外,淀粉短期回生阶段降温速率也会对回生晶核的形成及完善产生影响,进而影响长期回生的程度。这种晶体协同增长现象,丰富了淀粉回生共性理论。
[1] TIAN Y Q, BAI Y X, LI Y, et al. Use of the resistance effect between retrograded starch and iodine for evaluating retrogradation properties of rice starch[J]. Food Chemistry, 2011, 125(4): 1 291-1 293.
[2] 田耀旗. 淀粉回生及其控制研究[D]. 无锡:江南大学, 2011.
[3] 韩雪, 井雪萍, 张莉丽,等. 大米淀粉回生特性及控制技术研究进展. 哈尔滨工业大学学报, 2016, 48(2): 126-130.
[4] 胡冰, 徐睿, 邱立忠,等. Ⅴ-型晶种对大米淀粉回生特性的影响[J]. 食品与发酵工业, 2019, 45(12): 62-66.
[5] CHEN L, REN F, ZHANG Z, et al. Effect of pullulan on the short-term and long-term retrogradation of rice starch[J]. Carbohydrate Polymers, 2015, 115: 415-421.
[6] 程科, 许永亮, 熊善柏,等. 结晶法分离纯化大米直链淀粉[J]. 中国粮油学报, 2008, 23(2): 170-173.
[7] 陈哲敏, 胡朋兵, 孟庆强. 动态光散射及电子显微镜纳米颗粒测量方法的比较研究[J]. 光散射学报, 2015, 27(1): 54-58.
[8] MA Z, YIN X, CHANG D, et al. Long- and short-range structural characteristics of pea starch modified by autoclaving, α-amylolysis, and pullulanase debranching[J]. International Journal of Biological Macromolucules, 2018, 120: 650-656.
[9] 孙冰华. 线性糊精的制备、相行为及应用[D]. 无锡:江南大学, 2018.
[10] BAIK M Y, KIM K J, CHEON K C, et al. Recrystallization kinetics and glass transition of rice starch gel system[J]. Journal of Agricultural and Food Chemistry, 1997, 45(11): 4 242-4 248.
[11] TAN I, FLANAGAN B M,HALLEY P J, et al. A method for estimating the nature and relative proportions of amorphous, single, and double-helical components in starch granules by13C CP/MAS NMR[J]. Biomacromolecules, 2007, 8(3): 885-891.