中国白酒是以粮谷类为材料,利用酒曲为糖化发酵剂,经过发酵、蒸馏、贮存和勾调而成的具有独特风味的蒸馏酒[1]。其产生涉及微生物生长、酶产生、物质转化等过程[2]。俗话说“生香靠发酵”,微生物对白酒风味的形成至关重要。微生物的来源主要有酿酒周围环境、生产工具、原料及酒曲[3]。自19世纪60年代起,白酒工作者通过分离鉴定,将酒曲中的微生物种类及其代谢产物进行了确认[2]。从此,打开了白酒生产新世界的大门。研究者们通过化学、微生物学、生物技术等来定向调控白酒中的风味物质[4-5],不仅提高了产品的产量和质量,降低了成本,而且可以根据消费者需求生产出具有特定风味和功能的白酒。
清香型白酒的主体香是乙酸乙酯和乳酸乙酯[6],乙酸乙酯的主要合成途径是酵母菌代谢,乳酸乙酯的主要合成途径是酸和醇在酯化酶作用下的化学合成[7],两者都需要微生物的参与。研究指出,白酒发酵中,产酯能力强的酵母有汉逊酵母、毕赤酵母[8-9]、假丝酵母、酒香酵母、白地霉[10]等。因此,我们可以通过调整产酯微生物的数量和种类来生产高酯白酒。
该文使用的功能曲为高酯曲,是将能产生特定功能酶的微生物接种于曲块,来产生酿酒所需的相应酶,是微生物和酶制剂的共同体。与大曲以一定比例进行搭配,辅助清香型大曲,产生具有独特风味的高酯白酒,作为调味酒用于勾调清香型大曲白酒,使其协调、平衡。
1 材料与方法
1.1 实验时间与地点
实验时间:2019年5月—7月;实验地点:山西省某大型清香型白酒厂。
1.2 实验材料
高粱、稻壳、谷糠、清香型大曲、高酯曲,均由山东徐旭酒曲有限公司提供。
1.3 酿酒工艺操作
添加比例:大曲用量为高粱用量的10%,高酯曲用量为3%。
使用方法:先把大曲和高酯曲混合均匀,在下曲阶段一并加到曲槽中。高粱粉碎、粮食摊晾、入池温度、发酵时间等工艺操作与原工艺相同。大、二楂均连续进行6 d实验,对中间4 d进行酒醅理化跟踪。
1.4 理化性质测定
发酵前将iButton温度信息纽扣(美国DALLA公司)埋入地缸中,置于酒醅材料的中心,深度约为50 cm,用于记录发酵期间酒醅的温度变化。发酵结束后,用TEMXVIEWER软件读取数据。对入缸发酵0、7、15 d、出缸酒醅使用Infraxact Lab近红外光谱仪(丹麦FOSS公司)进行水分、淀粉和还原糖的检验。新产酒的总酸和总酯含量采用GB/T 10345—2007 白酒分析方法中的规定测定。使用Clarus 680 GC气相色谱仪(美国Perkin Elmer公司)对新产酒的挥发性组分进行检验。另外,将添加高酯曲的生产设为实验组,将不添加高酯曲的常规生产设为对照组,对照不进行酒醅跟踪,只对新产酒进行理化分析。
1.5 数据分析
各种酿酒参数的多次重复进行平均值及标准误计算。实验组(添加高酯曲实验)和对照组(不添加高酯曲的常规生产)各变量之间的显著性差异均采用单因素方差分析[11],使用SPSS 19.0和Excel 2013软件进行结果分析。用R语言中“Vegan”程序包的Adonis(analysis of variance using distance matrices)函数分析实验组和对照组之间理化性质的总体差异[12]。显著性水平设为P<0.05,当P<0.05时,两者存在显著差异;否则,两者不存在显著差异;当P<0.01时,两者存在极显著差异。用小写字母表示不同分组之间,同一性质的差异,含有相同字母的两者表示之间无显著差异;不含相同字母的两者表示之间有显著差异,没有字母表示各个对象之间均无差异。
2 结果与分析
2.1 酒醅理化性质
2.1.1 酒醅发酵品温变化
从图1中可以看出,添加高酯曲后的大楂发酵符合“前缓、中挺、后缓落”的品温变化规律[13]。
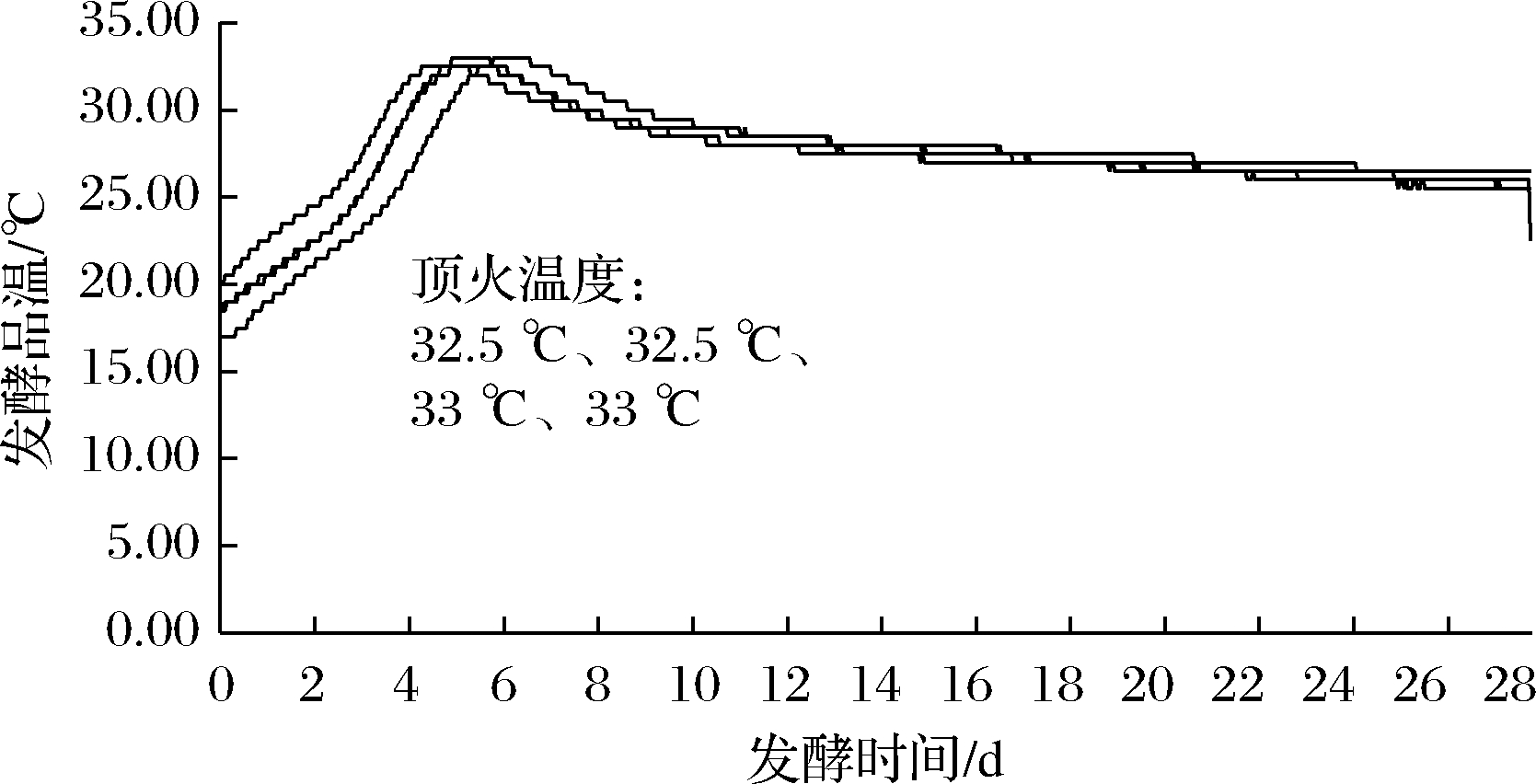
图1 大楂发酵品温变化
Fig.1 Temperature change of the first round fermentation products
注:图示为平行实验跟踪曲线(下同)
从得到的品温变化数据可以得知,大楂发酵的顶火温度为32.5~33 ℃。夏天常规生产的顶火温度一般为28~33 ℃[14]。
常规生产的二楂品温变化也呈先增加后降低的趋势。而从图2可以看出,有两次发酵在1 d时就达到顶火温度。说明添加高酯曲后,二楂前期的微生物增殖速度加快,其品温变化有别于正常生产。大楂没有此种情况是因为,大楂入温和入缸水分与二楂不同。大楂入温为13.9~15 ℃,入缸水分为52.5%~54.0%。而二楂入温为21.8~22.0 ℃,入缸水分为60.5%~61.0%。
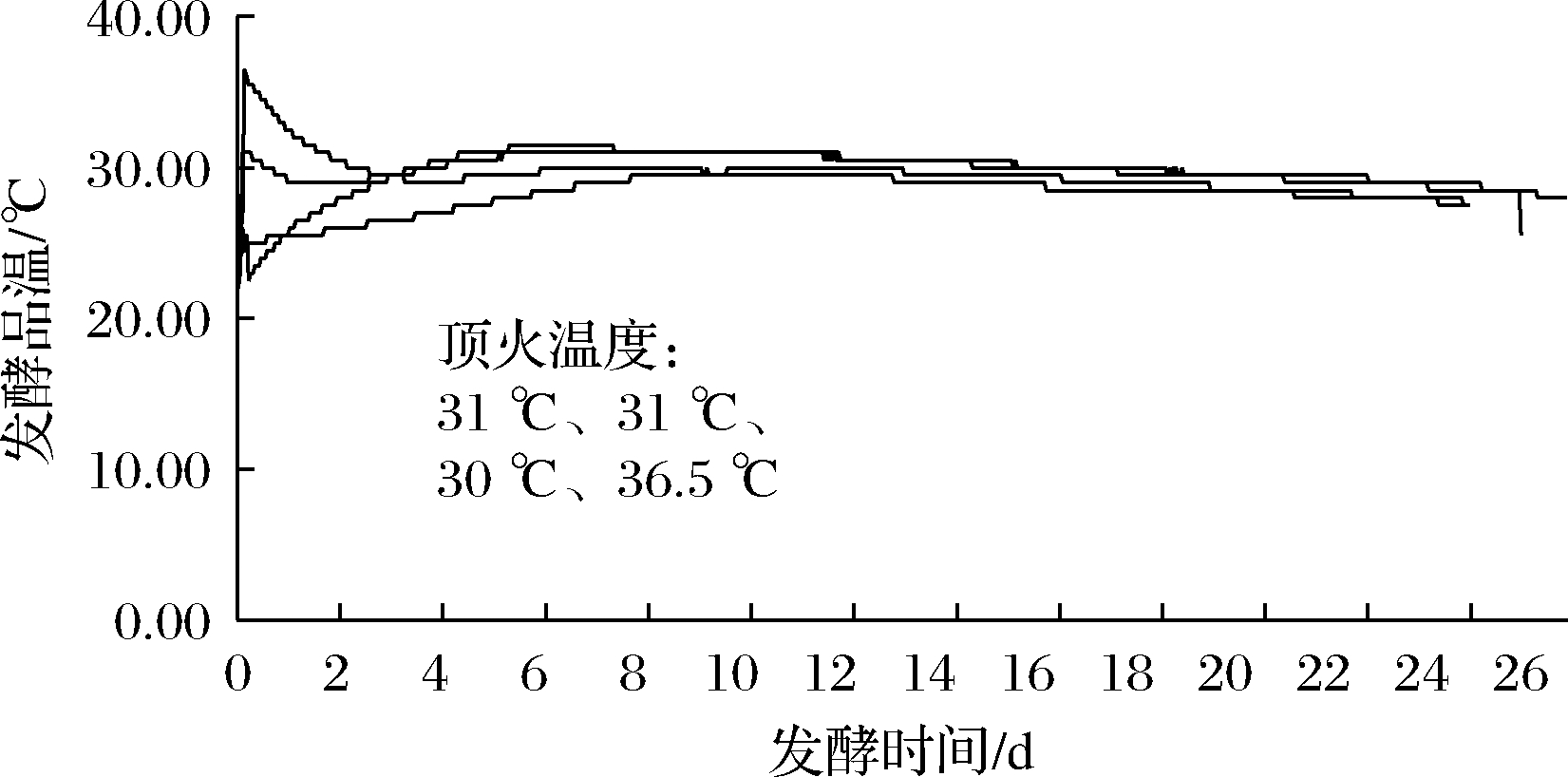
图2 二楂发酵品温变化
Fig.2 Temperature change of the second round fermentation products
2.1.2 酒醅水分变化
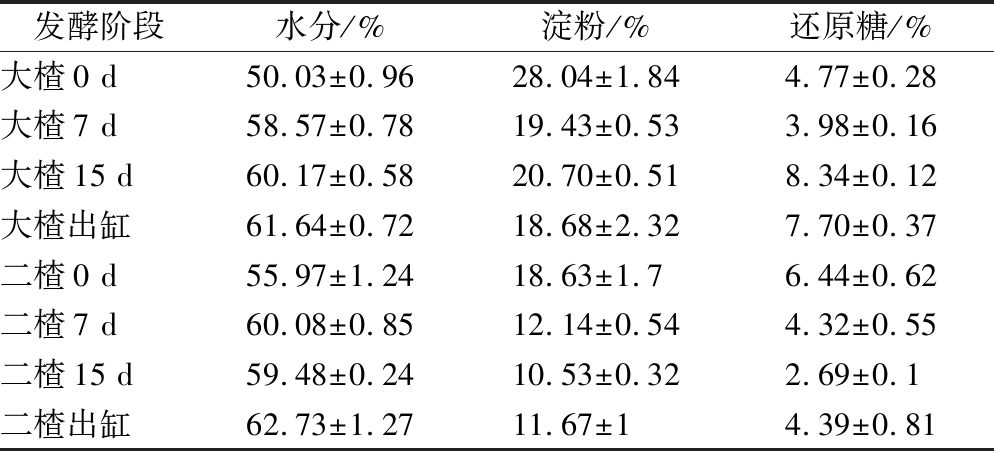
从表1可以看出,添加高酯曲后的大楂酒醅水分逐步增加,0~7 d时水分增加迅速;7 d以后增势变缓。发酵初期霉菌数量较多,主要起糖化的作用,在霉菌及糖化酶的作用下,淀粉被水解,释放出大量水分[15]。
表1 发酵期间酒醅的理化性质
Table 1 Physicochemical properties of fermented grains during fermentation
发酵阶段水分/%淀粉/%还原糖/%大楂0 d50.03±0.9628.04±1.844.77±0.28大楂7 d58.57±0.7819.43±0.533.98±0.16大楂15 d60.17±0.5820.70±0.518.34±0.12大楂出缸61.64±0.7218.68±2.327.70±0.37二楂0 d55.97±1.2418.63±1.76.44±0.62二楂7 d60.08±0.8512.14±0.544.32±0.55二楂15 d59.48±0.2410.53±0.322.69±0.1二楂出缸62.73±1.2711.67±14.39±0.81
注:表中数据为平均值±标准误
二楂酒醅在0~7 d水分增速同样较快;在7~15 d之间水分有轻微降低,这个时期主要是酒精发酵不产水,但是前期的水分有部分会渗漏到地缸底部。由于我们采集的是中上部的酒醅,所以检测到的水分减少。而大楂发酵不添加辅料,结构紧密,难以渗漏,所以大楂7~15 d没有此现象。15 d后水分开始增长。
2.1.3 酒醅淀粉变化
从表1中可以看出,0~7 d是淀粉分解的高峰期,此时氧气较多,利于糖化菌和淀粉酶发挥作用。7~15 d淀粉含量有所上升,是因为红糁进一步变软,将其中难糊化的淀粉释放出来。这时,霉菌消失、淀粉酶分解及葡萄糖产物的负反馈,导致淀粉水解速率下降。到了后期,耐酸微生物可能产生淀粉酶,使淀粉含量略有下降[15]。
二楂酒醅从入缸开始淀粉含量逐渐下降,15 d以后,检测到的淀粉含量有所提高。
2.1.4 酒醅还原糖变化
由表1可知,大楂入缸之后还原糖减少,这是因为酒精发酵消耗还原糖。7~15 d由于酒精生成的速度小于淀粉分解成还原糖的速度,所以含量增加。15 d后,由于霉菌消失,淀粉酶减少,还原糖生成量减少。但是产酒、产酸、产酯以及耐酸微生物的生长消耗还原糖,所以含量下降[15]。
15 d前,二楂还原糖一直减少。15 d后,由于耐酸微生物产生少量淀粉酶,产生少量还原糖。
2.2 新产酒理化指标
2.2.1 新产酒品评
从表2可以看到,添加高酯曲生产和正常生产的大楂新产酒在评分以及质量等级方面基本相同。
表2 大楂新产酒每日品评结果
Table 2 Daily sensory evaluation results of first round of Baijiu

大楂流酒日期评语评分均分等级实验组2019.6.11味杂632019.6.12味杂632019.6.13味杂662019.6.14带异香612019.6.15带异香、带糊杂612019.6.16带异香、带酸、带糊杂6162.5一级一级优级一级一级一级对照组2019.6.18带异香、带糊杂622019.6.19带异香612019.6.20带异香6763.3一级一级优级
添加高酯曲的二楂新产酒评分和质量等级低于正常生产产品(表3)。评语中多次提到“带异香”,说明实验组的二楂新产酒与对照组风味有所不同。
2.2.2 新产酒产量
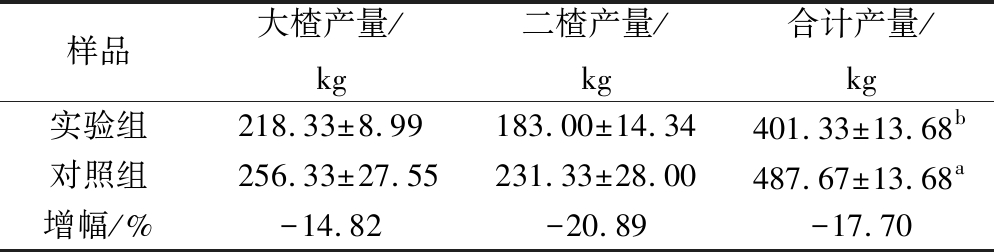
从表4看出,实验组与对照相比,大、二楂酒产量均降低,总产量显著降低了17.70%。酯的合成会利用葡萄糖,经过酵母菌代谢或醇和酸化学反应合成酯,消耗了部分葡萄糖和酒精,所以产量会有所降低[7]。
表3 二楂新产酒每日品评结果
Table 3 Daily sensory evaluation results of second round of Baijiu

二楂流酒日期评语评分均分等级实验组2019.7.9带焦、带异、带糊622019.7.9带腻、带异香632019.7.10带异香、带杂612019.7.10带异香、带杂632019.7.11带糊杂、带酸、带异香622019.7.11带异香6162一级一级一级一级一级一级对照组2019.7.13寡淡712019.7.13味杂6367优级一级
表4 大、二楂新产酒产量
Table 4 Baijiu production
样品大楂产量/kg二楂产量/kg合计产量/kg实验组218.33±8.99183.00±14.34401.33±13.68b对照组256.33±27.55231.33±28.00487.67±13.68a增幅/%-14.82-20.89-17.70
注:同一列不同小写字母表示具有显著性差异(P<0.05)
2.2.3 新产酒中的酸酯含量
从图3中可以看出,添加高酯曲显著提高了大楂新产酒中的总酸(实验组0.83 g/L,对照组0.59 g/L)和总酯(实验组7.06 g/L,对照组4.71 g/L)含量,但对二楂新产酒的总酸、总酯含量影响不大。这是因为二楂酒醅入缸时就有较高的酸度,从而影响酯化酶的活力,导致高酯曲不能充分发挥作用。

图3 新产酒的总酸、总酯含量
Fig.3 Total acid and total ester content of new Baijiu
注:不同小写字母表示具有显著性差异(P<0.05)
2.2.4 新产酒挥发性组分
首先把所有挥发性组分作为整体进行Adonis分析,不管是大楂还是二楂,组间差异的显著性均小于0.05,说明添加高酯曲对大、二楂酒的挥发性成分组成有显著影响[16]。
此外,将各个指标按物质类型对实验组和对照组进行Adonis分析(表5),实验组和对照组大楂酒之间的差异,主要是酯类和醛类,显著性分别为0.024和0.035。二楂酒的差异主要在酯类、醇类和醛类,显著性分别为0.009、0.014和0.016。
表5 实验组与对照组新产酒各类物质Adonis显著性分析
Table 5 Analysis of Adonis of various substances in the experimental and the control group

酸类酯类醇类醛类大楂0.3950.024∗0.3890.035∗二楂0.3410.009∗∗0.014∗0.016∗
注:*表示具有显著性差异(P<0.05);**表示具有极显著性差异(P<0.01)
然后,我们又对实验组和对照组的每个挥发性组分进行了比较。从表6中可以看到,实验组(3 869.44 mg/L)的乙酸乙酯含量显著高于对照组(2 702.37 mg/L),乙酸乙酯为白酒带来一种水果香,极大影响酒体的感官和风味[17]。此外,实验组的乳酸乙酯含量略高于对照组(实验组3 938.48 mg/L,对照组3 268.67 mg/L)。可见,添加高酯曲有助于清香型白酒主体香含量的提高。醇类物质中,实验组大楂酒的正戊醇、醋嗡与对照相比有显著提高。高级醇类是白酒中重要的风味物质,适量的高级醇类能赋予白酒浓郁、芬芳、醇甜等特殊感官特征[18]。实验组的3种酸类物质含量均高于对照组。适当的酸类物质能够增加白酒的后味。
添加高酯曲后,二楂酒的乙醛和乙缩醛含量均有显著提高。醛类物质增加,会增加白酒的刺激感。实验组的乙酸乙酯(实验组2 723.74 mg/L, 对照组1 794.25 mg/L)含量显著高于对照组,但是乳酸乙酯(实验组1 979.5 mg/L, 对照组3 243.48 mg/L)含量显著低于对照组。二楂中添加高酯曲只能提高乙酸乙酯含量,不能提高乳酸乙酯含量。醇类物质中,除甲醇、3-甲基-1-丁醇和醋嗡外,其他醇类均为实验组含量低于对照组。酸类物质中,异丁酸含量显著降低,乙酸和异戊酸含量提高(表6)。
3 结论与讨论
温度是判断及预测酒醅发酵状态的重要指标。在添加高酯曲后,大楂品温呈现“前缓、中挺、后缓落”的趋势,这是由于在生产中,地缸、土壤和发酵室环境形成一个有机整体,地缸与土壤的温差导致地缸热量传递到土壤,进而传递到空气,彼此进行热交换导致的[13, 19]。二楂酒醅温度变化有别于常规生产,意味着二楂微生物发酵过程发生了变化,影响酒醅的理化,最终影响新产酒的性质。从新产酒理化分析也可以看出,实验组和对照组的新产酒产量、酸酯和挥发性组分都有显著差异(表4、5、6,图3)。
表6 大楂新产酒挥发性组分
Table 6 Volatile components of first round new Baijiu
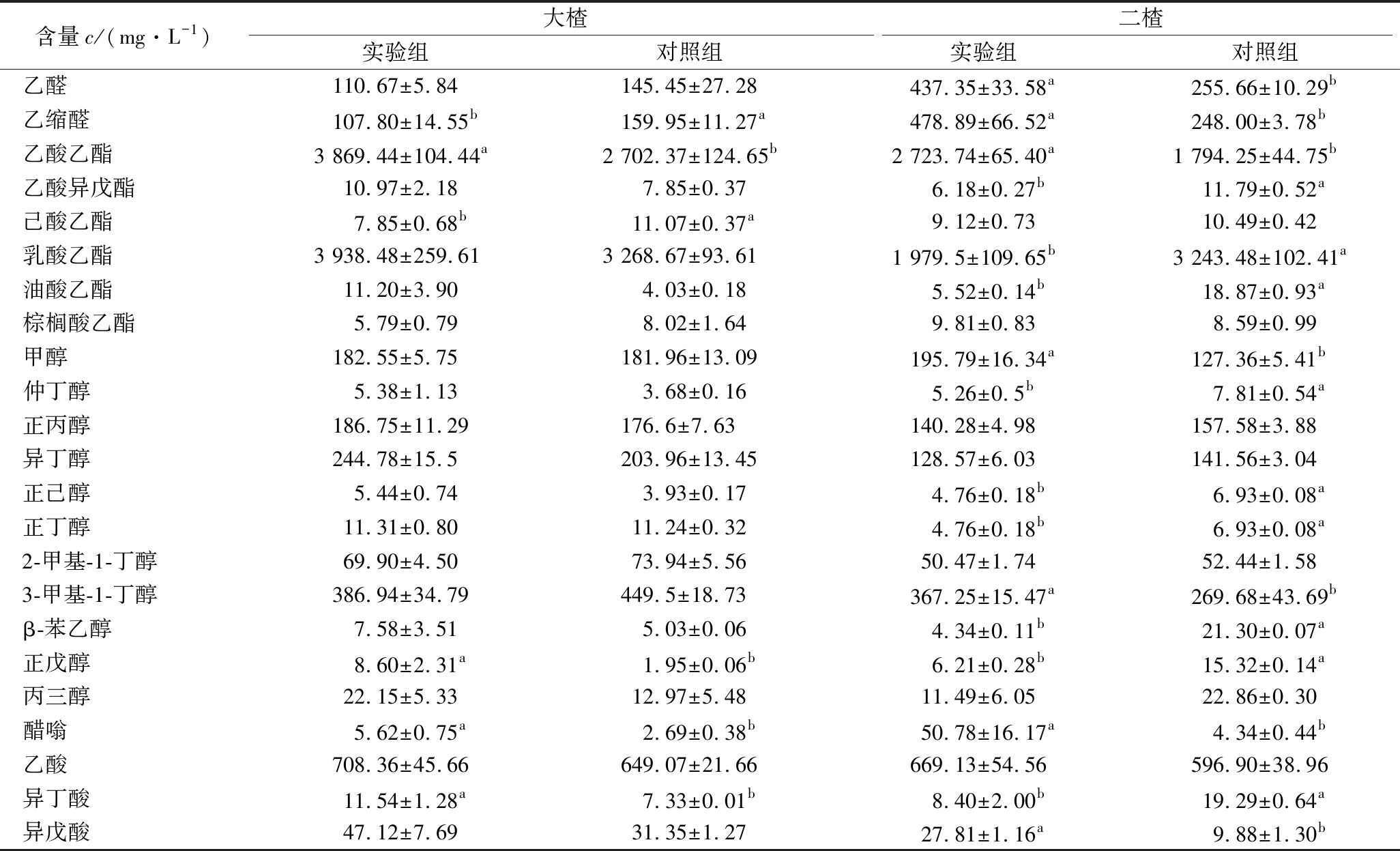
含量c/(mg·L-1)大楂二楂实验组对照组实验组对照组乙醛110.67±5.84145.45±27.28437.35±33.58a255.66±10.29b乙缩醛107.80±14.55b159.95±11.27a478.89±66.52a248.00±3.78b乙酸乙酯3 869.44±104.44a2 702.37±124.65b2 723.74±65.40a1 794.25±44.75b乙酸异戊酯10.97±2.187.85±0.376.18±0.27b11.79±0.52a己酸乙酯7.85±0.68b11.07±0.37a9.12±0.7310.49±0.42乳酸乙酯3 938.48±259.613 268.67±93.611 979.5±109.65b3 243.48±102.41a油酸乙酯11.20±3.904.03±0.185.52±0.14b18.87±0.93a棕榈酸乙酯5.79±0.798.02±1.649.81±0.838.59±0.99甲醇182.55±5.75181.96±13.09195.79±16.34a127.36±5.41b仲丁醇5.38±1.133.68±0.165.26±0.5b7.81±0.54a正丙醇186.75±11.29176.6±7.63140.28±4.98157.58±3.88异丁醇244.78±15.5203.96±13.45128.57±6.03141.56±3.04正己醇5.44±0.743.93±0.174.76±0.18b6.93±0.08a正丁醇11.31±0.8011.24±0.324.76±0.18b6.93±0.08a2-甲基-1-丁醇69.90±4.5073.94±5.5650.47±1.7452.44±1.583-甲基-1-丁醇386.94±34.79449.5±18.73367.25±15.47a269.68±43.69bβ-苯乙醇7.58±3.515.03±0.064.34±0.11b21.30±0.07a正戊醇8.60±2.31a1.95±0.06b6.21±0.28b15.32±0.14a丙三醇22.15±5.3312.97±5.4811.49±6.0522.86±0.30醋嗡5.62±0.75a2.69±0.38b50.78±16.17a4.34±0.44b乙酸708.36±45.66649.07±21.66669.13±54.56596.90±38.96异丁酸11.54±1.28a7.33±0.01b8.40±2.00b19.29±0.64a异戊酸47.12±7.6931.35±1.2727.81±1.16a9.88±1.30b
注:同一行不同小写字母表示具有显著性差异(P<0.05)
据前人的研究可知[15],本次实验和常规生产的大楂酒醅理化差异主要在淀粉和还原糖。常规生产的淀粉含量持续下降。而本次实验在7~15 d有小幅度的上升,然后才继续下降。常规生产的酒醅还原糖在10 d前呈指数增长,10 d以后呈抛物线下降。而本次实验在0~7 d还原糖有小幅度降低,7~15 d增加,15 d以后减少。
近年来,在白酒生产中应用功能曲或微生物菌剂的研究越来越多。在二锅头白酒生产中添加生香酵母,酒体中的总酯含量平均提高了0.40 g/L,乙酸乙酯的含量提高了0.30 g/L[20]。而我们的实验,大楂酒总酯提高了2.35 g/L,乙酸乙酯提高了1 167.07 mg/L。而且二楂酒乙酸乙酯也提高了929.49 mg/L。与二锅头生香酵母实验相比,我们的总酯和乙酸乙酯含量提升幅度更大。
另外,从清香型酒醅中筛选出1 株高产乙酸乙酯酵母菌,其固态发酵产物不仅有乙酸乙酯,还有苯乙醇、异戊酸、苯乙醛等[21]。同样地,本次实验添加高酯曲不仅影响了酯类物质的含量,而且多元醇和酸类物质均有提高。高酯曲的作用效果和高产乙酸乙酯酵母菌相似。
综上所述,可以得出以下结论:
1.在大曲中添加高酯曲,可以改变酒醅发酵品温、淀粉和还原糖的变化趋势,进而改变新产酒理化性质和口感风味。
2.添加高酯曲虽然在一定程度上降低了新产酒产量,但是对新产酒的总酯、总酸、乙酸乙酯含量有极大提高。而且对醇、酸、醛等物质成分也有极大改变,进一步产生风格独特的新产酒,可以用于调味。
[1] 王文晶, 朱会霞, 李泽霞, 等. 白酒固态发酵酒醅中微生物研究概况[J]. 酿酒, 2016,43(2):27-32.
[2] JIN G, ZHU Y, XU Y. Mystery behind Chinese liquor fermentation[J]. Trends in Food Science & Technology, 2017,63:18-28.
[3] WANG X, DU H, ZHANG Y, et al. Environmental microbiota drives microbial succession and metabolic profiles during Chinese liquor fermentation[J]. Applied and Environmental Microbiology, 2018,84(4):e2 317-e 2369.
[4] 徐岩, 范文来, 吴群, 等. 风味技术导向白酒酿造基础研究的进展[J]. 酿酒科技, 2012(1):17-23.
[5] 徐岩, 范文来, 王海燕, 等. 风味分析定向中国白酒技术研究的进展[J]. 酿酒科技, 2010(11):73-78.
[6] 沈正祥, 韩建书. 清香型白酒的特点优势及发展趋势[J]. 酿酒, 1997,34(3):9-11.
[7] PARK Y C, SHAFFER C E H, BENNETT G N. Microbial formation of esters[J]. Applied Microbiology and Biotechnology, 2009,85(1):13-25.
[8] TABACHNICK J, JOSLYN M A. Formation of esters of Yeast. I. The production of ethyl acetate by standing surface cultures of Hansenula anomala[J]. Journal of Bacteriology, 1953,65(1):1-9.
[9] TABACHNICK J, JOSLYN M A. Formation of esters by yeast. II. investigations with cellular suspensions of Hansenula anomala.[J]. Plant Physiology, 1953,28(4):681-692.
[10] PASTORE G M, SATO H H, YANG T S, et al. Production of fruity aroma by newly isolated yeast[J]. Biotechnology Letters, 1994,16(4):389-392.
[11] 景炬辉, 刘晋仙, 李毳, 等. 中条山铜尾矿坝面土壤细菌群落的结构特征[J]. 应用与环境生物学报, 2017,23(3):527-534.
[12] CAO M, JIA T, MI J, et al. Relative roles of niche and neutral processes on turnover of plant, fungal and bacterial communities in arid and semi-arid areas at the regional scale[J]. Basic and Applied Ecology, 2019,40:43-54.
[13] 陈丙友, 韩英, 张鑫, 等. 酒醅温度调控对清香型白酒发酵过程的影响[J]. 食品与发酵工业, 2016,42(6):44-49.
[14] 常贵明. 汾酒厂工人培训教材(酿酒岗)[M]. 汾阳:山西杏花村汾酒厂, 1993.
[15] 刘志磊. 清香型白酒发酵过程主要功能微生物代谢特性研究[D]. 郑州:河南工业大学, 2011.
[16] ZHAO P, LIU J, JIA T, et al. Environmental filtering drives bacterial community structure and function in a subalpine area of northern China[J]. Journal of Basic Microbiology, 2019,59(3):337-347.
[17] DONG J, WANG P, FU X, et al. Increase ethyl acetate production in Saccharomyces cerevisiae by genetic engineering of ethyl acetate metabolic pathway[J]. Journal of Industrial Microbiology & Biotechnology, 2019,46(6):801-808.
[18] 纪媚, 邓楠, 邱阳, 等. 风味导向的白酒功能微生物组合发酵[J]. 食品与发酵工业, 2018,44(11):69-75.
[19] 沈怡方. 白酒生产技术大全[M]. 北京: 中国轻工业出版社, 1998.
[20] 皮聪. 功能微生物在发酵中的应用[J]. 酿酒科技, 2014(2):112.
[21] 程伟, 彭兵, 汪焰胜, 等. 清香型酒醅中一株产乙酸乙酯酵母菌的筛选及其应用性能分析[J]. 酿酒, 2018,45(5):43-47.