表1 急性毒性实验结果
Table 1 Results of the acute toxicity test
性别剂量/[g·(kg·BW)-1]动物数/只体重/g初始末期动物死亡数/只MTD/[g·(kg·BW)-1]雄性20.01019.24±0.6132.86±0.920>20.0雌性20.01019.62±0.6429.75±0.950>20.0
L-精氨酸是一种非必需碱性氨基酸,主要来源于饮食、蛋白质降解和自身合成,在体内合成速度较慢,具有增强免疫力、保护胃黏膜、促进蛋白合成等生理功能[1-3],但对于婴幼儿为必需氨基酸,可以起到一定的解毒作用。L-精氨酸增强免疫力的重要作用机制为精氨酸—一氧化氮(nitric oxide, NO)调控模式。L-精氨酸经一氧化氮合成酶(nitric oxide synthase, NOS)催化生成具有生物活性的NO。NO在生物体内承担着重要的生物功能,包括抗炎、降血压、舒张血管等[4-7]。
天然抗氧化物剂含有大量能清除过量自由基的抗氧化成分,如山楂提取物、知母提取物、虾青素等,具有辅助保护心血管、调节免疫、抗氧化、降血糖等功能[8-9]。山楂提取物含有黄酮、原花青素、三萜酸等抗氧化物质,具有保护心血管、抗氧化、抗炎等作用[10],知母宁具有清热泻火,滋阴润燥,退热消炎,抑菌杀菌,降血糖等功能[11-12]。虾青素属类胡萝卜素,是存在于鱼、虾和藻类中的一种强抗氧化剂,其抗氧化活性高于β-胡萝卜素的10倍、VE的100倍[13]。
该研究重点开展了含L-精氨酸和抗氧化物质(山楂提取物、知母提取物和虾青素)组方的安全性毒理学评价,以期为其临床应用及保健食品研发提供毒理学方面的科学依据。
组方样品由L-精氨酸(L-Arg)、山楂提取物、知母提取物和虾青素为原料,按质量比1∶1∶2∶2制成。敌克松(dexon),上海晶纯试剂有限公司;2-氨基芴,上海晶纯试剂有限公司;1,8-二羟基蒽醌,Sigma-Aldrich公司;美国胎牛血清,浙江天航科技有限公司;环磷酰胺,Sigma-Aldrich公司;Giemsa染料,salarbio公司;甲醇,天津市康科德技术有限公司;羧甲基纤维素钠,国药集团化学试剂有限公司。
BP211D电子天平、BS323S电子天平、BSA42002S电子天平,德国Sartorius公司;BX51生物显微镜,Olympus公司; BSC-1360ⅡA2生物安全柜,北京中联哈尔仪器有限公司;ADVI2120i血液分析仪,西门子公司。
SPF级雄性ICR小鼠、SD大鼠,济南朋悦实验动物繁育有限公司,饲养于屏障级动物房,温度20~26 ℃,相对湿度40%~70%,照明时间12 h。设毒理组和对照实验组,分溶剂对照组和样品低、中、高3个剂量组,每组10只动物。
1.4.1 急性毒性试验
L-精氨酸和天然抗氧化剂组方样品,按相当于人体剂量的750倍,即20.0 g/(kg·BW),连续经口灌胃14 d。记录动物中毒表现和死亡情况,试验结束后进行剖检并记录大体解剖结果。
1.4.2 Ames试验
设8、40、200、1 000和5 000 mg/皿,5个剂量,称取1.25 g样品,加灭菌注射用水至25 mL,混匀,在0.055 MPa条件下灭菌20 min,4 ℃保存,临用时,加灭菌注射用水按1∶4体积比依次稀释成50 000 (不稀释)、10 000、2 000、400、80 mg/mL,试验时,每皿加入各个试剂组样品0.1 mL。
1.4.3 骨髓细胞微核试验
试验设样品组、溶剂对照组和阳性对照组,L-精氨酸和天然抗氧化剂组方样品组按低、中、高3个剂量,分别为2.5、5.0和10.0 g/(kg·BW),用5 g/L羧甲基纤维素钠(sodium carboxymethyl cellulose,CMC-Na)溶液配制成0.125、0.25和0.5 g/mL混悬液。阳性对照组经灌胃给予2.0 mg/mL的环磷酰胺溶液,总剂量为40.0 mg/(kg·BW)。溶剂对照组给予0.5% CMC-Na溶液。经口灌胃容积均为20 mL/(kg·BW)。
1.4.4 小鼠精子畸形试验
试验设样品组、溶剂对照组和阳性对照组,L-精氨酸和天然抗氧化剂组方样品组按低、中、高3个剂量,分别为2.5、5.0和10.0 g/(kg·BW),用5 g/L CMC-Na溶液配制成0.125、0.25和0.5 g/mL混悬液。阳性对照组经灌胃给予2.0 mg/mL的环磷酰胺溶液,总剂量为40.0 mg/(kg·BW)。溶剂对照组给予5 g/L CMC-Na溶液。经口灌胃,给予容积均为20 mL/(kg·BW)。连续给予5 d,首次给予后第35天处死小鼠。
1.4.5 大鼠喂养试验
30 d喂养SD大鼠组方样品,以0.67、1.33和2.67 g/(kg·BW)(相当人体推荐量的25、50和100倍) 3个剂量掺入饲料,大鼠摄入饲养量按10 g/(100 g·BW)计,掺入质量分数分别为0.67%、1.33%和2.67%,采用逐级放大法将样品掺入饲料中。空白对照组喂食不添加组方样品的普通饲料。
1.5.1 急性毒性试验
小鼠检疫合格后,取试验小鼠20只,雌雄各半,禁食不禁水16 h后,经灌胃给予质量浓度为0.5 g/mL试验样品20 mL/(kg·BW),1 d内给予2次,2次间隔时间4 h,每天观察1次,观察14 d,记录动物中毒表现及死亡情况。试验结束后进行剖检并记录大体解剖结果。
1.5.2 Ames试验
采用平板掺入法,将冷冻保存的实验菌株TA97、TA98、TA100、TA102分别接种于营养肉汤培养基10 mL, 37 ℃振荡(100次/min)培养10 h。将含组氨酸(0.5 mmol/L)、生物素(0.5 mmol/L)的顶层培养基2 mL分装于试管中,50 ℃水浴保温,然后每管依次加入0.1 mL实验菌株液,0.1 mL样品溶液和S9混合液0.5 mL(需代谢活化时),充分混匀,迅速倾入底层琼脂板上,转动平板,使之分布均匀。水平放置待冷凝固化后,倒置于37 ℃培养箱孵育48 h,计数每皿回变菌落数。每个剂量均做3个平行板,同时设空白对照组、溶剂对照组和阳性对照组。
1.5.3 小鼠骨髓细胞微核试验
采用ICR小鼠50只,雌雄各半,雄性体重25.68~28.91 g,雌性体重26.24~29.12 g。实验设置对照组和阳性对照组。样品组设低、中、高3个剂量,经口灌胃,采用30 h/2次给予法,2次间隔24 h,第2次给予后6 h取材。首末给予均称动物重量并记录。动物颈椎脱臼法处死小鼠,取胸骨,用止血钳挤出骨髓液与载玻片一端的胎牛血清混匀,常规涂片。空气干燥后,用甲醇固定10 min。将固定好的涂片放入Giemsa应用液中,染色10 min,用水轻轻冲洗,凉干。在光学显微镜下,观察200个嗜多染红细胞(polychromatic erythrocyte,PCE),同时计数正染红细胞(normochromatic erythrocyte,NCE),计算观察PCE/NCE比值,每只动物计数1 000个嗜多染红细胞。观察含有微核的嗜多染红细胞数,微核率以千分率表示。
1.5.4 小鼠精子畸形试验
采用ICR小鼠25只,雄性,体重25.68~28.91 g。实验设置对照组和阳性对照组。样品组设低、中、高3个剂量,经口灌胃,连续给予5 d,首次给予后第35 d处死小鼠。颈椎脱臼法处死小鼠,取出两侧附睾,放入盛有约1 mL生理盐水的小烧杯中,用眼科剪纵向剪1~2刀,静止3 min,轻轻摇动。用4层擦镜纸过滤,滤液涂片。空气干燥后,用甲醇固定5 min,晾干后用1%伊红染色1 h,用水轻轻冲洗,干燥。用低倍镜下找到背景清晰,精子重叠较少的部位,用高倍镜检查精子的形态。精子畸形按照无钩、香蕉形、胖头、无定型、双头、双尾、尾折叠进行记录。每只动物检查1000个精子。记录畸变的类型和数量,计算精子畸形率。
1.5.5 大鼠喂养试验
检疫合格后,取试验动物L-精氨酸和天然抗氧化剂组方对人体推荐量为l.6 g/60 (kg·BW)。动物受试物毒理实验剂量按人体推荐的25、50和100倍3个剂量掺入饲料,饲喂SD大鼠30 d。第31天后,在禁食16 h称重。腹腔注射戊巴比妥钠麻醉,处死动物,取肝、脾、肾、睾丸、卵巢等脏器和胸腺称重,计算脏/体比值;将肝、脾、肾、睾丸、卵巢等脏器固定保存好,并进行病理检查。取血进行血液指标测定包括血红蛋白(hemoglobin,HGB)浓度、红细胞(red blood cell,RBC)数、白细胞(white blood cell,WBC)数、嗜中性粒细胞(neutrophils,NEU)百分率、淋巴细胞(lymphocyte,LYM)百分率、单核细胞(monocyte,MONO)百分率、酸性粒细胞(eosinophil,EOS)百分率和嗜碱性粒细胞(basophils,BASO)百分率;以血清生化指标测定包括谷丙转氨酶(alanine aminotransferase,ALT)、谷草转氨酶(aspartate transaminase,AST)、总蛋白(total protein,TP)、白蛋白(albumin,ALB)、血糖(glucose,GLU)、肌酐(creatinine,CREA)、尿素(urea,UREA)、总胆固醇(total cholesterol,TCHO)和甘油三酯(triglyceride,TG)。
采用SPSS 19.0统计软件以X2检验进行数据处理,P<0.05表示差异显著,P<0.01表示差异极显著。
根据《保健食品检验与评价技术规范》(2003年版)[14],每个剂量组与溶剂对照组分别进行比较,畸变率为溶剂对照组的2倍及以上有统计学差异,并有剂量反应关系,可判断为实验结果阳性。
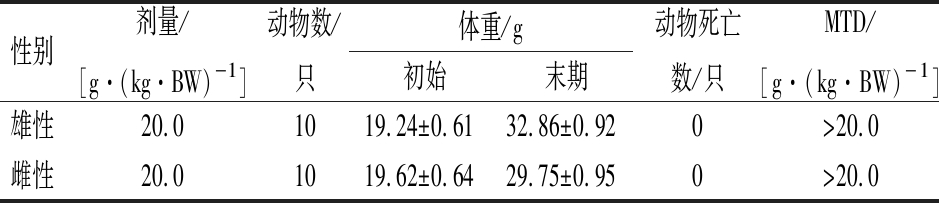
小鼠在观察期内未出现死亡及中毒状况,该组方样品急性经口小鼠试验最大耐受剂量(maximum tolerated doses,MTD)均>20.0 g/(kg·BW)(表1),结果显示该组方属无毒级。
表1 急性毒性实验结果
Table 1 Results of the acute toxicity test

性别剂量/[g·(kg·BW)-1]动物数/只体重/g初始末期动物死亡数/只MTD/[g·(kg·BW)-1]雄性20.01019.24±0.6132.86±0.920>20.0雌性20.01019.62±0.6429.75±0.950>20.0
注:表中结果![]() (下同)
(下同)
如表2所示,2次试验中组方各剂量在加和不加S9条件下各菌株回变菌落数均未超过自发回变菌落数的2倍,各剂量组间亦无剂量反应关系。因此,在加和不加S9的条件下,组方对鼠伤寒沙门氏菌TA97、TA98、TA100、TA102共4株菌株均未呈现遗传毒性;即在本试验条件下,在加与不加代谢活化系统的情况下,该组方对鼠伤寒沙门氏菌为致突变阴性。
表2 Ames试验结果
Table 2 Results of Ames test

组别剂量/(μg·皿-1)TA97TA98TA100TA102+S9-S9+S9-S9+S9-S9+S9-S95 000131±13105±1231±629±2139±6139±8276±8269±101 000136±13123±1234±534±4145±14147±10279±15276±12样品200142±11129±1135±631±2150±5142±12289±14283±1140139±9125±1334±432±2142±14147±7283±14288±168135±10131±936±433±2148±6144±8295±14284±11溶剂对照-128±6118±735±232±3142±10140±11281±4283±7空白对照-132±6121±737±331±5141±6139±9279±6274±82-氨基芴(10)2 016±99-2 403±62-1 045±112---阳性对照1,8-二羟基蒽醌(50)------933±81-敌克松(50)-2 192±254-2 445±85-996±46--MMC(0.5)-------1 847±70
注:-表示无(下同)
如表3所示,组方各剂量PCE/NCE比值未少于溶剂对照组的20%,表明该组方在实验剂量下无细胞毒性。环磷酰胺阳性对照组与溶剂对照组相比,微核率有较显著性差异(P<0.01), 而组方各剂量组微核率与溶剂对照组相比无显著性差异(P>0.05)。因此,在该实验条件下,该组方不会引起小鼠的骨髓嗜多染红细胞突变作用。
表3 骨髓细胞微核试验结果
Table 3 Results of micronucleus rate in bone marrow
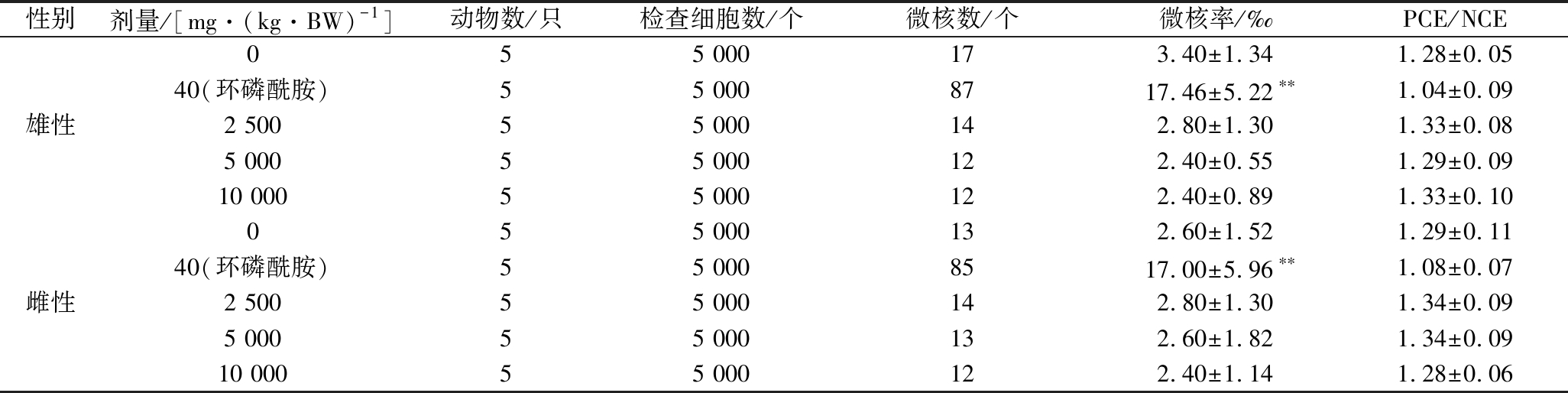
性别剂量/[mg·(kg·BW)-1]动物数/只检查细胞数/个微核数/个微核率/‰PCE/NCE055 000173.40±1.341.28±0.0540(环磷酰胺)55 0008717.46±5.22∗∗1.04±0.09雄性2 50055 000142.80±1.301.33±0.085 00055 000122.40±0.551.29±0.0910 00055 000122.40±0.891.33±0.10055 000132.60±1.521.29±0.1140(环磷酰胺)55 0008517.00±5.96∗∗1.08±0.07雌性2 50055 000142.80±1.301.34±0.095 00055 000132.60±1.821.34±0.0910 00055 000122.40±1.141.28±0.06
注:**表示与溶剂对照组比较,P<0.01(双侧t检验)(下同)
如表4所示,组方各剂量组小鼠精子畸形率与溶剂对照组相比,无显著性差异(P>0.05)。环磷酰胺阳性对照组与溶剂对照组相比,有较显著性差异(P<0.01),因此,在该实验条件下,该组方对小鼠精子畸形试验结果为阴性。
表4 小鼠精子畸形试验结果
Table 4 Results of sperm abnormality test in mice
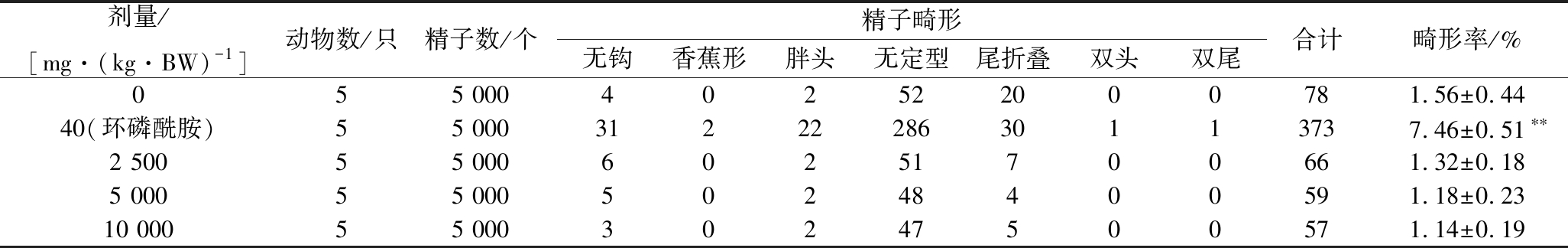
剂量/[mg·(kg·BW)-1]动物数/只精子数/个精子畸形无钩香蕉形胖头无定型尾折叠双头双尾合计畸形率/%055 000402522000781.56±0.4440(环磷酰胺)55 0003122228630113737.46±0.51∗∗2 50055 00060251700661.32±0.185 00055 00050248400591.18±0.2310 00055 00030247500571.14±0.19
L-精氨酸和天然抗氧化剂组方按人体推荐量的25、50和100倍3个剂量掺入饲料,饲喂SD大鼠30 d,未发现与对照有显著改变。30 d后处死动物,取肝、脾、肾、睾丸、卵巢等脏器和胸腺称重。如表5和表6所示,3个剂量组动物的体重以及脏器/体重比值与对照组动物相比均无显著性差异。对肝、脾、肾、睾丸和卵巢等脏器进行病理检查也未发现显著的病理变化。对血液学检查结果和血清生化指标检查结果如表7和表8所示。与对照组比较,血清生化可见雄性动物低、高剂量组ALB显著降低,P<0.01和P<0.05;可见雄性动物低、中、高剂量组CREA显著降低,P<0.01;可见雌性动物低、高剂量组ALB显著降低,P<0.01和P<0.05;上述指标均在本单位正常值范围内,可认为不存在生物学意义。其他各项指标均与对照组没有明显不同。综上,该组方喂养30 d各项观察指标未见明显毒性作用。
表5 大鼠体重
Table 5 Body weight of the mice
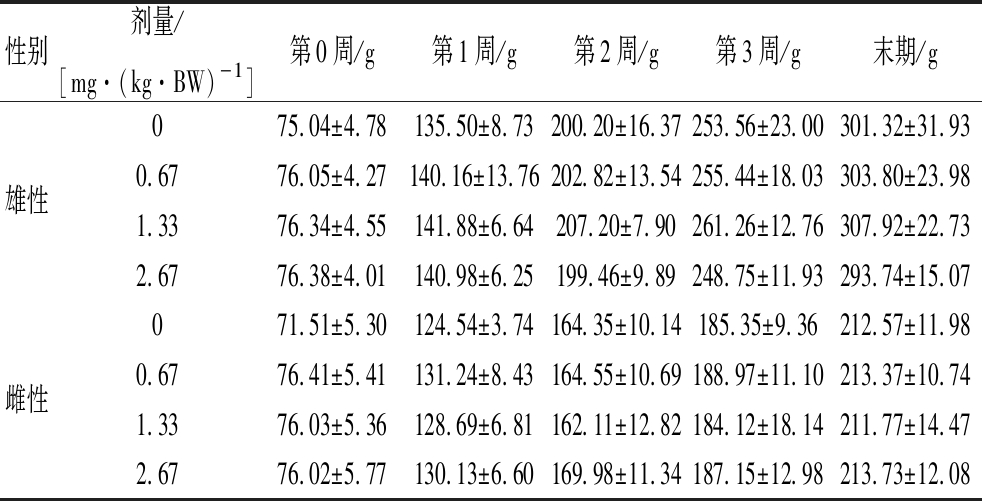
性别剂量/[mg·(kg·BW)-1]第0周/g第1周/g第2周/g第3周/g末期/g075.04±4.78135.50±8.73200.20±16.37253.56±23.00301.32±31.93雄性0.6776.05±4.27140.16±13.76202.82±13.54255.44±18.03303.80±23.981.3376.34±4.55141.88±6.64207.20±7.90261.26±12.76307.92±22.732.6776.38±4.01140.98±6.25199.46±9.89248.75±11.93293.74±15.07071.51±5.30124.54±3.74164.35±10.14185.35±9.36212.57±11.98雌性0.6776.41±5.41131.24±8.43164.55±10.69188.97±11.10213.37±10.741.3376.03±5.36128.69±6.81162.11±12.82184.12±18.14211.77±14.472.6776.02±5.77130.13±6.60169.98±11.34187.15±12.98213.73±12.08
表6 大鼠脏器/体重比值
Table 6 Organ/body weight of the mice
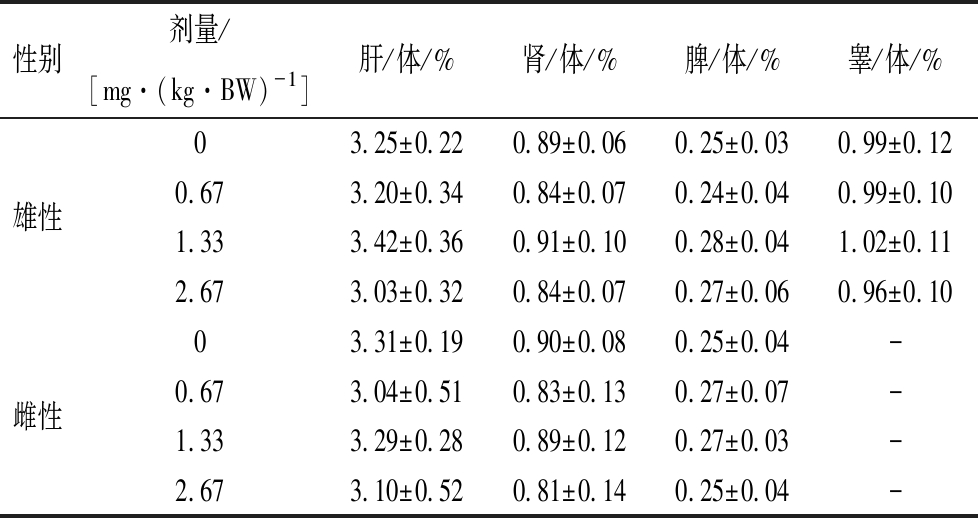
性别剂量/[mg·(kg·BW)-1]肝/体/%肾/体/%脾/体/%睾/体/%03.25±0.220.89±0.060.25±0.030.99±0.12雄性0.673.20±0.340.84±0.070.24±0.040.99±0.101.333.42±0.360.91±0.100.28±0.041.02±0.112.673.03±0.320.84±0.070.27±0.060.96±0.1003.31±0.190.90±0.080.25±0.04-雌性0.673.04±0.510.83±0.130.27±0.07-1.333.29±0.280.89±0.120.27±0.03-2.673.10±0.520.81±0.140.25±0.04-
L-精氨酸具有调节免疫、促进蛋白质合成、保护胃黏膜等多种独特的生理和药理功能,在临床营养治疗中发挥着重要作用[1-3]。山楂提取物、知母提取物、虾青素等天然抗氧化物剂,含有大量能清除过量自由基的抗氧化成分,具有辅助保护心血管、降血压、降血脂、降血糖以及抑制神经退行性疾病等功能[15-16]。
本组方由L-精氨酸和天然抗氧化物质(山楂提取物、知母提取物和虾青素)组成,本实验按《保健食品检验与评价技术规范》(2003年版)对该组方的毒理学进行评价。研究结果显示,该组方对小鼠急性毒性试验中的MTD值>20.0 g/(kg·BW),依据急性毒性分级标准,该组方属于无毒级。小鼠Aems试验、小鼠骨髓细胞微核试验、小鼠精子畸形试验均未发现该组方样品有致突变作用。按人体推荐量的25、 50和100倍3个剂量,饲喂SD大鼠30 d,各组动物生长发育良好,体重、脏器重量、脏器系数、血液学检查结果和血清生化指标等均未见异常。
表7 大鼠血液学检查结果
Table 7 Results of hematological indices in mice
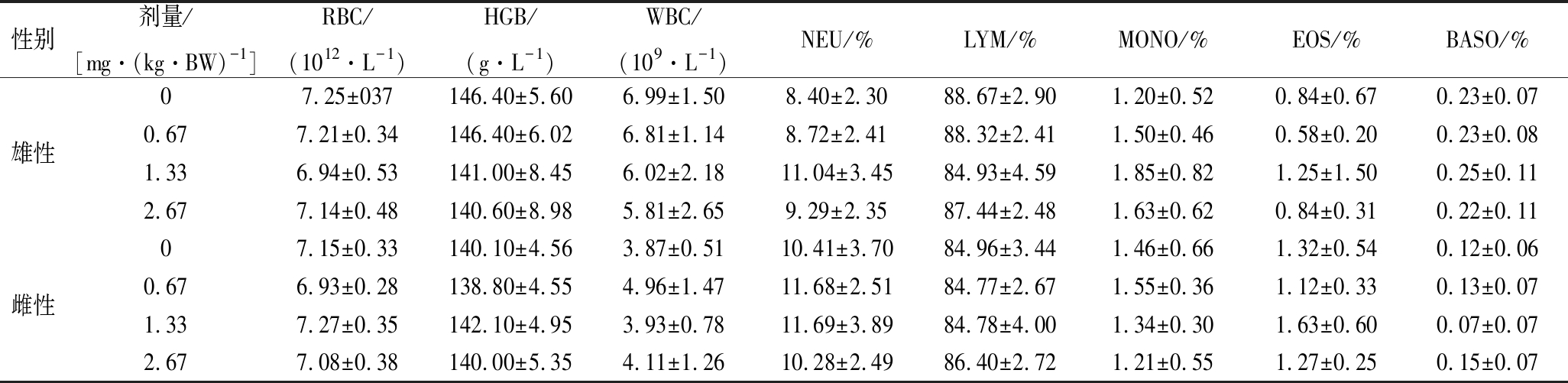
性别剂量/[mg·(kg·BW)-1]RBC/(1012·L-1)HGB/(g·L-1)WBC/(109·L-1)NEU/%LYM/%MONO/%EOS/%BASO/%07.25±037146.40±5.606.99±1.508.40±2.3088.67±2.901.20±0.520.84±0.670.23±0.07雄性0.677.21±0.34146.40±6.026.81±1.148.72±2.4188.32±2.411.50±0.460.58±0.200.23±0.081.336.94±0.53141.00±8.456.02±2.1811.04±3.4584.93±4.591.85±0.821.25±1.500.25±0.112.677.14±0.48140.60±8.985.81±2.659.29±2.3587.44±2.481.63±0.620.84±0.310.22±0.1107.15±0.33140.10±4.563.87±0.5110.41±3.7084.96±3.441.46±0.661.32±0.540.12±0.06雌性0.676.93±0.28138.80±4.554.96±1.4711.68±2.5184.77±2.671.55±0.361.12±0.330.13±0.071.337.27±0.35142.10±4.953.93±0.7811.69±3.8984.78±4.001.34±0.301.63±0.600.07±0.072.677.08±0.38140.00±5.354.11±1.2610.28±2.4986.40±2.721.21±0.551.27±0.250.15±0.07
表8 大鼠血清生化指标检查结果
Table 8 Results of serum biochemical indices in mice
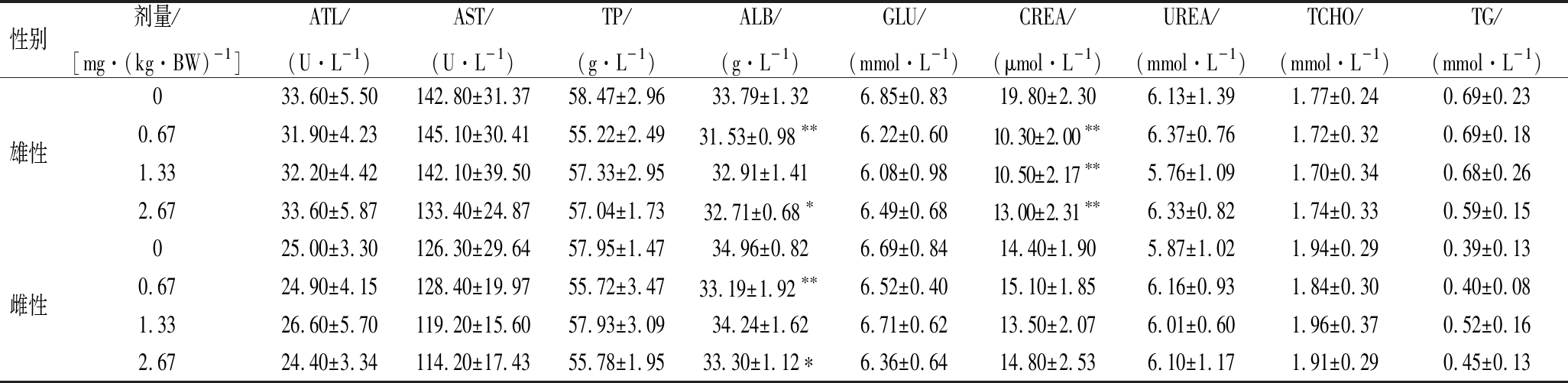
性别剂量/[mg·(kg·BW)-1]ATL/(U·L-1)AST/(U·L-1)TP/(g·L-1)ALB/(g·L-1)GLU/(mmol·L-1)CREA/(μmol·L-1)UREA/(mmol·L-1)TCHO/(mmol·L-1)TG/(mmol·L-1)033.60±5.50142.80±31.3758.47±2.9633.79±1.326.85±0.8319.80±2.306.13±1.391.77±0.240.69±0.23雄性0.6731.90±4.23145.10±30.4155.22±2.4931.53±0.98∗∗6.22±0.6010.30±2.00∗∗6.37±0.761.72±0.320.69±0.181.3332.20±4.42142.10±39.5057.33±2.9532.91±1.416.08±0.9810.50±2.17∗∗5.76±1.091.70±0.340.68±0.262.6733.60±5.87133.40±24.8757.04±1.7332.71±0.68∗6.49±0.6813.00±2.31∗∗6.33±0.821.74±0.330.59±0.15025.00±3.30126.30±29.6457.95±1.4734.96±0.826.69±0.8414.40±1.905.87±1.021.94±0.290.39±0.13雌性0.6724.90±4.15128.40±19.9755.72±3.4733.19±1.92∗∗6.52±0.4015.10±1.856.16±0.931.84±0.300.40±0.081.3326.60±5.70119.20±15.6057.93±3.0934.24±1.626.71±0.6213.50±2.076.01±0.601.96±0.370.52±0.162.6724.40±3.34114.20±17.4355.78±1.9533.30±1.12∗6.36±0.6414.80±2.536.10±1.171.91±0.290.45±0.13
综上,本实验结果表明该组方是安全的,为其进一步开发健康食品及药品提供了毒理学方面的科学依据。
[1] GEIGER R, RIECKMANN J C, WOLF T, et al. L-arginine modulates T cell metabolism and enhances survival and anti-tumor activity[J]. Cell, 2016, 167(3):829-842.
[2] XIONG L,TENG J L,BOTELHO M G,et al. Arginine metabolism in bacterial pathogenesis and cancer therapy[J].Int J Mol Sci,2016,17(3):363.
[3] 欧阳暂,姜雅慧,张剑波,等.精氨酸强化的免疫营养支持对胃癌患者术后免疫功能影响的Meta分析[J].循证医学,2017,17(6):350-360.
[4] PALMER R M, FERRIGE A G, MONCADA S, Nitric oxide release accounts for the biological activity of endothelium-derived relaxing factor. Nature, 1987,327(6 122): 524-526.
[5] FURCHGOTT R F, VANHOUTTE P M. Endothelium-derived relaxing and contracting factors[J]. The FASEB J, 1989, 3(9): 2 007-2 018.
[6] 赵保路.一氧化氮自由基[M].北京:科学出版社,2008.
[7] 赵保路.一氧化氮自由基生物学和医学[M].北京:科学出版社,2016.
[8] SHEN G, LI M, XIN W J, et al. Effects of Chinonin on nitric oxide free radical, myocardial damage and arrhythmia in ischemia-reperfusion injury in vivo[J]. Appl Magn Reson,2000,19:9-19.
[9] ZHANG D L, ZHANG Y T,YIN J J, et al. Oral administration of Crataegus extraction protects against ischemia/reperfusion brain damage in the Mongolian gerbils[J]. J Neur Chem,2004,90(1):211-219.
[10] WEIHMAYR T, EMST E. Therapeutic effectiveness of crataegus[J]. For-schritte der Medizin, 1996, 114(1-2): 27-29.
[11] WALKER A F, MARAKIS G, MORRIS A P, et al, Promising hypotensive effect of hawthorn extract: A randomized double-blind pilot study of mild, essential hypertension[J]. Phytotherapy Research, Ptr, 2002, 16(1): 48-54.
[12] PETKOV E, NIKOLOV N, UZUNOV P.Inhibitory effect of some flavonoids and falvonoid mixtures on cyclic amp phosphodiesterase activity of rat heart[J]. Planta Med, 1981, 43(10):183-186.
[13] HIGUERA-CIAPARA I, FELIX-VALENZUELA L, GOYCOOLEA F. Astaxanthin: A review of its chemistry and applications[J]. Crit Rev Food Sci Nutr, 2006,46(2):185-196.
[14] 中华人民共和国卫生部.保健食品检验与评价技术规范 (2003年版)[M].北京:中国标准出版社,2003.
[15] SHEN J G, GUO X S, JIANG B, et al. Chinonin, a novel drug against cardiomyocyte apoptosis induced by hypoxia and reoxygenation [J]. Biochim Biophyscs Acta, 2 000(1 500):217-226.
[16] CHEN M, ZHANG J, LI C, et al. Preventive and therapeutic effects of nitric oxide and natural antioxidants on Alzheimer′s disease[J]. Hans Journal of Food and Nutrition Science, 2016, 5: 105-113.