“米酸汤”是贵州苗、侗民族的传统食品,可直接作为饮料,加入火锅中可以改善适口性和风味[1]。目前大多数研究停留在米酸汤的初级配方上,存在发酵耗时长、产酸低,质量不稳定等诸多弊端[2-5]。因此,研制出发酵周期短、产酸高、质量稳定的米酸汤对丰富调味品品种、增加其营养价值,同时改善米酸汤单一口味和提高产品附加值等具有重要意义[6-8]。
食品在贮藏过程中的品质变化可通过化学动力学模型表达[9]。李明[10]研究了果汁型豆酸汤饮料稳定性动力学模型;RUSTOM等[11]研究了超高温灭菌花生奶贮藏期品质变化和贮存稳定性的关系。赵慧[12]研究了复合菌发酵米乳饮料的配方优化及其贮藏品质变化;目前虽有少部分对米酸汤或米乳饮料在贮藏期间品质变化的研究,但其贮存稳定性的预测研究鲜见报道。
本文以米浆糖化液为原料,鼠李糖乳杆菌、玉米乳杆菌、植物乳杆菌为混合发酵菌,先通过单因素实验和响应面分析法,确定米酸汤发酵的最佳工艺条件,为生产设计提供了良好的技术支持,有一定实用价值。再以自制米酸汤为研究对象,采用贮藏期加速实验的方法,研究在不同温度条件下,米酸汤在贮藏过程中理化指标与感官评价之间的相关性、理化指标与贮藏时间之间的关系,获得其化学反应动力学和热力学参数,并建立化学动力学和热力学快速预测模型,为米酸汤稳定性快速预测提供科学依据。
鼠李糖乳杆菌(Lactobacillus rhamnosus strain)、玉米乳杆菌(Lactobacillus zeae strain)、植物乳杆菌(Lactobacillus plantarum strain),湖南省果蔬清洁加工重点实验室提供;粳米、糯米,市售;液化酶(酶活4 000 U/g)、糖化酶(酶活120 000 U/g),百斯杰公司提供;其他化学试剂均为分析纯。
SW-CJ-2FD超净工作台,康恒仪器公司;GI54DWS灭菌锅,长沙艾迪生物科技有限公司;DH-360恒温培养箱、VELOCITY18R台式冷冻离心机,北京海天友臣科技有限公司;CR-400色彩色差计,常州三丰仪器科技有限公司;NDJ-5S旋转黏度计、WJL-628激光粒度仪,无锡杰博仪器科技有限公司;电子鼻和电子舌,湖南弘林科学仪器有限公司。
1.2.1 米酸汤制作工艺流程
米酸汤制作工艺流程如下:
糯米→浸泡→胶体磨磨碎→糊化→液化→糖化→灭菌→接种→培养→杀菌→成品
1.2.2 操作要点
浸泡:称取m(粳米)∶m(糯米)=2 ∶1共100 g,净水洗涤1~2次,在室温25 ℃左右浸泡约6 h。
液化:在温度降为85 ℃时,调pH值到6.5,添加1%(质量分数)的液化酶,液化25 min。
糖化:在温度降为55 ℃时,调pH值到4.0时,添加0.02%(质量分数)的糖化酶,糖化1 h。
灭菌:105 ℃、8 min进行灭菌。
接种:通过前期预实验在本实验室已筛选、分离、鉴定的6珠乳酸菌条件下,进行单株发酵米酸汤实验,选择发酵产酸最高,而且感官评分较高的乳酸菌为鼠李糖乳杆菌、玉米乳杆菌、植物乳杆菌,然后再通过不同组合配比优化实验,研究出鼠李糖乳杆菌、玉米乳杆菌、植物乳杆菌最佳比例为1∶1∶1。
杀菌:酸汤发酵完全后95 ℃,15 min进行灭菌。
1.3.1 单因素实验
通过单因素变量法,以总酸和感官评分为评价指标,分别确定最佳发酵时间(92、96、100、104、108 h)、菌种接种量(3%、4%、5%、6%、7%)、发酵温度(30、33、36、39、42 ℃)、初始pH(5.8、6.2、6.6、7、7.4)。
1.3.2 响应面实验
在单因素试验基础上,以发酵时间、发酵温度、pH值、菌种接种量为响应因素,以总酸为评价值,采用Box-Behnken设计原理进行4因素3水平响应面分析试验。
1.4.1 贮藏期间理化参数动力学与热力学[15]
贮藏期间品质理化参数的变化如公式(1)所示:
(1)
式中:C,t时的物化参数值;K,反应速率常数;n,反应级数。
贮藏时间与反应温度有关的变化,用Arrhenius方程计算,如公式(2)所示:
(2)
式中:A0,Arrhenius常数;Ea,活化能(kJ/mol);R,绝对气体常数(8.314 J/mol);T,绝对温度(0K)。
为了更深入反应机理,根据绝对反应速率理论可以计算反应热力学参数,ΔH*、ΔS*、ΔG*,如公式(3)~公式(5)所示:
ΔH*/(kJ·mol-1)=Ea-RT
(3)
(4)
ΔG*/(kJ·mol-1)=ΔH-TΔS*
(5)
式中:ΔS*,J/mol°K;Kb,Boltzmann常数(1.38×10-23J/0K);h,Plank常数(6.626×10-31J·s)。
1.4.2 米酸汤快速贮藏实验[16]
以自制的米酸汤为样品进行贮存稳定性试验, 依照Arrhenius方程, 将样品分别放入25、35、45 ℃的恒温箱中保存。样品测定时间为从第1天开始, 间隔10 d测定1次直到第90天,检测时每个温度处理随机取3袋平行样进行检测。初步将感官评分低于60分时设为产品贮存稳定性终点, 然后对试验数据进行统计分析, 再按上述原理预测出自制米酸汤的贮存稳定性。测试内容包括离心沉淀率、粒径、黏度、色差值、pH值、感官评分。
1.5.1 总酸含量测
参照GBT 12456—2008食品中总酸的测定[17]。
1.5.2 离心沉淀率[18]
称量20 g样品放入离心管中,设定离心机参数为4 ℃、10 000 r/min、15 min。离心结束后,倒立静置5 min沥干后称量,进行3次平行测定,离心沉淀率取平均值。
1.5.3 色差值[19]
用移液枪准确移取混匀的米酸汤2 mL, 以蒸溜水为对照,测定米酸汤的L*、a*、b* 值 然后按照下式求出 ΔE值,ΔE越大表示样品颜色差异越大,如公式(6)所示:
(6)
1.5.4 黏度测定
量取20 mL米酸汤,采用NDJ-5S旋转黏度计进行测试。
1.5.5 感官评定
由20名有经验的酸汤评品员,分别对米酸汤的4个组分进行评定,采用百分制,具体的感官评价标准见表1。
表1 米酸汤感官评定指标
Table 1 The sensory evaluation index of rice sour soup

因素优(40分)良(30分)中(20分)差(10分)色泽米白色,明亮略白,半透明黄色,暗淡暗沉无光内部形态无沉淀,均匀略有沉淀出现,无分层有沉淀,有分层现象有杂质,有明显分层现象滋味酸甜爽口,无颗粒感略有颗粒感,酸甜感适宜酸甜感不适宜有难闻异味香气米香浓郁,香气融洽有米香,不太融洽香气不协调,不香有难闻的气味
量取15 mL米酸汤,采用电子鼻、电子舌进行测试。每个样品平行测定5次。
运用IBM SPSS Statistics 22软件进行数据处理分析,且每组实验重复3次(结果均以平均值±标准差表示)与相关性分析,应用Origin 9画图。
由图1-a可知,在P<0.01时,发酵酸度与发酵时间pearson相关系数为0.973,呈极正相关。在发酵的前100 h,总酸增长速率较快,有显著性,在发酵100 h之后,总酸增长缓慢,没有显著性差异,但随着发酵的不断进行,发酵菌产总酸不断积累,发酵液的pH也随之降低,由于高浓度总酸的反馈抑制,发酵菌的生长繁殖受到抑制,米酸汤的口感也出现了下降的趋势。综上所述,100 h为最优发酵时间。
由图1-b可知,发酵菌均是乳酸菌耐热性差的微生物。温度较低时抑制发酵菌中一些酶的活性,其生长繁殖能力差,产酸能力弱,导致酸度不高;温度过高时,发酵菌中一些不耐高温的酶将会失活,一些生理生化活性丧失,从而也会影响米酸汤的总酸和风味。综上所述,36 ℃为米酸汤的最佳发酵温度。
由图1-c可知,随着pH值的增加,总酸先增大后减小。由于本实验混合菌均为乳酸菌,pH较高或较低时都会抑制其生长繁殖,而pH 6.6时,适宜其生长繁殖,发酵菌产酸高,所以产品的酸度也高。但是随着pH的增大或减小,发酵菌的生长繁殖过程被抑制,发酵效果不理想,酸度降低,而且感官性能也受到一定的影响。综上所述,pH值为6.6时最佳。
由图1-d可知,随着菌种接种量的增加,米酸汤的酸度和感官评分呈先增大后减小的趋势。可能是当菌种添加量过低时,不能充分利用米汤中的氮源和碳源转化为有机酸,使总酸和感官评分降低,但当菌种添加量过高时,在生长环境容量一定的条件下,菌种大量繁殖,形成种内竞争关系,导致发酵后期菌种大量死亡,菌体自溶产生苦涩味,感官评分降低,总酸也无明显增加。因此最佳菌种接种量为5%。
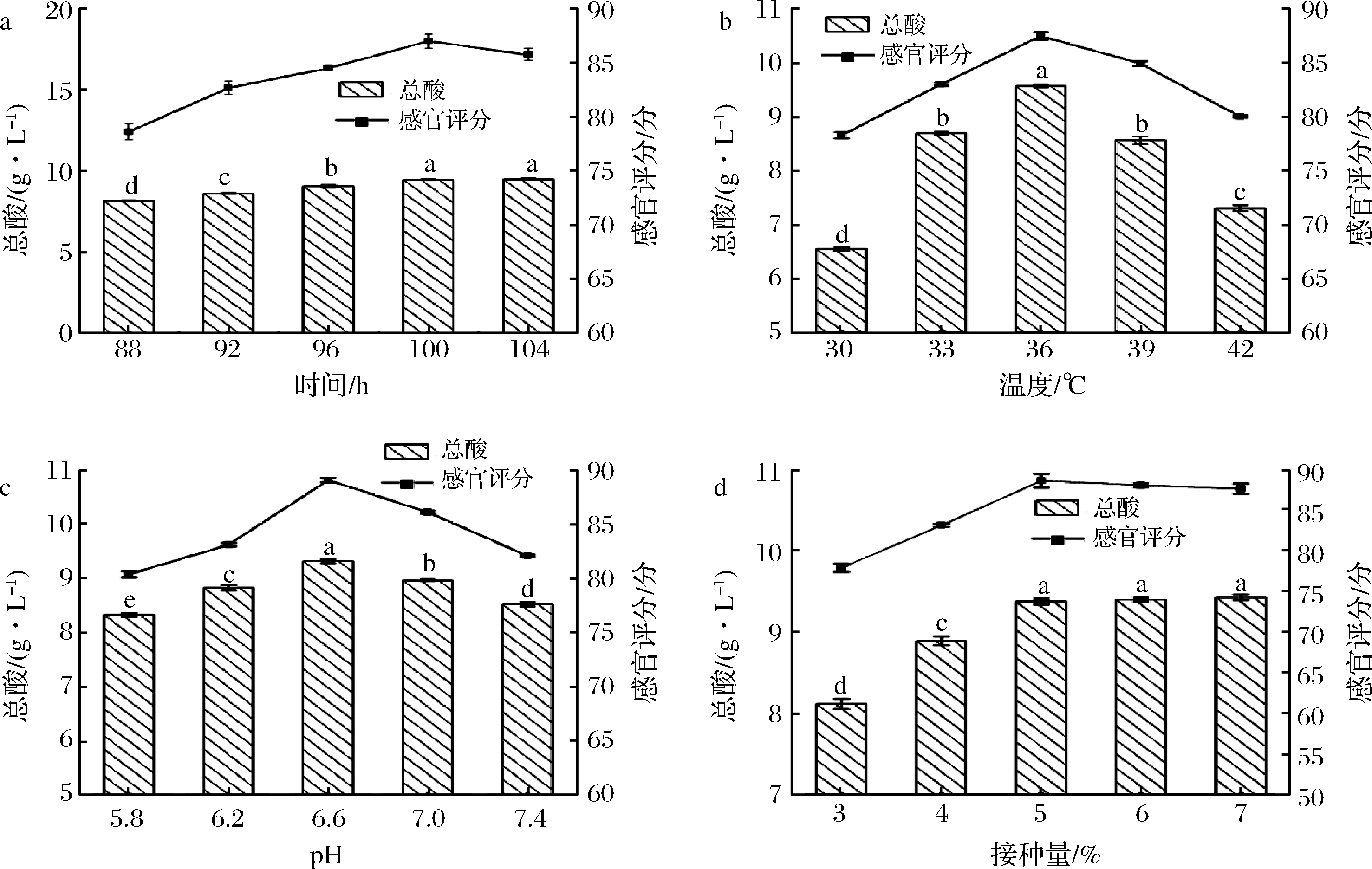
a-时间;b-温度;c-pH;d-接种量
图1 单因素试验结果(n=3)
Fig.1 Results of one-factor-at-a-time experiments
注:图中a~e字母代表不同水平之间有显著性差异(P<0.05)
2.2.1 响应面试验
由表2可知,对所得数据进行分析整理,发酵酸度(Y1)二次回归方程为Y1=9.46+0.63A+0.088B+0.012C+0.018D+0.075AB-0.030AC-0.065AD-0.027BC+0.038BD+0.092CD-0.1A2-0.86B2-0.097C2-0.51D2。由表3可知,对发酵酸度回归模型进行分析,该二次多项式回归模型P<0.01,具有差异显著性,失拟项P=0.385 9>0.05,差异不显著。该模型的复相关系数R2=0.97,调整确定系数![]() 表明该模型能解释92.71%的响应值变化,可用该模型对米酸汤工艺进行分析与预测[21-22]。
表明该模型能解释92.71%的响应值变化,可用该模型对米酸汤工艺进行分析与预测[21-22]。
2.2.2 验证试验
以总酸为主要评测指标,通过二次回归模型的预测米酸汤发酵的最佳工艺条件,发酵时间104 h、接种量为5.11%、发酵温度36.32 ℃、pH值6.59。此时米酸汤的酸度为9.43 g/L。根据响应面最佳条件进行3次平行实验得到米酸汤酸度(9.48±0.08) g/L,接近理论预测值,相对误差为0.73%,说明响应面分析法适用于米酸汤发酵工艺的优化研究。
2.3.1 贮藏期间理化指标随时间的变化
由图2-a可知,在同一温度下,样品的离心沉淀率随时间延长而增加,在同一时间下,离心沉淀率随温度的升高而变大,米酸汤的稳定性也就越差。说明贮藏时间越长,大分子之间发生聚集的次数越多,沉淀积累越多,温度的升高也加快了大分子物质之间的碰撞频率,使得分子之间更容易聚集,降低了米酸汤的稳定性。
表2 响应面设计方案及响应值结果
Table 2 Response surface design scheme and response value results
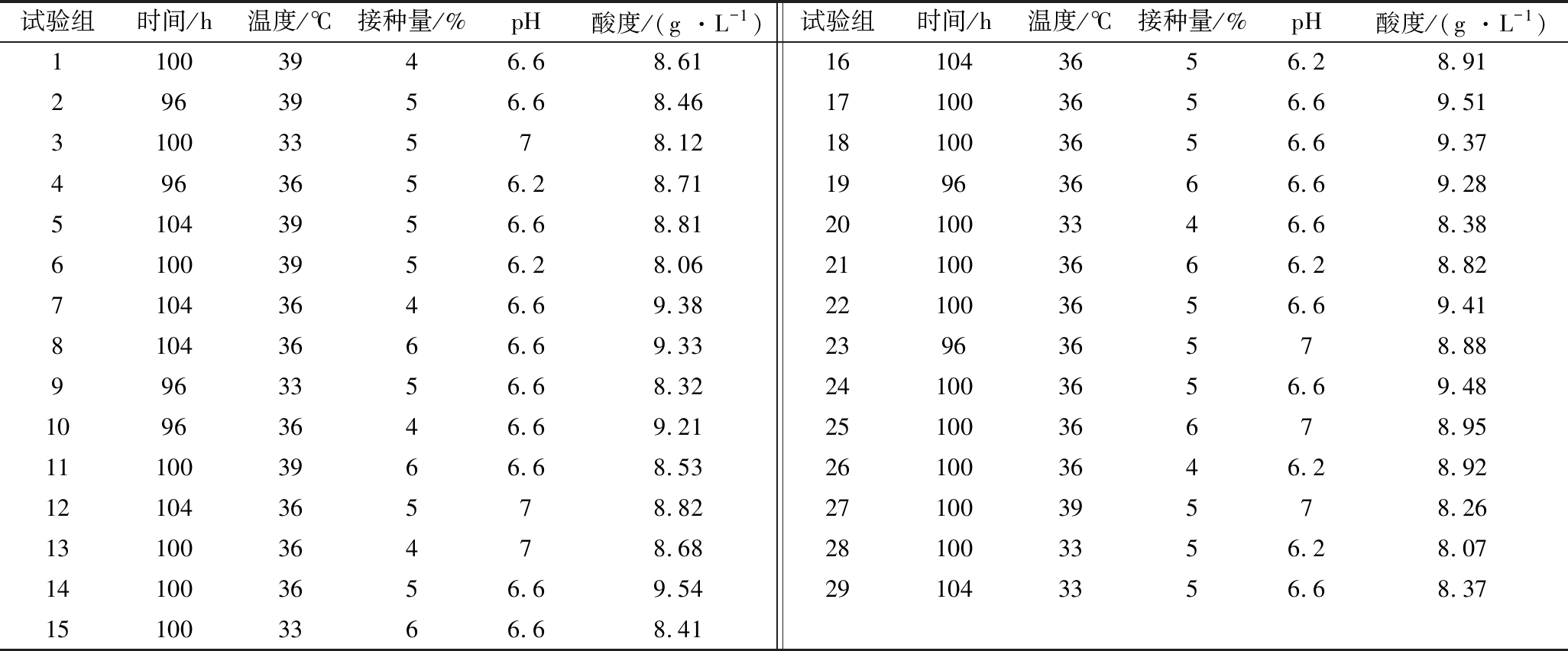
试验组时间/h温度/℃接种量/%pH酸度/(g ·L-1)试验组时间/h温度/℃接种量/%pH酸度/(g ·L-1)11003946.68.61161043656.28.912963956.68.46171003656.69.51310033578.12181003656.69.374963656.28.7119963666.69.2851043956.68.81201003346.68.3861003956.28.06211003666.28.8271043646.69.38221003656.69.4181043666.69.33239636578.889963356.68.32241003656.69.4810963646.69.212510036678.95111003966.68.53261003646.28.921210436578.822710039578.261310036478.68281003356.28.07141003656.69.54291043356.68.37151003366.68.41
表3 总酸回归模型方差的分析结果
Table 3 Analysis results of variance of total acid regression model

方差来源平方和自由度均方F值P值显著性模型6.01140.4365.56<0.000 1极显著残差0.092146.55×10-3失拟项0.072107.18×10-31.450.385 9不显著纯误差0.0244.97×10-3总差异6.128
由图2-b可知,在同一温度下,粒径随贮藏时间延长而增大,说明米酸汤贮藏过程中悬浮颗粒不断聚集。同一时间下,温度越大粒径的聚集速度越快,从而改变原有颗粒的粒径大小,使得粒径值变大。
由图2-c可知,在同一温度下,样品的黏度随时间延长而减少,在同一时间下,温度越高样品的黏度越小,说明米酸汤在贮藏期间一些直链或支链淀粉等大分子物质继续水解,降低了直链或支链淀粉在胶体中的比例,使黏度下降。
由图2-d可知,在在同一时间下,米酸汤的色差值随温度上升而增加。表明米酸汤贮藏过程中蛋白质或氨基酸与葡萄糖之间发生Mailard反应[23],导致米酸汤颜色变深,温度越高,Mailard反应越快,色差值越大。
由图2-e可知,在贮藏(0~30) d时,pH值随时间和温度的变化基本不变;在贮藏30 d后,同一温度下样品的pH值随时间延长而增大。在同一时间下,温度越高,样品的pH值越大,表明米酸汤在贮藏期间,体系中碱性化合物增加或产生碱性细菌,导致pH值增大。
由图2-f可知,在不同贮藏温度的条件下,米酸汤的感官评分随贮藏温度的增加而减少;在同一温度下贮藏时,贮藏时间越长,感官评分越低。表明米酸汤贮藏过程中的颗粒聚集,黏度下降,米酸汤的内部形态下降,感官评分降低。在贮藏时间相同时,感官评分值随贮藏温度增大而降低。表明温度升高,Mailard反应加快,米酸汤色泽变深,没有光泽,口感降低。
2.3.2 米酸汤理化指标和感官指标的相关性
在贮藏期间,米酸汤的理化指标与感官评分的Pearson相关性如表4所示。由表4可知,在贮藏温度为25、 34、 45 ℃时,离心沉淀率和色差值的Pearson最大,均>0.99,(P<0.01)与感官评分极显著负相关,分别是0.990、0.995、0.998、0.995、0.998、0.997;可能是米酸汤贮藏过程中的悬浮颗粒发生聚集现象,导致离心沉淀率变大,也可能是米酸汤储存过程中发生Mailard反应,导致样品颜色变深。由表5可知,离心沉淀率和色差值与感官评分的回归方程在不同温度下R2均>0.9,表明其与感官评分的相关性关系很好。综上所述,可以把离心沉淀率和色差值作为米酸汤品质变化和贮存稳定性动力学和热力学预测模型的主要因素。
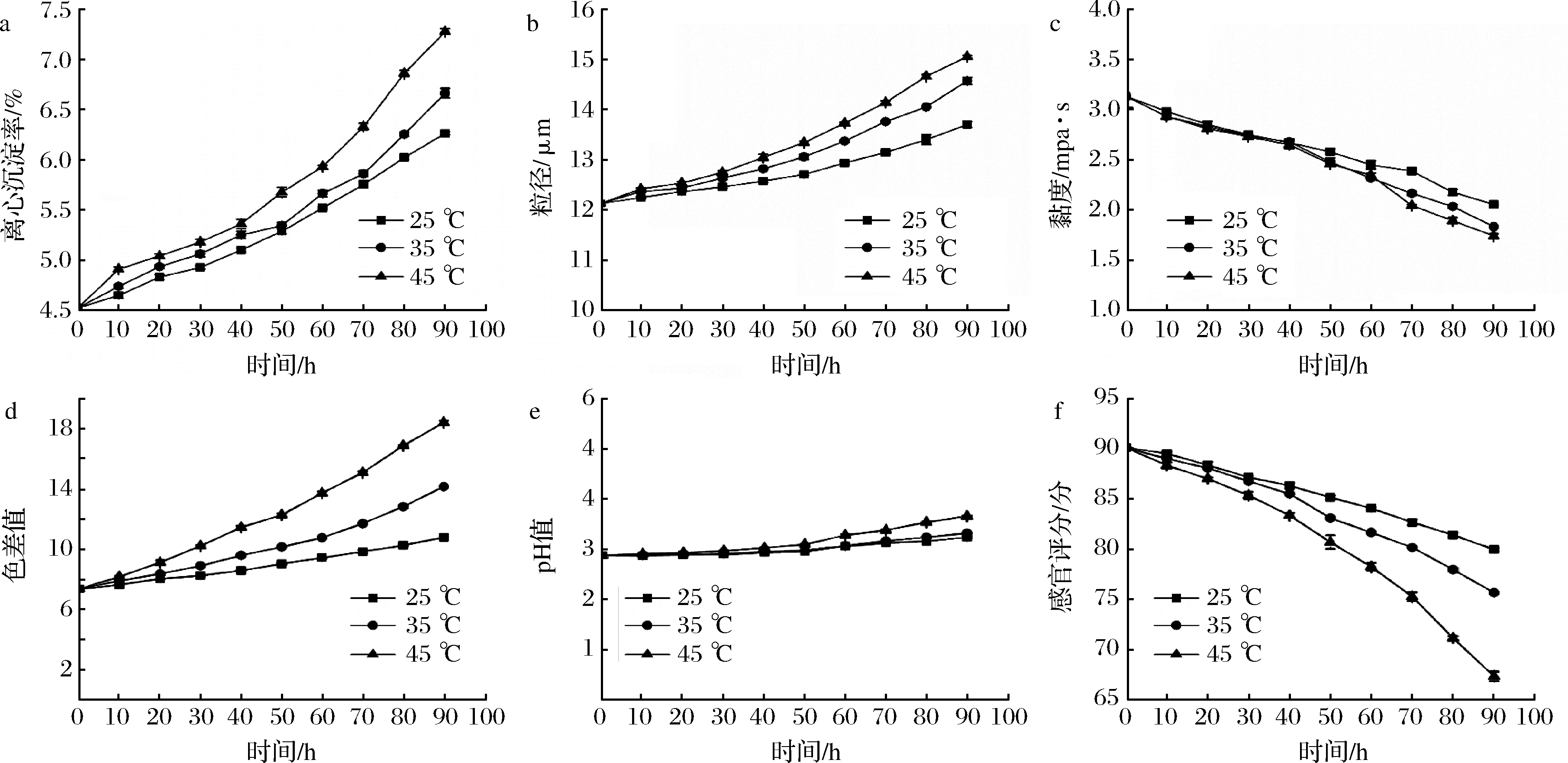
a-离心沉淀率;b-粒径;c-黏度;d-色差值;e-pH值;f-感官评分
图2 米酸汤产品的理化指标随储存时间变化的曲线(n=3)
Fig.2 The curve of physical and chemical indexes of rice sour soup products with storage time
表4 米酸汤在25、35、45℃贮藏期间理化指标和感官评分之间的 Pearson相关系数
Table 4 Pearson correlation coefficient between physical and chemical indexes and sensory score of rice sour soup during storage at 25,35,45℃
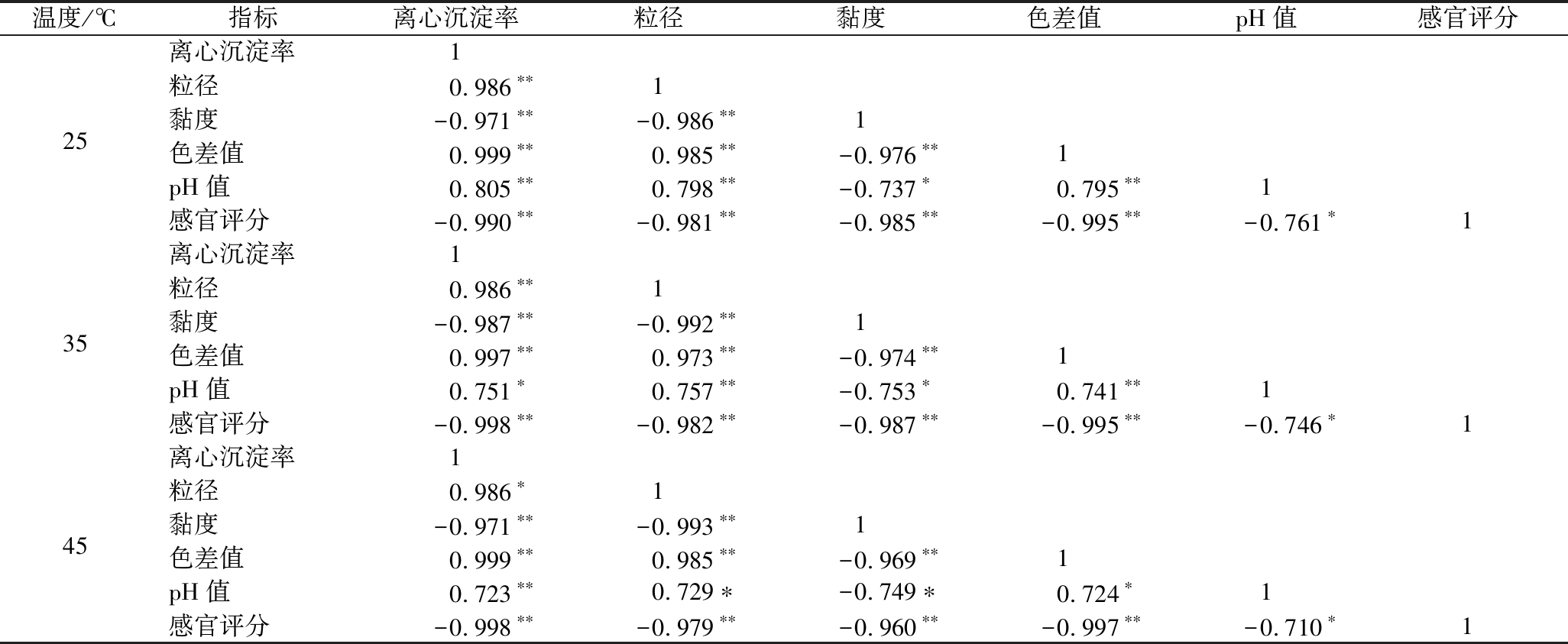
温度/℃指标离心沉淀率粒径黏度色差值pH值感官评分离心沉淀率1粒径0.986∗∗125黏度-0.971∗∗-0.986∗∗1色差值0.999∗∗0.985∗∗-0.976∗∗1pH值0.805∗∗0.798∗∗-0.737∗0.795∗∗1感官评分-0.990∗∗-0.981∗∗-0.985∗∗-0.995∗∗-0.761∗1离心沉淀率1粒径0.986∗∗135黏度-0.987∗∗-0.992∗∗1色差值0.997∗∗0.973∗∗-0.974∗∗1pH值0.751∗0.757∗∗-0.753∗0.741∗∗1感官评分-0.998∗∗-0.982∗∗-0.987∗∗-0.995∗∗-0.746∗1离心沉淀率1粒径0.986∗145黏度-0.971∗∗-0.993∗∗1色差值0.999∗∗0.985∗∗-0.969∗∗1pH值0.723∗∗0.729∗-0.749∗0.724∗1感官评分-0.998∗∗-0.979∗∗-0.960∗∗-0.997∗∗-0.710∗1
注:*,显著相关(P<0.05);**,极显著相关(P<0.01)
2.3.3 贮藏期间米酸汤理化参数变化的热力学和动力学分析
按照公式(1)分别计算米酸汤贮藏期间离心沉淀率、色差值零级和一级的反应级数,如表6所示,在25、35、45 ℃下零级、一级回归方程的R2均>0.9,表明拟合程度很好。但是离心沉淀率和色差值的ΣR2均较零级的大,因此符合一级反应化学动力学。根据公式(2)求出反应活化能,再根据公式(3)~公式(5)可计算反应的热力学参数,如表7所示,Ea越小,表示反应越容易进行,离心沉淀率和色差值的Ea都比较小,离心沉淀率的活化能低,体系中络合物容易产生,导致沉淀发生,离心沉淀率也随温度的升高而增大;温度越高越能促进络合物的形成,体系的稳定性越差[24]。色差值的活化能低,米酸汤中的蛋白质或氨基酸与葡萄糖之间发生羰氨缩合的Mailard反应越容易,导致颜色加深,温度高也能促进Mailard反应,体系的颜色变化越大。Gibbs自由能表示反应物的能量和活化状态之间的变化,在化学热力学中为判断过程进行的方向,离心沉淀率Gibbs自由能为(83.17~87.89) kJ/mol,色差值Gibbs自由能为(82.65~85.90) kJ/mol,故反应都为非自发反应[25]。Gibbs自由能随温度增加而递增,建立Gibbs自由能与温度回归方程以表明化学反应与宏观物理变化之间的相关性。离心沉淀率的Gibbs自由能与温度之间回归方程的相关系数为0.999 1,色差值Gibbs自由能与温度之间回归方程的相关系数为0.999 7,如表8所示。
表5 不同温度下色差值和离心沉淀率的回归方程
Table 5 regression equation of color difference and centrifugal sedimentation rate at different temperatures
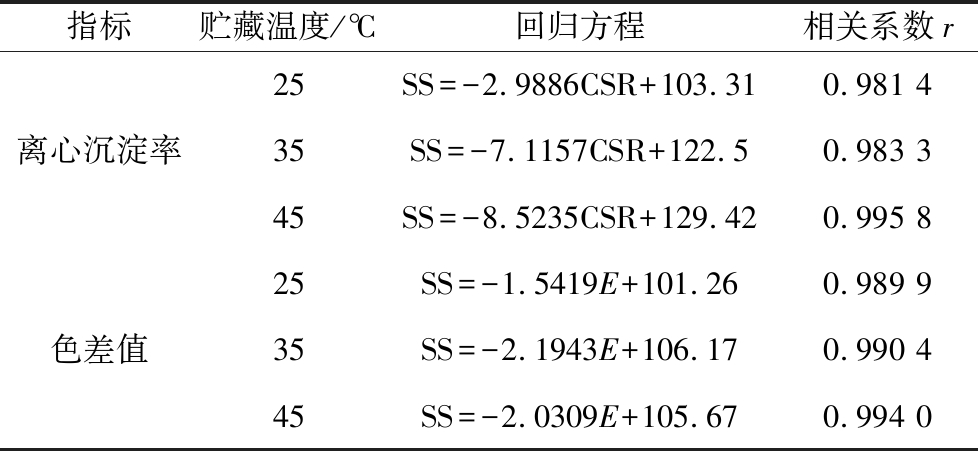
指标贮藏温度/℃回归方程相关系数r离心沉淀率25SS=-2.9886CSR+103.310.981 435SS=-7.1157CSR+122.50.983 345SS=-8.5235CSR+129.420.995 8色差值25SS=-1.5419E+101.260.989 935SS=-2.1943E+106.170.990 445SS=-2.0309E+105.670.994 0
注:SS,感官评分;CSR,离心沉淀率;d,粒径;E,色差值
2.4.1 预测米酸汤稳定性的动力学和热力学模型
把离心沉淀率、色差值与感官评分的回归方程(表5)和ΔG*与T的回归方程(表8),代入公式(1)~(5),可获得米酸汤离心沉淀率和色差值的动力学和热力学的稳定性模型,为![]()
表6 米酸汤在不同贮藏温度下品质变化的动力学模型参数
Table 6 Kinetic model parameters of quality change of rice sour soup at different storage temperatures
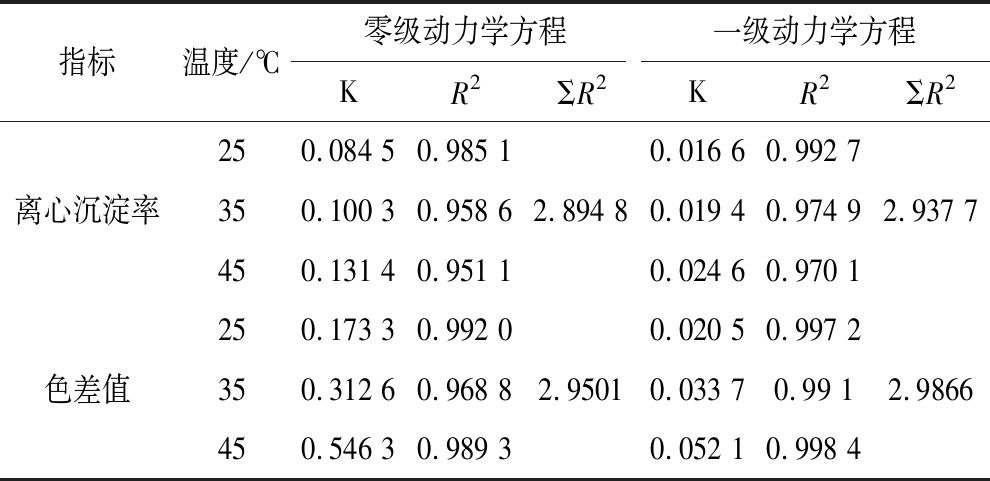
指标温度/℃零级动力学方程一级动力学方程KR2ΣR2KR2ΣR2250.084 50.985 10.016 6 0.992 7离心沉淀率350.100 30.958 62.894 80.019 40.974 92.937 7450.131 40.951 10.024 60.970 1250.173 30.992 00.020 50.997 2色差值350.312 60.968 82.95010.033 70.99 12.9866450.546 30.989 30.052 1 0.998 4
表7 米酸汤动力学与热力学参数
Table 7 Kinetic and Thermodynamic parameters of rice sour soup
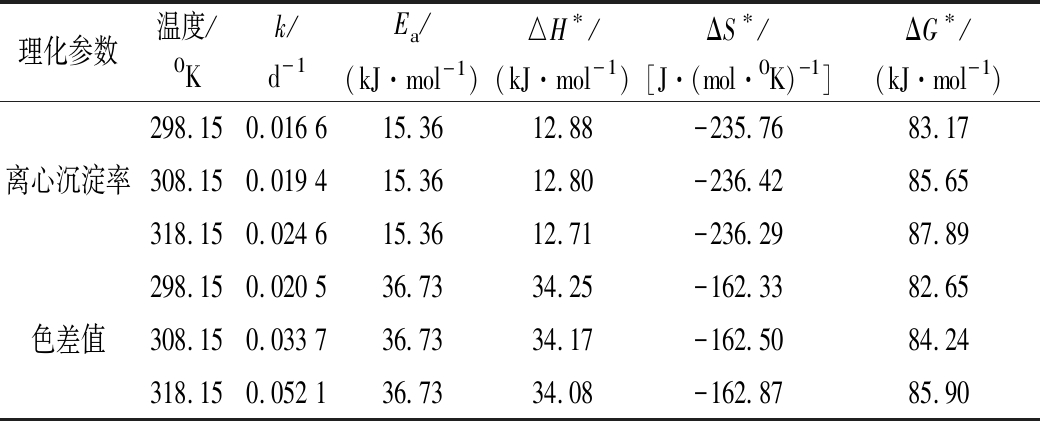
理化参数温度/0Kk/d-1Ea/(kJ·mol-1)△H∗/(kJ·mol-1)ΔS∗/[J·(mol·0K)-1]ΔG∗/(kJ·mol-1)298.150.016 615.3612.88-235.7683.17离心沉淀率308.150.019 415.3612.80-236.4285.65318.150.024 615.3612.71-236.2987.89298.150.020 536.7334.25-162.3382.65色差值308.150.033 736.7334.17-162.5084.24318.150.052 136.7334.08-162.8785.90
表8 米酸汤理化参数吉布斯自由能与温度的回归方程
Table 8 Regression equation between free energy and temperature of physical and chemical parameters of rice sour soup

理化参数回归方程r2离心沉淀率Y = 0.235 9X + 12.8920.999 1色差值Y = 0.162 6X + 34.1740.999 7
注:回归方程表示为ΔG*(kJ/mol)=f(T)
2.4.2 米酸汤稳定性预测模型的精确度评价
根据实验的实测值和模型预测值,计算出米酸汤稳定性预测标准差、模型误差。由表9可知,离心沉淀率与色差值预测模型误差平均值分别为13.46%、6.07%,均<15%,表明预测模型的精确度良好,可以满足预测米酸汤的稳定性要求。
表9 米酸汤的稳定性预测模型的残差变异系数
Table 9 residual coefficient of variation of stability prediction model of rice sour soup
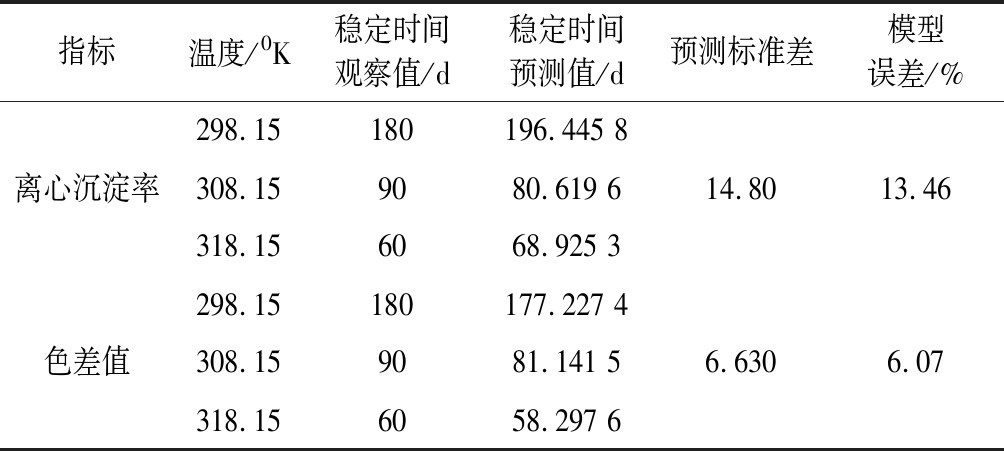
指标温度/0K稳定时间观察值/d稳定时间预测值/d预测标准差模型误差/%298.15180196.445 8离心沉淀率308.159080.619 614.8013.46318.156068.925 3298.15180177.227 4色差值308.159081.141 56.6306.07318.156058.297 6
图3表示米酸汤在不同贮藏温度下180 d的电子鼻区分度(discrimination index,DI)达99.3%,电子舌区分度达99.98%,一般情况下认为DI值>80%区分效果较好,DI值越大表示样品间的距离越远,区分的效果越理想。由此可见,米酸汤在不同贮藏温度下180 d的挥发性气味和风味成分有明显区别。
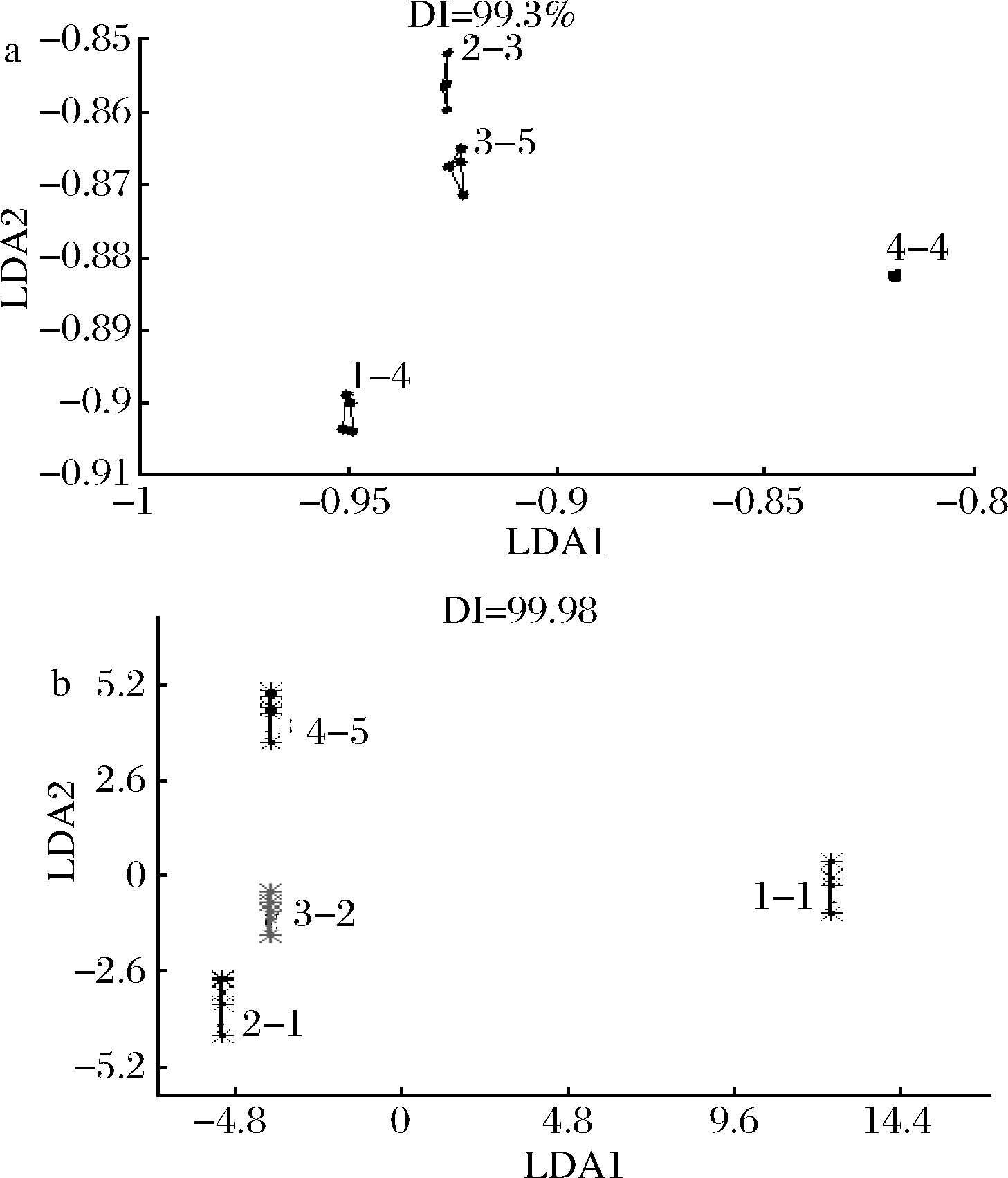
a-主成分得分;b-判别函数分析
图3 米酸汤不同贮藏温度下电子鼻和电子舌的主成分结果分析
Fig.3 Principal component analysis of electronic nose and electronic tongue under different storage temperature of rice sour soup
注:1,米酸汤贮藏0 d;2,25 ℃贮藏180 d;3,35 ℃贮藏180 d;4,45 ℃贮藏180 d
响应面优化后工艺条件参数为发酵时间104 h、接种量为5%、发酵温度36℃、pH值6.6,得到的酸度为(9.48±0.08) g/L,与模型预测值酸度9.43 g/L分基本一致,通过响应面优化米酸汤发酵有一定的现实指导意义。
通过米酸汤理化指标在不同贮藏温度下随时间的变化关系,建立米酸汤离心沉淀率和色差值与感官评分、贮藏温度、贮藏时间之间的动力学和热力学数学模型,建立该产品的预测模型。计算出离心沉淀率和色差值预测模型误差CV平均值分别为13.46%、6.07%,均<15%。因此,根据米酸汤在贮藏期间的离心沉淀率与色差值2个指标所建立的预测模型可以较好地预测 25~45 ℃条件下米酸汤的贮存稳定性,为预测其贮藏稳定性提供参考。
电子鼻和电子舌主成分分析DI值均>99%,可以说明米酸汤在不同贮藏温度下180 d的挥发性气味成分和风味成分有明显区别。
[1] 许桂香.浅谈贵州苗族传统饮食文化[J].凯里学院学报,2009,27(5):8-11.
[2] 江萍,张倩,秦礼康,等.凯里“酸汤”的微生物区系调查及营养成分分析[J].中国酿造,1997(4):18-20.
[3] 陈大卫,杨壮壮,黄玉军,等.米汤发酵乳乳酸菌的筛选及其制备工艺[J].农产品加工,2017(23):22-26.
[4] 石敏, 袁玮.“酸汤”发酵过程中酸度的动态变化[J].凯里学院学报,2007,25(3):30-31.
[5] 后立琼,陈安均.苗族发酵型白酸汤的生产工艺[J].食品科学,2012,33(24):356-359.
[6] 后立琼.苗族酸汤中乳酸菌的分离鉴定及发酵动力学模型研究[D].雅安:四川农业大学,2012:1-9.
[7] 郑莎莎,宋煜婷,罗意,等.凯里白酸汤的优化工艺[J].山地农业生物学报,2016,35(2):80-85.
[8] 曹旭鸿.苗族白酸汤饮料的开发[D].雅安:四川农业大学,2014:1-5.
[9] 王芳梅,张鑫,谷盼盼.新疆打瓜籽油氧化稳定性的研究及货架期预测[J].食品与发酵工业,2019,45(5):164-169.
[10] 李明,赵良忠,王容,等.果汁型豆酸汤饮料稳定性动力学模型初探[J].食品安全质量检测学报,2019,10(9):2 555-2 561.
[11] RUSTOM I Y S, LOPEZ-LEIVA M M,NAIR B M.UHT-sterilized peanut beverages: Kinetics of physicochemical changes during storage and shelf-life prediction modeling[J].J Food Sci,2006,61(1):198-203.
[12] 赵慧,薛冰莹,贾才华,等.复合菌发酵米乳饮料的配方优化及其储藏品质变化[J].食品工业科技,2019,40(6):229-235.
[13] WALZ M M,SPOEL D V D.Temperature dependence of structure, dynamics and thermodynamics[J].Physical Chemistry Chemical Physics,2019,21(10):11 755-11 763.
[14] LU O M,RONCAL
O M,RONCAL S P, P RONCALEA, DJENANE D,et al.Beef shelf life in low O2 and high CO2 atmospheres containing different low CO concentrations[J].Meat Science,2000,55(4):413-419.
S P, P RONCALEA, DJENANE D,et al.Beef shelf life in low O2 and high CO2 atmospheres containing different low CO concentrations[J].Meat Science,2000,55(4):413-419.
[15] 张立永.酸乳饮料贮藏期理化参数变化动力学及产品稳定性预测方法研究[D].无锡:江南大学,2007.
[16] 清源,周洁,尹胜,等.块菌天然复配保鲜剂的配方优化及货架期预测[J].食品与发酵工业:2020,46(1):191-196.
[17] GB/T 12456——2008食品中总酸的测定[S].北京:中国标准出版社,2008.
[18] 余振宇.芋头浊汁饮料的加工工艺及贮藏稳定性研究[D].合肥:合肥工业大学,2015.
[19] 朱凤妹.番茄制汁的工艺条件优化及货架期预测模型的建立[J].食品安全质量检测学报,2019,10(9):2 567-2 574.
[20] 江振桂,王秋普,张震,等.不同凝固剂对豆腐品质的影响[J].食品与发酵工业,2019,45(7):229-234.
[21] TABARAKI R,NATEGHI A.Optimization of ultrasonic-assisted extraction of natural antioxidants from rice bran using response surface methodology[J].Ultrasonics Sonochemistry,2011,18(6):1 279-1 286.
[22] 巫永华,陆文静,刘梦虎,等.响应面优化超声波辅助双水相提取牛蒡多糖及抗氧化分析[J/OL].食品与发酵工业:1-12[2020-02-29].http://doi.org/10.13995/j.cnki.11-1802/ts.022554.
[23] 吴周山,陆利霞,熊晓辉,等.糖基化反应改善植物蛋白乳浊液稳定性的研究进展[J].食品工业科技,2017, 38(14): 336-341.
[24] PERON D V,FRAGA S,ANTELO F.Thermal degradation kinetics of anthocyanins extracted from juçara (Euterpe edulis Martius) and "Italia" grapes (Vitis vinifera L.), and the effect of heating on the antioxidant capacity[J].Food Chemistry,2017,232:836-840.
[25] MERCALI G D,JAESCHKE D P,TESSARO I C,et al.Degradation kinetics of anthocyanins in acerola pulp: Comparison between ohmic and conventional heat treatment[J].Food Chem,2013,136(2):853-857.