近年来由于细菌耐药性问题及食品加工中化学防腐剂的使用严重危害了人类的生命健康,研究发现,一些天然植物具有抗菌谱广、毒性小、来源广泛等优点,为研究和开发安全、高效的天然食品防腐剂提供了新的思路[1]。
刺山柑(Capparis spinosa L.)为白花菜科山柑属植物,又名老鼠瓜、槌果藤,俗称野西瓜[2-4]。国外主要分布于亚洲西部、欧洲、北美和大洋洲[5],我国主要分布于新疆、西藏、甘肃等地的荒漠及干旱地区。在新疆地区,刺山柑作为传统的民族药物,其药用历史悠久,民间常将其鲜果捣碎敷于患处,用于治疗风湿性关节炎、痛风[6-8]等。现代研究表明,刺山柑活性部位中主要含有吲哚类、黄酮类、酚酸类等化学成分[9],具有抗炎[10-12]、抗氧化[13]、抗菌[14-16]、降血糖[17]、降血脂[18]、保肝[19]等作用。在抑菌活性方面,徐琦[14]通过实验证明了,刺山柑乙酸乙酯萃取物对大肠杆菌具有显著的抑制作用;MAHASNEH[15]对刺山柑95%乙醇提取物进行了抗菌实验,发现乙醇提取物对革兰氏阳性菌和真菌有一定的抑制作用。ALI-SHTAYE等[16]研究发现刺山柑水提液可完全抑制2种表皮真菌的生长。可见刺山柑作为天然食品防腐剂具有潜在的开发价值,目前对刺山柑萃取物的抑菌稳定性的研究还未见报道。因此,本实验对刺山柑4种萃取物体外抑菌活性进行探讨,并考察温度、紫外光照、pH对刺山柑乙酸乙酯及正丁醇萃取物的影响,以期为将刺山柑开发成天然的食品防腐剂奠定理论基础。
1 材料与方法
1.1 材料与试剂
刺山柑:新疆吐鲁番野生果实。
供试菌种:金黄色葡萄球菌(Staphylococcus aureus)、大肠杆菌(Escherichia coli)、枯草芽孢杆菌(Bacillus subtilis),由新疆农业大学食品科学与药学学院微生物实验室提供。
试剂:蛋白胨、酵母浸粉、NaCl和琼脂,北京奥博星生物技术有限责任公司;乙醇、二甲基亚砜、石油醚、氯仿、乙酸乙酯和正丁醇等,均为国产分析纯。
1.2 仪器与设备
AL204-IC型电子天平,梅特勒-托多利仪器有限公司;XL-02A粉碎机,烨昌机械有限公司;JBT/C-YCL400T/3P(D)超声波药品处理机,济宁金佰特工程机械有限公司;RE-52B旋转蒸发仪,上海亚荣生化仪器厂;DSX-280KB24手提式压力蒸汽灭菌器,上海申安医疗器械厂;JQ000453无菌操作台,苏净集团安泰公司制造;THZ-82A气浴恒温振荡器,江苏省金坛市医疗仪器厂;DHP-9052恒温培养箱,上海恒科科技有限公司。
1.3 方法
1.3.1 刺山柑萃取物的制备
参照任远[20]方法并稍作修改,取刺山柑干燥果实200 g,粉碎成粗粉,以1∶10(g∶mL)的料液比,分别用体积分数的80%及50%乙醇各超声提取2次,提取时间50 min,将乙醇提取液合并,55 ℃条件下减压浓缩至膏状,得乙醇提取物,将其混悬于等量的蒸馏水中,然后按照1∶2的体积比,依次用石油醚、氯仿、乙酸乙酯、正丁醇溶剂(溶剂极性由小至大)对乙醇提取物进行分级萃取,各极性溶剂于室温下重复萃取4次,分别收集萃取液,55 ℃条件下减压浓缩至10 mL,于通风橱内进行风干,得到4种刺山柑萃取物。实验前用二甲基亚砜(dimethyl sulfoxide,DMSO)将4种萃取物溶解,4 ℃冷藏备用。
1.3.2 培养基的配置
LB液体和固体培养基配置参考綦国红等[21]方法。
1.3.3 菌种的活化与菌悬液制备
分别挑取3种供试菌株的单个菌落于LB液体培养基中进行活化,置于37 ℃恒温振荡器振荡培养18~24 h,用灭菌生理盐水将活化好的供试菌株稀释成浓度为106~107CFU/mL的菌悬液,4 ℃保存备用。
1.3.4 琼脂打孔法测定抑菌圈直径的大小
参照李敏[22]方法并稍作修改,分别取已定量稀释的3种供试菌种菌悬液,置于无菌培养皿内,倒入50 ℃左右融化后的LB固体培养基,厚度3~5 mm,轻轻摇晃均匀,待其冷却凝固后,用6 mm灭菌金属打孔器在平板内等距打4个孔,挑出孔内的琼脂,向每孔中分别加入50 μL质量浓度为200 mg/mL刺山柑4种萃取物药液及对照品溶液(DMSO),然后将各培养皿放置于37 ℃恒温培养箱中静置培养18~24 h,采用十字交叉法测量抑菌圈直径的大小。抑菌圈直径取3个平行孔的平均值为测定结果。
1.3.5 最小抑菌浓度测定(minimal inhibitory concentration,MIC)
采用试管二倍稀释法将刺山柑4种溶剂萃取物分别配制为200、100、50、25、12.5、6.25 mg/mL的样品溶液,参照吴永祥等[23]及王建军等[24]方法。结果以肉眼无可见菌落生长的最小质量浓度为其MIC。
1.4 刺山柑萃取物的抑菌稳定性[25-27]
分别测定不同温度、紫外光照时间、pH值对刺山柑萃取物样品溶液抑菌活性稳定性。以打孔法测定样品溶液对3种供试菌种的抑菌圈直径。
1.5 数据处理
运用SPSS 19.0对实验数据进行单因素方差分析(one-way ANOVA),利用Duncan’s多重比较法分析样本间的差异显著性,图表采用origin 8.5绘制,结果以平均值±标准误差(Mean±SD)表示。
2 结果与分析
2.1 刺山柑萃取物对3种供试菌的抑菌活性
由图1及表1可知,刺山柑4种溶剂萃取物在相同浓度下,对3种供试菌种均有一定的抑制作用。对枯草芽孢杆菌及金黄色葡萄球菌的抑制作用以乙酸乙酯萃取物活性最佳,对大肠杆菌的抑制作用以正丁醇萃取物活性最佳,徐琦[14]研究得出,大肠杆菌对刺山柑乙酸乙酯萃取物较乙醇提取物、石油醚、正丁醇萃取物更为敏感,与本实验结果有所差异,可能由于提取方式的不同,导致抑菌成分在各萃取物中分布不同,因而表现出不同的抑菌效果。以上实验结果表明,刺山柑4种溶剂萃取物对革兰氏阳性菌的抑菌效果强于革兰氏阴性菌,由于革兰氏阴性菌的细胞壁由外膜和周质间隙组成,外膜由脂多糖、磷脂、蛋白质和脂蛋白等复合构成,周质间隙是一层薄的肽聚糖。外膜的存在构成了不对称的膜结构,因此形成了对亲水性及疏水性物质的渗透屏障[28],影响了抑菌效果。
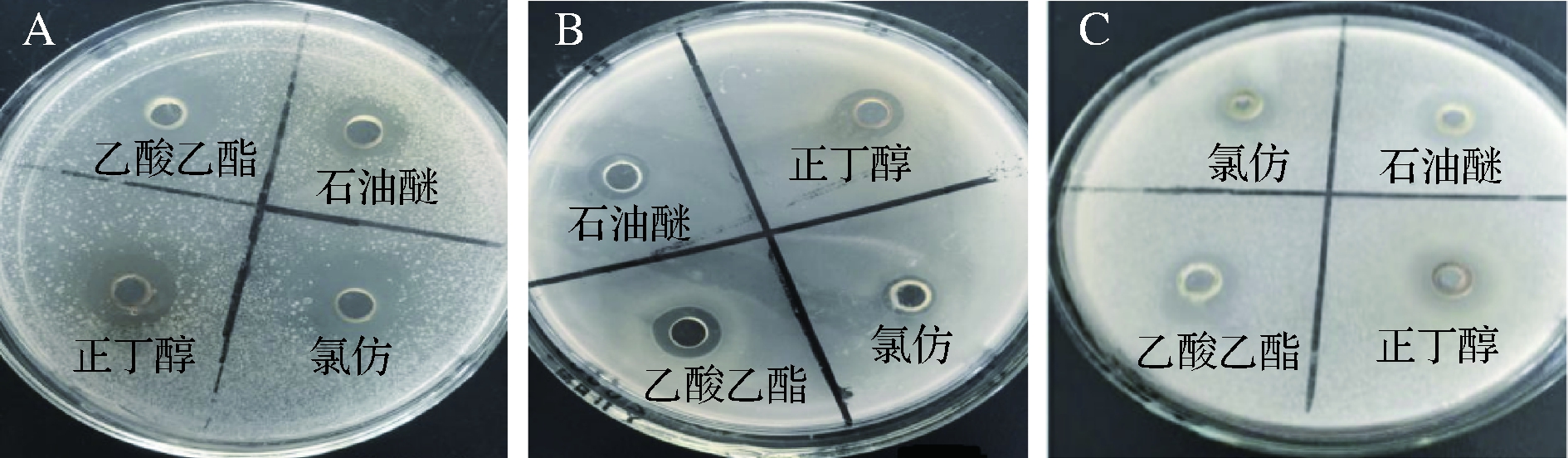
A-枯草芽孢杆菌;B-金黄色葡萄球菌;C-大肠杆菌
图1 刺山柑4种萃取物对3种供试菌抑菌圈直径大小
Fig.1 Diameter of bacteriostasis circle of four extracts from Capparis spinosa L. against three species
表1 刺山柑萃取物的抑菌效果![]()
Table 1 The bacteriostatic effect of different polar solvent extracts from Capparis spinosa L.

萃取物抑菌圈直径大小/mm枯草芽孢杆菌金黄色葡萄菌大肠杆菌石油醚 11.83±0.5810.17±0.299.33±0.29氯仿 11.33±0.299.83±0.769.67±0.29乙酸乙酯22.00±0.8716.50±0.5012.33±0.29正丁醇 20.00±0.0014.50±0.5013.67±0.29DMSO ---
注:-表示抑菌圈直径为0
2.2 刺山柑萃取物最小抑菌浓度(MIC)的测定
由于最小抑菌浓度(MIC)可作为评价抑菌物质体外抑菌活性强弱的指标,其值越小,表明该样品对受试菌种的抑制作用越强。如表2所示,刺山柑乙酸乙酯、正丁醇萃取物对3种供试菌的抑菌效果更好,其中对枯草芽孢杆菌的抑制作用最强,MIC为6.25 mg/mL;其次为金黄色葡萄球菌,MIC为25 mg/mL;而对大肠杆菌,正丁醇萃取物具有较好的抑菌效果,MIC为25 mg/mL。因此,为了充分研究刺山柑萃取物的抑菌效果,本实验筛选刺山柑乙酸乙酯和正丁醇萃取物进行后续稳定性实验研究。
2.3 刺山柑萃取物的抑菌稳定性研究
2.3.1 不同温度对刺山柑萃取物抑菌活性的影响
由图2可知,随着温度逐渐升高,刺山柑乙酸乙酯萃取物对枯草芽孢杆菌、金黄色葡萄球菌的抑菌圈直径差异均不显著(P<0.05);对大肠杆菌抑菌圈直径在121 ℃时最大,与20 ℃相比差异显著(P<0.05),说明乙酸乙酯萃取物具有较好的热稳定性,周怡等[27]研究发现,胜红蓟提取物在100 ℃抑菌圈直径最好为(12.37±0.71) mm,4 ℃时抑菌圈直径最小为(11.24±0.18)mm,二者相比差异显著(P<0.05),这与本实验结果相似,具体原因有待进一步研究。刺山柑正丁醇萃取物对枯草芽孢杆菌的抑菌圈直径在121℃时最小,与100 ℃以下相比差异显著(P<0.05);对金黄色葡萄抑菌圈直径在20~60 ℃逐渐增大,在60 ℃时抑菌圈直径最大,60~121 ℃逐渐减小,121 ℃时抑菌圈直径与20 ℃空白对照组相比差异不显著(P<0.05),说明在一定温度范围内,可以促进正丁醇萃取物的抑菌活性。
表2 刺山柑萃取物对3种供试菌的MIC
Table 2 MIC of Capparis spinosa L. extracts against three tested bacteria
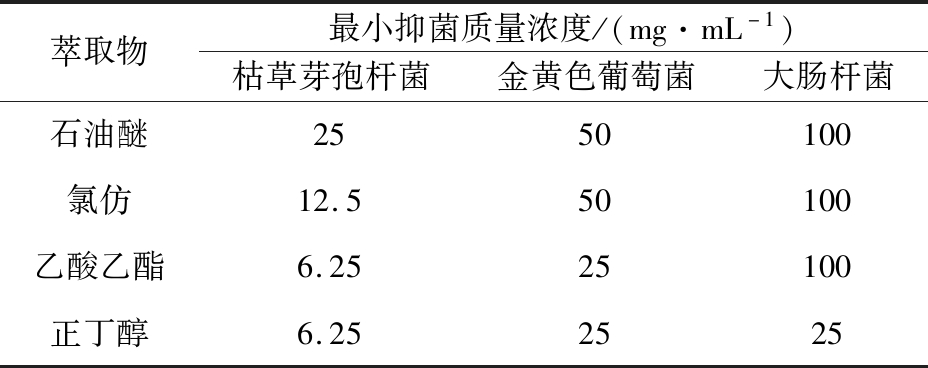
萃取物最小抑菌质量浓度/(mg·mL-1)枯草芽孢杆菌金黄色葡萄菌大肠杆菌石油醚2550100氯仿12.550100乙酸乙酯6.2525100正丁醇6.252525
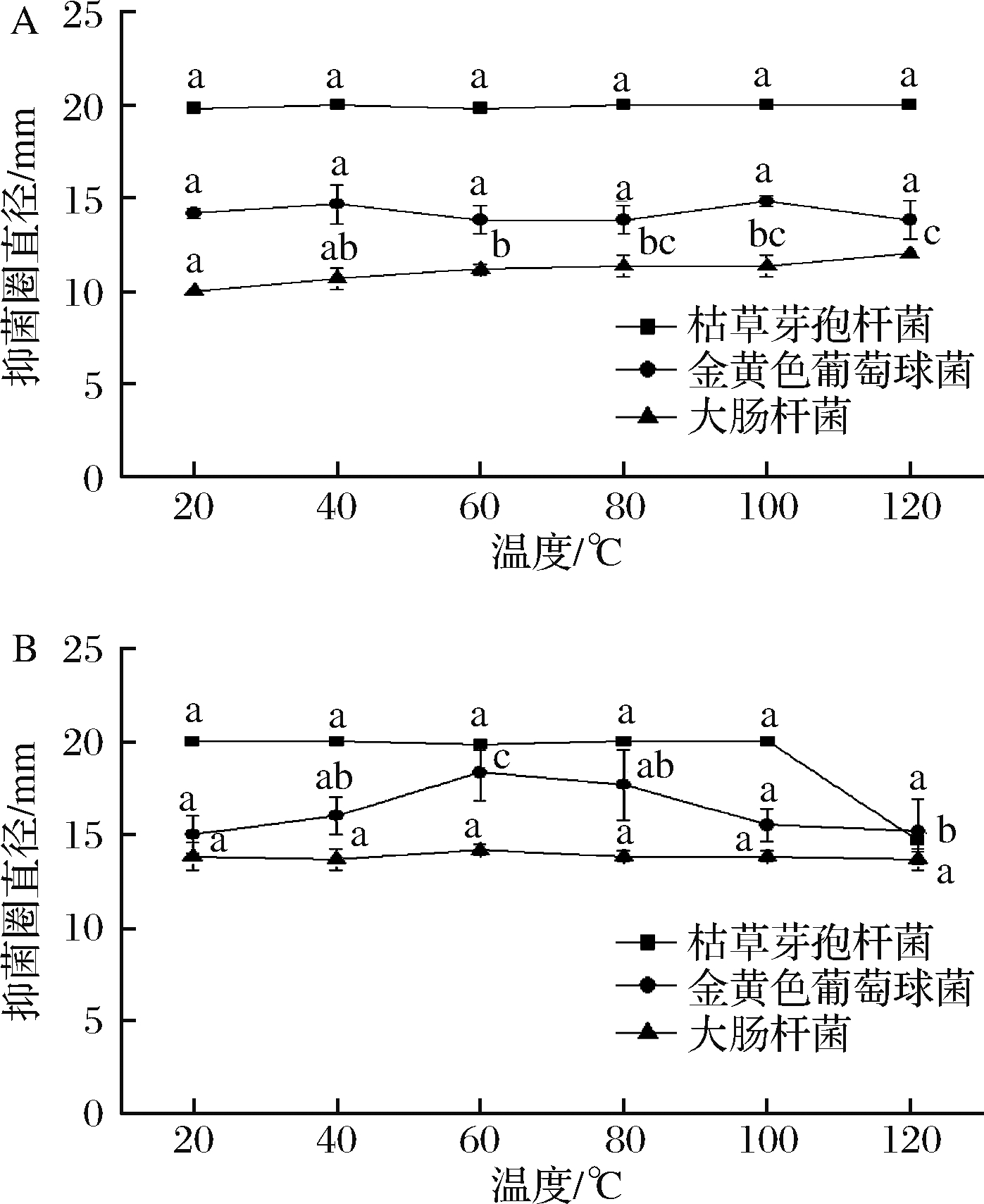
A-刺山柑乙酸乙酯萃取物;B-刺山柑正丁醇萃取物
图2 不同温度对刺山柑萃取物抑菌效果的影响
Fig.2 Effect of different temperatures on bacteriostatic activity of extracts from Capparis spinosa L.
注:图中不同小写字母表示差异显著(下同)
2.3.2 不同紫外光照射时间对刺山柑萃取物抑菌活性的影响
由图3可知,在经过不同时间紫外光照射之后,刺山柑乙酸乙酯萃取物对枯草芽孢抑菌圈直径差异不显著(P<0.05);对金黄色葡萄球抑菌圈直径与空白对照组相比差异均不显著(P<0.05);对大肠杆菌抑菌圈直径在0~25 min先增大后减小;刺山柑正丁醇萃取物对枯草芽孢杆菌的抑菌圈直径在10~25 min先减小后增大;对金黄色葡萄球菌抑菌圈直径在0~10 min时减小,10~15 min增大,15~20 min时减小,20~25 min增大;对大肠杆菌的抑菌圈直径在10~15 min时增大,15~30 min时与空白对照组相比差异显著(P<0.05)。由此可见,刺山柑乙酸乙酯、正丁醇萃取物中某些抑菌活性成分对紫外光照较为敏感。于洋[29]、任远[20]从乙酸乙酯萃取物中分离出9种单体化合物,包括5种酚酸类化合物,如香草酸、对羟基苯甲酸、原儿茶酸等,可能是由于萃取物中的这些酚类物质见光易分解,使其抑菌活性减弱。
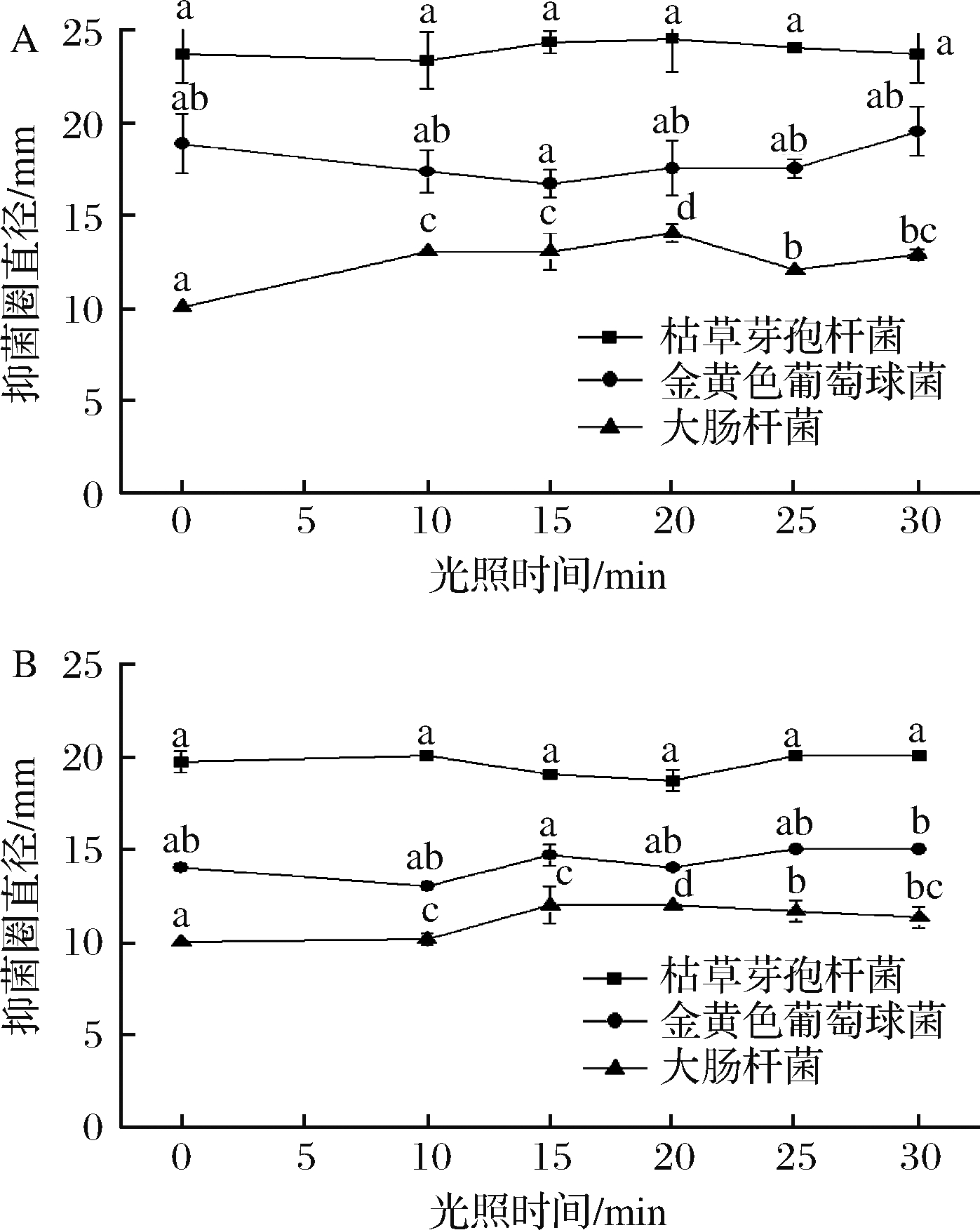
A-刺山柑乙酸乙酯萃取物;B-刺山柑正丁醇萃取物
图3 不同紫外光照射时间对刺山柑萃取物抑菌效果的影响
Fig.3 Effect of different ultraviolet irradiation time on the bacteriostatic effect of extracts from Capparis spinosa L.
2.3.3 不同pH对刺山柑萃取物抑菌活性的影响
由图4可知,在经过酸碱处理后,刺山柑乙酸乙酯萃取物对枯草芽孢杆菌和金黄色葡萄球菌抑菌圈直径在pH=3~5时减小,pH=5~7时增大,pH=7~11时急剧减小,当pH=7(空白对照组)时,未经酸碱处理的刺山柑乙酸乙酯萃取物对枯草芽孢杆菌及金黄色葡萄球菌的抑菌圈直径与其他pH相比差异显著(P<0.05);对大肠杆菌抑菌圈直径pH=3时,与空白对照组相比差异显著(P<0.05);刺山柑正丁醇萃取物对枯草芽孢杆菌抑菌圈直径在pH=9~11时减小;对金黄色葡萄球菌在pH=5~11时逐渐减小;对大肠杆菌在pH=9~11时丧失了抑菌活性。综上所述,乙酸乙酯和正丁醇萃取物对pH不稳定,可能是由于萃取物中的某些酚酸类物质在自然情况下呈酸性,pH的降低能引起其所带酚羟基电离度变小,疏水性增强,使其抑菌效果增强,而在碱性环境下萃取物中的酚酸类物质会发生水解生成醌类,从而引起抑菌活性能力的减弱[30]。

A-刺山柑乙酸乙酯萃取物;B-刺山柑正丁醇萃取物
图4 不同pH对刺山柑萃取物抑菌效果的影响
Fig.4 Effect of different pH on antibacterial activity of extracts from Capparis spinosa L.
3 结论
本文对比了刺山柑4种不同极性溶剂萃取物的抑菌活性并模拟了食品体系中主要因素对萃取物抑菌活性的影响,通过对抑菌圈直径及最小抑菌浓度的测定,得出抑菌活性主要集中在乙酸乙酯及正丁醇萃取物中;乙酸乙酯及正丁醇萃取物对温度、紫外光照射、pH不稳定,但在一定范围内,有助于促进萃取物的抑菌活性。本研究为刺山柑萃取物应用于食品防腐、抑菌提供了理论依据,但对刺山柑萃取物中有效抑菌成分的明确、抑菌机理及毒理学评价等方面还有待进一步研究。
[1] 张正海,董艳,姬妍茹,等.汉麻叶提取物抑菌活性及抑菌稳定性研究[J].食品安全质量检测学报,2019,10(4):927-933.
[2] 耿东升,邬建杰,梁敬军.刺山柑的化学成分和药理研究[J].解放军药学学报,2007,23(5):369-371.
[3] 杨涛,刘玉琴,王长虹,等.刺山柑的化学成分、药理活性与临床应用研究进展[J].中国中药杂志,2008,33(21):2 453-2 458.
[4] 甘永祥,陈文,王新春,等.刺山柑果实的化学成分[J].石河子大学学报(自然科学版),2009,27(3):335-336.
[5] 谢丽琼,薛淑媛,颜雪,等.维药刺山柑化学成分和药理研究进展[J].西北药学杂志,2007,22(4):225-226.
[6] 罗俊,谢阳.维药刺山柑果治疗痛风风湿病15例[J].中国民族医药杂志,1999,5(2):3.
[7] 任解莉.老鼠瓜单味外用治疗肩周炎121例[J].新疆中医药,2002,20(4):133.
[8] 周文涛,周晓涛,孟栋红,等.维药槌果藤及传统中药对佐剂型关节炎大鼠模型组织中TNF-α及血清中IL-17a表达水平的影响——第十二届全国免疫学学术大会摘要汇编[C].天津:中国免疫学会,2017:426.
[9] 杨涛,程雪梅,于富生,等.刺山柑果实的化学成分研究[J].西北药学杂志,2010,25(4):260-263.
[10] EL AZHARY K,JOUTI N T,EL KHACHIBI M,et al.Anti-inflammatory potential of Capparis spinosa L. in vivo in mice through inhibition of cell infiltration and cytokine gene expression[J].BMC Complementary and Alternative Medicine,2017,17(1):81-83.
[11] 周海凤,乐心逸,王娴娴,等.刺山柑果实精制提取物抗类风湿关节炎的实验研究[J].实验动物与比较医学,2018,38(3):227-230.
[12] 包晓玮,韩海霞,张青梅,等.刺山柑总黄酮对大鼠佐剂性关节炎的药效学研究[J].华西药学杂志,2012,27(4):458-460.
[13] JIMÉNEZ-L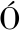 PEZ J,RUIZ-MEDINA A,ORTEGA-BARRALES P,et al.Phytochemical profile and antioxidant activity of caper berries (Capparis spinosa L.):Evaluation of the influence of the fermentation process[J].Food Chemistry,2018,250:54-59.
PEZ J,RUIZ-MEDINA A,ORTEGA-BARRALES P,et al.Phytochemical profile and antioxidant activity of caper berries (Capparis spinosa L.):Evaluation of the influence of the fermentation process[J].Food Chemistry,2018,250:54-59.
[14] 徐琦,马梦佳,关晔华,等.维药刺山柑对大肠杆菌生物膜的作用研究——中国转化医学和整合医学研讨会(广州站)论文综合刊[C].广州:中国转化医学和整合医学研究会、中华高血压杂志社,2015:2.
[15] MAHASNEH A M.Screening of some indigenous Qatari medicinal plants for antimicrobial activity[J].Phytotherapy Research,2002, 16(8):751-3.
[16] ALI-SHTAYEH M S,ABU GHDEIB S I.Antifungal activity of plant extracts against dermatophytes[J].mycoses,1999,42(11-12):665-672.
[17] EDDOIKS M,LEMHADRI A,MICHEL J B.Hyperlipidemic activity of aqueous extract of Capparis spinosa L.in normal and-diabetic rats[J].Journal of Ethnopharmacol,2005,98(3):345-350.
[18] 喻建军,戴畅,李建军.刺山柑提取物降血脂作用动物试验研究[J].中兽医医药杂志, 2010,29(1):30-31.
[19] KALANTARI H,FORUOZANDEH H,KHODAYAR M J,et al.Antioxidant and hepatoprotective effects of Capparis spinosa L. fractions and Quercetin on tert-butyl hydroperoxide-induced acute liver damage in mice[J].Journal of Traditional and Complementary Medicine, 2018, 8(1): 120-127.
[20] 任远.维药刺山柑果实化学成分及其生物活性的研究[D].乌鲁木齐:新疆医科大学,2010.
[21] 綦国红,陈金辉,陈贵堂.肉桂提取物对铜绿假单胞菌生物膜产生的抑制作用研究[J].食品与生物技术学报,2018,37(8):29-33.
[22] 李敏.五倍子提取物抑菌效果及稳定性研究[J].氨基酸和生物资源,2016,38(3):48-52.
[23] 吴永祥,程满怀,江海涛,等.白及萃取物的抑菌活性及其二氯甲烷萃取物化学成分分析[J].食品与机械,2017,33(12):76-79.
[24] 王建军,赵宝玉,张为民,等.茎直黄芪提取物的体外抑菌作用[J].西北农业学报,2007,16(2):108-112.
[25] 张正海,董艳,姬妍茹,等.汉麻叶提取物抑菌活性及抑菌稳定性研究[J].食品安全质量检测学报,2019,10(4):927-933.
[26] 刘海燕,张建伟.明日叶提取物抑菌活性成分稳定性的研究[J].食品研究与开发,2016,37(10):39-42.
[27] 周怡,陈雅婷,王奇志,等.假臭草和胜红蓟提取物抑菌活性及稳定性研究[J].热带农业科学,2018,38(3):81-86.
[28] VAARA M.Agents that increase the permeability of the outer membrane[J].Microbiological Reviews,1992,56(3):395-411.
[29] 于洋.刺山柑化学成分的研究[D].沈阳:沈阳药科大学,2007.
[30] 赵磊,文轩,迟茜等.甜叶菊废渣提取物抑菌活性及抑菌稳定性研究[J].食品工业科技,2016,37(24):168-172.