氰化物是一种剧毒物质,在所有的氰化物中,氰化氢的毒性最大,CN-能够抑制细胞色素C氧化酶的活性,阻断呼吸链使组织缺氧,进而产生乳酸等大量酸性物质,最终导致代谢性酸中毒从而引起一系列神经系统症状[1]。白酒中氰化物的主要来源与其制作原料有关,如木薯、豆类、高粱等食物中都有氰苷的存在。食用植物中的氰化物多以氰苷配糖体形式存在,其种类有苦杏仁氰苷、亚麻氰苷、棉豆氰苷等[2],氰苷在发酵过程中水解产生HCN。因此,氰化物是酒类的一项重要监测指标,其检测结果的准确性对白酒质量安全有重要意义。
目前,白酒中氰化物的检测方法有化学分析法、分光光度法、色谱法、原子吸收法[3]。而GB 5009.36—2016食品安全国家标准 食品中氰化物的测定中规定了2种定量方法(分光光度法、气相色谱法)和1种定性方法,本文根据白酒氰化物的判定标准GB 2757—2012食品安全国家标准 蒸馏酒及其配制酒对GB 5009.36—2016第一法分光光度法测量白酒中氰化物方法进行了系统、完整的不确定度评定,分析整个实验过程中的不确定度来源,并分别进行计算,通过各个分量在整体不确定度中的占比,分析其对最终检测结果的影响,为调整实验过程进行指导,有效减少实验结果的误差,确保测量结果的准确度。
1 材料与方法
1.1 方法依据
测量依据GB 5009.36—2016 食品安全国家标准 食品中氰化物的测定中第一法分光光度法[4],在碱性条件下加热除去高沸点有机物,然后在pH=7.0条件下,CN-与氯胺-T反应生成CICN,CICN再与异烟酸作用,水解后生成戊烯二醛,最后与吡唑酮缩合成蓝色染料[5],与标准系列比较定量。该标准未规定测定时样品的温度,参照GB 5009.225—2016 食品安全国家标准 酒中乙醇浓度的测定[6]中的要求,统一规定为在20 ℃下样品中氰化物的含量。
1.2 试剂与仪器
白酒样品使用45%vol优级浓香型白酒;实验室环境温度(20±2) ℃。水中氰成分分析标准物质(标准物质编号GBW(E)080115),ρ(CN-)=50.0 μg/mL,相对扩展不确定度Ur=1%。
Cary 60 UV—Vis紫外可见分光光度计,安捷伦科技有限公司;SCG-4恒温水浴锅(精密度0.1 ℃),宁波新型生物。具塞比色管(10 mL);单标吸量管(2 mL);流出式分度吸量管(1、2 mL);容量瓶(100 mL)(A级)。
1.3 测定方法
1.3.1 标准使用溶液配制
取2 mL水中氰成分分析标准物质,用2 g/L NaOH溶液定容至100 mL容量瓶中,标准使用溶液质量浓度为1.00 μg /mL。
1.3.2 标准溶液系列配制
用分度吸量管分别吸取1.00 μg/mL标准使用溶液0、0.4、0.8、1.2、1.6、2.0 mL于10 mL具塞比色管中,加2 g/L NaOH至5 mL。
1.3.3 样品处理
吸取1.0 mL试样于50 mL烧杯中,加入5 mL 2 g/L NaOH溶液,混匀后放置10 min,然后放于120 ℃电加热板上加热至溶液剩余约1 mL,取下放至室温,用2 g/L NaOH溶液转移至10 mL具塞比色管中,最后加2 g/L NaOH至5 mL。
1.3.4 显色测定过程
于试样及标准管中分别加入2滴酚酞指示剂,加入体积分数为4%的乙酸溶液调至红色褪去,再用2 g/L NaOH溶液调至近红色,然后加2 mL磷酸盐缓冲溶液(0.5 mol/L,pH=7.0),放入25~30 ℃水浴中10 min,再加入0.2 mL氯胺-T溶液(10 g/L),摇匀放置3 min,加入2 mL异烟酸-吡唑啉酮溶液(异烟酸溶液Ⅰ:称取1.5 g异烟酸溶于24 mL 20 g/L NaOH溶液中,加水至100 mL;吡唑啉酮溶液Ⅱ:称取0.25 g吡唑啉酮,溶于20 mL无水乙醇中。使用时将溶液Ⅰ、Ⅱ按体积比5 ∶1混合[7]),加水稀释至刻度,加塞振荡混合均匀,在37 ℃恒温水浴锅中放置40 min,取出冷却至室温。用1 cm 比色皿以空白管调节零点,于638 nm处测量吸光度。标准系列各点及样品溶液分别测量3次。
1.4 样品测量数据及计算结果
样品测量数据及测量结果如表1所示。
表1 样品测量数据及测量结果
Table 1 Sample measurement data and measurement results
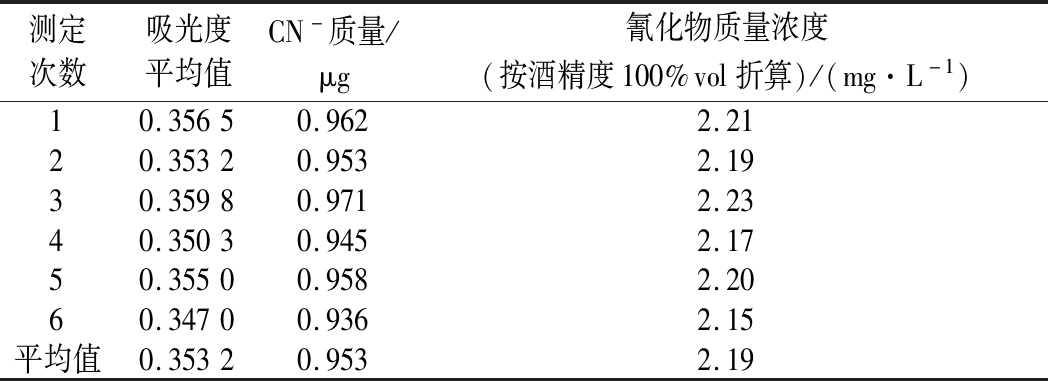
测定次数吸光度平均值CN-质量/μg氰化物质量浓度(按酒精度100%vol折算)/(mg·L-1)10.35650.9622.2120.35320.9532.1930.35980.9712.2340.35030.9452.1750.35500.9582.2060.34700.9362.15平均值0.35320.9532.19
2 数学模型建立及测量不确定度来源分析
2.1 白酒氰化物计算
根据白酒氰化物的判定标准GB 2757—2012食品安全国家标准 蒸馏酒及其配制酒中氰化物(以HCN计)质量浓度≤8.0 mg/L,且按酒精度100%vol折算[8],将GB 5009.36—2016中计算修改为公式(1):
(1)
式中:X,白酒样品中氰化物质量浓度(以HCN计)(按酒精度100%vol折算),mg/L;c,样品溶液中氰根的质量,μg;V,样品体积,mL;27.0,HCN摩尔质量的数值,g/mol;26.0,CN- 摩尔质量的数值,g/mol;100,换算为酒精度100%vol,%vol;E,白酒样品实际酒精度,%vol;R,回收率,%。
2.2 测量不确定度来源分析
分光光度计检测溶液的吸光度与溶液中目标物的浓度成正比,因此显色液的定容体积也是测量不确定度的一个分量,将其合并至标准溶液系列和样品溶液质量含量的不确定度评定中,标准溶液和样品溶液浓度不确定度模型如公式(2)、公式(3)所示:
c标 =f(c1,V3,V4)
(2)
c=f′(c标,c拟,V2)
(3)
式中:c1, 氰标准使用液浓度;V3,吸取氰标准使用液的体积;V4,标准溶液系列的定容体积;c拟,标准溶液系列曲线拟合;V2,样品溶液显色定容体积。
因此样品不确定度的测量模型如公式(4)所示:
X=F(c,V1,MHCN,MCN-,E,R)
(4)
式中:c,样品溶液中氰化物的质量,μg;V1,样品取样体积,mL;MHCN,HCN摩尔质量的数值,g/mol;MCN-,CN- 摩尔质量的数值,g/mol;E,白酒样品实际酒精度,45.2 %vol;R,回收率,%。
根据测量模型,将模型中样品溶液中氰化物质量的不确定度分量按照JJF1059.1—2012 测量不确定度评定与表示[9]要求展开,分光光度法测量白酒中氰化物含量的不确定度因果分析如图1所示。

图1 氰化物测定不确定度来源
Fig.1 A graphical representation of the source of uncertainty in cyanide determination
3 测量不确定度评定
3.1 评定A类不确定度
A类不确定度就是测量重复性的不确定度,等于测量结果平均值的标准偏差[10]。6次测量结果的标准偏差、测量平均值的标准偏差、相对不确定度为:
![]()
![]() 即
即![]()
3.2 评定样品吸取体积的不确定度u(V1)
3.2.1 单标吸量管容量引入的不确定度u1(V1)
1 mL A级单标吸量管容量允差为±0.007 mL[11],按均匀分布![]() 得:
得:
3.2.2 温度波动对单标吸量管引入的不确定度u2(V1)
45%vol白酒的体积膨胀系数根据《新编酒精密度浓度和温度常数数据表》[12]中表Ⅱ“酒精溶液密度与温度和体积浓度关系表”, 45%vol酒精在20 ℃附近的密度如表2所示。
表2 45%vol酒精在不同温度下的密度
Table 2 Density of 45%vol alcohol at different temperatures
温度/℃1819202122密度/(g·L-1)940.97940.26939.54938.82938.10
根据表2求得,45%vol酒精溶液体积膨胀系数为7.7×10-4/℃,实验室环境温度变化为(20±2)℃,其波动按均匀分布![]() 则温度波动产生的不确定度为:
则温度波动产生的不确定度为:
3.2.3 取样体积不确定度u(V1)的合成
容量允差和温度对取样体积产生的不确定度是互相独立的,根据公式合成得到取样体积的不确定度和相对不确定度为:
3.3 样品溶液显色定容体积的不确定度u(V2)
3.3.1 比色管容量允差引入的不确定度u1(V2)
10 mL比色管容量允差[13]为±0.10 mL,按均匀分布![]() 得:
得:
![]()
3.3.2 温度波动引入的不确定度
样品测定与标准系列配制在同一室温下进行,温度稳定,操作时间较短,温度变化较小,可忽略温度波动所带来的影响,下文中标准曲线各点配制过程中的定容体积也忽略了温度波动对体积的影响。因此得到定容体积的不确定度和相对不确定度为:
u(V2)= u1(V2)=0.057 7 mL
3.4 标准溶液系列配制引入的不确定度u(c标)
3.4.1 标准使用溶液配制引入的不确定度u(c1)
3.4.1.1 水中氰成分分析标准物质(储备液)引入的不确定度u1(c1)
查证书得相对扩展不确定度为1%(k=2),相对不确定度为:
3.4.1.2 吸取标准物质(储备液)引入的不确定度u2(c1)
2 mL A级单标吸量管的容量允差为±0.010 mL[11],按均匀分布![]() 得:
得:
温度波动对2 mL A级单标吸量管引入的不确定度u22(c1),实验室环境温度变化为(20±2)℃,储备液膨胀系数取水的膨胀系数为2.1×10-4/℃,温度波动按均匀分布![]() 则温度波动产生的不确定度和相对不确定度为:
则温度波动产生的不确定度和相对不确定度为:
3.4.1.3 定容体积引入的不确定度u3(c1)
A级100 mL容量瓶容量允差为±0.10 mL[11],按均匀分布![]() 得:
得:
3.4.1.4 标准使用溶液配制相对不确定度的合成
标准使用溶液配制相对不确定度为:
3.4.2 标准溶液系列配制引入的不确定度u(V标)
标准系列各个点的配制过程引入的不确定度主要由分度吸量管容量允差、比色管定容和温度组成,而温度在较短时间内变化较小,故忽略温度对其的影响。
标准系列吸取体积分别(V3)为0、0.4、0.8、1.2、1.6、2.0 mL,按均匀分布![]() 按照公式
按照公式![]() 计算取液体积不确定度,如表3所示。
计算取液体积不确定度,如表3所示。
A级1、2 mL流出式分度吸量管容量允差分别为±0.008 mL、±0.012 mL[11],当吸取0.4和1.2 mL时,根据GB 12807—1991实验室玻璃仪器 玻璃量器[14]标准要求,应当将其容量允差减半后再进行计算,按均匀分布![]() 公式
公式![]() 进行计算。10 mL比色管容量允差为±0.10 mL[13],按均匀分布
进行计算。10 mL比色管容量允差为±0.10 mL[13],按均匀分布![]() 具体结果如表3所示。
具体结果如表3所示。
表3 各浓度的不确定度及其分量计算结果
Table 3 Uncertainty of each concentration and calculation results of its components

标准系列标准使用液不确定度移液管吸取体积(容量允差)吸取体积不确定度ur(V3)定容体积不确定度ur(V4)合成相对不确定度00.0058100000.40.005810.4(±0.004)0.005770.005770.01000.80.005810.8(±0.008)0.005770.005770.01001.20.005811.2(±0.006)0.002890.005770.008681.60.005811.6(±0.012)0.004330.005770.0092620.005812.0(±0.012)0.003460.005770.00889
3.4.3 标准溶液系列配制不确定度的合成
按每个浓度相对不确定度算术平方和开方得到[15]不确定度为:
ur(c)=
3.5 拟合标准曲线引入的不确定度u(c拟)
标准溶液系列共6个浓度,每个浓度测量3次,得到线性方程为A=0.366 8 m+0.003 65,R2=0.999 8,在测量范围内,吸光度值对CN-线性关系良好;每份样品溶液测量3次,以吸光度平均值计算溶液中氰根质量。由表1可知样品溶液氰根的平均质量为0.953 μg。标准溶液系列具体测量结果如表4所示。
表4 标准系列各点吸光度的测量值
Table 4 measurement values of absorbance at each point in the standard series
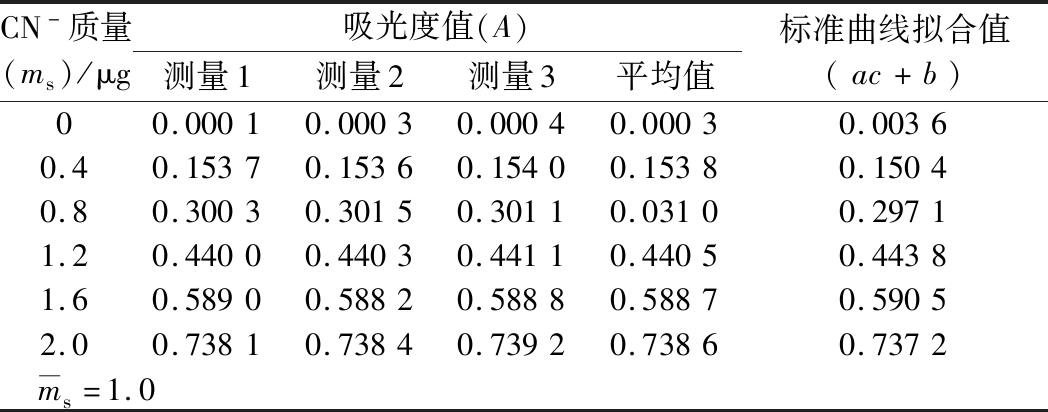
CN-质量(ms)/μg吸光度值(A)测量1测量2测量3平均值标准曲线拟合值(ac+b)00.00010.00030.00040.00030.00360.40.15370.15360.15400.15380.15040.80.30030.30150.30110.03100.29711.20.44000.44030.44110.44050.44381.60.58900.58820.58880.58870.59052.00.73810.73840.73920.73860.7372m—s=1.0
样品溶液由拟合曲线引入的不确定度[16]为:
式中,s(Ar)为标准曲线峰面积比的残差,s(Ar)=0.003 20;a为标准曲线的斜率,a=0.366 8;P为样品溶液的测量次数,P=3;N为标准溶液总测量次数,N=6×3=18;m为样品溶液平均值,μg;mi为标准溶液浓度,![]() 标准溶液浓度的平均值,μg。
标准溶液浓度的平均值,μg。
标准曲线峰面积比的残差计算为:
式中:Ai为标准溶液吸光度;M为标准溶液曲线点数,M=6;n为标准溶液每点测量次数,n=3。
拟合标准曲线引入的相对不确定度为:
3.6 白酒酒精度不确定度的评定u(E)
酒中酒精度测定的不确定度的来源主要有酒精度的测量重复性、容量瓶取样和蒸馏后的定容体积、蒸馏液20 ℃下密度的测定、酒精度测量结果的修约,具体评定过程见《密度瓶法测量白酒中酒精度的不确定度评定》[17],评定结果为酒精度45.2%vol,扩展不确定度u(E) =0.1%vol,相对不确定度为:
3.7 评定摩尔质量比值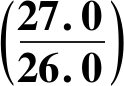 的不确定度u(M比)
的不确定度u(M比)
公式(1)中HCN和CN-摩尔质量一般修约为3位有效数字,分别是27.0和26.0,摩尔质量比值应看做![]() 不能认为M(HCN)和M(CN-)是相互独立的,需按模型
不能认为M(HCN)和M(CN-)是相互独立的,需按模型![]() 综合评定摩尔质量比值
综合评定摩尔质量比值![]() 的不确定度。灵敏系数为:
的不确定度。灵敏系数为:
元素的标准不确定度的计算按均匀分布[18],即![]() 在一般应用中,以a,b平均值为元素的原子量值。具体数值如表5所示。
在一般应用中,以a,b平均值为元素的原子量值。具体数值如表5所示。
表5 国际原子量数值及其标准不确定度
Table 5 international atomic weight values and their standard uncertainties
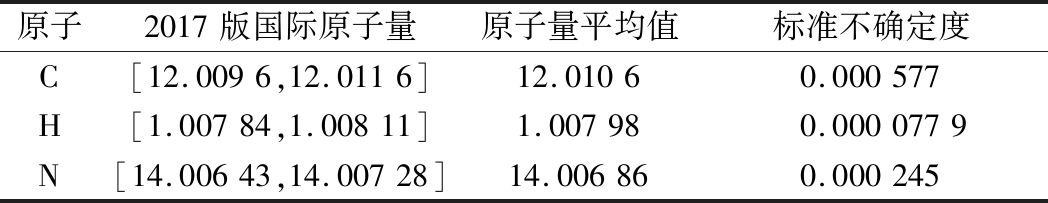
原子2017版国际原子量原子量平均值标准不确定度C[12.0096,12.0116]12.01060.000577H[1.00784,1.00811]1.007980.0000779N[14.00643,14.00728]14.006860.000245
M(H+)、M(CN-)的不确定度由原子量和数据修约2部分组成, H+、CN-修约为3位有效数字,其中M(CN-)的不确定度由C和N两部分组成,不确定度计算结果如表6所示:
表6 M(H+)、M(CN-)不确定度计算结果
Table 6 uncertainty calculation results of M(H+)、M(CN-)

M(i)M(H+)M(CN-)原子量引入的不确定度 0.00007790.000627数据修约引入的不确定度0.02890.0289合成不确定度 0.02890.0289
不确定度和相对不确定度为:
0.001 11
3.8 加标回收率R的不确定度评定
平均回收率![]() 的不确定度
的不确定度![]() 由测量结果平均值的标准偏差和加标标准物质两部分组成[19-20]。
由测量结果平均值的标准偏差和加标标准物质两部分组成[19-20]。
加标试验的具体过程:吸取水中氰成分分析标准物质溶液1.00 mL于100 mL容量瓶中,并用体积分数为45%的乙醇溶液定容,摇匀,即加标物质溶液浓度为0.5 μg/mL,后续测定过程同1.3,分别进行6次加标回收实验,测定结果如表7所示。
表7 回收率试验结果
Table 7 Results of recovery rate test

测量次数加标量(Xs)/μg测定结果(yi)/μg测定结果平均值(y-)/μg回收率(R)/%回收率平均值(R-)/%10.50.501100.220.50.49699.230.50.4900.49398.098.640.50.48797.450.50.49398.660.50.49298.4
3.8.1 平均回收率测量重复性引入的不确定度u(xs)
测定结果重复性引入的不确定度![]() 直接以平均回收率的标准偏差进行计算:测量平均值的标准偏差为
直接以平均回收率的标准偏差进行计算:测量平均值的标准偏差为![]() 即
即![]() 相对不确定度为:
相对不确定度为:
3.8.2 加标标准物质引入的不确定度u(xs)
加标标准物质引入的不确定度有水中氰成分分析标准物质(储备液)、吸取标准溶液、定容体积,具体评定过程参考3.4.1。
水中氰成分分析标准物质(储备液)、吸取标准溶液定容体积相对不确定度分别为:
![]()
加标标准物质引入的不确定度合成为:
3.8.3 平均回收率![]() 的不确定度
的不确定度![]()
平均回收![]() 的不确定度为:
的不确定度为:
3.8.4 回收率R显著性检验
在95%置信区间下包含因子k=2,若T=︱![]() ︱≤k,则实际回收率与1之间无显著性差异,若T=︱
︱≤k,则实际回收率与1之间无显著性差异,若T=︱![]() ︱>k,则实际回收率与1之间有显著性差异[21]。通过计算得出T=1.87<2,因此,回收率与1(100%回收)没有显著差异,可不必用回收率校正结果,样品测量结果也不必评定回收率不确定度。
︱>k,则实际回收率与1之间有显著性差异[21]。通过计算得出T=1.87<2,因此,回收率与1(100%回收)没有显著差异,可不必用回收率校正结果,样品测量结果也不必评定回收率不确定度。
3.9 评定标准测量不确定度
根据评定过程可知,氰化物测量重复性、样品的取样体积、样品的定容体积、标准溶液系列、标准曲线拟合、酒精度折算及摩尔质量这7部分互相独立,因此合成相对不确定为:
=0.013 7
4 扩展不确定度及不确定度报告
取包含因子k=2,U=k×ur×X=2×0.013 7×2.19=0.06 mg/L,白酒中氰化物报告:X=(2.19±0.06)mg/L,k=2,各类相对不确定度主要分量及贡献如表8及图2所示。
5 结论
通过对白酒氰化物分光光度检测方法不确定度的评定,当测量结果为2.19 mg/L时,扩展不确定度为0.06 mg/L,通过此次评定,可以得出标准溶液系列配制引入的不确定度分量是该测量结果不确定度中占比最大的,因此在实验过程中,对于标准溶液系列配制时要严格按照实验要求规范操作,降低其引入的不确定度,确保检测结果的准确性。

图2 各类不确定度主要分量占比
Fig.2 Schematic diagram of the proportion of major components of various uncertainties
表8 各类相对不确定度主要分量及贡献
Table 8 Major components and contributions of various relative uncertainties
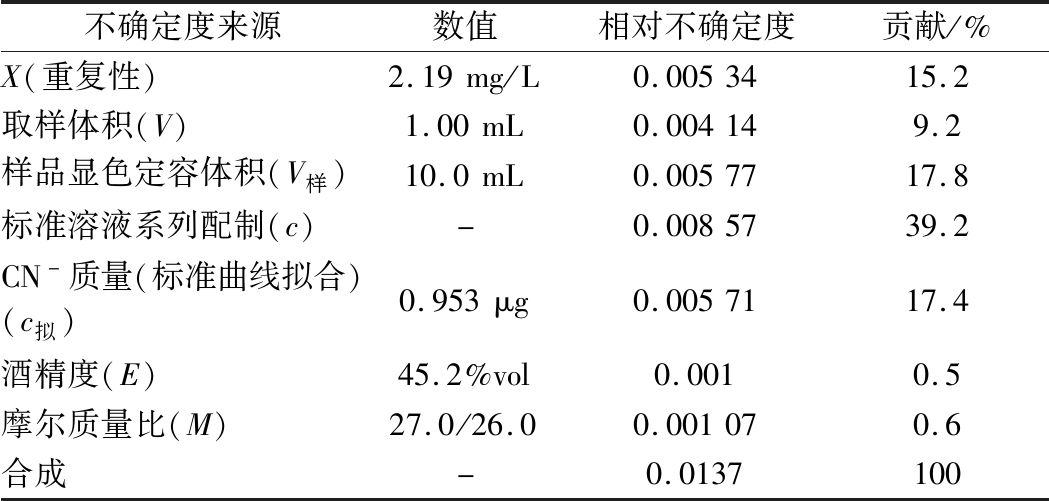
不确定度来源数值相对不确定度贡献/%X(重复性)2.19mg/L0.0053415.2取样体积(V)1.00mL0.004149.2样品显色定容体积(V样)10.0mL0.0057717.8标准溶液系列配制(c)-0.0085739.2CN-质量(标准曲线拟合)(c拟)0.953μg0.0057117.4酒精度(E)45.2%vol0.0010.5摩尔质量比(M)27.0/26.00.001070.6合成-0.0137100
注:-代表无
[1] 左晨艳,杨波波,吴婷,等.氰化物中毒及解毒的研究进展[J].毒理学杂志,2016,30(4):311-316.
[2] 郭忠,张文德.食品中的氰化物来源及其安全性的研究进展[J].中国食品卫生杂志,2014,26(4):404-408.
[3] 王欢,张义明,彭小东,等.白酒中氰化物的研究进展[J].酿酒科技,2017(8):112-115.
[4] GB 5009.36——2016 食品安全国家标准 食品中氰化物的测定[S].北京:中国标准出版社,2016.
[5] 李腾,黄桂兰,袁铃,等. 氰化物分析研究进展[J]. 化学分析计量,2017,26(2):115-119.
[6] GB 5009.225—2016 食品安全国家标准 酒中乙醇浓度的测定[S].北京:中国标准出版社,2016.
[7] 王超,刘倩倩,刘楚楚,等. 白酒中氰化物测定所用异烟酸-吡唑啉酮溶液配制方法的探讨[J]. 酿酒,2017,44(5):79-82.
[8] GB 2757—2012 食品安全国家标准 蒸馏酒及其配制酒[S].北京:中国标准出版社,2012.
[9] JJF1059.1—2012 测量不确定度评定与表示[S].北京:中国标准出版社,2012.
[10] CNAS-GL05—2011 测量不确定度要求的实施指南[S].北京:中国标准出版社,2011.
[11] 国家质量技术监督局.JJG 196—2006常用玻璃量器检定规程[S].北京:中国计量出版社,2006.
[12] 李兴华,陈大舟,徐彦发.新编酒精密度浓度和温度常用数据表[M].北京:中国计量出版社,2008:9.
[13] JJG 10—2005, 专用玻璃量器[S].北京:中国标准出版社,2005.
[14] GB 12807—1991, 实验室玻璃仪器 分度吸量管[S].北京:中国标准出版社,1991.
[15] JJF 1135—2005, 化学分析测量不确定度评定[S].北京:中国标准出版社,2005.
[16] 杨铭.CNAS-GL28 石油石化领域理化检测测量不确定度的评估指南用实例[M].北京:中国计量出版社,2010.
[17] 王开宇,张露月,都芸,等.密度瓶法测量白酒中酒精度的不确定度评定[J].酿酒科技,2019(7):104-109.
[18] ANON Interpreting and propagating the uncertainty of the standard atomic weights(iupac technical report)[J].Chemisty International The News Magzine of IUPAC,2018,40(2):42.
[19] 李慎安. 回收率及其不确定度[J]. 中国计量,2007(1):89-90.
[20] 刘庆,万力,王新平,等. 如何评估回收率测量结果不确定度[J]. 中国测试,2015,41(S1):82-84.
[21] 卢晓华. 标准物质在化学测量结果不确定度评定中的应用举例[J]. 中国计量,2008(1):68-69.