褐色酸奶是近两年兴起的酸奶品类,与普通酸奶的区别主要是在配料中添加了还原糖,经长时间的高温热处理后,形成的一种具有褐色并伴有焦甜风味的酸奶,所以又称熟酸奶、烤酸奶、碳烧酸奶或俄罗斯风味酸奶[1]。褐色酸奶独特的颜色和风味来源于美拉德反应,主要指氨基化合物和羰基化合物之间经交叉、分解、缩合、聚合生成棕色或黑色聚合物的过程,故又称羰氨反应,是所有食品加工过程中都可能发生的一种非酶褐变反应[2]。乳中的美拉德反应主要经过3个阶段,各阶段中产生的物质即为美拉德反应产物[3-4],国内外学者对乳品体系中的美拉德反应产物的研究主要针对美拉德反应产物的抗氧化特性及安全性等进行报道。李光磊[5]研究了蔗糖和氨基酸模拟体系中美拉德反应健康危害物的产生规律,发现生成美拉德反应产物的种类与氨基酸的种类有显著关系,其中在谷氨酸体系中产生的5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)和丙酮醛(methylgyoxal,MGO)等物质含量最高。I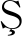 IL等[6]研究了超高温杀菌乳中产生的二羰基化合物、羟甲基糠醛和糠氨酸等美拉德反应产物含量主要受乳中强化成分的影响,它们在乳糖水解乳中的产物含量较高。ANNE等[7]研究发现,超高温脱脂和全脂牛奶在不同温度下贮藏24周,其美拉德反应的相关参数变化不同,中间阶段对温度变化最敏感。NARANJO等[8]研究了乳糖水解乳粉和含碳水化合物混合体系的美拉德反应动力学,发现水分活度和温度影响储存期间产品品质的变化,尤其是影响有效赖氨酸的含量,控制储存温度有利于产品的储存稳定性。HAN等[9]对棕色发酵乳生产和储存过程中潜在的有害美拉德反应产物丙烯酰胺和甲基乙二醛等进行研究,发现产物的形成和变化受多种因素影响,其中乳酸菌菌种的选择对提高发酵乳品质具有重要意义。
IL等[6]研究了超高温杀菌乳中产生的二羰基化合物、羟甲基糠醛和糠氨酸等美拉德反应产物含量主要受乳中强化成分的影响,它们在乳糖水解乳中的产物含量较高。ANNE等[7]研究发现,超高温脱脂和全脂牛奶在不同温度下贮藏24周,其美拉德反应的相关参数变化不同,中间阶段对温度变化最敏感。NARANJO等[8]研究了乳糖水解乳粉和含碳水化合物混合体系的美拉德反应动力学,发现水分活度和温度影响储存期间产品品质的变化,尤其是影响有效赖氨酸的含量,控制储存温度有利于产品的储存稳定性。HAN等[9]对棕色发酵乳生产和储存过程中潜在的有害美拉德反应产物丙烯酰胺和甲基乙二醛等进行研究,发现产物的形成和变化受多种因素影响,其中乳酸菌菌种的选择对提高发酵乳品质具有重要意义。
美拉德反应进程受pH、水分活度、储存温度和时间以及产品理化成分的影响[10]。本研究主要通过测定市售褐色酸奶在4和10 ℃储存温度下储存21 d,期间美拉德反应在不同阶段产物糠氨酸、5-HMF、MGO、乙二醛(glyoxal,GO)以及2,3-丁二酮的含量变化,研究褐色酸奶在储藏过程中美拉德反应副产物的形成规律,以期控制褐色酸奶在储存过程中潜在有害产物的生成,提高褐色酸奶的质量和安全性。
1 材料和方法
1.1 试剂与设备
糠氨酸盐酸盐标准品,上海安谱实验科技有限公司;5-HMF标准品,上海摩贝试剂公司;MGO、GO、2,3-丁二酮标准品,美国Sigma公司;甲醇(色谱纯)、乙腈(色谱级)、甲酸(色谱纯)、三氟乙酸(色谱纯)、乙酸铵、浓盐酸,北京国药有限公司;褐色酸奶,北京幸福荣耀超市。
色差仪(Minolta CR-400),日本柯尼卡美能达公司;酶标仪(SPARK 20M),美国Bio-Rad公司;电热恒温鼓风干燥箱(DHG-9123A),上海精宏实验设备有限公司;超高效液相色谱仪(YQ107-02),美国Waters公司。
1.2 样品制备
酸奶样品包括1种品牌的普通酸奶和5种品牌的褐色酸奶,均于产品生产后第2天购买。样品信息见表1。
表1 样品信息 单位:%
Table 1 Sample information sheet

编号添加糖种类发酵菌种蛋白质含量脂肪含量碳水化合物含量普通酸奶1(P1)聚葡萄糖嗜热链球菌、保加利亚乳杆菌2.83.55.5褐色酸奶1(H1)白砂糖、食用葡萄糖嗜热链球菌、保加利亚乳杆菌、副干酪乳杆菌2.83.414.3褐色酸奶2(H2)白砂糖、食用葡萄糖嗜热链球菌、保加利亚乳杆菌、乳双歧杆菌2.62.913.2褐色酸奶3(H3)白砂糖、食用葡萄糖乳酸乳球菌乳酸亚种、乳酸乳球菌乳脂亚种、嗜热链球菌、植物乳杆菌、鼠李糖乳杆菌2.62.912.5褐色酸奶4(H4)白砂糖、食用葡萄糖嗜热链球菌、保加利亚乳杆菌、乳酸乳球菌乳酸亚种2.63.013.8褐色酸奶5(H5)白砂糖、食用葡萄糖嗜热链球菌、保加利亚乳杆菌2.52.510.0
1.3 储存条件
将不同品牌的酸奶样品分别贮藏在4和10 ℃,在货架期内监测产品指标变化,贮藏时间设定为0、5、10、15、20 d,每种试样重复3次,共18个样品。
1.4 糠氨酸的测定
参照NY/T 939—2016《巴氏杀菌乳和UHT灭菌乳中复原乳的测定》,改变部分条件进行测定。试样经过盐酸水解后测定蛋白质含量,水解液经稀释后采用超高效液相色谱(ultra high performance liquid chromatography,UHPLC),在280 nm波长下测定牛乳中糠氨酸的峰面积,依据标准样品所制得的标准曲线对糠氨酸外标法定量。利用UHPLC在柱温35 ℃下用色谱柱HSS T3 (100 mm×4.6 mm,2.5 μm)高强度硅胶颗粒进行样品分离测定,0.1%三氟乙酸水溶液为流动相A,甲醇为流动相B,采用洗脱速度为0.5 mL/min进行梯度洗脱。
1.5 5-羟甲基糠醛的测定
按照NY/T 1332—2007《乳与乳制品中5-羟甲基糠醛含量的测定》中的高效液相色谱法(high performance liquid chromatography,HPLC)测定。分别吸取10.0 g牛奶样品于50 mL离心管中,向各样品离心管中加入5 mL草酸溶液混匀,80 ℃水浴加热30 min,冷却至室温,再加入10 mL甲醇混匀后加入3 mL亚铁氰化钾和3 mL乙酸锌混匀,振摇后静置15 min,然后将样液以6 000 r/min离心10 min,将上清液置于50 mL容量瓶中,沉淀中加入10 mL甲醇,再于6 000 r/min离心10 min,合并2次上清液,用滤纸过滤后用甲醇定容至50 mL,用0.22 μm有机滤膜过滤待测。采用C18柱(250 mm×4.6 mm,5 μm)在柱温30 ℃下以1 mL/min的流速和波长284 nm下进行HPLC的测定。
1.6 α-二羰基化合物的测定
采用UHPLC方法测定美拉德反应中期产物α-二羰基化合物中GO、MGO和2,3-丁二酮的含量。分别配制不同质量浓度的3种化合物的标准溶液,取1 mL进行衍生反应,加入10 mg/mL的邻苯二胺水溶液300 μL,在50 r/min 60 ℃水浴条件下反应30 min,冰水冷却后经过0.22 μm有机滤膜过滤,待仪器进行分析后,以目标物浓度为横坐标,对应的响应值为纵坐标,分别绘制目标物的线性标准曲线。吸取2 mL样品于15 mL离心管中,加入8 mL甲醇,涡旋振荡1 min,10 000×g离心15 min使蛋白沉淀,上清液备用。取3 mL上清液于密封棕色瓶中,加入400 μL 10 mg/mL邻苯二胺水溶液,60 ℃水浴振荡30 min。后经0.22 μm有机滤膜过滤,进行UHPLC检测。
1.7 颜色的测定
采用电子眼测量不同品牌褐色酸奶中美拉德反应的色泽差异。测定指标中的b*值,表示为黄蓝度,正值越大,表示黄蓝色越深,褐变反应越充分。样品重复测定3次。按公式(1)(2)进行计算:
(1)
(2)
式中:L*,亮度值;a*,红绿值;b*,黄蓝值;ΔE*,总色差;BI,褐变指数。
1.8 荧光强度的测定
利用酶标仪测定荧光强度,从而反映美拉德反应程度。先进行乳清蛋白的分离,取混匀后的酸奶样品0.5 g置于10 mL离心管中,加入4.5 mL pH 4.6的乙酸盐缓冲液,振荡后在4 000×g下离心10 min,使用滤纸过滤后,取0.5 mL上清液加4.5 mL超纯水,4 ℃下保存待测。测定高级美拉德产物荧光强度(fluorescence of advanced Maillard reaction products, FAMP)时,激发波长设定为360 nm,发射波长为440 nm。测定色氨酸荧光强度(fluorescence of tryptophan, FTrp)时,激发波长设定为290 nm,发射波长为340 nm。综合热损伤指数(fluorescence of advanced Maillard products and soluble tryptophan, FAST)反映了单位蛋白质中FAMP的相对含量,可以综合指示牛乳热处理损伤程度。按公式(3)计算FAST指数:
(3)
式中:FAST,综合热损伤指数;FAMP,高级美拉德反应产物荧光强度;FTrp,色氨酸荧光强度。
1.9 数据分析
所有实验数据均采用SPSS 18.5和Microsoft Excel 2016软件进行统计处理与作图分析。各实验均平行重复3次,试验结果以平均值±标准差表示。
2 结果与讨论
2.1 不同褐色酸奶美拉德反应早期反应程度的变化
糠氨酸是一种人造氨基酸,是Amadori化合物在110 ℃下用6 mol/L的盐酸水解24 h形成,大约30%~40%的Amadori化合物会转变成糠氨酸[11]。由于早期美拉德产物无明显颜色且在280 nm下无紫外吸收峰,而转变成的糠氨酸在280 nm下有强烈的紫外吸收,可通过HPLC测定含量[12],从而判断美拉德反应早期阶段重排产物的生成量,进一步反映出美拉德反应早期阶段的反应程度。
由图1可知,在4和10 ℃条件下储存的不同品牌的酸奶随着储存时间的延长,糠氨酸含量呈现增加的趋势,与普通酸奶相比,每种褐色酸奶的糠氨酸含量均显著高于普通酸奶,而且随着储存时间的增加,普通酸奶中糠氨酸含量的增加幅度小于褐色酸奶,与ANNE等[7]在测定超高温奶储存于10和20 ℃下糠氨酸含量随储存时间的增加而增加的结论相一致。5种褐色酸奶在4 ℃下储存10~15 d时,糠氨酸含量突增后趋于稳定。10 ℃与4 ℃储存下相比,酸奶在储存第5天含量迅速增加,储存后期保持低速增加的趋势。由此可见,糠氨酸含量的变化受酸奶的储存时间和储存温度影响较大,而不同品牌的酸奶在储存期间糠氨酸含量的差异性可能是由各市售品牌的酸奶的加工工艺条件和其中的糖类成分、蛋白质以及脂肪含量的差异性引起。结合CHENG等[13]研究发现在55 ℃下储存的乳粉中发生的蛋白质降解和脂质氧化可能会加速美拉德反应产物的形成。糠氨酸含量变化反映出美拉德反应在储存过程中仍在进行,且早期反应程度受储存温度和时间影响较显著。
a-4 ℃储存; b-10 ℃储存
图1 不同品牌酸奶在不同温度下贮藏21 d的 糠氨酸含量变化
Fig.1 Changes of furosine content in different brands of yoghurt stored at different temperatures for 21 days
2.2 不同褐色酸奶美拉德反应中期反应程度的变化
2.2.1 5-HMF含量的变化
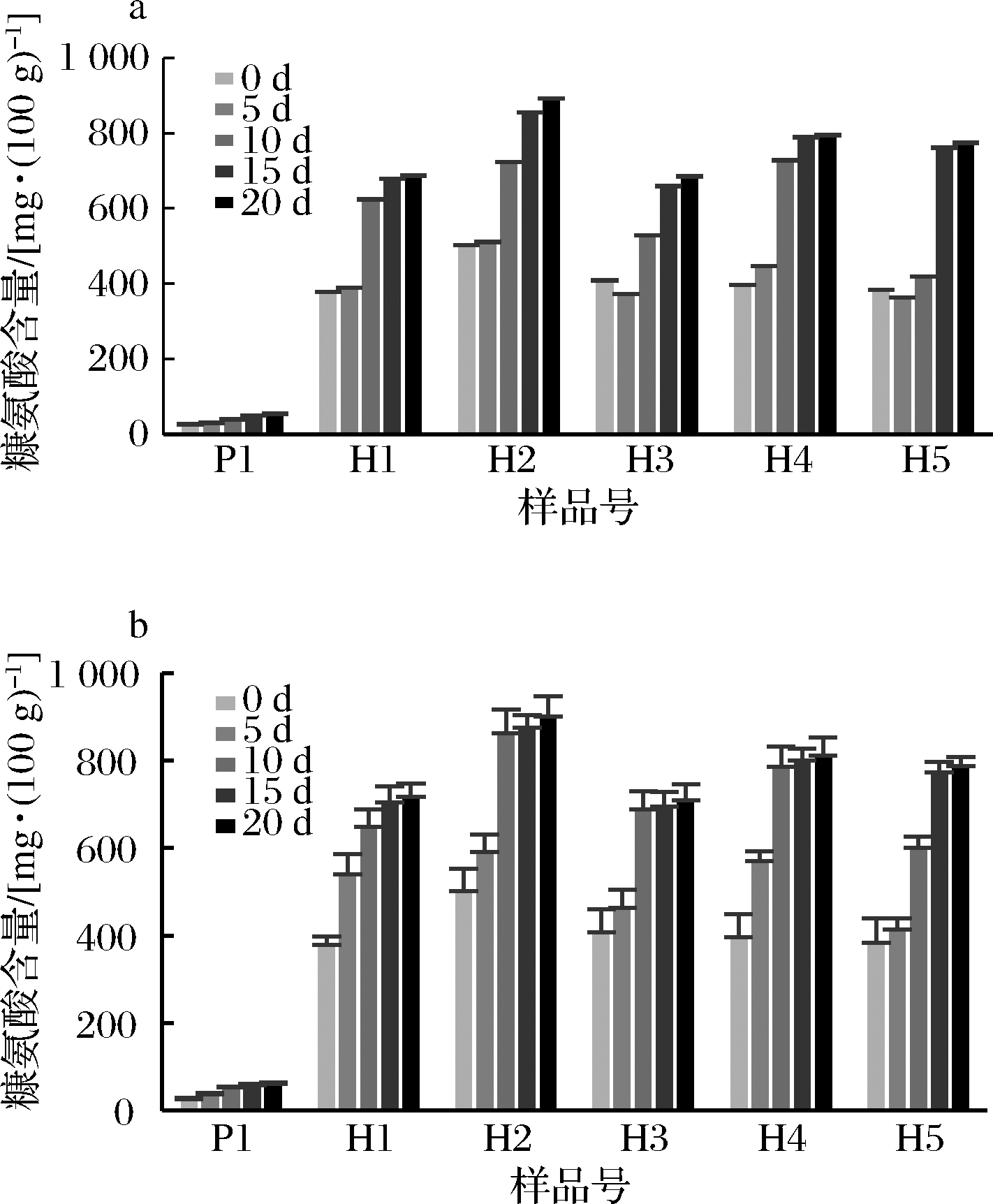
美拉德反应中间产物如5-HMF和二羰基化合物等产物无明显颜色或呈现黄色,且在一定波长下有强烈的紫外吸收峰,故可以通过测定中间代表产物的含量来判断美拉德反应中期反应程度[14]。由图2可知,在4和10 ℃条件下储存的不同品牌酸奶的5-HMF含量在第10 天达到最大,随着时间的进一步延长,含量呈现降低的趋势。每种褐色酸奶的5-HMF含量均显著高于普通酸奶,普通酸奶在4 ℃储存的货架期内含量较低,最低值为(0.32±0.05) mg/kg,储存10 d时达到最高值(0.71±0.04) mg/kg,但整体含量变化较小。而5种褐色酸奶在4 ℃储存的货架期内5-HMF的含量在(9.87±0.90)~(26.67±0.49) mg/kg变化。刘畅等[15]测得褐色酸奶中的5-HMF含量为3.86~12.91 mg/kg,而普通酸奶中含量为0~0.45 mg/kg,与本实验结果相近。每种酸奶的5-HMF变化规律有一定的差异,其中H2品牌的褐色酸奶在4 ℃储存时间内无明显差异。10 ℃储存的的5-HMF含量与4 ℃下相比差异不显著,且在21 d储存期内的总体变化趋势是相同的。总体上来看,5-HMF的含量受储存时间的影响较大。而酸奶在储存时间内在pH、酸度和质地等理化指标方面会发生变化,尤其随着储存时间的增加,酸奶的pH会降低,酸度会增加[16],这是由于在酸性环境下乳糖与蛋白质反应产生的Amadori化合物会水解形成5-HMF,而且乳糖分解成葡萄糖和半乳糖,会加速5-HMF的形成。本研究发现在储存10 d时5-HMF含量突增后又下降,原因可能与不稳定的中间产物相互作用有关。
a-4 ℃储存; b-10 ℃储存
图2 不同品牌酸奶在不同温度下贮藏21 d的 5-HMF含量变化
Fig.2 Changes of 5-HMF content in different brands of yoghurt stored at different temperatures for 21 days
2.2.2 三种α-二羰基化合物含量的变化
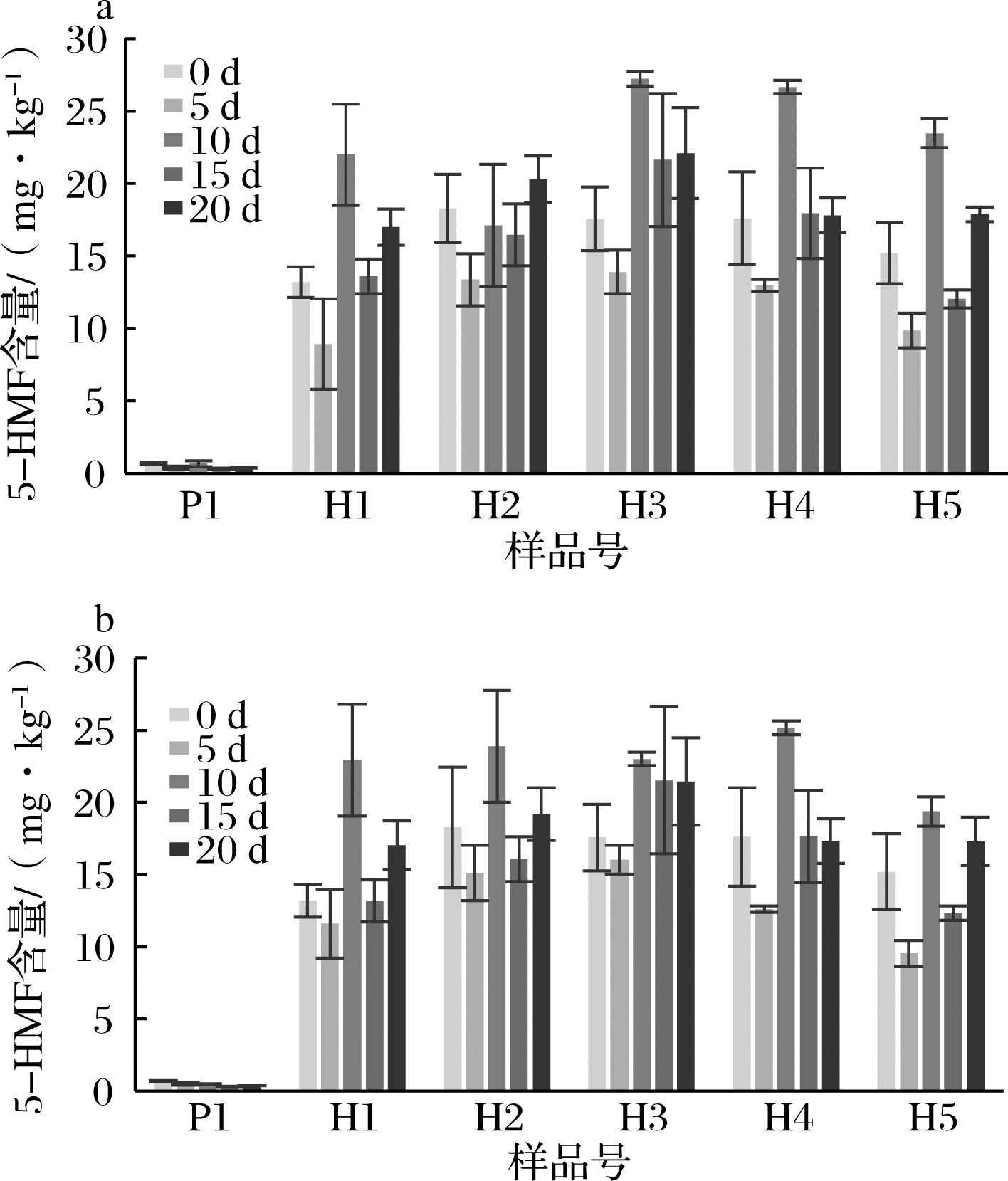
由图3可知,在4和10 ℃条件下不同品牌的酸奶随着储存时间的延长,GO、MGO和2,3-丁二酮含量均呈现先增加后降低的趋势,在储存第15天时3种物质含量均有显著升高。
a-4 ℃储存的乙二醛;b-10 ℃储存的乙二醛;c-4 ℃储存的丙酮醛;d-10 ℃储存的丙酮醛; e-4 ℃储存的2,3-丁二酮;f-10 ℃储存的2,3-丁二酮
图3 不同品牌酸奶在不同温度下贮藏21 d的3种二羰基化合物含量的变化
Fig.3 Changes of three dicarbonyl compounds content in different brands of yoghurt stored at different temperatures for 21 days
在4 ℃储存下普通酸奶3种物质的含量范围分别为0.10~0.28、0.05~0.80和0.16~0.64 mg/L。每种褐色酸奶的GO和MGO含量均高于普通酸奶,是普通酸奶的2~10倍,平均含量范围分别为0.27~2.45、0.11~2.55和0.45~1.86 mg/L。HAN等[9]测得褐色发酵乳生产储存过程中MGO含量范围为0.12~1.38 mg/L。4 ℃下储存褐色酸奶的α-二羰基化合物含量与其差异不显著,可判断含量变化受储存温度影响不大。5种褐色酸奶的3种α-二羰基化合物含量存在一定差异,其中2,3-丁二酮的含量差异显著,H3的含量显著高于其他4种品牌酸奶的含量,这可能与H3中使用的发酵菌种最多有关,也可能与其加工工艺条件的不同相关[17]。
GO、MGO和2,3-丁二酮都属于美拉德反应中间产物α-二羰基化合物中的重要代表性产物,形成途径包括焦糖化、美拉德反应、脂肪氧化、微生物发酵等[18]。其中干酪乳杆菌参与乳品发酵,并主要释放GO、MGO和2,3-丁二酮等[19],故对发酵乳来说发酵菌种的选择对α-二羰基化合物产生量具有重要的影响。这3种美拉德反应中间产物性质不稳定,易受外界因素影响,具有高度反应性,在胺化合物的存在下将进一步反应形成杂环芳族化合物,而且还会与高级糖基化化合物(羧甲基赖氨酸)反应,影响乳品的品质[20]。
2.3 不同褐色酸奶美拉德反应后期颜色指数的变化
不同品牌的褐色酸奶在不同储存时间和储存温度条件下的颜色参数值(a*、b*、L*、ΔE*和BI)如表2所示。4 ℃储存21 d,普通酸奶与褐色酸奶的颜色参数值存在显著差异,普通酸奶的a*在-1.72左右浮动,b*在8.70左右浮动,而褐色酸奶的a*在9.62左右浮动,b*在23.28左右浮动,说明在酸奶储存过程中,不同品牌酸奶的黄绿度和红蓝度均在一定数值范围内波动,无明显变化趋势。而样品亮度的L*值呈现一定的先降低后增加趋势,但稳定在一定范围内,表明样品颜色在储存时间内的变化不明显,而总ΔE*值和BI也无明显变化趋势。由表3可知,10 ℃下的颜色参数与4 ℃下相比,同时期的各参数值偏大,但无明显差异。不同品牌的褐色酸奶之间的颜色参数值差距同样较小。由此可以看出,酸奶储存时间和储存温度对酸奶颜色的变化无明显影响,美拉德后期色素物质的形成较少,后期反应程度较小。相关研究表明,经热处理后的牛乳在储存过程中会发生颜色变化,而且变化速度取决于储存的温度[21],只有当储存温度高于30 ℃时才会有明显变化,同时牛乳颜色的变化受牛乳pH值和乳糖含量的影响[22]。
表2 不同品牌酸奶在4 ℃下储存21 d时的颜色参数变化
Table 2 Color parameters of different brands of yoghurt stored at 4 ℃ for 21 days
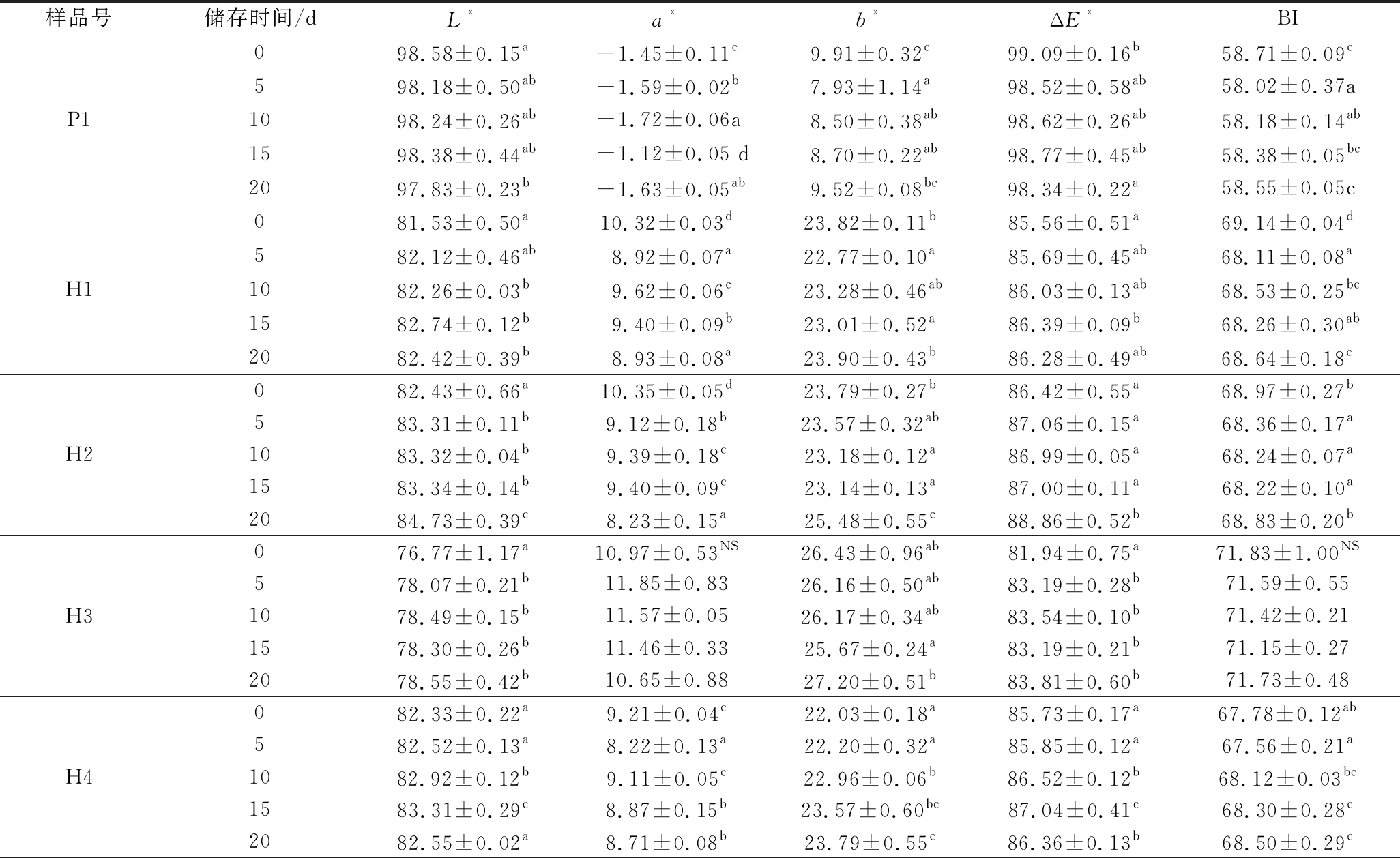
样品号储存时间/dL*a*b*ΔE*BIP1098.58±0.15a-1.45±0.11c9.91±0.32c99.09±0.16b58.71±0.09c598.18±0.50ab-1.59±0.02b7.93±1.14a98.52±0.58ab58.02±0.37a1098.24±0.26ab-1.72±0.06a8.50±0.38ab98.62±0.26ab58.18±0.14ab1598.38±0.44ab-1.12±0.05 d8.70±0.22ab98.77±0.45ab58.38±0.05bc2097.83±0.23b-1.63±0.05ab9.52±0.08bc98.34±0.22a58.55±0.05cH1081.53±0.50a10.32±0.03d23.82±0.11b85.56±0.51a69.14±0.04d582.12±0.46ab8.92±0.07a22.77±0.10a85.69±0.45ab68.11±0.08a1082.26±0.03b9.62±0.06c23.28±0.46ab86.03±0.13ab68.53±0.25bc1582.74±0.12b9.40±0.09b23.01±0.52a86.39±0.09b68.26±0.30ab2082.42±0.39b8.93±0.08a23.90±0.43b86.28±0.49ab68.64±0.18cH2082.43±0.66a10.35±0.05d23.79±0.27b86.42±0.55a68.97±0.27b583.31±0.11b9.12±0.18b23.57±0.32ab87.06±0.15a68.36±0.17a1083.32±0.04b9.39±0.18c23.18±0.12a86.99±0.05a68.24±0.07a1583.34±0.14b9.40±0.09c23.14±0.13a87.00±0.11a68.22±0.10a2084.73±0.39c8.23±0.15a25.48±0.55c88.86±0.52b68.83±0.20bH3076.77±1.17a10.97±0.53NS26.43±0.96ab81.94±0.75a71.83±1.00NS578.07±0.21b11.85±0.8326.16±0.50ab83.19±0.28b71.59±0.551078.49±0.15b11.57±0.0526.17±0.34ab83.54±0.10b71.42±0.211578.30±0.26b11.46±0.3325.67±0.24a83.19±0.21b71.15±0.272078.55±0.42b10.65±0.8827.20±0.51b83.81±0.60b71.73±0.48H4082.33±0.22a9.21±0.04c22.03±0.18a85.73±0.17a67.78±0.12ab582.52±0.13a8.22±0.13a22.20±0.32a85.85±0.12a67.56±0.21a1082.92±0.12b9.11±0.05c22.96±0.06b86.52±0.12b68.12±0.03bc1583.31±0.29c8.87±0.15b23.57±0.60bc87.04±0.41c68.30±0.28c2082.55±0.02a8.71±0.08b23.79±0.55c86.36±0.13b68.50±0.29c
续表2

样品号储存时间/dL*a*b*ΔE*BIH5083.50±2.21NS8.53±0.32b22.69±0.03a86.95±2.02NS67.74±0.42b584.03±1.83NS8.07±0.37a22.62±0.22a87.40±1.6767.49±0.50ab1084.82±0.74NS7.90±0.19a21.84±0.20b87.95±0.6566.94±0.25a1584.58±0.28NS7.67±0.10a22.01±0.18b87.73±0.2966.99±0.09a2083.65±0.14NS8.58±0.10b24.98±0.40c87.72±0.1868.87±0.22c
注:L*代表亮度,a*代表绿/红,b*代表蓝/黄,ΔE*为总色差,BI为褐变指数;a,b,c为显著性分析(n=3,P<0.05),NS为无显著差异(下同)
表3 不同品牌酸奶在10 ℃下储存21 d时的颜色参数变化
Table 3 Color parameters of different brands of yoghurt stored at 10 ℃ for 21 days
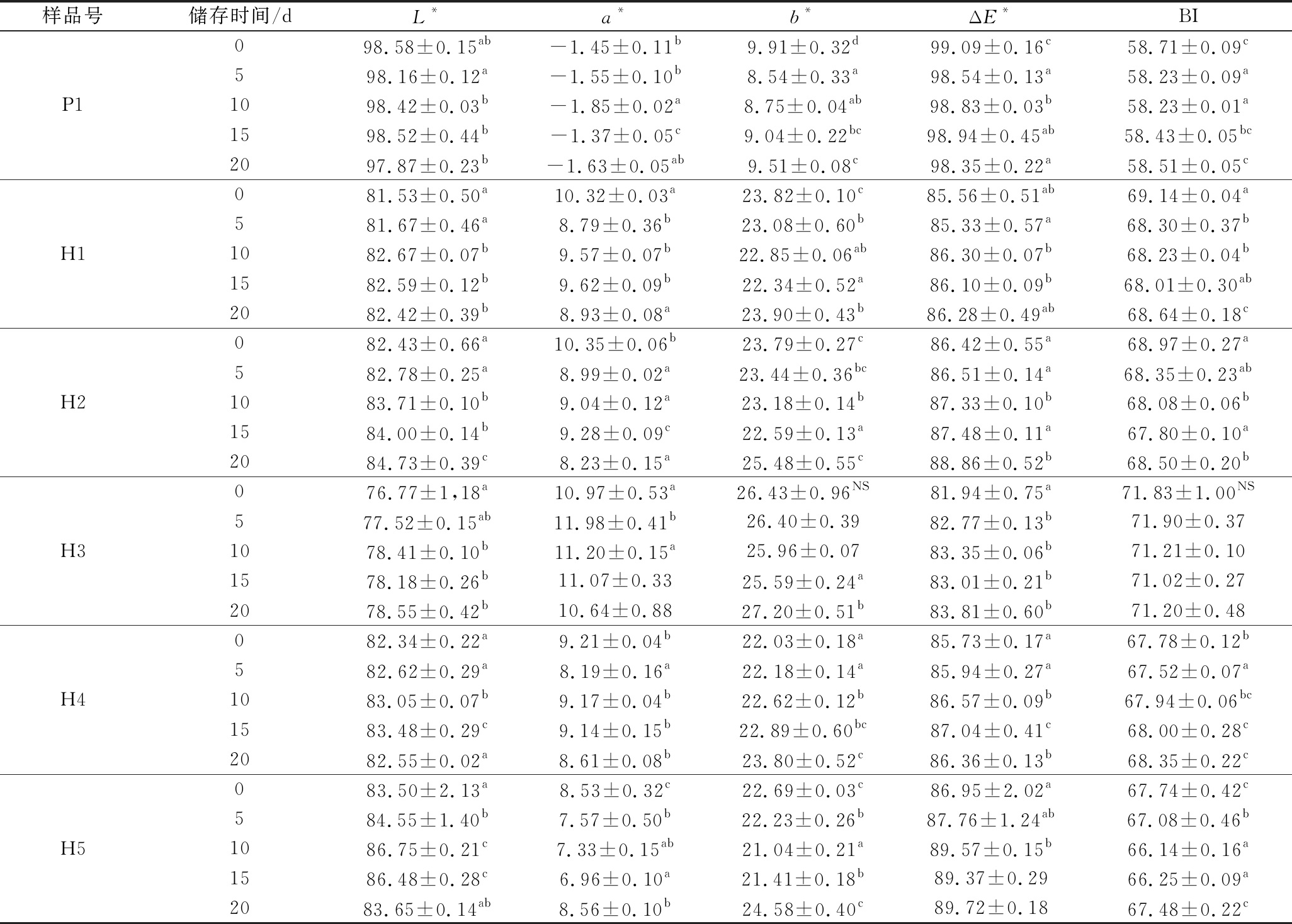
样品号储存时间/dL*a*b*ΔE*BIP1098.58±0.15ab-1.45±0.11b9.91±0.32d99.09±0.16c58.71±0.09c598.16±0.12a-1.55±0.10b8.54±0.33a98.54±0.13a58.23±0.09a1098.42±0.03b-1.85±0.02a8.75±0.04ab98.83±0.03b58.23±0.01a1598.52±0.44b-1.37±0.05c9.04±0.22bc98.94±0.45ab58.43±0.05bc2097.87±0.23b-1.63±0.05ab9.51±0.08c98.35±0.22a58.51±0.05cH1081.53±0.50a10.32±0.03a23.82±0.10c85.56±0.51ab69.14±0.04a581.67±0.46a8.79±0.36b23.08±0.60b85.33±0.57a68.30±0.37b1082.67±0.07b9.57±0.07b22.85±0.06ab86.30±0.07b68.23±0.04b1582.59±0.12b9.62±0.09b22.34±0.52a86.10±0.09b68.01±0.30ab2082.42±0.39b8.93±0.08a23.90±0.43b86.28±0.49ab68.64±0.18cH2082.43±0.66a10.35±0.06b23.79±0.27c86.42±0.55a68.97±0.27a582.78±0.25a8.99±0.02a23.44±0.36bc86.51±0.14a68.35±0.23ab1083.71±0.10b9.04±0.12a23.18±0.14b87.33±0.10b68.08±0.06b1584.00±0.14b9.28±0.09c22.59±0.13a87.48±0.11a67.80±0.10a2084.73±0.39c8.23±0.15a25.48±0.55c88.86±0.52b68.50±0.20bH3076.77±1,18a10.97±0.53a26.43±0.96NS81.94±0.75a71.83±1.00NS577.52±0.15ab11.98±0.41b26.40±0.3982.77±0.13b71.90±0.371078.41±0.10b11.20±0.15a25.96±0.0783.35±0.06b71.21±0.101578.18±0.26b11.07±0.3325.59±0.24a83.01±0.21b71.02±0.272078.55±0.42b10.64±0.8827.20±0.51b83.81±0.60b71.20±0.48H4082.34±0.22a9.21±0.04b22.03±0.18a85.73±0.17a67.78±0.12b582.62±0.29a8.19±0.16a22.18±0.14a85.94±0.27a67.52±0.07a1083.05±0.07b9.17±0.04b22.62±0.12b86.57±0.09b67.94±0.06bc1583.48±0.29c9.14±0.15b22.89±0.60bc87.04±0.41c68.00±0.28c2082.55±0.02a8.61±0.08b23.80±0.52c86.36±0.13b68.35±0.22cH5083.50±2.13a8.53±0.32c22.69±0.03c86.95±2.02a67.74±0.42c584.55±1.40b7.57±0.50b22.23±0.26b87.76±1.24ab67.08±0.46b1086.75±0.21c7.33±0.15ab21.04±0.21a89.57±0.15b66.14±0.16a1586.48±0.28c6.96±0.10a21.41±0.18b89.37±0.2966.25±0.09a2083.65±0.14ab8.56±0.10b24.58±0.40c89.72±0.1867.48±0.22c
2.4 不同褐色酸奶美拉德反应后期高级反应产物荧光程度的变化
美拉德反应的高级阶段是棕色的含氮聚合物以及褐黑色的共聚物类黑精的形成,该反应过程伴随着共轭体系的形成与增加,并导致紫外可见光区的吸收[23]。共聚物类黑精的具体成分尚不清楚,而在乳制品中的类黑精主要与蛋白质有关,而且赖氨酸在美拉德反应最终阶段会有损失[24]。故后期反应程度主要根据呈现的颜色及高级产物的荧光特性来判断。产品颜色褐变程度越深,高级美拉德反应产物的荧光强度越大,表示后期反应程度越剧烈[25]。
由图4可知,在4 ℃下储存的酸奶随着储存时间的增长,FAMP值整体呈现降低的趋势。每种褐色酸奶的FAMP值均高于普通酸奶,总体变化规律相似但部分品牌的FAMP值无明显变化,品牌之间的具体变化程度存在一定的差异。在10 ℃下储存酸奶的FAMP值与4 ℃下相比,FAMP值均在储存第5天时达到最大值,之后储存期内的值降低并趋于稳定。FAMP值变化现象反映出美拉德反应的后期反应阶段受储存时间的影响不大,受储存温度的影响较显著,而这一变化规律受酸奶环境的多种因素作用影响。
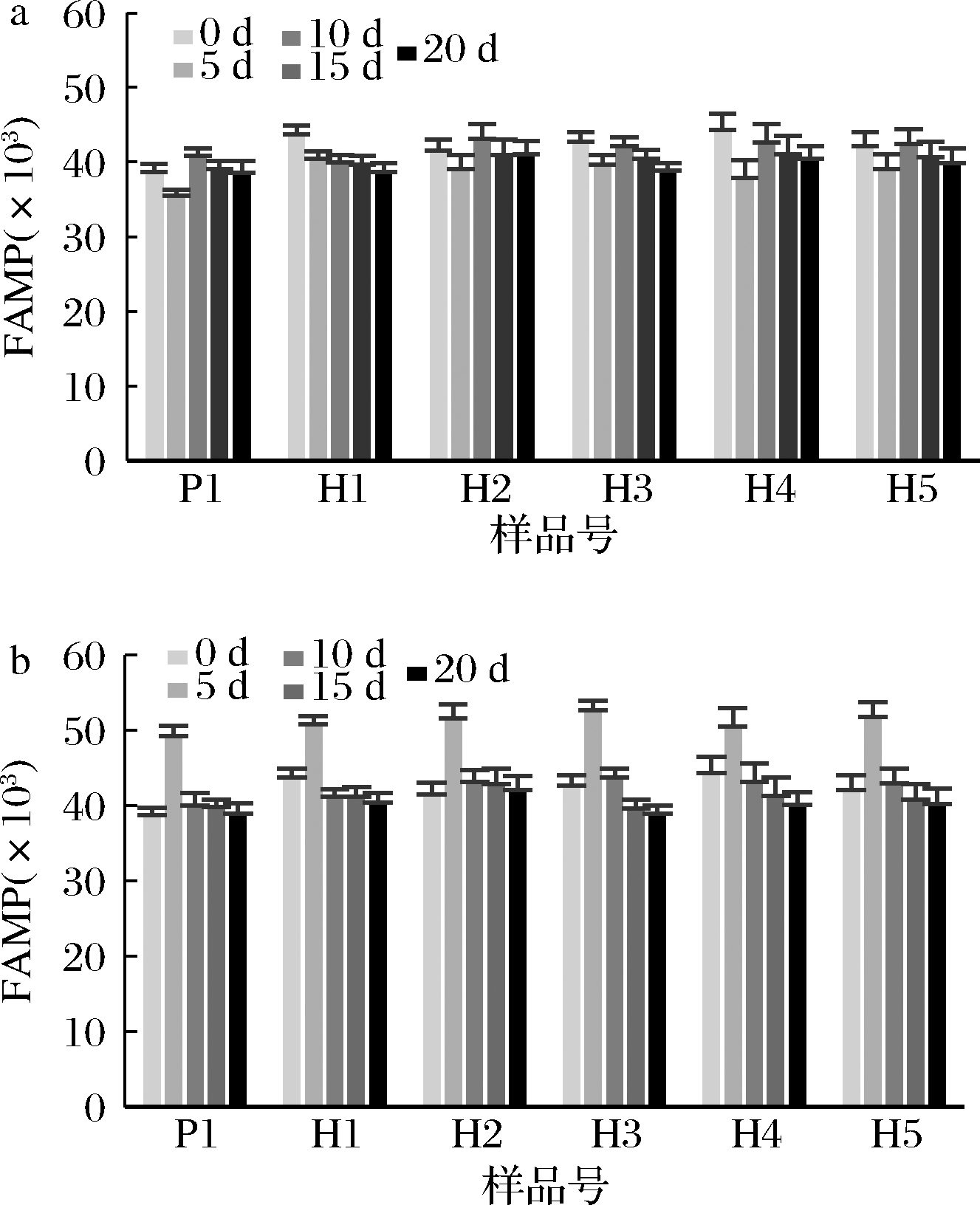
a-4 ℃储存;b-10 ℃储存
图4 不同品牌酸奶在不同温度下贮藏21 d的 FAMP值变化
Fig.4 Changes of FAMP in different brands of yoghurt stored at different temperatures for 21 days
2.5 不同褐色酸奶综合热损伤FAST指数的变化
由于牛乳加热过程中蛋白质发生降解,色氨酸的荧光性降低,随着美拉德反应产物的积累,会出现荧光性增加的过程,故结合色氨酸的荧光强度(FTrp)和后期美拉德反应荧光产物的荧光性(FAMP),计算FAST值来评价酸奶的综合热损伤程度变化[26]。
如图5所示,在不同储存温度和时间条件下,FAST指数变化呈现浮动趋势,且每种品牌的酸奶变化规律有一定的差异,总体上来看,FAST指数变化受储存时间的变化影响不大,但受储存温度的变化影响较大。美拉德后期产物荧光积累越多,色氨酸荧光值降低,FAST指数越大,表明酸奶的受热损伤程度越高,美拉德反应程度越剧烈[27]。其中也有部分人对牛乳热处理后荧光强度的变化进行测定,INÉS等[28]提出用FAST 指数来综合研究不同热处理条件下色氨酸及美拉德反应产物荧光强度的变化规律,评价牛乳的热处理强度。卜登攀等[29]在研究 FAST指数在复原乳检测方法中的应用时发现,FAST指数可以灵敏地区分生鲜乳和巴氏杀菌乳。LOURDES等[30]将荧光和颜色作为标记来研究谷类婴儿牛奶食品贮存期间的美拉德反应,发现在贮藏期间随贮藏温度增加,牛乳颜色和荧光强度呈现梯度增加。故综合评价储藏期间褐色酸奶热损伤变化主要受储存温度的影响,温度越高,综合热损伤程度越高。
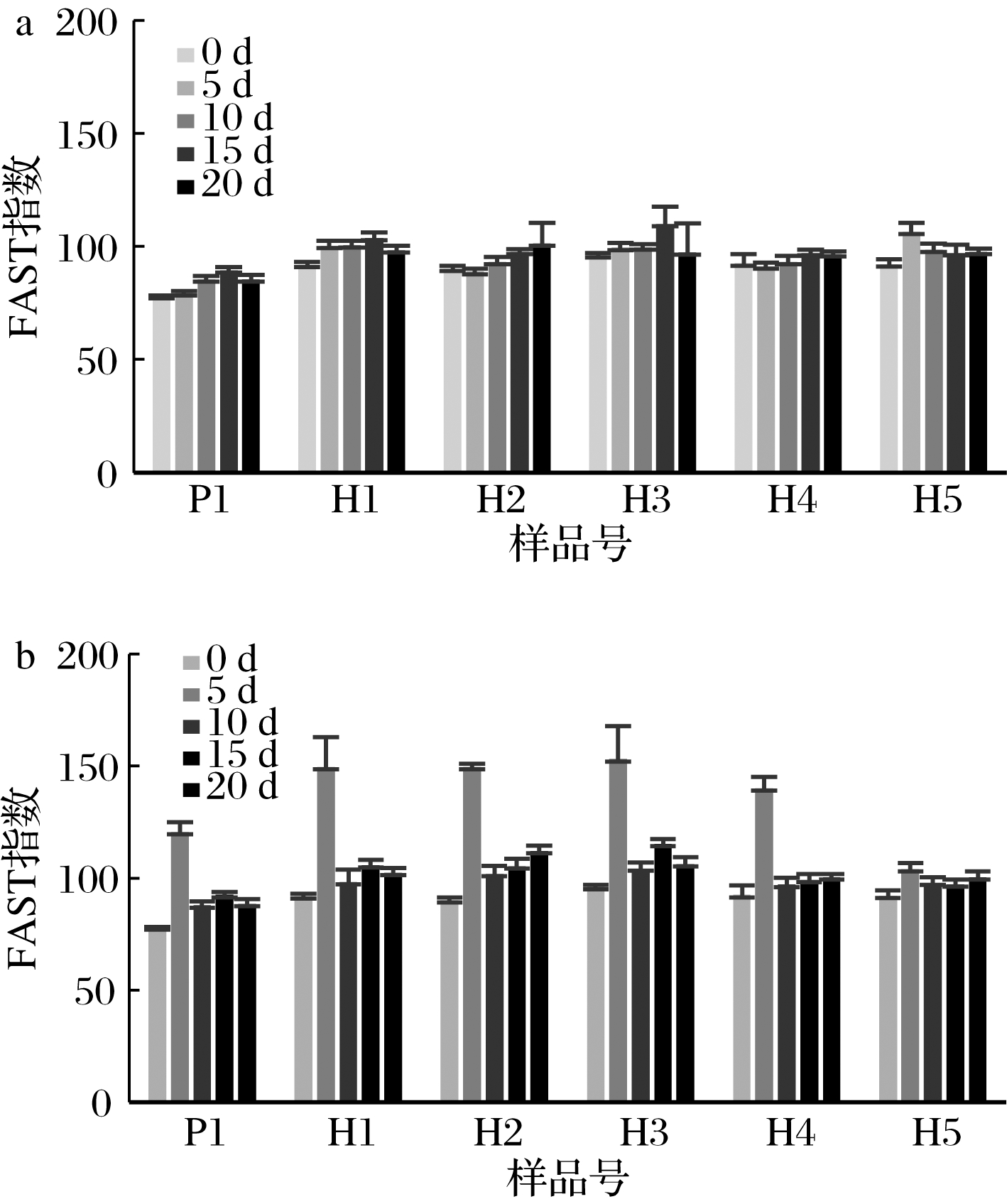
a-4 ℃储存;b-10 ℃储存
图5 不同品牌酸奶在不同温度下贮藏21 d的 FAST指数变化
Fig.5 Changes of FAST index in different brands of yoghurt stored at different temperatures for 21 days
3 结论
本研究综合评估分析了褐色酸奶在不同贮藏条件下的美拉德不同反应阶段的变化历程,得出结论是,褐色酸奶在贮藏过程中美拉德反应仍在进行,且不同反应阶段进行程度不同,美拉德反应早期阶段产物形成较多,而且受贮藏温度影响,温度越高,反应越剧烈。美拉德反应中期指标5-HMF和3种α-二羰基化合物的含量变化主要受贮藏时间影响,随着时间的延长,含量有一定程度的增加。美拉德反应后期,反应程度随着贮藏时间的延长和贮藏温度的升高的变化不显著,由于不同品牌酸奶中所含糖类、蛋白质、脂肪以及发酵菌种的种类数量不同导致酸奶储藏中各阶段美拉德反应变化规律有一定差异,故在控制美拉德反应程度和反应副产物生成方面,不仅要注意加工工艺条件的选择,还要选择合适的贮藏条件。综合评价褐色酸奶贮藏期间的安全性,建议将市售褐色酸奶严格控制在4 ℃贮藏并于货架期内食用,其质量和安全性较好。
[1] 张俊山.褐色酸奶的褐变机制及工艺优化[D].哈尔滨:东北农业大学,2018.
ZHANG J S.Browning mechanism and process optimization of brown yoghurt [D].Harbin:Northeast Agricultural University, 2018.
[2] NOOSHKAM M,VARIDI M,BASHASH M.The Maillard reaction products as food-born antioxidant and antibrowning agents in model and real food systems.[J].Food Chemisty,2019,275:644-660.
[3] DIEGO A,CORTÉS Y,MAITE G,et al.Antioxidant activity developed at the different stages of Maillard reaction with milk proteins[J].LWT-Food Science and Technology,2018,89:344-349.
[4] ASIKIN Y,KAMIYA A,MIZU M,et al.Changes in the physicochemical characteristics, including flavour components and Maillard reaction products, of non-centrifugal cane brown sugar during storage.[J].Food Chemisty,2014,149:170-177.
[5] 李光磊. 美拉德反应中健康危害物的产生规律研究[D].天津:天津科技大学,2016.
LI G L.Study on the formation of health hazards prodected in millard reaction [D].Tianjin:Tianjin University of Science and Technology, 2016.
[6] I IL G A,AYTÜL H,VURAL G.Lactose hydrolysis and protein fortification pose an increased risk for the formation of Maillard reaction products in UHT treated milk products[J].Journal of Food Composition and Analysis,2019,84:103 308.
IL G A,AYTÜL H,VURAL G.Lactose hydrolysis and protein fortification pose an increased risk for the formation of Maillard reaction products in UHT treated milk products[J].Journal of Food Composition and Analysis,2019,84:103 308.
[7] ANNE V S,VALENTIN M R,JOHN S,et al.Maillard reaction progress in UHT milk during storage at different temperature levels and cycles[J].International Dairy Journal,2018,77:56-64.
[8] NARANJO G B,PEREYRA G A S,LEIVA G E, et al.The kinetics of Maillard reaction in lactose-hydrolysed milk powder and related systems containing carbohydrate mixtures.[J].Food Chemistry,2013,141(4):3 790-3 795.
[9] HAN Z H,GAO J X,WANG X M,et al.Formation and alterations of the potentially harmful maillard reaction products during the production and storage of brown fermented milk[J].Molecules,2019,24(2):272-284.
[10] WEI Q Y,LIU T, SUN D W.Advanced glycation end-products (AGEs) in foods and their detecting techniques and methods:A review[J].Trends in Food Science & Technology,2018,82:32-45.
[11] AALAEI K,RAYNER M,SJÖHOLM I.Chemical methods and techniques to monitor early Maillard reaction in milk products:A review[J].Critical Reviews in Food Science and Nutrition,2019,59(12):1 829-1 839.
[12] ERBERSDOBLER H F,SOMOZA V.Forty years of furosine-forty years of using Maillard reaction products as indicators of the nutritional quality of foods[J].Molecular Nutrition & Food Research,2007,51(4):423-430.
[13] CHENG H,ZHU R G,HENRIETTE E,et al.High temperature storage of infant formula milk powder for prediction of storage stability at ambient conditions[J].International Dairy Journal,2017,73:166-174.
[14] CLAEYS W L,LUDIKHUYZE L R,HENDRICKX M E.Formation kinetics of hydroxymethylfurfural, lactulose and furosine in milk heated under isothermal and non-isothermal conditions[J].The Journal of Dairy Research,2001,68(2):287-301.
[15] 刘畅,钱方.褐色酸奶中5-羟甲基糠醛测定方法探究[J].中国食品添加剂,2018(12):180-185.
LIU C,QIAN F.Study on the determination method of 5-hydroxymethylfurfural in brown yoghurt[J].China Food Additives, 2018(12):180-185.
[16] ARENA S,RENZONE G,D’AMBROSIO C,et al.Dairy products and the Maillard reaction:A promising future for extensive food characterization by integrated proteomics studies[J].Food Chemistry,2017,219:477-489.
[17] ALESSANDRA A,GIOVANNI M,MARIA D.Cytotoxicity of α-dicarbonyl compounds submitted to in vitro simulated digestion process[J].Food Chemistry,2013,140(4):654-659.
[18] HONG P K,BETTI M.Non-enzymatic browning reaction of glucosamine at mild conditions:Relationship between colour formation, radical scavenging activity and α-dicarbonyl compounds production[J].Food Chemistry,2016,212:234-243.
[19] 马毛毛.α-二羰基化合物的产生规律和机制[D].天津:天津科技大学,2017.
MANG M M.The regulation and mechanism of α-Dicarbonyl compounds formation[D].Tianjin:Tianjin University of Science and Technology, 2017.
[20] SARA I.F.S M,WIM M.F J,MARTINUS A.A review of Maillard reaction in food and implications to kinetic modelling[J].Trends in Food Science & Technology,2000,11(9-10):364-373.
[21] DEGEN J,HELLWIG M,HENLE T.1,2-dicarbonyl compounds in commonly consumed foods[J].Journal of Agricultural and Food Chemistry,2012,60(28):7 071-7 079.
[22] EMMA B,MIKE L,DOUGLAS M.Predicting safety and quality parameters for UHT-processed milks[J].International Journal of Dairy Technology,2001,54(3):111-120.
[23] GIOVANNI R,SIMONA A,ANDREA S.Proteomic characterization of intermediate and advanced glycation end-products in commercial milk samples[J].Journal of Proteomics,2015,117:12-23.
[24] M.A.J.S.VAN BOEKEL.Effect of heating on Maillard reactions in milk[J].Food Chemistry,1998,62(4):403-414.
[25] CÉCILE R,DELPHINE L,EMILIE R,et al.Mitigation strategies of acrylamide, furans, heterocyclic amines and browning during the Maillard reaction in foods[J].Food Research International,2016,90:154-176.
[26] LEIVA G E,NARANJO G B,MALEC L S.A study of different indicators of Maillard reaction with whey proteins and different carbohydrates under adverse storage conditions[J].Food Chemistry,2017,215:410-416.
[27] MASTROCOLA D,MUNARI M.Progress of the Maillard reaction and antioxidant action of Maillard reaction products in preheated model systems during storage[J].Journal of Agricultural and Food Chemistry,2000,48(8):3 555-3 559.
[28] INÉS B A,MARINA N,ARNAUD M,et al.A rapid fluorimetric method to estimate the heat treatment of liquid milk[J].International Dairy Journal,1998,8(9):771-777.
[29] 卜登攀,李树聪,张瑞超,等.FAST指数在复原乳区分中的应用初探[J].中国农学通报,2006(11):1-7.
BU D P, LI S C, ZHANG R C, et al.Application of FAST method in determination of the presence of reconstitued milk[J].Chinese Agricultural Science Bulletin, 2006(11):1-7.
[30] LOURDES B,AMPARO A,ROSAURA F,et al.Fluorescence and color as markers for the Maillard reaction in milk-cereal based infant foods during storage[J].Food Chemistry,2007,105(3):1 135-1 143.