鸡蛋清蛋白质具有独特的功能特性,例如发泡性、乳化性和凝胶特性。近年来,蛋粉因其货架期长、贮存成本低、运输成本低等优点在烘焙、敷料和糖果产品中得到了广泛的应用[1]。喷雾干燥由于干燥时间短,产品温度相对较低[2]等优势,成为工业上制备蛋粉的常用方法。
目前,关于喷雾干燥加工蛋粉的研究受到了国内外学者的青睐。例如,SCHOLES等[3]基础研究了不同干燥程序对鸡蛋功能的影响。KATO等[4]报道在干燥加热状态下样品的孵育加热时间的增加可以增强发泡力、发泡稳定性、乳化性能和喷雾干燥蛋清粉末的凝胶强度。FRANKE等[5]发现随着进气温度的升高,蛋白质溶解度和发泡功率降低。AYADI等[6]研究了适度喷雾干燥条件对干白和全蛋粉功能的影响。KOC等[7]发现喷雾干燥可以制备稳定和功能性的粉末产品,喷雾干燥的蛋粉在处理和卫生方面对食品工业具有重要意义。孙临政等[8]研究了不同喷雾干燥流量、进料温度、进风温度对蛋清粉最终成品的溶解性和分散性的影响,并优化了工艺参数,使得最终得到冲调性良好的蛋清粉。沈青等[9]研究了采用喷雾干燥与真空冷冻干燥两种干燥方式制备全蛋粉并对干燥后得到的全蛋粉的理化性质和功能性质进行了对比。涂宗财等[10]利用动态高压均质处理蛋清蛋白,发现乳清蛋白的结构及其流变性和黏度在微射流作用下发生改变,蛋白粒径减小,黏度增加。
目前国内外对于喷雾干燥制备蛋清粉的研究多集中于工艺优化和功能特性方面,而针对不同喷雾干燥温度对蛋清蛋白流变和结构特性的影响研究却鲜有报道,因此开展该领域的研究具有十分重要的理论意义。本研究的目的是探究喷雾干燥入口温度对蛋清蛋白的流变特性、水分迁移、二级结构及微观结构的影响,并从蛋白质结构变化分析其作用机理,以期为指导和优化喷雾干燥工业化生产制备高品质蛋粉提供理论依据。
1 材料与方法
1.1 材料与试剂
鲜鸡蛋,河南省洛阳市大张超市;KBr,分析纯,上海强顺化学试剂有限公司。
1.2 仪器与设备
6000Y实验型喷雾干燥机,上海Bilon仪器有限公司;TF-FD-27S真空冷冻干燥机,上海田枫实业有限公司;DHR-1流变仪,美国TA公司;Spectrum 10傅里叶红外光谱(Fourier transform infrared spectroscopy,FT-IR)仪,上海铂金埃尔默仪器有限公司;NMI20-030H-I低场核磁共振(low field nuclear magnetic resonance,LF-NMR)分析与成像系统,上海纽迈电子科技有限公司;JSM-7500F扫描电子显微镜(scanning electron microscope,SEM),富瑞博国际有限公司。
1.3 实验方法
1.3.1 样品的制备
喷雾干燥鸡蛋清粉是由鸡蛋清先经过巴氏杀菌、脱糖,然后再直接喷雾干燥而得。巴氏杀菌条件:60 ℃,杀菌4 min;脱糖处理:将经过前处理的蛋清蛋白液放置于洁净器皿,在干净环境25 ℃自然发酵48 h脱糖;喷雾干燥条件:入口温度分别为140、160、180 ℃,蛋清液质量浓度为290 g/L,进料速度为466 mL/h,出口温度为显示值,非人为控制,干燥后在4 ℃保存备用[11]。
1.3.2 流变特性的测定
将蛋清粉配制成70 g/L的蛋清液,放置适量样品于流变仪测试平台上,然后下降平板,下降至剪切间隙为1 050 μm时刮边,最后测量距离在1 000 μm以下开始做实验,采用直径40 mm平行板测量,每次测试均需更换样品。
1.3.2.1 静态流变测定
设置仪器平台温度为25 ℃,测量剪切速率从0.01~1 000 s-1逐步递增,研究表观黏度的变化。采用Herschel-Bulkley模型[12]对数据进行回归拟合,计算方法如公式(1)所示:
σ/Pa=σ0+kγn
(1)
式中:σ,剪切应力,Pa;γ,剪切速率,s-1;σ0,屈服应力,Pa;k,稠度系数,Pa/sn;n,流动特性指数。
1.3.2.2 动态黏弹性测定
设置仪器平台温度为25 ℃,扫描应变1%,测定频率为0.1~100 rad/s储能模量(G′)和损耗模量(G″)的变化[13]。
1.3.3 LF-NMR分析
试验中应用低场核磁共振分析仪,测定条件:温度(32±0.05)℃,将称量(1.0±0.005) g样品放入LF-NMR专用玻璃管中,随后打开低场核磁共振分析软件,对每个样品进行信号采集。并且采用多脉冲回波序列测定样品的弛豫时间T2,重复测定3次以补充数据[14]。
1.3.4 FT-IR分析
将干燥的KBr与待测蛋清粉按质量比100∶10充分混合,然后用玛瑙研磨至细粉末状后置于专用压片机中,在60~70 N压力下保持1 min,压制成均匀的圆形透明薄片,空白对照为单纯KBr压片。然后使用仪器做全波段扫描(4 000~400 cm-1),分辨率为4 cm-1,扫描次数为32。通过采用OMNIC软件对酰胺I带进行基线校正,平滑处理,再采用PEAK FIT软件,在二阶导数基础上对其进行拟合处理,从而可以确定各子峰与其对应的二级结构单元之间的关系,最后根据峰面积再计算各二级结构组分的相对百分含量[15]。
1.3.5 SEM分析
将蛋清粉及对照样分布载物台的导电双面胶上,然后置于SEM中观察,选取最佳放大倍数观察样品的,最后选择有代表性的区域进行观察拍摄。
1.4 数据处理
每个样品重复3次试验,并进行误差分析。采用Origin 9.0软件作图。
2 结果与分析
2.1 静态流动扫描分析
2.1.1 表观黏度分析
不同干燥入口温度对蛋清蛋白的静态流动扫描的影响,如图1所示。
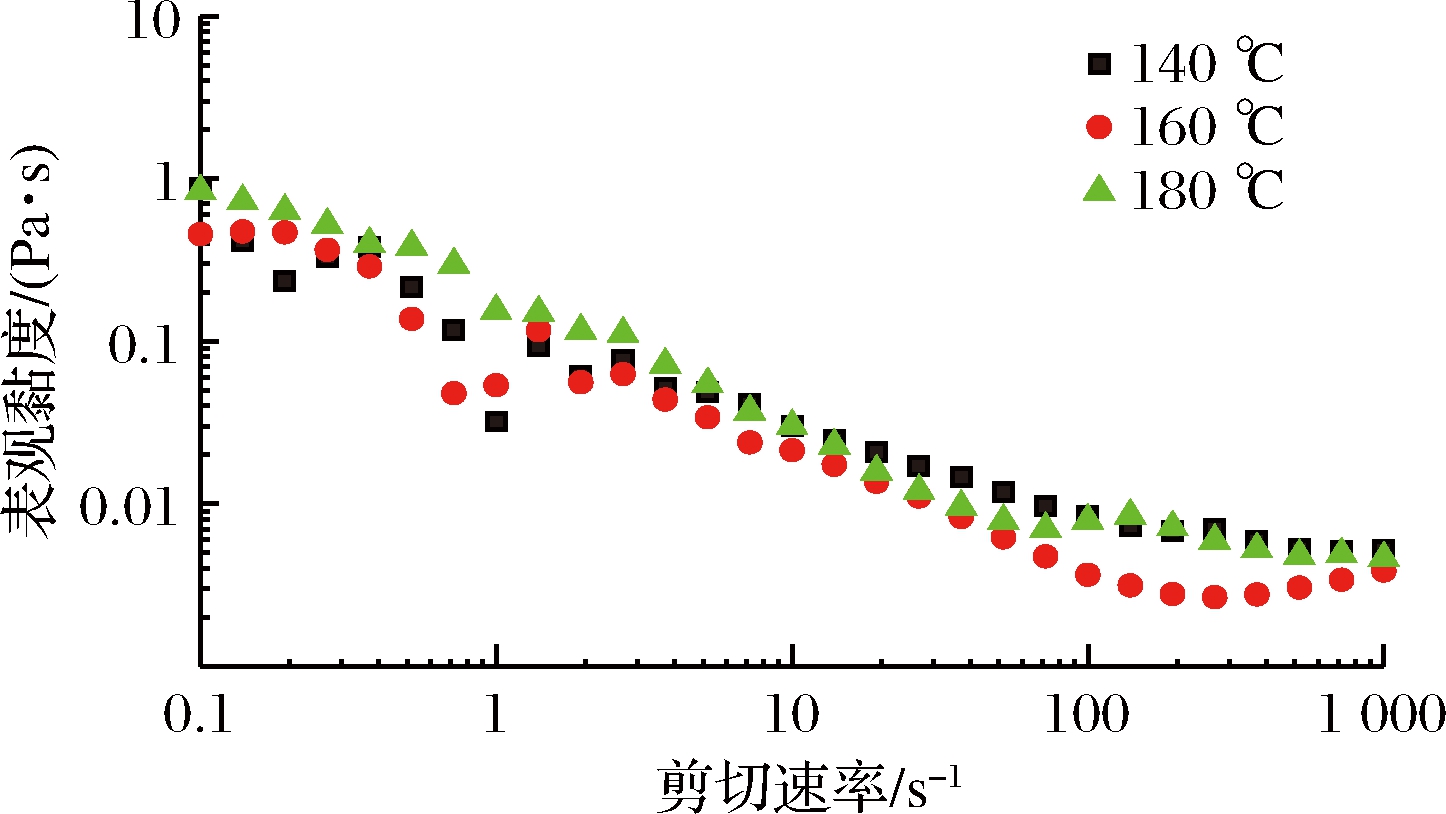
图1 不同干燥温度对蛋清蛋白溶液表观黏度的影响
Fig.1 Effect of different drying temperature on the viscosity of egg white protein solutios
由图1可知,不同干燥温度制备蛋清蛋白的表观黏度都随着剪切速率的增加而降低,表现出剪切变稀的非牛顿流体假塑性流动特征,这是由于剪切速率较低时,蛋清蛋白分子取向混乱,随着剪切速率的增大,分子取向逐渐一致,表观黏度降低。在剪切速率<1 s-1时,表观黏度随着剪切速率的增大而急剧下降,表现出剪切变稀的流体特征,这是因为流速场中,蛋清蛋白液形成的絮体变性。在剪切速率>1 s-1时,表观黏度基本保持稳定。平稳时,表观黏度由高到低分别为:140 ℃>180 ℃>160 ℃,在不同的干燥温度中,140 ℃蛋清蛋白粉的表观黏度最高,160 ℃蛋清蛋白粉的表观黏度最低,这可能是由于140 ℃分子之间运动加剧,导致蛋清蛋白链状大分子在液体中悬浮时发生凝结和缠绕,分子取向不一,增加固形物与流体之间的阻力,不利于流动[16],从而表现出表观黏度大;而160 ℃分子链断裂,使得平均分子质量最小,从而导致蛋清蛋白粉表观黏度低。
2.1.2 流变模型分析
不同干燥温度蛋清蛋白粉静态流变的变化曲线如图2、表1所示。
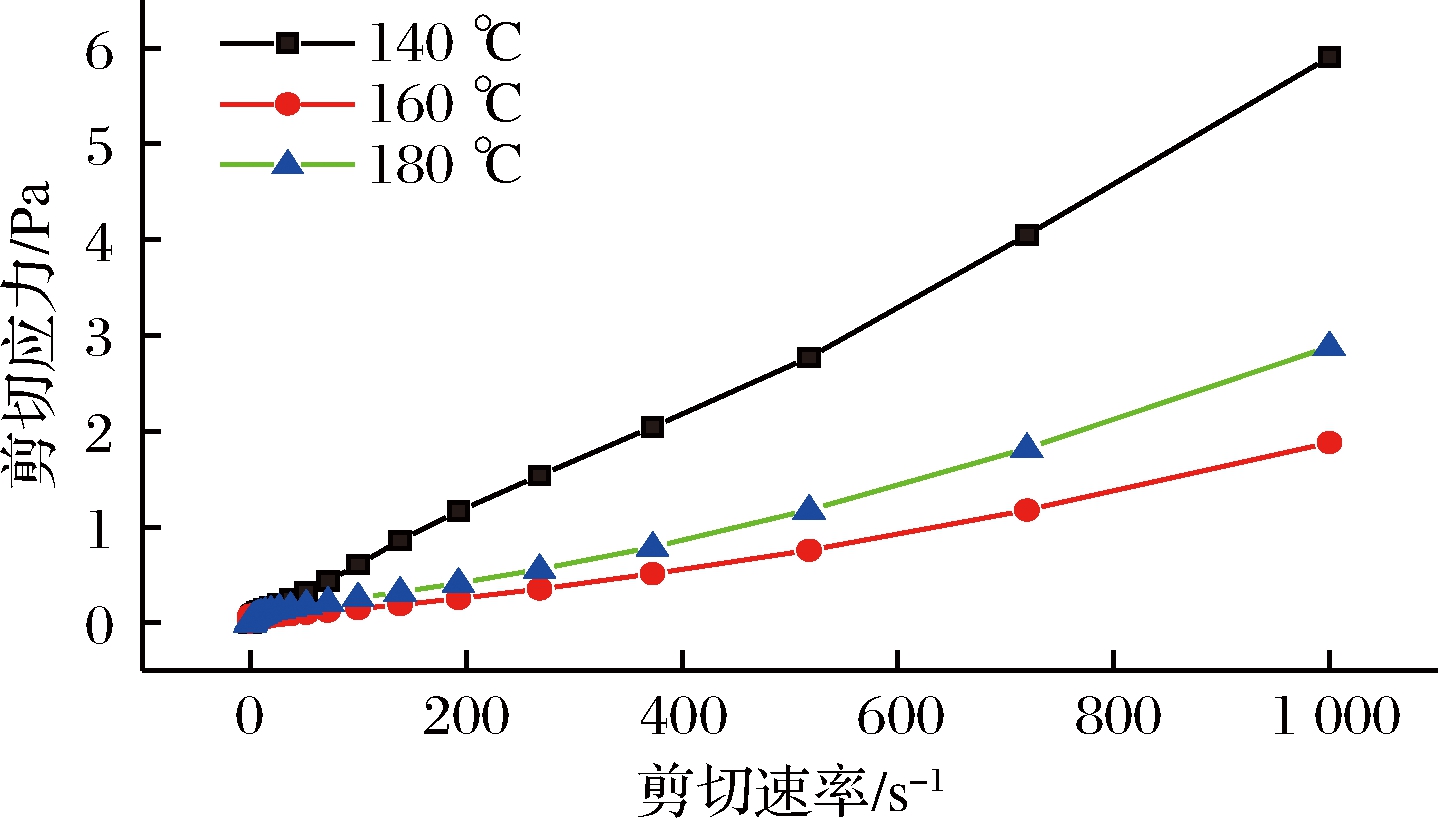
图2 不同干燥温度蛋清蛋白粉静态流变曲线
Fig.2 Static rheological curves of egg white protein powder with different drying temperatures
表1 不同干燥温度蛋清蛋白粉静态剪切曲线的拟合结果
Table 1 The fitting result of static shear curves of egg white protein powders with different drying temperatures

注:同列小写字母不同表示组间差异显著(P<0.05)(下同)
温度/℃屈服应力σ/Pa黏度系数k/(Pa·sn)流变特性指数n决定系数R21400.12±0.003b0.02±0.001a0.83±0.003c0.9941600.11±0.01c0.01±0.002c0.99±0.003a0.9971800.13±0.001a0.01±0.003b0.84±0.002b0.992
图2是不同干燥温度蛋清蛋白粉的静态剪切流变曲线,各曲线对Herrschel-Bulkey模型的拟合结果见表1。可知,不同干燥温度蛋清蛋白粉的剪切应力随剪切速率的的增加而增加,随着喷雾干燥入口温度的上升,体系所需的剪切应力逐渐减小,主要因为随着剪切速率的增大,蛋清蛋白溶液的流速加快,速度梯度随之变大,导致缠绕在一起的大分子物质发生变形或解体,从而剪切应力也随之降低。
根据Herrschel-Bulkey对流变数据点进行拟合,结果显示所有的曲线R2>0.99,说明不同干燥温度蛋清蛋白粉对Herrschel-Bulkey模型具有很好的相关性,拟合精度较高,模型较好。由表1可知,所有样品的流体指数n<1,表明样品均呈假塑性流体,具有剪切变稀性。在不同干燥温度中,140 ℃蛋清蛋白粉的n值最小,流体表现出的假塑性最强,这与稳态表观黏度曲线的变化趋势相对应。剪切稀化的现象对食品加工过程有重要影响,在物料体系中通过设置不同的喷雾干燥温度,改善其流变性能,适宜于高剪切速率下加工,改进物料输送和优化工艺条件,使能量消耗减少,能够更加易于产品加工。
2.2 动态频率扫描分析
不同干燥入口温度对蛋清蛋白的动态流动扫描的影响,如图3所示。
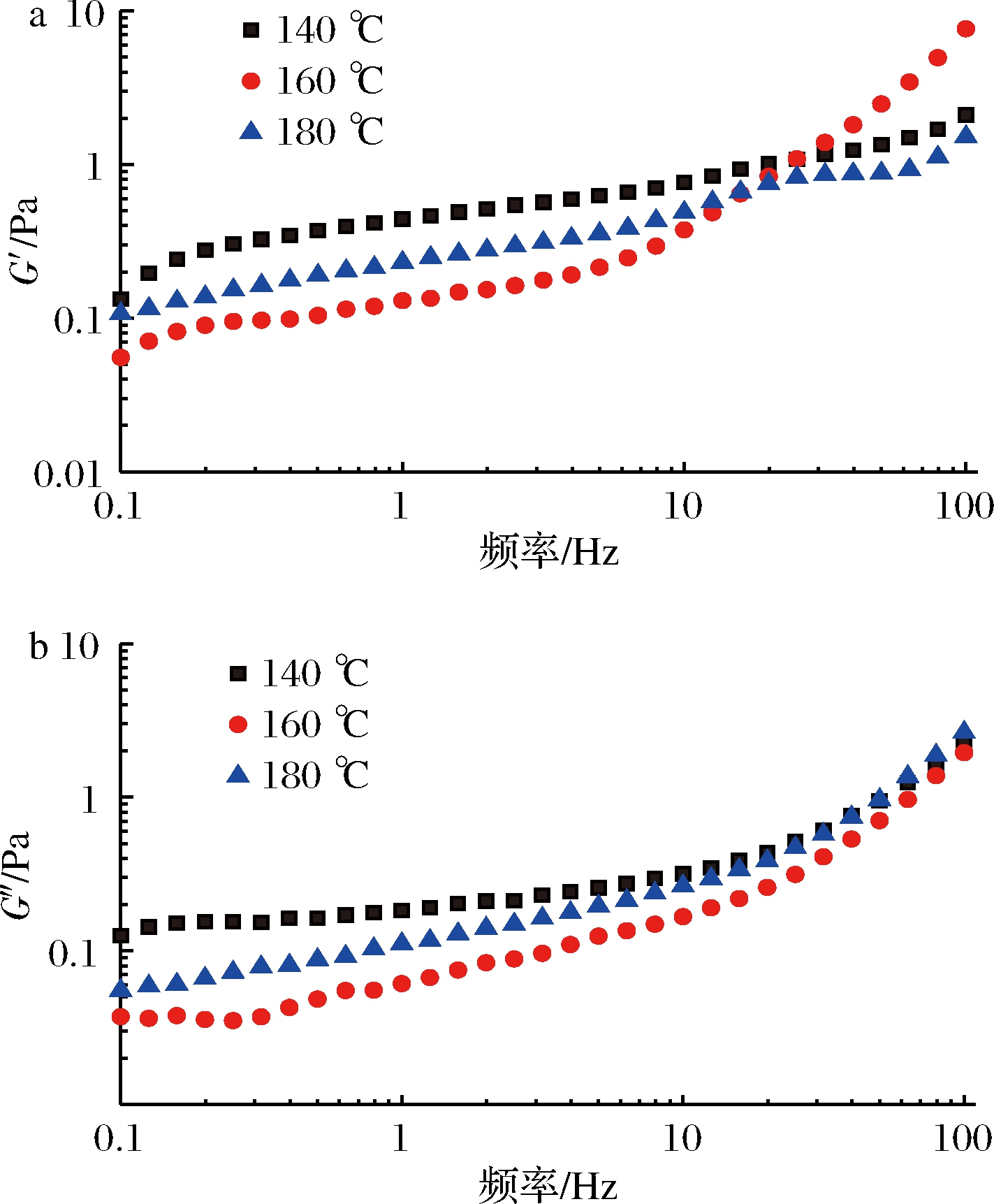
a-储能模量;b-损耗模量
图3 不同干燥温度的蛋清蛋白粉G′、G″随频率变化关系
Fig.3 Effect of different of egg wtite protein powder on G′ and G″ of dough as a function of frequency
在整个频率范围内,3种不同干燥温度蛋清蛋白粉的储能模量(G′)和损耗模量(G″)随角频率均成规律性的逐渐增加,3个样品的G′均高于G″,这表明所有样品的弹性大于黏性,即样品中弹性成分更突出,表现出黏弹性固体的性质[17]。
在频率增大的过程中,3个样品在0.836 2~20 Hz的低频率范围内,G′和G″急剧上升,达到20 Hz后上升的趋势变慢。在频率增大的过程中,3个样品的G′、G″的变化基本趋向一致。这与KANG等[18]研究结果一致。说明此弱凝胶体系在低频条件下体现出较好的弹性体性质,进一步验证干燥温度影响弱凝胶结构的强韧度。在20~78.53 Hz的高频区随着频率增加,G′出现陡增趋势,表明高频区各样品结构容易被破坏,产生切流变行为。在高频区G′的稳定性大小:160 ℃>140 ℃>180 ℃,这是由干燥温度引起蛋白质聚集、交联,使黏性胶体转变为有弹性的凝胶网络结构所致。
2.3 LF-NMR分析
不同干燥入口温度对蛋清蛋白弛豫时间的影响,如图4、表2所示。
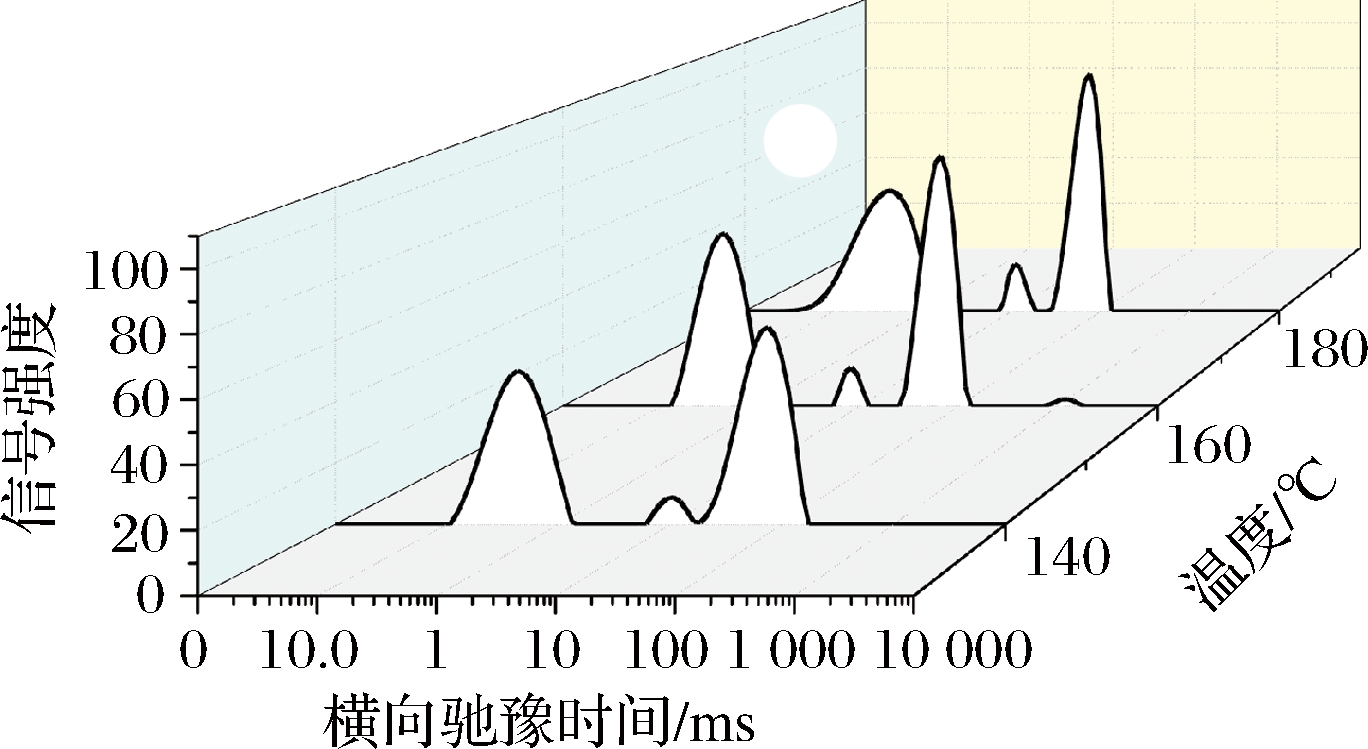
图4 蛋清蛋白粉横向弛豫时间T2变化的三维瀑布图
Fig.4 A three-dimensional waterfall plot for the transverse relaxation time T2 changes of egg white protein flour
表2 不同干燥温度对蛋清蛋白弛豫时间(T2)值变化的影响
Table 2 Effect of different drying temperature on the change of relaxation time (T2) value of egg white protein
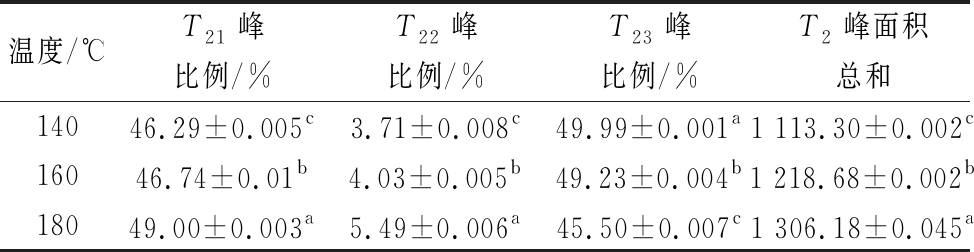
温度/℃T21峰比例/%T22峰比例/%T23峰比例/%T2峰面积总和14046.29±0.005c3.71±0.008c49.99±0.001a1 113.30±0.002c16046.74±0.01b4.03±0.005b49.23±0.004b1 218.68±0.002b18049.00±0.003a5.49±0.006a45.50±0.007c1 306.18±0.045a
如图4所示,3种不同干燥入口温度下制备蛋清蛋白粉的图谱上均有3个峰,代表样品中水分的不同存在状态,T21(0.01~5 ms)表示结合水,其是指与蛋白分子内部紧密结合的水质子;T22(5~20 ms)表示吸附水,其是指与蛋白分子表面结合的水质子;T23(20~1 000 ms)表示自由水,其是指蛋白质分子周围的游离水质子。另外,随着干燥温度的增加,信号幅值不断降低,水分逐渐被脱除。说明干燥温度能为蛋清蛋白的水质子提供能量,减弱与蛋白分子内部结合紧密的水分的吸附力,从而提高水分的迁移能力。观察结合水、自由水的水分状态分布可以发现,随着干燥温度的不断提高,自由水逐渐减少,且波峰逐渐往左偏移,表明蛋清蛋白在干燥过程中随着水分不断散失,蛋清蛋白内部自由水数量不断减少,自由水在蛋清蛋白内部流动性减弱,可迁移性降低。
由表2可知,在3种干燥温度条件下,结合水(T21)和吸附水(T22)峰比例显著增加(P<0.05),在180 ℃下T21和T22峰比例比其他2个温度下都高,T21峰比例增加意味着结合水的比例增加,这可能是由于总体上水分质量的减少引起的,也可理解为随着干燥温度的升高,自由水被脱除后,吸附水开始逐渐减少,一部分吸附水向外迁移为与蛋白质大分子紧密结合的结合水[19],导致结合水比例增大。此外,T22峰比例升高意味着吸附水比例的增大幅度较明显,随着脱水的进行,高自由度水分向低自由度水分的迁移转化速率加快[20]。
干燥温度对自由水(T23)峰比例有显著影响。自由水(T23)峰比例显著降低(P<0.05),在180 ℃下T23峰比例比其他2个温度下都低,可能是因为当干燥温度升高时,自由水含量在起始位置仍未变化,甚至由于不可移动水的转化还有一些增加。随着干燥的持续进行,不可移动水的含量大大减少,自由水含量也大大降低,这是由于水分受热蒸发散失所致。说明提高干燥温度使干燥介质产生了更多热能,提高自由水的内能及流动性,从而加快自由水的迁移与脱除,这与王雪媛等[21]研究结果相一致。通过干燥过程中各组分水比例的变化,可以看出不同干燥温度对蛋清蛋白内部水分迁移的影响不同。
此外,3个样品的T2峰面积总和存在显著差异(P<0.05),可能是干燥损失、干燥温度及干燥后处理样品等因素所导致的。
2.4 FT-IR分析
利用傅里叶红外光谱仪对不同干燥温度制备的蛋清蛋白进行全波段扫描,结果如图5、表3所示。
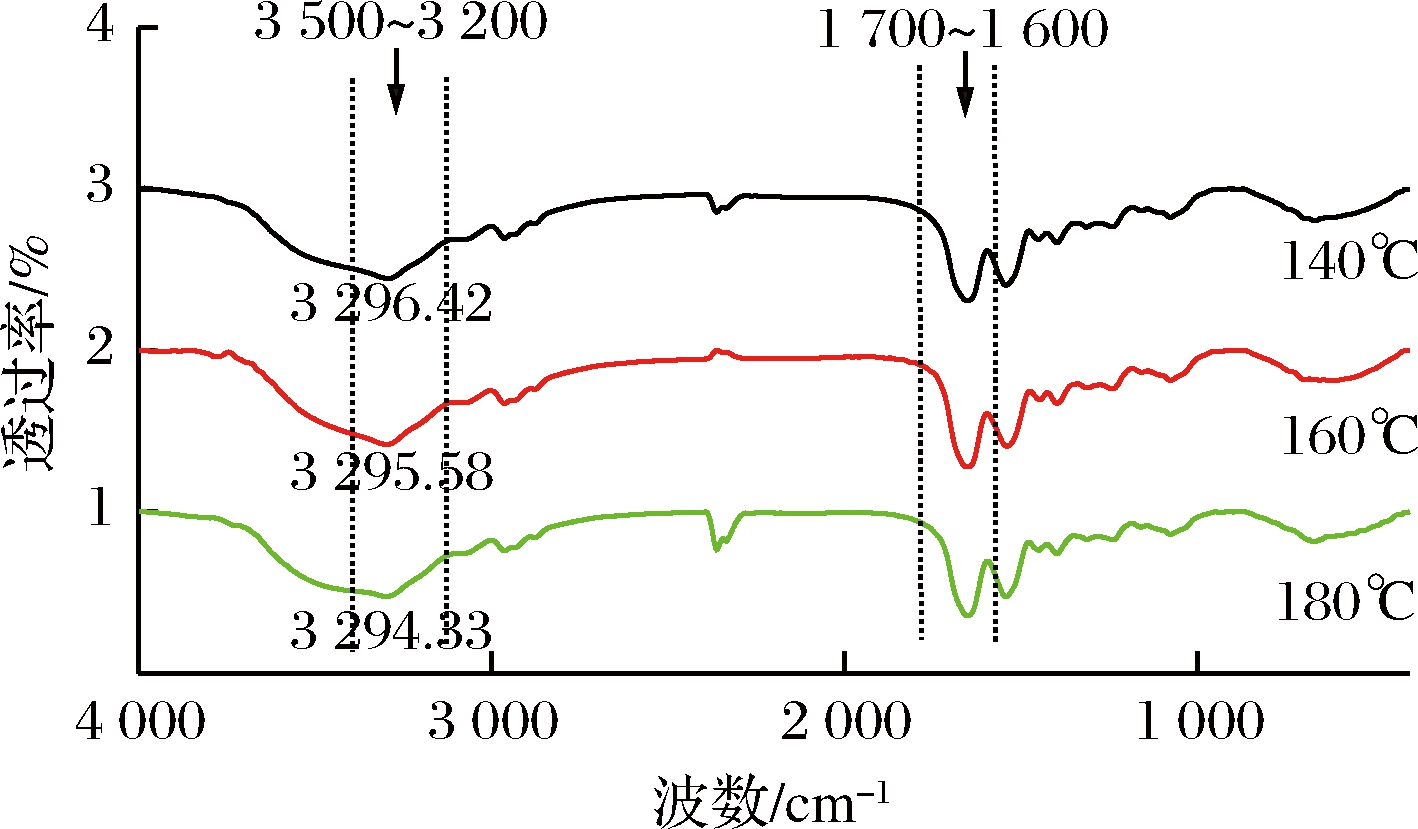
图5 不同干燥温度条件下蛋清蛋白FT-IR谱图
Fig.5 FT-IR spectra of egg white protein samples subjected to different drying temperatures
由图5可知,3种喷雾干燥温度制备的蛋清蛋白FT-IR谱图的谱型之间无较大差异。游离态O—H的特征吸收峰为3 500~3 200 cm-1,当它与分子内或分子间氢键缔合时,羟基的吸收峰将向低波数发生移动,且与N—H的特征吸收峰发生重叠从而使峰形变宽,说明缔合程度较大[22]。同时,蛋清蛋白的酰胺I带(1 600~1 700 cm-1)信号较强,主要由羰基(C![]() O)键伸缩振动引起[23]。酰胺I带的峰形随着干燥温度的升高,峰形由尖锐趋于平缓。采用Peak fit 4.12软件对不同干燥温度制备蛋清蛋白的酰胺I带峰强进行分析可知1 650~1 660 cm-1处峰表示α-螺旋结构;1 610~1 640 cm-1处峰表示β-折叠结构;1 660~1 695 cm-1处峰表示β-转角结构;1 640~1 650 cm-1处峰表示无规卷曲结构[24],常被用于蛋白质的二级结构分析。通常高温等处理会破坏分子内的氢键作用,影响蛋白质的二级结构单元,使得峰位迁移。
O)键伸缩振动引起[23]。酰胺I带的峰形随着干燥温度的升高,峰形由尖锐趋于平缓。采用Peak fit 4.12软件对不同干燥温度制备蛋清蛋白的酰胺I带峰强进行分析可知1 650~1 660 cm-1处峰表示α-螺旋结构;1 610~1 640 cm-1处峰表示β-折叠结构;1 660~1 695 cm-1处峰表示β-转角结构;1 640~1 650 cm-1处峰表示无规卷曲结构[24],常被用于蛋白质的二级结构分析。通常高温等处理会破坏分子内的氢键作用,影响蛋白质的二级结构单元,使得峰位迁移。
从峰位变化分析,140 ℃的酰胺I带为1 650.90 cm-1,160 ℃和180 ℃喷雾干燥蛋清蛋白的酰胺I带向低波数方向分别红移约0.91 cm-1和1.36 cm-1,即从1 650.90 cm-1分别位移至1 649.99 cm-1和1 649.54 cm-1,可见干燥温度使蛋白质高级结构出现展开或变性,游离氨基酸残基间形成分子间氢键[25],导致羰基键(C![]() O)的电子云密度降低,峰位发生位移,最终导致分子中的二级结构的单元组成发生了变化。对酰胺I带进行高斯曲线拟合分析,根据积分面积计算3个样品二级结构的相对百分含量,结果见表3。
O)的电子云密度降低,峰位发生位移,最终导致分子中的二级结构的单元组成发生了变化。对酰胺I带进行高斯曲线拟合分析,根据积分面积计算3个样品二级结构的相对百分含量,结果见表3。
表3 蛋清蛋白粉的二级结构含量(红外光谱)
Table 3 The secondary structure fractions of egg white protein powder (FT-IR)

温度/℃β-折叠/%α-螺旋/%β-转角/%无规卷曲/%14026.14±0.015b26.55±0.011a28.91±0.011b17.22±0.012c16027.38±0.012a21.81±0.01b30.12±0.014a21.97±0.004a18024.52±0.007c17.62±0.01c26.91±0.008c17.95±0.011b
结合表3可知,蛋清蛋白粉的二级结构以β-折叠和β-转角为主,随着喷雾干燥温度的升高蛋清蛋白粉二级结构发生变化,β-折叠和β-转角呈上升趋势,干燥温度在160 ℃时升到最高27.38%和30.12%,主要因为β-折叠结构含量增加与卵转铁蛋白热变性有关,所以当蛋清蛋白中的卵转铁蛋白发生了热变性并促进分子间的聚集时,β-折叠和β-转角含量增加;干燥温度在180 ℃时有所下降,可能是随着温度继续升高,卵转铁蛋白进一步形成更大的热聚合物,导致内部疏水基团暴露,表面疏水作用力增强[24],样品结构形成热聚集体,分子间的β-折叠结构易转变为β-转角结构。α-螺旋呈下降趋势,干燥温度在180 ℃时达到最低值17.62%。可能是因为随着干燥温度的升高,蛋清蛋白的结构稳定性降低,其热变性导致α-螺旋中的氢键断裂,发生解螺旋现象,从而导致α-螺旋结构比例降低[26]。无规卷曲呈上升趋势,干燥温度在160 ℃时升到最高21.97%,结果表明蛋清蛋白部分有序结构逐渐向无规卷曲结构转化,蛋白变性明显,其结构的随机性增强[27]。干燥温度在180 ℃时,无规卷曲结构比例反而下降,其原因可能是构象改变、转化等所致。T2峰面积总和存在显著差异(P<0.05),喷雾干燥温度可以降低蛋清蛋白粉的水分含量,随着喷雾干燥温度升高,能够明显提高干燥效率,改变蛋清蛋白中水的结合状态和水分分布。
2.5 SEM分析
对不同干燥温度制备的蛋清蛋白粉进行扫描电镜分析,结果见图6。

a-140 ℃;b-160 ℃;c-180 ℃
图6 三种干燥温度制备的鸡蛋清蛋白的SEM图(×1 000)
Fig.6 Scanning electron microscopy spectra of and egg white powders prepared by three inlet drying temperatures(×1 000)
由图6可知,干燥温度140 ℃下处理的蛋清蛋白的表面颗粒(图6-a)呈现完整的球状圆形外部结构,孔径处圆滑凹陷,而将干燥温度提高到160 ℃后(图6-b),蛋清蛋白的表面出现许多孔隙,略微凹凸不平,但仍然保持完整的颗粒结构;当干燥温度达到180 ℃时(图6-c),蛋清蛋白表面完整性遭到破坏,边界不明显,呈破损状。这些微观形貌的变化可能是由于喷雾干燥过程中水分脱除速度、剪切力等致使蛋白质分子间的氢键和范德华力发生断裂,破坏蛋白质分子之间的交联。毛莹等[28]研究喷雾干燥粉末出现的结构特征可能与样品的水分含量、操作温度、进料速率有关,与我们的研究结果相一致。有研究指出,蛋清蛋白的微观结构与其持水性关系密切,多孔洞球状结构更易于溶解。
3 结论
针对不同喷雾干燥入口温度(140、160、180 ℃)制备的鸡蛋清蛋白流变和结构特性的研究,发现蛋清蛋白溶液经干燥温度处理后可使表观黏度下降,且表观黏度随喷雾干燥温度的增加而降低,表观黏度由高到低分别为:140 ℃>180 ℃>160 ℃,不同干燥温度蛋清蛋白溶液的剪切应力随剪切速率的的增加而增加,喷雾干燥温度越高,G′和G″越小,在高频区G′的稳定性大小:160 ℃>140 ℃>180 ℃。随着干燥温度的逐渐升高,蛋清蛋白粉在干燥过程中水分不断散失,蛋清蛋白粉内部自由水数量不断减少,尤其是180 ℃蛋清蛋白粉的弛豫峰谱最为显著;随着喷雾入口温度升高,蛋清蛋白的红外图谱发生红移,三者的α-螺旋结构、β-折叠结构和β-转角结构含量均呈现先增加后减少的变化趋势,蛋清蛋白粉由颗粒完整的球状结构逐渐变为多孔隙破损状形态。因此,通过调节干燥温度,可制备出不同特性的高品质蛋清粉,对比3种不同蛋清粉样品可知,160 ℃蛋清蛋白粉的作用效果更加明显,可以更有效地改善蛋清蛋白的流变特性。
[1] SILVIA G, RAFFAELE V, CRISTINA A. An exploratory study for the technological classification of egg white powders based on infrared spectroscopy[J]. LWT, 2018, 96: 469-475.
[2] KATEKHONG W, BHANDARI B, JITTANIT W, et al. Effect of carbonation of fresh egg white prior to spray drying on physical and functional properties of powder[J]. Drying Technology, 2018,36(10):1 224-1 235.
[3] SCHOLES M S. Comparison of frozen, foam-spraydried, freeze-dried, and spray-dried eggs 7. soft meringues prepared with a carrageenan stabilizer[J]. Journal of Food Science, 1970,35(5):699-701.
[4] KATO A, IBRAHIM H R, WATANABE H, et al. New approach to improve the gelling and surface functional properties of dried egg white by heating in dry state[J]. Journal of Agricultural and Food Chemistry, 1989, 37(2):433-437.
[5] FRANKE K, KIEβLING M. Influence of spray drying conditions on functionality of dried whole egg[J]. Journal of the Science of Food & Agriculture, 2002, 82(15): 1 837-1 841.
[6] AYADI M A, KHEMAKHEM M, BELGITH H, et al. Effect of moderate spray drying conditions on functionality of dried egg white and whole egg[J]. Journal of Food Science, 2008, 73(6): 281-287.
[7] KOC B, YILMAZER M S, BALKIRr P, et al. Spray drying of yogurt: Optimization of process conditions for improving viability and other quality attributes[J]. Drying Technology, 2010, 28(4): 495-507.
[8] 孙临政, 迟玉杰, 王欢, 等. 喷雾干燥条件对蛋清粉冲调效果的影响[J]. 中国家禽, 2014, 36(2): 29-33.
SUN L Z, CHI Y J, WANC H, et al. Effect of condition of spray drying on egg white powder[J]. China Poultry, 2014, 36(2): 29-33.
[9] 沈青, 赵英, 迟玉杰, 等. 真空冷冻与喷雾干燥对鸡蛋全蛋粉理化性质及超微结构的影响[J]. 现代食品科技, 2015, 31(1): 147-152.
SHEN Q, ZHAO Y, CHI Y J, et al. Effects of freeze-drying and spray-drying on the physicochemical properties and ultrastructure of whole-egg powder[J]. Modern Food Science and Technology, 2015, 31(1): 147-152.
[10] 涂宗财, 王辉, 刘成梅, 等. 动态超高压均质对蛋清蛋白溶液的粒度和流变性影响[J]. 食品科学, 2007, 28(6): 27-29.
TU Z C, WANG H, LIU C M, et al. Effects of microfluidization on particle size and rheological properties of egg white proteins solution[J]. Food Science, 2007, 28(6): 27-29.
[11] 罗湛宏. 鸡蛋全粉酶解工艺的优化研究[J]. 农产品加工, 2019(1): 37-39.
LUO Z H. Optimization of the enzymatic hydrolysis technology of whole egg powder[J]. Academic Periodical of Farm Products Processing, 2019(1): 37-39.
[12] RAZI S M, MOTAMEDZADEGAN A, SHAHIDI A, et al. The effect of basil seed gum (BSG) on the rheological and physicochemical properties of heat-induced egg albumin gels[J]. Food Hydrocolloids, 2018, 82: 268-277.
[13] KIM C, YOO B. Rheological properties of rice starch-xanthan gum mixtures[J]. Journal of Food Engineering, 2006, 75(1): 120-128.
[14] 刘云宏, 孙畅莹, 曾雅. 直触式超声功率对梨片超声强化热风干燥水分迁移的影响[J]. 农业工程学报, 2018, 34(19): 284-292.
LIU Y H, SUN C Y, ZENG Y. Effect of contact ultrasound power on internal moisture migration of pear slices during uultrasound enhanced hot air drying[J]. Transactions of the Chinese Society of Agricultural Engineering, 2018, 34(19): 284-292.
[15] IMED H, PHILIPPE B, SABER H, et al. Interaction of milk alpha- and beta-caseins with tea polyphenols [J]. Food Chemistry, 2011, 126(2): 630-639.
[16] LEE K Y, LEE S, LEE H G. Effect of the degree of enzymatic hydrolysis on the physicochemical properties andin vitrodigestibility of rice starch[J]. Food Science & Biotechnology, 2010, 19(5): 1 333-1 340.
[17] ZHANG B X, WEI B X, HU X T, et al. Preparation and characterization of carboxymethyl starch microgel with different crosslinking densities[J]. Carbohydrate Polymers, 2015, 124:245-253.
[18] KANG Z L, LI B, MA H J, et al. Effect of different processing methods and salt content on the physicochemical and rheological properties of meat batters[J]. International Journal of Food Properties, 2016, 19(7): 1 604-1 615.
[19] YANG S L, LIU X Y, ZHANG M G, et al. Moisture-absorption and water dynamics in the powder of egg albumen peptide, Met-Pro-Asp-Ala-His-Leu[J]. Journal of Food Science, 2016, 82(1):53-60.
[20] KRISHNAMURTHY K, KHURANA H K, SOOJIN J, et al. Infrared heating in food processing: An overview[J]. Comprehensive Reviews in Food Science & Food Safety, 2010, 7(1): 2-13.
[21] 王雪媛, 高琨, 陈芹芹, 等. 苹果片中短波红外干燥过程中水分扩散特性[J]. 农业工程学报, 2015, 31(12): 275-281.
WANG X Y, GAO K, CHEN Q Q. et al. Water diffusion characteristics of apple slices during short and medium-wave infrared drying[J]. Transactions of the Chinese Society of Agricultural Engineering, 2015, 31(12): 275-281.
[22] 秦洋, 邱超, 曹金苗, 等. 干热处理对稻米复配粉及米蛋白性质的影响[J]. 现代食品科技, 2015, 31(9): 180-184.
QIN Y, QIU C, CAO J M, et al. Effect of dry heat treatment on the properties of glutinous rice mixed flour and rice proteins[J]. Modern Food Science & Technology, 2015, 31(9): 180-184.
[23] MORAND M, GUYOMARC′H F, PEZENNEC S, et al. On how κ-casein affects the interactions between the heat-induced whey protein/κ-casein complexes and the casein micelles during the acid gelation of skim milk[J]. International Dairy Journal, 2011, 21(9):670-678.
[24] 张同刚, 罗瑞明, 李亚蕾, 等. 拉曼光谱分析牛肉贮藏过程中肌红蛋白结构的变化[J]. 食品科学, 2019, 40(7): 15-19.
ZHANG T G, LUO R M, LI Y L, et al. Structural changes of myoglobin during beef storage as analyzed by raman spectroscopy[J]. Food Science, 2019, 40(7): 15-19.
[25] 石燕, 刘凡, 葛辉, 等. 微胶囊形成过程中蛋白质二级结构变化的红外光谱分析[J]. 光谱学与光谱分析, 2012, 32(7):1 815-1 819.
SHI Y, LIU F, GE H, et al. Study on secondary structural changes of protein in the formation of microcapsule by ftir spectroscopy[J]. Spectroscopy and Spectral Analsis, 2012, 32(7):1 815-1 819.
[26] 吴黎明, 周群, 周骁, 等. 蜂王浆不同贮存条件下蛋白质二级结构的Fourier变换红外光谱研究[J]. 光谱学与光谱分析, 2009, 29(1): 82-87.
WU L M, ZHOU Q, ZHOU X, et al. FTIR assessment of the secondary structure of proteins in royal jelly under different storage conditions[J]. Spectroscopy and Spectral Analsis, 2009, 29(1): 82-87.
[27] SHILPASHREE B G, ARORA S, CHAWLA P, et al. Effect of succinylation on physicochemical and functional properties of milk protein concentrate[J]. Food Research International, 2015, 72:223-230.
[28] 毛莹, 帅晓艳, 王惠玲, 等. 基于内源乳化法和喷雾干燥优化制备花色苷微胶囊及其稳定性分析[J]. 食品科学, 2020, 41(2): 267-275.
MAO Y, SHUAI X Y, WANG H L, et al. Preparation and stability evaluation of anthocyanin microcapsules by emulsification/internal gelation with optimized spray drying[J]. Food Science, 2020, 41(2):267-275.