西藏传统青稞酒,藏语叫做“穹chong”,[1]是藏族人民最主要的酒精饮料,至今已有1 000多年的历史[2]。西藏传统青稞酒以青藏高原特有的青稞为原料,以藏曲为糖化发酵剂酿造而成。它的酿造方法是将青稞浸泡后加水煮熟,待其冷却后加入藏曲,保温发酵3 d左右,加水充分浸泡后过滤酿成新鲜可口的传统青稞酒[3]。该酒酒味酸甜,酒香浓郁,饮后不上头,不口渴,风格独特,深受青藏高原人民的喜爱,被视作西藏传统文化的一部分。
藏曲是西藏传统青稞酒的核心,藏曲是西藏人民按照传统接种方式以及自己的理解制作而成的西藏传统青稞酒糖化发酵剂的统称[4]。因此藏曲种类丰富,并直接影响青稞酒的风味与品质,而藏曲中的菌种更是产生西藏传统青稞酒独特风味的主要因素之一。藏曲中微生物种类复杂,袁亦舟等[5]用高通量测序鉴定了藏曲中主要的微生物有霉菌,酵母与细菌3类,霉菌主要起糖化作用,而酵母主要起产酒作用。如其他发酵酒一样,西藏传统酿造青稞酒生产中酵母的发酵作用,贯穿了整个酿造过程[6]。杜木英[7]分离鉴定了藏曲中含有酿酒酵母,扣囊复膜孢酵母,汉逊德巴利酵母等,他还分别分离筛选了糖化力较强和酒化力较强的酵母。刘清斌等[8]研究不同菌种和不同菌种接种量对青稞酒发酵的影响时,发现在青稞酒中酿酒酵母产酒能力最强。酵母菌作为酿酒的一类主要微生物,其作用不仅限于酒精代谢,也发挥着重要的风味代谢功能[9],然而现在对于传统酿造青稞酒中酵母风味代谢的研究较少,而在其他发酵酒中研究发现酵母菌以及混菌发酵的风味代谢对酿酒的品质具有重要的影响。唐洁等[10]发现在清香型白酒中将酿酒酵母与异常毕赤酵母混合发酵,在保证酵母发酵性能的前提下,能够形成更多的酯类物质,总酸和高级醇含量却相对较低,能有效提升发酵液的风味特征。邱并生[11]基于2种酵母混菌发酵能提升发酵产品的风味特性这一特点,在小曲白酒的生产上采用了功能酵母纯种制曲,提升了白酒的品质。陈景桦、许维娜等[12-13]研究了多种酵母以及多种酿酒酵母的混菌发酵,都能提升葡萄酒的品质,使得葡萄酒表现出更复杂馥郁的特征。张文文等[14]发现采用东方伊萨酵母和酿酒酵母发酵杨梅酒能提升发酵效率,减少涩味,提升品质。因此多种酵母混菌发酵能有效提升酒的品质,研究西藏传统青稞酒中酵母的风味代谢功能十分必要。基于现在对于西藏传统青稞酒酿酒酵母类型以及风味代谢功能研究的不足,本文通过可培养方法分离鉴定了不同地域藏曲中的酵母菌,找到了藏曲中的主要酵母菌,并通过模拟发酵实验,从产酒和产风味物质两个层面全面分析了藏曲中主要酵母菌的酿造功能。这对西藏传统青稞酒品质的科学控制提供了依据,也为其工业化生产提供了理论基础。
1 材料与方法
1.1 材料与试剂
藏曲,分别采购生产于拉萨、林芝、日喀则及山南地区的5种不同形态藏曲样品;青稞,由西藏天佑德青稞酒业有限责任公司提供。
苯酚、氯仿、KH2PO4、溴甲酚绿、曲拉通、氨苄青霉素(分析纯),国药集团;酵母膏、蛋白胨(分析纯),Oxiod公司;琼脂(分析纯),BioSHARP公司;实验用水均为煮沸5 min后冷却至室温的超纯水。
1.2 培养基
YPD培养基(质量分数):酵母膏1%,蛋白胨2%,葡萄糖2%,琼脂粉2%(固体培养基)。WL培养基[15](g/L):酵母粉4.0,蛋白胨5.0,葡萄糖50,琼脂20.0,KH2PO4 0.55,KCl 0.425,MgSO4 0.125,FeCl30.002 5,MnSO4 0.002 5,溴甲酚绿22.0,曲拉通X-1002,氨苄青霉素0.1。青稞汁培养基:取脱壳青稞1 500 g洗净后加水浸泡3 h,蒸煮1 h后加入1%(质量分数)的糖化酶、液化酶、蛋白酶,加入矿泉水3 000 mL,放入45 ℃烘箱中糖化6 h,测得糖度17 °Bx。纱布过滤后离心机6 000 r/min离心10 min后装瓶,放-20 ℃冰箱冷冻保藏。
1.3 仪器与设备
3K15冷冻离心机,美国 Sigma-Aldrich公司;GC 6890 N-MSD5975气相色谱质谱联用仪、GC6890 N气相色谱仪,美国Agilent公司;BSP-250生化培养箱,上海博迅实业有限公司医疗设备;AS2060B超声波清洗器,德国Elma公司;超高效液相色谱仪,美国Waters公司。
1.4 酵母菌分离与纯化
根据所需平板量准确配制WL培养基筛选酵母菌;取粉碎好的青稞酒曲5 g,10倍逐级稀释;采用10-5,10-6,10-7三个梯度,每个梯度2个平行;将平板置于30 ℃培养箱培养3~4 d;配制YPD平板;根据WL平板上酵母菌落形态有选择地挑选数株菌转移到YPD平板上,划线培养,30 ℃培养2~3 d,保存备用。
1.5 酵母菌鉴定
采用试剂盒提取法提取分离菌种基因组,进行聚合酶链式反应(polymerase chain reaction,PCR)扩增,PCR体系为超纯水10.5 μL,Mix酶12.5 μL,引物1(NL1)0.5 μL,引物2(NL4)0.5 μL,模板1.0 μL。PCR产物经0.8%(质量分数)凝胶电泳检测。
1.6 酵母形态的电镜分析
将菌体用磷酸缓冲液洗去培养基,加入3%(体积分数)戊二醛固定5 h以上;用磷酸缓冲液浸泡洗涤6次,每次20 min;用体积分数为30%、40%、50%、60%、70%、80%、90%、100%的乙醇,逐级脱水,每级15 min。用叔丁醇置换2次,1次20 min,最后将样品置于电子显微镜下观察[16]。
1.7 不同种类酵母菌发酵性能与风味代谢分析
1.7.1 不同种类酵母菌发酵性能分析
每类酵母挑选3株菌株接种到装有青稞汁培养基的15 mm×150 mm试管中,摇床30 ℃培养24 h;将种子液接种到装有115 ℃灭菌30 min的150 mL青稞汁的三角瓶中,接种量为5%,加上发酵栓,用5 mol/L的硫酸液封;30 ℃培养箱发酵5 d左右。参照韩德权等[17]采用二硝基水杨酸法,测量发酵液中残余还原糖含量。参照林艳等[18]通过安捷伦1200液相仪检测乙醇含量。参照徐勇等[19]通过超高效液相色谱(ultra performance liquid chromatography,UPLC)检测有机酸含量,色谱条件如下,色谱柱ACQUITY UPLC HSS T3(i.d 2.12.1 UPL,1.8 2.);流动相20.00 mmol/L的NaH2PO4溶液(pH 2.7);检测波长210 nm,柱温30 ℃,流速0.25 mL/min,进样1 μL。
1.7.2 青稞汁发酵液挥发性风味成分分析
参照陈双[20]报告的香气物质提取和分离方法。顶空固相微萃取(head space-solid phase microextraction,HS-SPME)及进样过程由Gerstel公司复合自动进样系统(MPS 2)完成,萃取头为2 cm 50/30 μm DVB/CAR/PDMS三相萃取头。萃取温度50 ℃,样品平衡时间5 min,萃取时间50 min,孵化器转速500 r/min。样品前处理流程:顶空瓶中称取2.5 g的NaCl,加入4 mL样品,4 mL去离子水,再加内标(81 mg/L 2-辛醇)10 μL,用带PTFE/蓝色硅胶隔垫的空心磁性金属盖密封后进行由MPS 2进行HS-SPME操作,完成萃取过程后萃取头于GC进样口250 ℃解吸附5 min后,用于气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)定性和定量分析。
GC条件:高纯氮气为载气,流速2 mL/min。不分流进样。色谱柱为DB-FFAP(60 m×0.32 mm×0.25 μm,Agilent)。起始温度为40 ℃,保持2 min,以5 ℃/min升温至230 ℃,保持10 min。
MS条件:电离方式为EI,电子能量70 eV,离子源温度230 ℃,扫描范围35.00~350.00 amu。未知化合物通过保留指数和标准品质谱图进行比对鉴定。化合物的定量采用内标半定量的方式进行定量分析。
2 结果与分析
2.1 西藏传统青稞酒酿造用藏曲中主要酵母的分离鉴定
选择来自西藏传统青稞酒主产地的拉萨、林芝、日喀则及山南地区的5种不同形态的藏曲样品,用WL鉴别培养基对5种藏曲分别进行分离培养,在培养中可以从酵母形态上观察藏曲中主要的酵母种类,根据它们的形态差异有选择的挑选主要酵母分离纯化:其中共分离出山南①号11株,山南②号11株,日喀则11株,林芝7株,拉萨8株。分别记为山南①号(S1)、山南②号(S2)、日喀则(R)、林芝(LN)和拉萨(LA)。提取上述分离出的菌株的基因组进行测序分析,测序结果与NCBI比对,比对结果如下,分离的酵母菌株中鉴定到种后主要分为3类:酿酒酵母(Saccharomyces cerevisiae,S.cerevisiae)31株,扣囊复膜孢酵母(Saccharomycopsis fibuliger,S.fibuligera)9株,Saccharomycopsis malanga(S.malanga) 3株。为进一步鉴定酵母采用了电镜观察,3种酵母的电镜照片如图1所示。其中酿酒酵母普遍存在于各种酒曲之中,产酒产香能力突出。扣囊复膜孢酵母曾被杜木英[7]在西藏传统酿造青稞酒中初步检测到并筛选了糖化力强的菌株,它在酿酒中起糖化、发酵、生香的作用。国内酿酒行业对扣囊复膜孢酵母研究主要集中于米酒、黄酒与清香型白酒[21],应玲云等[22]发现烧酒曲中存在扣囊复膜孢酵母,但它在清香、酱香、浓香3种大曲中也常被发现。郝文军等[23]发现牛栏山酒中含扣囊复膜孢酵母。THAKUR等[24]在印度的传统青稞酒饮料中发现酿酒酵母,扣囊复膜孢酵母。同时NAOKO等[25]发现扣囊复膜孢酵母能分泌胞外淀粉酶,对青稞淀粉的液化水解起到一定作用。而S.malanga在国内青稞酒中未见报道,此次为首次发现其为藏曲中的主要菌。BHARDWAJ等[26]在位于喜马拉雅山脉的印度青稞酒饮料中发现了S.malanga。

A- S.cerevisiae;B-S.fibuligera;C-S.malanga
图1 西藏传统酿造青稞酒酿造用藏曲中主要酵母菌电镜图
Fig.1 Electron micrographs of main yeasts in Zangqu of traditional Tibetan Qingke wine
2.2 藏曲中主要酵母菌的酿造性能分析
酵母菌作为青稞酒酿造的一类主要功能微生物,为了解析不同酵母在青稞酒酿造中的功能,研究从分离的3类酵母中分别选择了3株酵母进行青稞汁模拟发酵实验,对不同酵母产酒、产酸和产挥发性风味物质的代谢能力进行了系统分析。
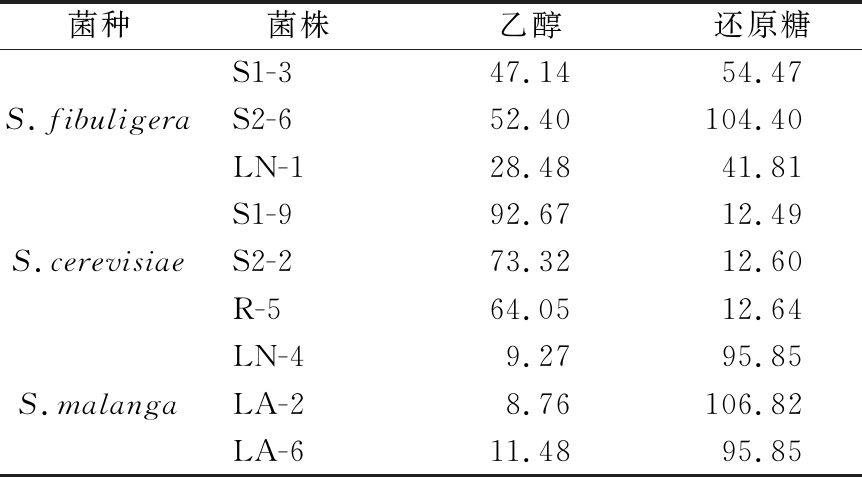
9株酵母发酵性能如表1所示,在无氧条件下,酵母通过发酵作用转化青稞汁中的还原糖为CO2与乙醇,发酵后发酵液中的还原糖含量越少,发酵反应越彻底,乙醇含量越高。接种了酿酒酵母发酵液的乙醇浓度最高,扣囊复膜孢酵母次之,S.malanga最低。同时接种酿酒酵母的青稞汁发酵后残余的还原糖含量远低于接种扣囊复膜孢酵母与接种S.Malanga的。说明接种了酿酒酵母的青稞汁发酵最为彻底,3种酵母中酿酒酵母发酵能力最强,扣囊复膜孢酵母次之。接种3株不同菌株酿酒酵母的青稞汁残余的还原糖含量较为接近,说明其发酵能力较为稳定。而接种不同菌株的扣囊复膜孢酵母与接种S.Malanga的青稞汁还原糖含量有较大波动,不同菌株的扣囊复膜孢酵母与S.Malanga的发酵能力有较大差异。
表1 西藏传统酿造青稞酒酿造用藏曲中主要酵母发酵性能分析 单位:g/L
Table 1 Analysis of fermentation performance of main yeasts in Zangqu used in traditional Tibetan Qingke wine
菌种菌株乙醇还原糖S1-347.1454.47S.fibuligeraS2-652.40104.40LN-128.4841.81S1-992.6712.49S.cerevisiaeS2-273.3212.60R-564.0512.64LN-49.2795.85S.malangaLA-28.76106.82LA-611.4895.85
2.3 产酸能力的检测与分析
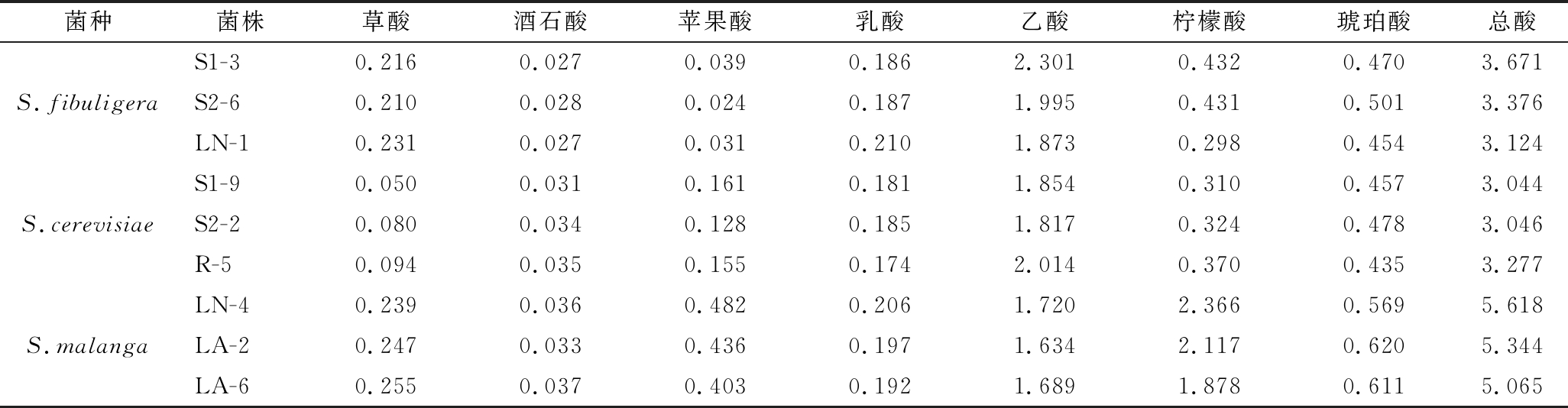
对不同酵母菌青稞汁发酵液有机酸含量的测量结果如表2所示。青稞汁发酵液中乙酸、琥珀酸和柠檬酸是主要的有机酸,而酒石酸、苹果酸和乳酸含量相对较低。乙酸有一种特有的味道,会对人的舌后部产生较强的刺激。而乳酸较涩感锐利。琥珀酸口味很复杂,除了有酸味外,还有一种咸味、苦味,在酒的风味形成过程中有助于形成丰富的酯类物质,是富于味觉反应的一种酸[27]。而苹果酸酸味较柠檬酸强,刺激爽口,略有苦涩感,呈味时间较长[28];柠檬酸给人一种清新宜人的口感,酸味圆润、清爽,后苦时间短[27]。在3种酵母中,产乙酸和乳酸含量相似,S.malanga产乙酸较弱而产乳酸较强。S.malanga产草酸含量高于扣囊复膜孢酵母,而酿酒酵母最低且与前两者有着数倍的差距。3种酵母中S.malanga产琥珀酸能力较强。苹果酸和柠檬酸是3种酵母模拟发酵液中含量差异较大的2种有机酸,扣囊复膜孢酵母基本不产苹果酸而S.malanga产苹果酸与柠檬酸量远高于其他2种酵母菌。同时在3种酵母中S.malanga产酸含量最高,扣囊复膜孢酵母其次,酿酒酵母最低。
表2 青稞汁发酵液有机酸分析 单位:g/L
Table 2 Organic acid analysis of fermentation broth of Qingke culture medium
菌种菌株草酸酒石酸苹果酸乳酸乙酸柠檬酸琥珀酸总酸S1-30.2160.0270.0390.1862.3010.4320.4703.671S.fibuligeraS2-60.2100.0280.0240.1871.9950.4310.5013.376LN-10.2310.0270.0310.2101.8730.2980.4543.124S1-90.0500.0310.1610.1811.8540.3100.4573.044S.cerevisiaeS2-20.0800.0340.1280.1851.8170.3240.4783.046R-50.0940.0350.1550.1742.0140.3700.4353.277LN-40.2390.0360.4820.2061.7202.3660.5695.618S.malangaLA-20.2470.0330.4360.1971.6342.1170.6205.344LA-60.2550.0370.4030.1921.6891.8780.6115.065
2.4 挥发性风味物质的检测与分析
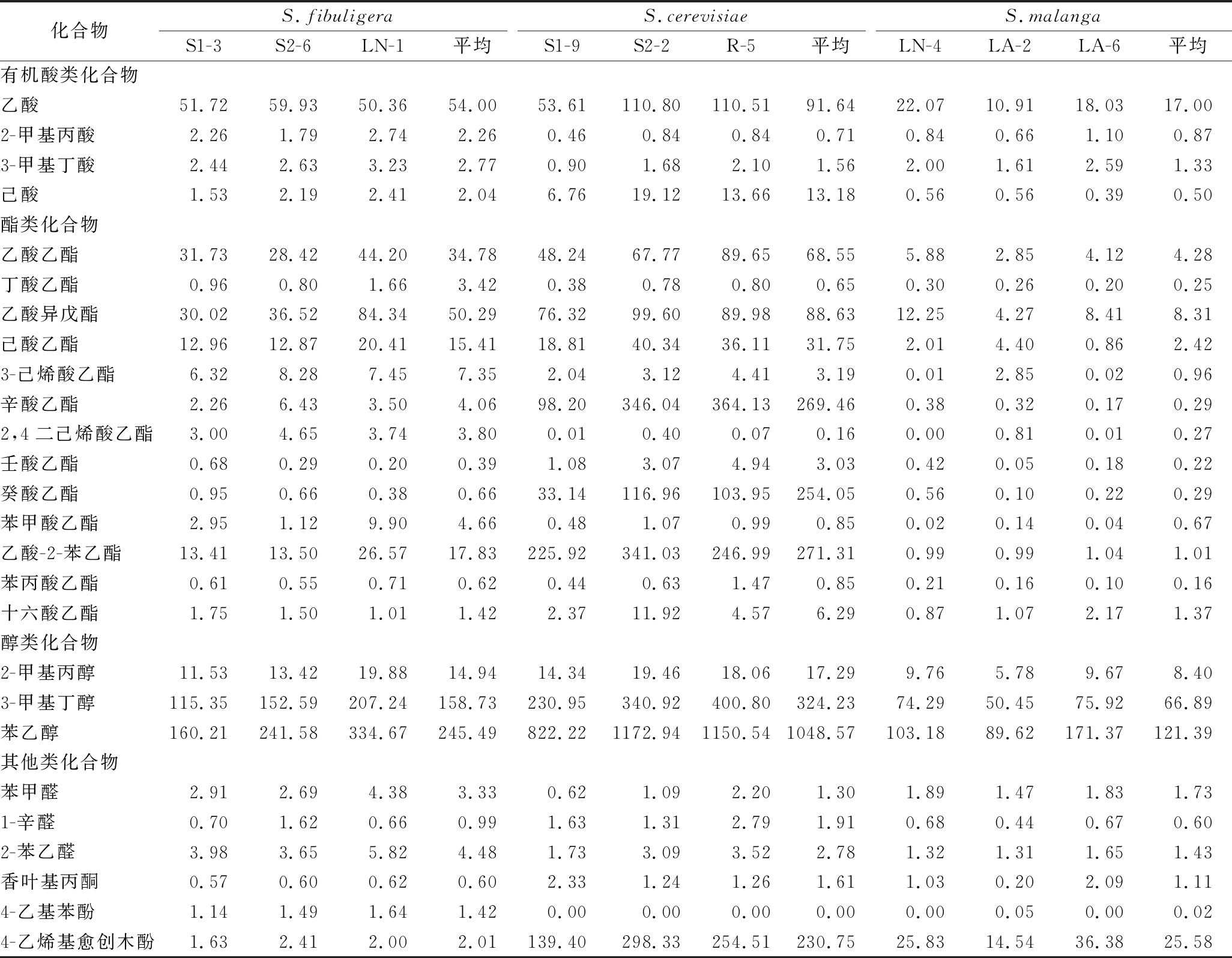
采用HS-SPME-GC-MS技术分析了不同酵母青稞汁发酵液中挥发性组分种类和含量差异,结果如表3所示。在青稞汁发酵液中检测出的风味物质共26种,包含4种挥发性有机酸,13种酯类化合物,3种醇类化合物,4种醛酮类化合物和2种挥发性酚类化合物。
比较不同种类酵母菌风味代谢特征可知,3种酵母发酵液中风味物质成分相差不大但风味物质含量却存在着显著差异,S.malanga产风味物质较少,除醇类化合物外,其他风味物质产量极低。3种酵母中,酿酒酵母产风味物质最多,各类风味物质总含量均高于其他2种酵母,其中少量物质含量低于扣囊复膜孢酵母。
在发酵培养基中,2,4二己烯酸乙酯,丁酸乙酯和3-己烯酸乙酯的含量扣囊复膜孢酵母略高于酿酒酵母。其他酯类物质含量酿酒酵母均高于扣囊复膜孢酵母与S.malanga。其中S.malanga酯类物质含量极低,显示其在酯类风味上的贡献较小;扣囊复膜孢酵母所产分子质量较小的酯类物质较多而产分子质量较大的酯类物质较少;酿酒酵母产乙酸乙酯、乙酸异戊酯、己酸乙酯、辛酸乙酯、癸酸乙酯与乙酸-2-苯乙酯含量较高,它们在酿酒酵母所产酯类物质含量占比达95%以上。酯类物质中乙酸乙酯、乙酸异戊酯、己酸乙酯和乙酸-2-苯乙酯都是重要的风味物质。乙酸乙酯、乙酸异戊酯与己酸乙酯均在接种酿酒酵母的发酵液中产量最高,略高于在接种了扣囊复膜孢酵母的发酵液中的产量。其中乙酸乙酯具有果香、酒香,乙酸异戊酯呈香蕉香,己酸乙酯似菠萝、香蕉水果香。因为酿酒酵母所产的酯类风味物质含量最高,而扣囊复膜孢酵母与酿酒酵母所产风味物质有着显著差异,因此在青稞酒曲中适量的酿酒酵母与扣囊复膜孢酵母有助于青稞酒风味的提升。孙思佳等[29]发现扣囊复膜孢酵母强化高温大曲能有效提升芝麻香型白酒的品质使其香气浓郁。王晓丹等[30]发现在酱香型白酒大曲中存在扣囊复膜孢酵母,其发酵物以乙酸乙酯、乙酸异戊酯、苯乙醇、乙酸苯乙酯、棕榈酸乙酯含量较高,与本文基本对应。
同时比较其他风味物质我们可以看出,酿酒酵母所产的3种醇类风味物质都远高于另2种酵母,S.malanga最低。苯乙醇平均含量高于其他检测出的风味组分。苯乙醇为玫瑰花香,月季花香,花粉香味,能对酒提供较好的风味[31],是一个很重要的天然香味物质。酿酒酵母发酵液中的4-乙烯基愈创木酚含量最高,十倍于S.malanga,百倍于扣囊复膜孢酵母。4-乙烯基愈创木酚有甜香,花香,水果香,香瓜香,是白酒、啤酒(特别是小麦啤酒)、葡萄酒、酱油等产品的重要呈香物质。正是不同的菌所产风味物质的含量与种类不同,藏曲中种类繁多微生物的配合作用产出了如此独特风味的西藏传统酿造青稞酒。
表3 不同酵母菌青稞汁发酵液挥发性风味组分含量差异分析 单位:μg/L
Table 3 Difference content analysis of volatile flavor components in fermentation Qingke culture medium with different yeasts
化合物S.fibuligeraS.cerevisiaeS.malangaS1-3S2-6LN-1平均S1-9S2-2R-5平均LN-4LA-2LA-6平均有机酸类化合物乙酸51.7259.9350.3654.0053.61110.80110.5191.6422.0710.9118.0317.002-甲基丙酸2.261.792.742.260.460.840.840.710.840.661.100.873-甲基丁酸2.442.633.232.770.901.682.101.562.001.612.591.33己酸1.532.192.412.046.7619.1213.6613.180.560.560.390.50酯类化合物乙酸乙酯31.7328.4244.2034.7848.2467.7789.6568.555.882.854.124.28丁酸乙酯0.960.801.663.420.380.780.800.650.300.260.200.25乙酸异戊酯30.0236.5284.3450.2976.3299.6089.9888.6312.254.278.418.31己酸乙酯12.9612.8720.4115.4118.8140.3436.1131.752.014.400.862.423-己烯酸乙酯6.328.287.457.352.043.124.413.190.012.850.020.96辛酸乙酯2.266.433.504.0698.20346.04364.13269.460.380.320.170.292,4二己烯酸乙酯3.004.653.743.800.010.400.070.160.000.810.010.27壬酸乙酯0.680.290.200.391.083.074.943.030.420.050.180.22癸酸乙酯0.950.660.380.6633.14116.96103.95254.050.560.100.220.29苯甲酸乙酯2.951.129.904.660.481.070.990.850.020.140.040.67乙酸-2-苯乙酯13.4113.5026.5717.83225.92341.03246.99271.310.990.991.041.01苯丙酸乙酯0.610.550.710.620.440.631.470.850.210.160.100.16十六酸乙酯1.751.501.011.422.3711.924.576.290.871.072.171.37醇类化合物2-甲基丙醇11.5313.4219.8814.9414.3419.4618.0617.299.765.789.678.403-甲基丁醇115.35152.59207.24158.73230.95340.92400.80324.2374.2950.4575.9266.89苯乙醇160.21241.58334.67245.49822.221172.941150.541048.57103.1889.62171.37121.39其他类化合物苯甲醛2.912.694.383.330.621.092.201.301.891.471.831.731-辛醛0.701.620.660.991.631.312.791.910.680.440.670.602-苯乙醛3.983.655.824.481.733.093.522.781.321.311.651.43香叶基丙酮0.570.600.620.602.331.241.261.611.030.202.091.114-乙基苯酚1.141.491.641.420.000.000.000.000.000.050.000.024-乙烯基愈创木酚1.632.412.002.01139.40298.33254.51230.7525.8314.5436.3825.58
3 结论
研究发现青稞酒中的主要酵母可能为酿酒酵母、扣囊复膜孢酵母与S.malanga,其中酿酒酵母的发酵能力最为优秀也能产出最多风味物质,S.malanga产酸能力最强,扣囊复膜孢酵母则居于两者中间,藏曲中含适量酿酒酵母,扣囊复膜孢酵母与S.malanga就极为重要,酿酒酵母过少将导致发酵能力下降,成品酒酒精度不高且风味物质较少,扣囊复膜孢酵母有分泌胞外淀粉酶的能力,对淀粉液化水解起一定作用,如果S.malanga过少将导致酸度不足,影响成品酒风格形成,合理配置藏曲中微生物成分与含量可有效提升酒的品质,对青稞酒发酵产生不可替代的影响。
青稞酒是我国独有的发酵酒,本次研究揭示了酿酒酵母,扣囊复膜孢酵母与S.malanga为青稞酒中主要酵母,也对比了三者的发酵能力、产酸和风味物质的能力,但是对青稞酒曲的微生物成分与含量的研究工作仍需继续进行,尤其是如何配比能提升酒的口感与风味,使青稞酒生产规范化。
[1] 杨晓梅, 次仁觉旦, 赵晓通.藏民族传统酿制的青稞酒有效成分测定及影响因素探讨[J].食品与发酵科技, 2008,44(2):15-17.
YANG X M, CI R J D, ZHAO X T.Determination of Tibetan traditional fermenting barley wine′s effective component and study of influence factors[J].Food and Fermentation Science & Technology, 2008, 44(2):15-17.
[2] 伍怡郦. 西藏传统青稞酒发酵技术的研究 [D].重庆:西南大学, 2006.
WU Y L.Studies on fermentation technique of tranditional highland barley wine in Tibet[D].Chongqing:Southwest University, 2006.
[3] 杜木英, 伍怡郦, 阚建全, 等.传统青稞酒发酵过程中化学成分动态变化的研究[J].食品工业科技, 2007,28(9):94-98.
DU M Y, WU Y L, KAN J Q, et al.Study on dynamic changes of chemical components in traditional highland barley wine during fermentation[J].Science and Technology of Food Industry, 2007, 28(9):94-98.
[4] 樊杉杉, 董雅君, 杨兴华, 等.不同地区来源藏曲对西藏传统酿造青稞酒风味特征的影响[J].食品与发酵工业,2019,45(2):7-14.
FAN S S, DONG Y J, YANG X H, et al.Effects of different Zangqu from different regions on the flavor of Tibetan traditional Qingke wine[J].Food and Fermentation Industries,2019,45(2):7-14.
[5] 袁亦舟, 张伟国, 徐建中.青稞酒曲微生物多样性分析及米根霉制曲条件优化[J].食品与发酵工业, 2018,44(5):39-45.
YUAN Y Z, ZHANG W G, XU J Z.Investigation of the microbial diversity in highland barley Qu and optimization of the Koji-making condition with Rhizopus oryzae[J].Food and Fermentation Industries, 2018,44(5):39-45.
[6] 王丽华. 西藏传统青稞酒的生产菌株选育及生产技术研究 [D].重庆:西南大学, 2008.
WANG L H.Studies on mutation screening and production technique of traditional highland barley wine in Tibet [D].Chongqing:Southwest University, 2008.
[7] 杜木英. 西藏青稞酒发酵微生物及酿造技术研究 [D].重庆:西南大学, 2008.
DU M Y.Studies on microorganisms and fermentation technology of highland barley wine [D].Chongqing:Southwest University, 2008.
[8] 刘清斌, 左勇.不同菌种对青稞酒发酵的影响[J].食品工业科技, 2005,26(12):79-81.
LIU Q B, ZUO Y.Effects of different fungi on fermentation of barley liquor[J].Science and Technology of Food Industry, 2005,26(12):79-81.
[9] 赵东. 西藏青稞酒酒曲微生物多样性的研究[D].泰安:山东农业大学, 2011.
ZHAO D.The study of the microbial biodiversity of the Jiuqu of Tibet highland barley wine[D].Tai′an:Shandong Agricultural University, 2011.
[10] 唐洁, 王海燕, 徐岩.酿酒酵母和异常毕赤酵母混菌发酵对白酒液态发酵效率和风味物质的影响[J].微生物学通报, 2012, 39(7):921-930.
TANG J, WANG H Y, XU Y.Effect of mixed culture of Saccharomyces cerevisiae and Pichia anomala on fermentation efficiency and flavor compounds in Chinese liquor[J].Microbiology China, 2012, 39(7):921-930.
[11] 邱并生. 混菌发酵对白酒液态发酵效率和风味物质的影响[J].微生物学通报, 2014, 41(7):1 477-1 478.
QIU B S.Effect of mixed culture on fermentation efficiency and flavor compounds in Chinese liquor[J].Microbiology China, 2014, 41(7):1 477-1 478.
[12] 陈景桦, 马小琛, 李婷,等.优选发酵毕赤酵母与酿酒酵母混合发酵的葡萄酒酿造应用潜力[J].食品科学技术学报, 2018,36(5):26-34.
CHEN J H, MA X C, LI T, et al.Evaluating application potential of mixed fermentation with Pichia fermentans and Saccharomyces cerevisiae[J].Journal of Food Science and Technology, 2018,36(5):26-34.
[13] 许维娜, 耿常乐, 任同同, 等.混菌发酵对葡萄酒感官品质和风味物质的影响[J].中外葡萄与葡萄酒, 2018(6):12-17.
XU W N, GENG C L, REN T T, et al.Effect of mixed fermentation on the sensory quality and flavor compounds of wine[J].Sino-Overseas Grapevine & Wine, 2018(6):12-17.
[14] 张文文, 翁佩芳, 吴祖芳.东方伊萨酵母和酿酒酵母混合发酵杨梅酒的发酵效率及风味特征分析[J].食品科学,2019,40(18):144-151.
ZHANG W W, WENG P F, WU Z F.Fermentation efficiency and flavor characteristics of bayberry wine with mixed starter culture of Issatchenkio orientalis and Saccharomyces cerevisiae[J].Food Science,2019,40(18):144-151.
[15] 薛军侠, 徐艳文, 杨莹, 等.WL培养基在酿酒酵母筛选中的应用[J].中国酿造, 2007(9):36-39.
XUE J X, XU Y W, YANG Y, et al.Screening and identification of Saccharomyces cerevisiae with WL medium[J].China Brewing, 2007(9):36-39.
[16] 梁青, 李文茹, 施庆珊, 等.山苍子油对白假丝酵母抗菌活性研究[J].生物技术通报, 2015, 31(10):205-210.
LIANG Q, LI W R, SHI Q S, et al.Antifungal activity of Litsea cubeba oil against Candida albicans[J].Biotechnology Bulletin, 2015, 31(10):205-210.
[17] 韩德权, 章佳佳.DNS法在普鲁兰多糖发酵液中糖测定的研究[J].食品工业科技, 2008,29(2):285-286;290.
HAN D Q, ZHANG J J.Application of DNS method to the determination of saccharide content in Pullulan fermentation broth[J].Science and Technology of Food Industry, 2008,29(2):285-286;290.
[18] 林艳, 单连菊, 张沛, 等.高效液相色谱法测定啤酒、发酵液和麦汁中的糖类和乙醇[J].分析化学, 1999(6):3-5.
LIN Y, SHAN L J, ZHANG P, et al.Determination of sugars and ethanol in beer, fermentation liquid and wort by high performance liquid chromatography[J].Chinese Journal of Analytical Chemistry, 1999(6):3-5.
[19] 徐勇, 郎召伟, 沈咪娜, 等.泸型酒酿造过程中上层和下层酒醅的有机酸变化分析[J].四川理工学院学报(自然科学版), 2018, 31(5):9-13.
XU Y, LANG Z W, SHEN M N, et al.Organic acids dynamics in the upper and bottom layers during Luzhou-flavor Baijiu fermentation[J].Journal of Sichuan University of Science & Engineering(Natural Science Edition), 2018, 31(5):9-13.
[20] 陈双. 中国黄酒挥发性组分及香气特征研究 [D].无锡:江南大学, 2013.
CHEN S.Characterization of the volatile and aroma profile of Chinese rise wine[D].Wuxi:Jiangnan University, 2013.
[21] 苏畅, 马莹莹, 杨建刚.扣囊复膜酵母在酿酒中的应用研究进展[J].食品研究与开发, 2018, 39(1):205-209;220.
SU C, MA Y Y, YANG J G.Research progress of Saccharomycopsis fibuligera in liquor-making industry[J].Food Research and Development, 2018, 39(1):205-209;220.
[22] 应玲云, 伍时华, 赵东玲, 等.烧酒曲中扣囊复膜酵母的分离及鉴定[J].食品与发酵工业, 2013, 39(1):146-150.
YING L Y, WU S H, ZHAO D L, et al.Isolation and identification of Saccharomycopsis fibuligera isolated from rice wine starter[J].Food and Fermentation Industries, 2013, 39(1):146-150.
[23] 郝文军, 刘红霞, 于晓涛, 等.牛栏山白酒酿造过程中扣囊复膜酵母的分离与产物分析[J].酿酒科技, 2019(2):49-52.
HAO W J, LIU H X, YU X T, et al.Isolation of S.fibuligera from the production process of niulanshan liquor and its metabolites[J].China Brewing, 2019(2):49-52.
[24] THAKUR N, SAVITRI, SARIS E J P,et al.Microorganisms associated with amylolytic starters and traditional fermented alcoholic beverages of North Western Himalayas in India[J].Food Bioscience, 2015,11:92-96.
[25] NAOKO T, RYOSUKE F, SHIGERU Y,et al.Identification of yeast strains isolated from marcha in Sikkim, a microbial starter for amylolytic fermentation[J].International Journal of Food Microbiology, 2005,99(2):135-146.
[26] BHARDWAJ K N, JAIN K K, KUMAR S,et al.Microbiological analyses of traditional alcoholic beverage(Chhang) and its starter(Balma) prepared by bhotiya tribe of Uttarakhand, India[J].Indian Journal of Microbiology, 2016,56(1):28-34.
[27] 向阳, 李崎, 顾国贤.国内啤酒有机酸组成及其综合评价[J].食品科学, 2007,28(1):266-270.
XIANG Y, LI Q, GU G X.Study on composition of organic acids in domestic beer for comprehensive evaluation[J].Food Science, 2007,28(1):266-270.
[28] 诸葛庆. 猕猴桃酒降酸降涩新工艺的研究 [D].无锡:江南大学, 2005.
ZHUGE Q.Study on the new technology of deacidification and reducing acerbity of kiwi fruit wine[D].Wuxi:Jiangnan University, 2005.
[29] 孙思佳, 翟磊, 许玲, 等.扣囊复膜孢酵母CICC 33077在芝麻香型白酒高温大曲生产中的应用[J].酿酒科技, 2018(7):76-82.
SUN S J, ZHAI L, XU L,et al.Application of Saccharomycopsis fibuligera CICC 33077 in the production of high-temperature Zhimaxiang Daqu[J].Brewing Science, 2018(7):76-82.
[30] 王晓丹, 陈美竹, 班世栋, 等.茅台大曲中酵母的分离、鉴定及其功能初探[J].食品科学, 2017, 38(4):51-57.
WANG X D, CHEN M Z, BAN S D,et al.Separation, identification and functional characterization of yeast strains from Moutai-flavor Daqu, a traditional Chinese liquor fermentation starter[J].Food Science, 2017, 38(4):51-57.
[31] 范文来, 徐岩.白酒79个风味化合物嗅觉阈值测定[J].酿酒, 2011, 38(4):80-84.
FAN W L, XU Y.Determination of odor thresholds of volatile aroma compounds in Baijiu by a forced-choice ascending concentration series method of limits[J].Brewing, 2011, 38(4):80-84.