韭菜(Allium tuberosum Rottl.ex spreng.)属百合科多年生宿根草本植物,又称起阳草、长生韭、扁菜等,在我国南北方均有种植和栽培,其茎、叶、花均可食用,因富含含硫化合物而具有独特香辛味,其中大量的甾体皂苷具有止咳、抗癌、治疗糖尿病等作用[1]。韭菜根是韭菜的地下部分,其中丰富的粗纤维可促进肠道蠕动、预防便秘[2],有一定食用和药用价值,贵州丹寨的村民成功用家乡的野生韭菜根开发出当地知名土特产[3]。然而实际栽培中种植一段时间后的韭菜由于生长能力下降,韭菜根往往在移栽时被丢弃,没有得到充分开发利用,造成一定的资源浪费。目前的研究主要集中在韭菜籽,关于韭菜根粗纤维的研究和开发鲜见报道。
膳食纤维指不能被人体消化,以纤维素、半纤维素、果胶和木质素等为主的多糖类化合物总称[4]。根据其水溶性分为可溶性膳食纤维和不溶性膳食纤维(insoluble dietary fiber,IDF)[5]。IDF具有良好持水力和膨胀性,能清除肠道毒素,促进胃肠道蠕动,对预防和缓解便秘、糖尿病、结肠癌、肥胖、中风、高血压等有重要作用[6-7]。目前已广泛应用于肉制品、面制品、饮料等食品生产中[8-10]。
本研究采用响应面法(response surface methodology,RSM)对超声辅助提取韭菜根IDF的工艺进行优化,分析产品化学组成、热稳定性和超微结构,有助于减少资源浪费,为韭菜根的综合利用和膳食纤维的深入研究提供理论依据。
1 材料与方法
1.1 材料与试剂
新鲜韭菜根,贵州省安顺市普定县化处镇水母河流域韭黄园区;金龙鱼大豆油,永辉超市北碚区天生丽街店;NaOH(优级纯)、KBr(光谱纯),成都市科龙化学品有限公司。
1.2 主要仪器
FW117中草药粉碎机,天津市泰斯特仪器有限公司;JA21002分析天平,上海精天电子仪器有限公司;DGG-9240B电热恒温鼓风干燥箱,上海森信实验仪器有限公司;TGL-16M台式高速冷冻离心机,长沙湘仪离心机仪器有限公司;KQ3200DV数控超声波清洗器(总功率650 W),昆山市超声仪器有限公司;Spectrun 100红外光谱仪,美国Perkin Elmer公司;TGA550热重分析仪,美国TA公司;Phenom扫描电子显微镜,复纳科学仪器(上海)有限公司。
1.3 实验方法
1.3.1 提取工艺流程
参考文献[11]的方法并略作修改。
韭菜根洗净→切段→烘干(60 ℃)→粉碎→过筛(60目)→取样→加NaOH溶液→超声波提取→提取液离心→取沉淀→水洗至中性→干燥→成品IDF
1.3.2 操作要点
称取样品5.0000 g,加入3 g/L的NaOH溶液,超声提取一定时间后在5 000 r/min下离心10 min,收集沉淀,用纯水洗至中性,60 ℃烘干称量,平行试验3次,按公式(1)计算IDF得率。
(1)
式中:R,IDF的得率,%;m1,干燥IDF质量,g;m2,干燥样品质量,g。
1.3.3 单因素试验
设定超声功率强度40%,超声温度40 ℃,超声时间30 min,考察液料比(mL∶g)在10、15、20、25、30、35时对韭菜根IDF得率的影响。
设定液料比20 mL/g,超声温度40 ℃,超声时间30 min,考察超声功率强度在40%、50%、60%、70%、80%、90%时对韭菜根IDF得率的影响。
设定液料比20 mL/g,超声功率强度40%,超声时间30 min,考察超声温度在20、30、40、50、60、70 ℃时对韭菜根IDF得率的影响。
设定液料比20 mL/g,超声功率强度40%,超声温度40 ℃,考察超声时间在10、20、30、40、50、60 min时对韭菜根IDF得率的影响。
1.3.4 响应面设计
基于Box-Behnken原理,选用3因素3水平响应面分析法,以韭菜根IDF得率为响应值进一步优化工艺,因素水平如表1所示。
表1 响应面试验设计的因素和水平
Table 1 Factors and levels of response surface experimental design
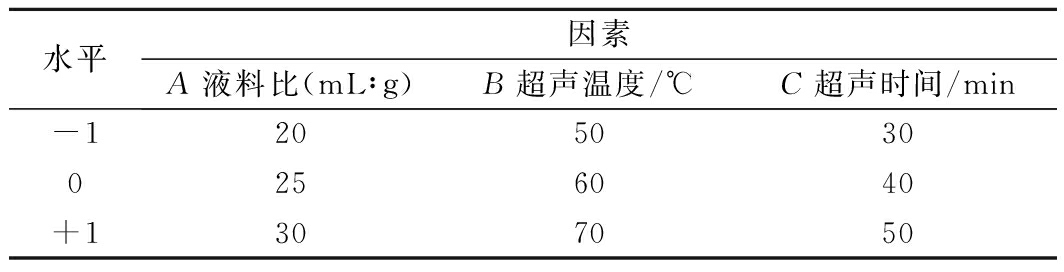
水平因素A液料比(mL∶g)B超声温度/℃C超声时间/min-12050300256040+1307050
1.4 韭菜根IDF特性测定
1.4.1 韭菜根IDF持水力测定[12]
取1.00 g韭菜根IDF(m1)置于100 mL离心管,加蒸馏水75 mL浸泡24 h,4 000 r/min离心30 min,除去上清液,称量吸水后的韭菜根IDF质量(m2)。重复3次,取平均值,按公式(2)计算IDF持水力。
持水力![]()
(2)
1.4.2 韭菜根IDF膨胀性测定[13]
准确称取0.20 g韭菜根IDF(m),置于10 mL量筒中,读取干品体积(V1),准确吸取25 ℃ 5 mL蒸馏水,振荡摇匀后静置24 h,记录其膨胀后的体积(V2)。重复3次,取平均值,按公式(3)计算IDF膨胀性。
膨胀性![]()
(3)
1.4.3 韭菜根IDF持油力测定[14]
取1.00 g韭菜根IDF(m1)与适量食用油在50 mL离心管中振荡均匀,室温下放置24 h,再在4 000 r/min下离心30 min,弃去上层清液,过滤、称质量(m2)。重复3次,取平均值,按公式(4)计算IDF持油力。
持油力![]()
(4)
1.5 结构表征
1.5.1 红外光谱分析[15]
用傅里叶红外光谱法将1 mg样品与100 mg KBr研磨均匀后压片,形成一个半透明薄片,用红外光谱仪扫描,扫描范围4 000~400 cm-1。
1.5.2 热稳定性分析[16]
取4 mg左右样品于热重分析仪中,仪器温度40 ℃,以15 ℃/min的速度升至550 ℃,逐渐分解热天平坩埚中的样品,记录试样质量随温度的变化,分析样品热稳定性。
1.5.3 超微结构分析[11]
取少量干燥好的样品,放置到贴上导电双面胶的载样台上,将待测样品固定好,在真空中喷镀金膜。把处理好的样品和载样台一起放入扫描电镜的样品室进行形态观察,拍摄电镜照片。
1.6 数据分析处理
单因素试验数据用Origin 2018分析作图。响应面优化试验数据用Design-Expert 8.0.5进行分析处理和绘图。
2 结果与分析
2.1 超声处理条件初选
2.1.1 液料比对韭菜根IDF得率的影响
IDF得率受液料比的影响详见图1。在10~25 mL/g范围,随液料比增加,韭菜根IDF得率总体呈上升趋势,这是由于随液料比增大,样品与碱液间接触面积增大,有利于样品IDF溶出,故IDF得率增加;当液料比>25 mL/g时,随液料比增加,IDF得率逐渐下降,这可能因为韭菜根中IDF含量有限,当IDF在碱液中扩散达到平衡后,得率不再上升,液料比继续增加反而可能破坏溶出的IDF,使其水解,另外,加入过多碱液还可能影响超声波作用[17],导致得率下降。因此,确定液料比20、25、30 mL/g为最佳优化范围。
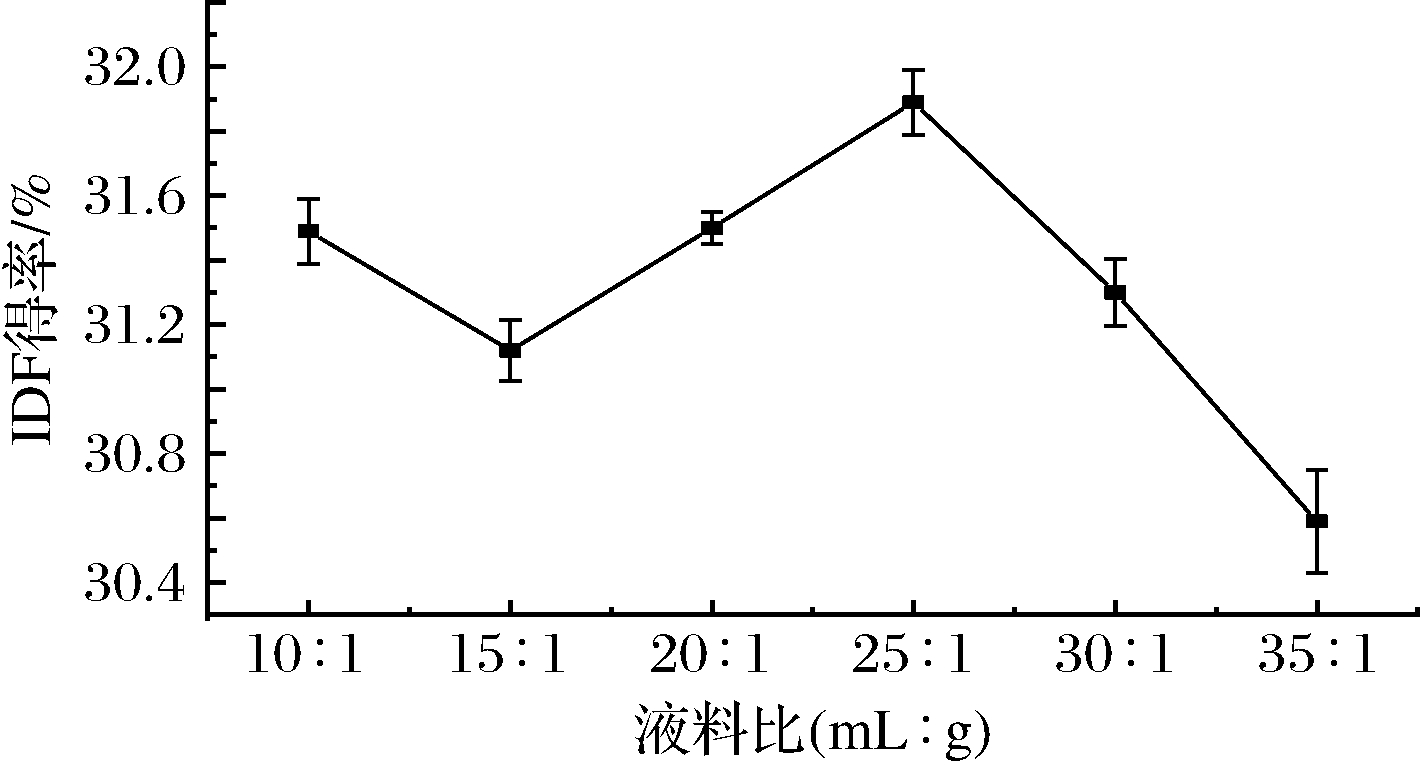
图1 液料比对韭菜根IDF得率的影响
Fig.1 Effect of liquid-solid ratio on the yield of insoluble dietary fiber
2.1.2 超声功率强度对韭菜根IDF得率的影响
超声功率强度为40%~60%时,随强度增加,韭菜根IDF得率先下降后上升(图2),这是由于在一定强度范围内超声波机械作用增强有助于IDF在溶剂中溶出;当超声功率强度为60%,IDF得率达到最大,之后随强度增加而下降,这可能由于超声功率强度达到一定程度时,空化效应过于强烈[18],从而导致膳食纤维网状结构被破坏,形成更小颗粒溶解在溶剂中,使IDF得率下降。综合考虑,确定最佳功率强度为60%。
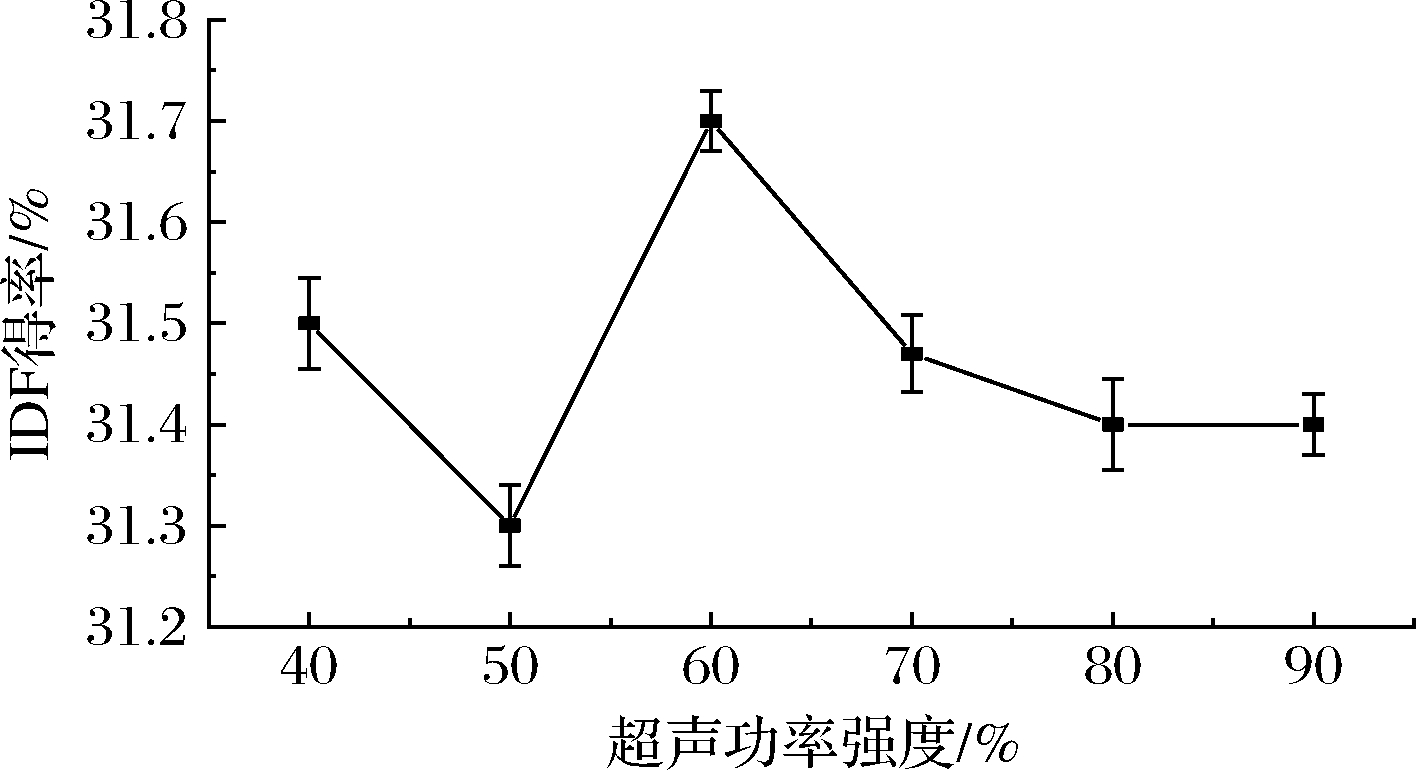
图2 超声功率强度对韭菜根IDF得率的影响
Fig.2 Effect of ultrasonic power intensity on the yield of insoluble dietary fiber
2.1.3 超声温度对韭菜根IDF得率的影响
图3反映了得率随超声温度的变化,在20~60 ℃范围,IDF得率随温度升高先下降后上升,在60 ℃达到峰值,之后逐渐下降。这是因为适宜的高温加速粒子运动,促进韭菜根中IDF溶出,提高IDF得率,但过高温度会破坏IDF结构,降低IDF得率。因此,选择超声温度50、60、70 ℃进行响应面优化试验为宜。
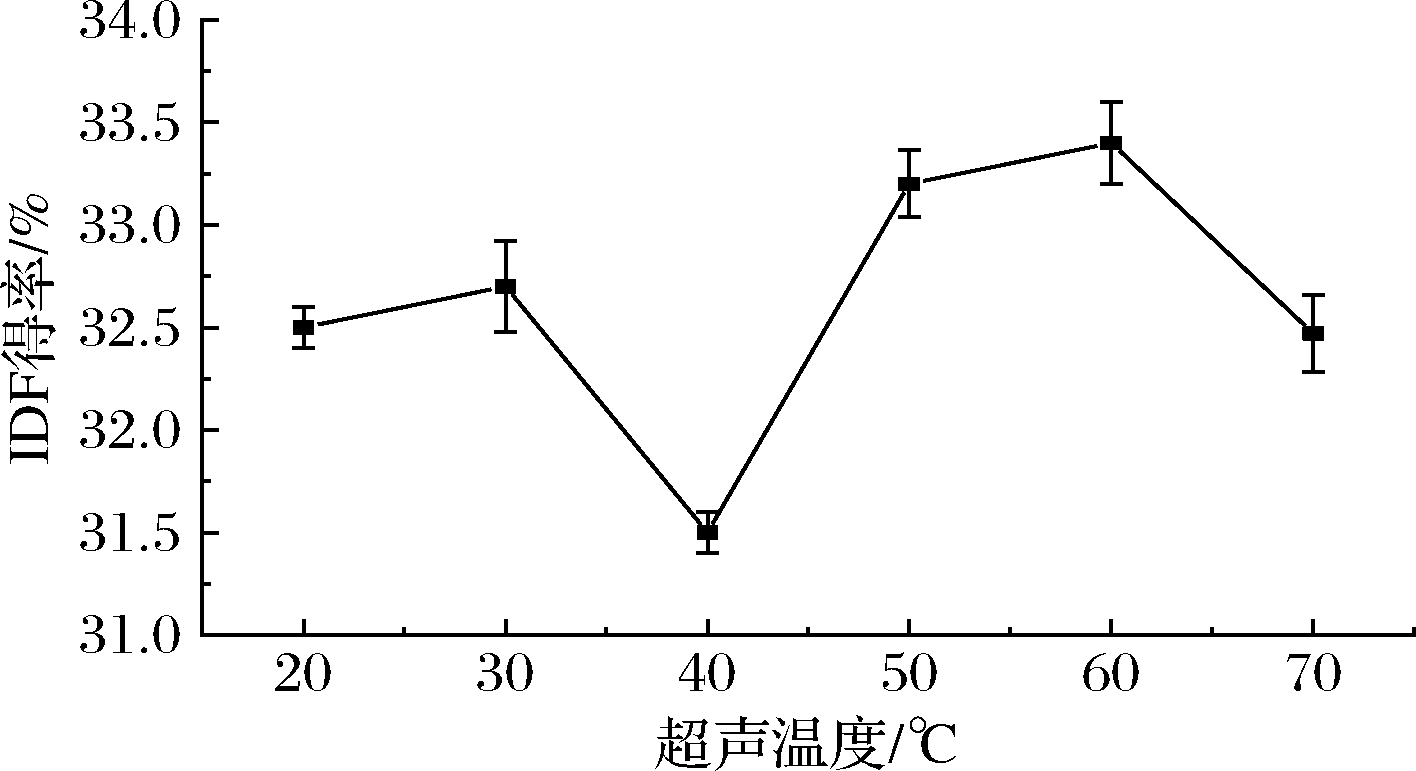
图3 超声温度对韭菜根IDF得率的影响
Fig.3 Effect of ultrasonic temperature on the yield of insoluble dietary fiber
2.1.4 超声时间对韭菜根IDF得率的影响
超声时间为10~40 min时,随时间增加,韭菜根IDF得率总体呈显著上升,在40 min最大,之后明显降低(图4)。可能因为在适当的超声时间范围内有利于固体和溶剂充分接触,同时使超声波机械作用充分发挥,提高IDF得率,但超声时间过长可能破坏IDF结构,加速IDF降解,影响IDF得率。因此,确定超声时间30、40、50 min进行优化。
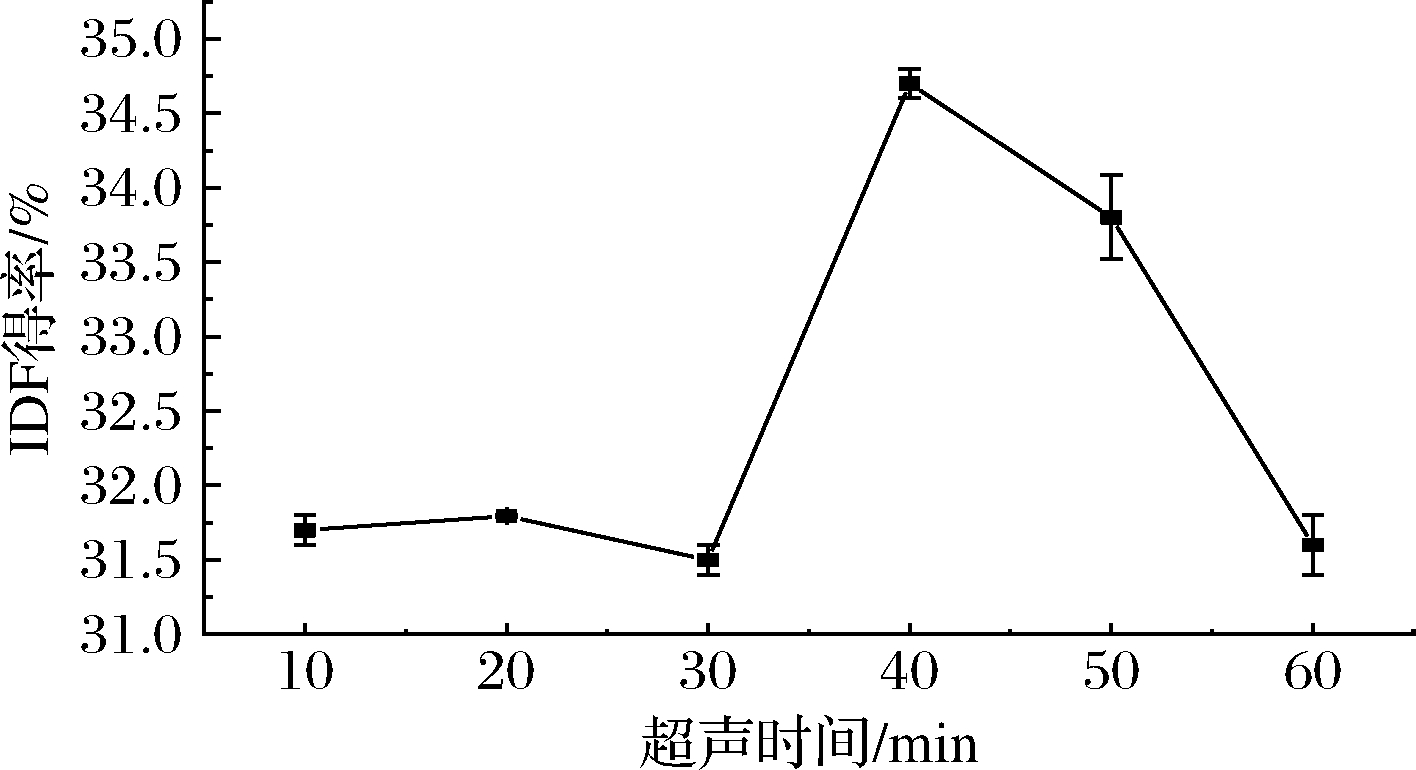
图4 超声时间对韭菜根IDF得率的影响
Fig.4 Effect of ultrasonic time on the yield of insoluble dietary fiber
2.2 响应面优化
2.2.1 回归模型建立与讨论
选择液料比(A)、超声温度(B)和超声时间(C)为评价因素,IDF得率(Y)为评价指标,进行3因素3水平的响应面试验分析,试验结果和方差分析见表2和表3。
将表2数据用Design.Expert 8.0.5软件进行二次线性回归拟合,得到如下回归方程:Y=33.70-0.20×A-0.71×B+0.10×C-0.55×AB+0.025×AC-0.017×BC-1.06×A2-1.01×B2-0.070×C2。由该方程知,二次项A2、B2和C2系数均为负,说明该方程存在最大值[17]。
由表3知,此回归模型极显著(P<0.01),实验值与预测值间相关性较高(R2=0.9012),表明此模型对实际实验方法拟合度较高;同时,B、A2、B2对响应值的影响均极显著(P<0.01),A、C、AB、AC、BC、C2对响应值均表现不显著,说明实验因素对韭菜根IDF得率的影响不是简单的线性关系。因此,可用此模型对韭菜根IDF提取工艺结果进行分析和预测。
表2 响应面分析结果
Table 2 The results of response surface analysis

试验号ABCY(IDF得率)/%1-1-1032.3021-1033.033-11031.33411029.875-10-132.40610-131.907-10133.20810132.8090-1-133.201001-132.47110-1132.801201132.001300033.701400033.701500033.701600033.701700033.70
由F值大小知,3个因素对IDF得率影响的主次顺序为:B>A>C,即超声温度>液料比>超声时间。
表3 响应面试验方差分析
Table 3 Variance analysis of response surface method
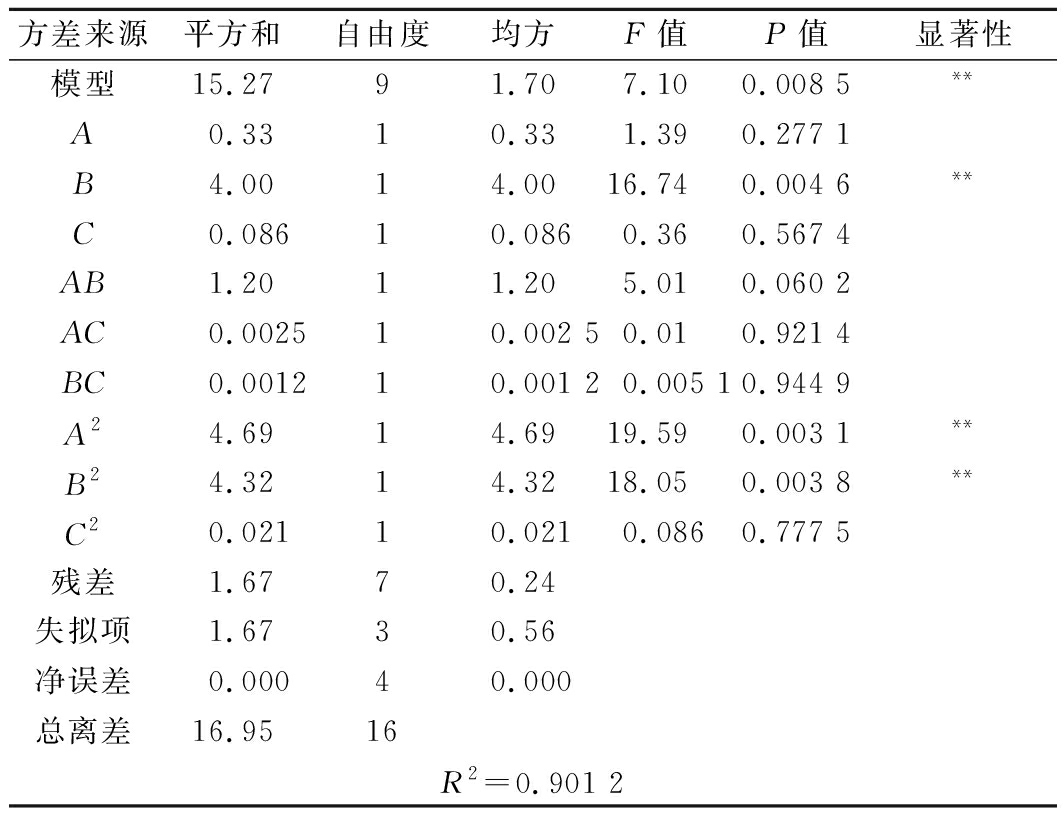
方差来源平方和自由度均方F值P值显著性模型15.2791.707.100.008 5**A0.3310.331.390.277 1B4.0014.0016.740.004 6**C0.08610.0860.360.567 4AB1.2011.205.010.060 2AC0.002510.002 50.010.921 4BC0.001210.001 20.005 10.944 9A24.6914.6919.590.003 1**B24.3214.3218.050.003 8**C20.02110.0210.0860.777 5残差1.6770.24失拟项1.6730.56净误差0.00040.000总离差16.9516R2=0.901 2
注:**差异极显著(P<0.01)
2.2.2 交互效应分析
考察各交互项对IDF得率的影响,响应面图见图5。等高线的密集程度反映了试验因素对响应值的影响,图5中等高线沿超声温度轴向最密集,沿液料比轴向的等高线相对稀疏,沿超声时间轴向的等高线最稀疏,表明超声温度对IDF得率的影响最大,其次是液料比,超声时间对IDF得率的影响最不显著,这与前述方差分析结果相符。

图5 液料比、超声温度、超声时间与IDF得率交互影响响应面图
Fig.5 Response surface plots showing the effects of liquid-to-solid ratio,ultrasonic temperature and time on IDF yield
2.2.3 最佳方案确定与验证
用Design Export 8.0.5软件对试验结果进行分析处理,最佳工艺参数为:液料比25.03 mL/g,超声温度56.42 ℃,超声时间47.87 min,此条件下IDF得率为33.87%。考虑实际操作,采用液料比25 mL/g,超声温度56 ℃,超声时间48 min,超声功率强度60%,重复验证3次,韭菜根IDF得率可达32.92%。
2.3 IDF理化特性
IDF持水力为11.90 g/g,高于苹果渣膳食纤维4.53 g/g[19]、蒜黄根膳食纤维8.63 g/g[20]、马铃薯渣膳食纤维3.71 g/g[21];其膨胀性为 8.23 mL/g,高于茶树菇膳食纤维2.7 mL/g[22]、苹果渣膳食纤维6.25 mL/g[19]、蒜黄根膳食纤维6.27 mL/g[20];其持油力为7.63 g/g,高于花生壳膳食纤维1.12 g/g[23]、蒜黄根膳食纤维6.57 g/g[20]以及马铃薯渣膳食纤维1.28 g/g[21]。可见,韭菜根是优质膳食纤维的良好来源。
2.4 IDF结构表征
2.4.1 红外光谱分析
膳食纤维由于成分复杂不易分析,目前多用红外光谱技术分析其化学组成和基团特性。由图6可知,3 418 cm-1处有一个较宽圆滑峰为羟基O—H伸缩振动峰,由于韭菜根IDF分子间和分子内富含氢键,所以波段较宽,主要是由果胶和半纤维素引起[16]。在3 000~2 800 cm-1内,2 919 cm-1和2 852 cm-1处吸收峰为糖类甲基或亚甲基的C—H键伸缩振动特征吸收峰,这是多糖类物质结构的典型特征[24]。2 000~1 500 cm-1内,1 740 cm-1处为木聚糖C![]() O伸缩振动吸收峰,是半纤维素的特征吸收峰,1 632 cm-1附近为芳香族化合物的特征吸收峰,表明存在木质素[25],1 450~1 300 cm-1间的一组峰是C—H的弯曲振动,这些峰是糖类的特征峰。1 200~950 cm-1间的波段被称为碳水化合物的“指纹”区域,因为此段可识别碳水化合物主要的化学基团[16]。1 159 cm-1处为纤维素、半纤维素C—O—C基的伸缩振动,1 243~1 057 cm-1处也出现了纤维素和半纤维素C—O基伸缩振动相应的特征峰,基本符合膳食纤维的结构[26]。1 034 cm-1为半乳糖醛酸C—O吸收峰,894 cm-1处吸收峰说明组成结构中含β型吡喃糖[26],618 cm-1是糖分子中β型C—H直立键的变角振动引起的吸收峰[27]。
O伸缩振动吸收峰,是半纤维素的特征吸收峰,1 632 cm-1附近为芳香族化合物的特征吸收峰,表明存在木质素[25],1 450~1 300 cm-1间的一组峰是C—H的弯曲振动,这些峰是糖类的特征峰。1 200~950 cm-1间的波段被称为碳水化合物的“指纹”区域,因为此段可识别碳水化合物主要的化学基团[16]。1 159 cm-1处为纤维素、半纤维素C—O—C基的伸缩振动,1 243~1 057 cm-1处也出现了纤维素和半纤维素C—O基伸缩振动相应的特征峰,基本符合膳食纤维的结构[26]。1 034 cm-1为半乳糖醛酸C—O吸收峰,894 cm-1处吸收峰说明组成结构中含β型吡喃糖[26],618 cm-1是糖分子中β型C—H直立键的变角振动引起的吸收峰[27]。
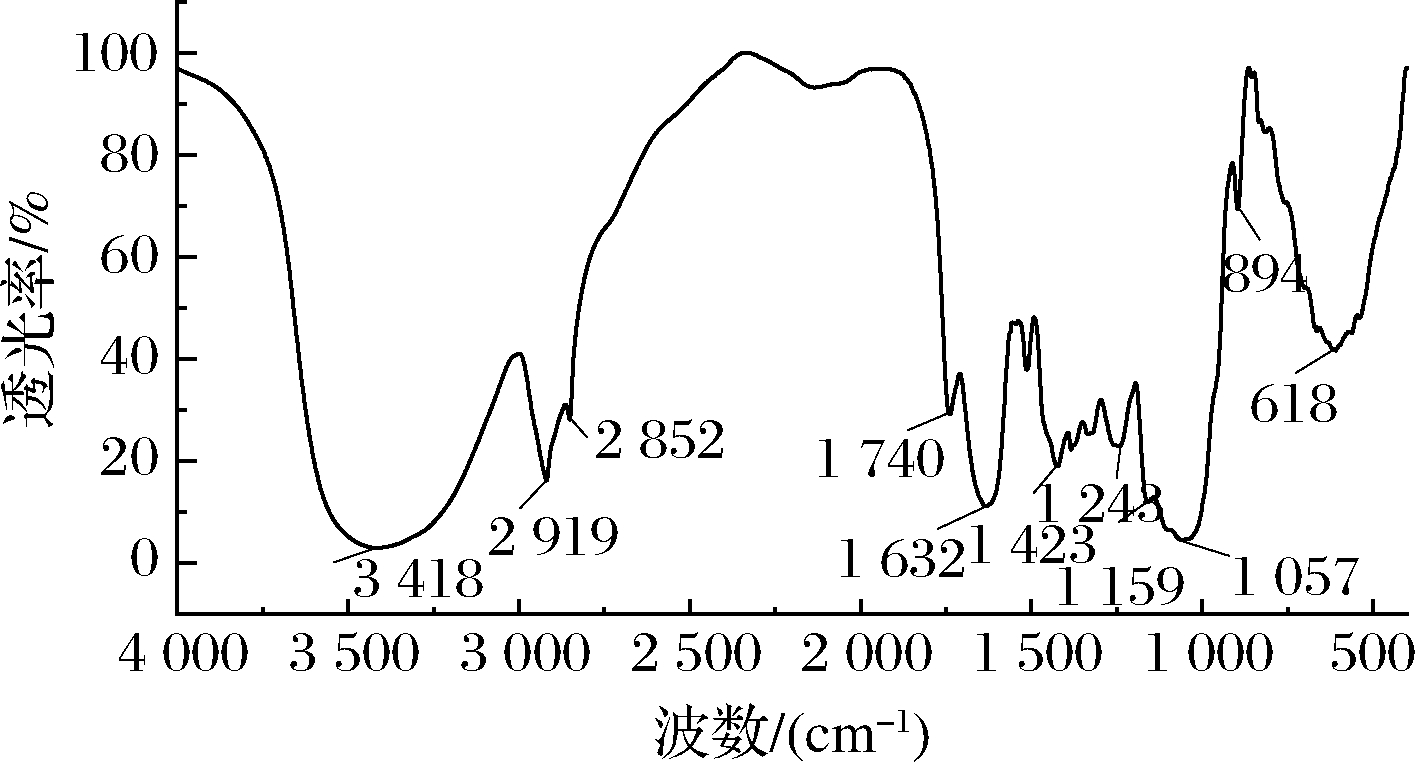
图6 韭菜根IDF的红外光谱图
Fig.6 Infrared scanning spectrogram of chive root IDF
2.4.2 热稳定性分析
热重分析是通过物质热分解过程来评价其热稳定性。由图7可知,IDF热分解过程可分为4个阶段,干燥阶段AB、预碳化阶段BC、碳化阶段CD、燃烧阶段DE[28]。AB段温度范围为27~117 ℃,失重率约11%,此阶段样品质量减少主要由IDF分子内自由水和结晶水在高温过程中损失引起,样品失重较明显,与2.3中IDF持水力较好的结果一致;BC段温度范围117~175 ℃,样品失重率约1.4%,失重不明显,样品质量的减少主要由大分子物质逐渐降解引起,这是一个缓慢向碳化过渡的阶段;CD段温度范围175~442 ℃,失重率约61%,这是IDF热分解的主要阶段,也是样品失重率最高的阶段,生物质热裂解生成小分子气体和大分子的可冷凝挥发成分而造成明显失重,样品在此阶段释放出较多热量[29];此后进入燃烧阶段,此阶段主要是碳化后残留物分解生成部分炭和灰分的过程,样品失重速率很缓慢,曲线最终趋于平稳,样品最终剩余质量约为原质量的21.9%。研究表明,在食品加工过程中一般将加热温度控制在200 ℃以下,以免破坏膳食纤维稳定性和优良性能[16],因此可通过改进提取方法和适当改性来提高膳食纤维热解温度和热稳定性,使其更广泛地应用于食品加工。
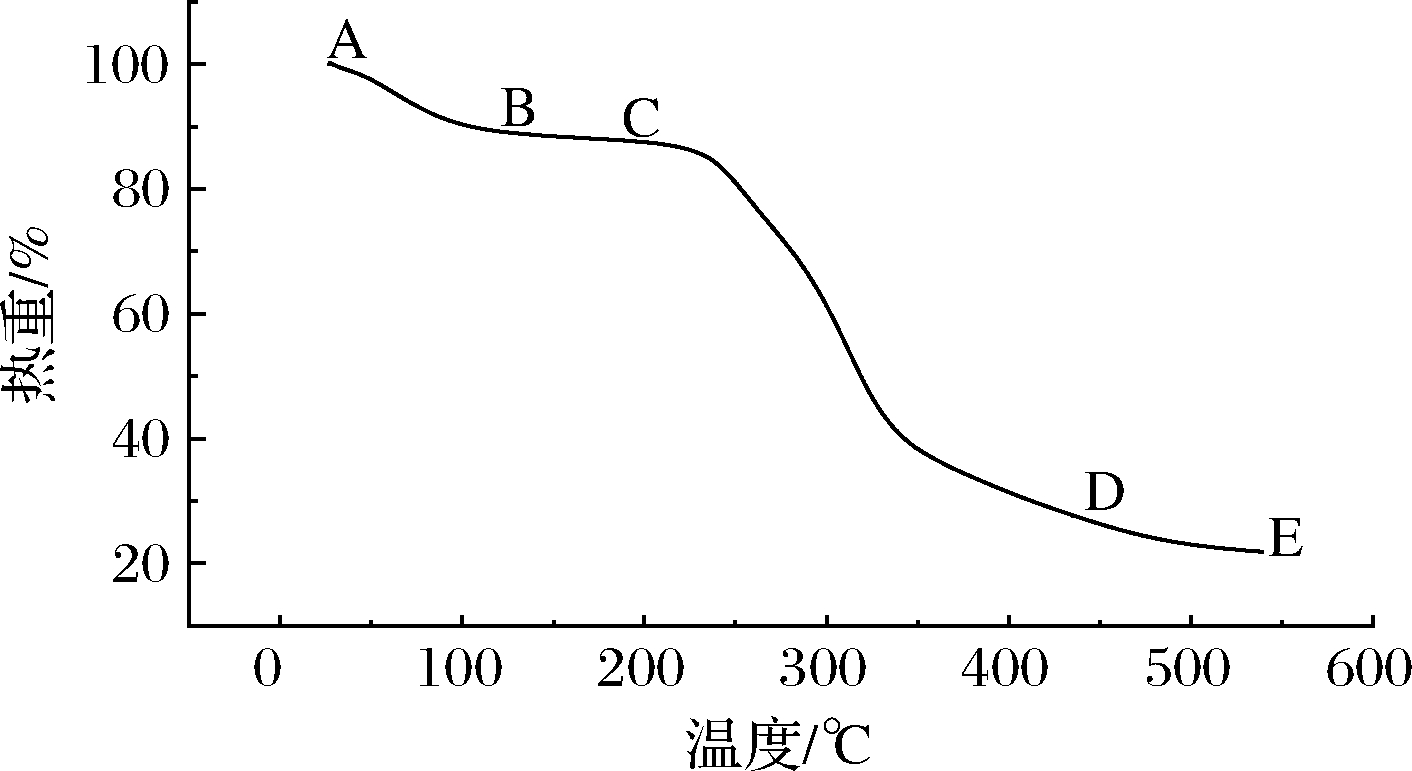
图7 IDF的热重图谱
Fig.7 The thermogravimetric drawing of chive root IDF
2.4.3 超微结构分析
由图8可知,原料表面光滑完整,整体较紧凑,表面附着一些小颗粒,可能是淀粉颗粒和粗蛋白类等物质,说明原料中含有较多淀粉和蛋白质等杂质;经过超声辅助提取的IDF较粗糙,结构疏松,表面明显断裂和破碎,呈不规则的片状,可能是由于超声波对膳食纤维结构造成不同程度的损坏,结构完整性被破坏,呈现带有裂缝的网状结构。微观结构与功能特性密切相关,后续研究可改进提取或改性方法,调整微观结构,以达到改善膳食纤维理化特性和生理功能的目的。

a-韭菜根;b-IDF;1-×500; 2-×2 000
图8 韭菜根和IDF的扫描电镜图
Fig.8 The scanning electron microscope of chive root and IDF
3 结论
本研究在单因素试验基础上,根据Box-Behnken原理,利用Design Export 8.0.5软件建立以韭菜根IDF得率为指标的二次多项式回归模型,用响应面法优化超声辅助提取韭菜根IDF的工艺。结果表明,最优工艺条件为:液料比25 mL/g、超声温度56 ℃、超声时间48 min、超声功率强度60%,韭菜根IDF得率可达32.92%;其持水力为11.90 g/g、膨胀性为8.23 mL/g、持油力为7.63 g/g,产品表征结果说明超声辅助处理会改变IDF结构和性质,为使其具有更优良的性质和今后更广泛地应用,还需深入探究改良结构和性质的物理、化学、生物学方法及其他新兴技术。响应面优化超声辅助提取韭菜根中IDF的工艺和结构表征,可为韭菜根膳食纤维的提取研究提供理论依据,为以后研发和推广性质优良的膳食纤维产品建立理论基础,有利于今后韭菜根的综合开发利用。
[1] 方云山. 藓叶卷瓣兰、芳香石豆兰和韭菜根的化学成分研究[D].昆明:云南大学,2016.
FANG Y S.Studies on the chemical constiuents of B.retusiusculum,B.ambrosia and the roots of A.tuberosum[D].Kunming:Yunnan University,2016.
[2] 周航,刘利,薛菲.腌韭菜根的营养价值及韭菜根开发应用研究[J].中国调味品,2017,42(9):173-176.
ZHOU H,LIU L,XUE F.The nutritional value of pickled Allium hookeri Thwaites root and the development and application research on Allium hookeri Thwaites root[J].China Condiment,2017,42(9):173-176.
[3] 王绍先,吴兴祥.开发“韭菜根”带富众乡亲[J].农产品加工,2012(9):52-53.
WANG S X,WU X X.Develop “chive roots” to enrich the folks[J].Farm Products Processing,2012(9):52-53.
[4] MONTAGNE L,PLUSKE J R,HAMPSON D J.A review of interactions between dietary fiber and the intestinal mucosa,and their consequences on digestive health in young non-ruminant animals[J].Animal Feed Science & Technology,2003,108(1):95-117.
[5] DAI F J,CHAU C F.Classification and regulatory perspectives of dietary fiber[J].Journal of Food and Drug Analysis,2017,25(1):37-42.
[6] 李琦,曾凡坤,华蓉,等.麦麸膳食纤维理化特性、制备方法及应用研究进展[J].食品工业科技,2020,41(17):352-357;367.
LI Q,ZENG F K,HUA R,et al.Research progress on the physicochemical properties,preparation methods and application of wheat bran dietary fiber[J].Science and Technology of Food Industry,2020,41(17):352-357;367.
[7] ANDERSON J W,BAIRD P,DAVIS R H,et al.Health benefits of dietary fiber[J].Nutrition Reviews,2009,67(4):188-205.
[8] TALUKDER S,SHARMA D P.Development of dietary fiber rich chicken meat patties using wheat and oat bran[J].Journal of Food Science and Technology,2010,47(2):224-229.
[9] 陶春生,陈存社,王克俭.挤压改性麦麸膳食纤维对面条品质的影响[J].食品科技,2017,42(9):132-136.
TAO C S,CHEN C S,WANG K J.Effects of extrusion modification of wheat bran dietary fiber on quality of noodle[J].Food Science and Technology,2017,42(9):132-136.
[10] 吴卫国,王金发.麦麸纤维保健型花生饮料的研制[J].食品工业,2000(2):21-23.
WU W G,WANG J F.Development of wheat bran fiber health-care peanut beverage[J].The Food Industry,2000(2):21-23.
[11] 雷登凤. 生姜中膳食纤维的提取及改性研究[D].贵阳:贵州大学,2015.
LEI D F.Study on the extraction and modification of ginger dietary fiber[D].Guiyang:Guizhou University,2015.
[12] 郭东辉,刘四新,李从发.腰果梨渣不溶性膳食纤维的提取[J].食品工业科技,2008,29(11):166-167;170.
GUO D H,LIU S X,LI C F.Extraction of insoluble dietary fiber from cashew apple dregs[J].Science and Technology of Food Industry,2008,29(11):166-167;170.
[13] RUPEREZ P,SAURA—CALIXTO F.Dietary fiber and physicochernical properties of edible Spanish[J].Eur Food Res Technol,2001,212(3):349-354.
[14] SANGNARK A,NOOMHORM A.Effect of particle sizes on functional properties of dietary fiber prepared from sugarcane bagass[J].Food Chemistry,2003,80:221-229.
[15] 程明明. 西番莲果皮水不溶性膳食纤维提取、改性及功能特性研究[D].广州:华南农业大学,2016.
CHENG M M.Study on extraction,modified and functional features of dietary fiber from passiflora edulis rind[D].Guangzhou:South China Agricultural University,2016.
[16] 杨妍.石榴皮渣(籽)膳食纤维制备与降脂功能研究[D].北京:中国农业科学院,2018.
YANG Y.Preparation of dietary fiber from pomegranate marcs(seed) and its antiobesity function[D].Beijing:Chinese Academy of Agricultural Sciences,2018.
[17] 唐小闲,邱培生,段振华,等.响应面法优化超声-微波辅助提取莲藕膳食纤维工艺研究[J].食品研究与开发,2019,40(6):132-139.
TANG X X,QIU P S,DUAN Z H,et al.Optimization of ultrasonic-microwave assisted extraction of dietary fiber from lotus root by respons surface methodology[J].Food Research and Development,2019,40(6):132-139.
[18] 程海涛,申献双.响应面优化超声波-微波协同提取葡萄籽原花青素工艺研究[J].中国油脂,2018,43(3):156-160.
CHEN H T,SHEN X S.Optimization of ultrasound-microwave-assisted extraction of proanthocyanidin from grape seeds by response surface methodology[J].China Oils and Fats,2018,43(3):156-160.
[19] 朱妞.微生物发酵法改性苹果渣膳食纤维理化特性分析[J].中国调味品,2020,45(6):88-91.
ZHU N.Analysis of physicochemical properties of apple pomace dietary fiber modified by microbial fermentation method[J].China Condiment,2020,45(6):88-91.
[20] 马斌,罗延丽,王永康,等.蒜黄根膳食纤维提取工艺优化及其理化性质分析[J/OL].食品工业科技:1-10[2020-06-29].http://kns.cnki.net/kcms/detail/11.1759.TS.20200603.1517.013.html.
MA B,LUO Y L,WANG Y K,et al.Optimization of extraction conditions of dietaryfiber from the root of blanched garlic leaves and its physicochemical properties analysis[J/OL].Science and Technology of Food Industry:1-10[2020-06-29].http://kns.cnki.net/kcms/detail/11.1759.TS.20200603.1517.013.html.
[21] 魏玉梅,哈斯其美格,刘华.响应面优化双酶法提取马铃薯渣膳食纤维工艺[J].食品与发酵科技,2020,56(2):33-39.
WEI Y M,HA S Q M G,LIU H.Response surface methodology optimize the extraction of the dietary fiber from potato residue by double-enzymatic method[J].Food and Fermentation Technology,2020,56(2):33-39.
[22] 刘学成,王文亮,黄泽天,等.茶树菇膳食纤维的提取工艺优化[J].中国酿造,2020,39(5):183-188.
LIU X C,WANG W L,HUANG Z T,et al.Optimization of extraction technology of dietary fiber from Agrocybe aegerita[J].China Brewing,2020,39(5):183-188.
[23] 朱妞,吴丽萍.花生壳膳食纤维理化特性研究[J].粮食与油脂,2014,27(2):38-41.
ZHU N,WU L P.Study on physical and chemical properties of peanut DF[J].Cereals and Oils,2014,27(2):38-41.
[24] CHEN H M,FU X,LUO,Z G.Properties and extraction of pectin-enriched materials from sugar beet pulp by ultrasonic-assisted treatment combined with subcritical water[J].Food Chemistry,2015,168:302-310.
[25] 周丽珍,孙海燕,刘冬,等.改性方法对豆渣膳食纤维的结构影响研究[J].食品科技,2011,36(1):143-147.
ZHOU L Z,SUN H Y,LIU D,et al.Influence of modification methods on the structure of dietary fiber from soybean residue[J].Food Science and Technology,2011,36(1):143-147.
[26] 阮之阳. 酶—超声联合处理植物废渣制备膳食纤维及其生物活性研究[D].广州:华南理工大学,2018.
RUAN Z Y.Preparation of dietary fiber from plant wastes by combined enzyme-ultrasound treatment and their bioactivities[D].Guangzhou:South China University of Technology,2018.
[27] 郭翠翠. 甜荞麦皮粉膳食纤维的制备及其物化特性研究[D].西安:陕西科技大学,2013.
GUO C C.Study on preparation and physicochemical characteristics of dietary fiber from buckwheat bran[D].Xi’an:Shaanxi University of Science & Technology,2013.
[28] 徐学玲. 大豆膳食纤维的超声提取及性质研究[D].合肥:合肥工业大学,2010.
XUX X L.Studies on the ultrasound-assisted extraction and characteristic of soybean dietary fiber[D].Hefei:Hefei University of Technology,2010.
[29] 廖艳芬,王树荣,骆仲泱,等.纤维素热裂解过程动力学的试验分析研究[J].浙江大学学报(工学版),2002(2):60-64;77.
LIAO Y F,WANG S R,LUO Z Y,et al.Research on cellulose pyrolysis kinetics[J].Journal of Zhejiang University Engineering Science,2002(2):60-64;77.