糖尿病是全球范围内一种常见的全身性代谢疾病,它以血糖的慢性增高为主要特征,严重影响着人们的身体健康。随着人们生活水平的提高、饮食结构的改变、体力活动的减少以及吸烟等不良生活习惯的形成[1],糖尿病的发病率正逐年升高。目前,除注射胰岛素外,口服降血糖/抗糖尿病药物是糖尿病最主要的治疗方式。双胍类药物和磺酰脲类药物是治疗糖尿病最常用的传统药物,但由于这些合成药物本身具有的一定毒性,存在加重肝肾负担、导致血糖过低或引起胃肠道不适[2]等缺陷,在现代的治疗中,渐渐无法满足临床的需求。与之相比,来源广泛的天然植物成分有着标本兼顾的优势,现已成为防治糖尿病研究的重点。
石斛作为一种传统的药食两用的资源,其功能活性引起了国内外学者的广泛关注,例如免疫调节、抗肿瘤、抗衰老、抗氧化、降血糖、扩张血管、抗血小板凝集等。石斛多糖作为石斛中的主要生物活性物质,具有生物活性强且毒性极弱的特点,在防治糖尿病等相关代谢性疾病方面有着非常良好的前景。由于多糖的生物活性由它自身的结构决定,因此探索出活性显著的抗糖尿病石斛多糖种类,全面了解影响它们药理作用发挥的因素具有重要意义。马忠宾[3]就铁皮石斛中主要成分的降血糖作用以及它们的作用机制进行综述。颜美秋等[4]针对常见石斛的多种活性成分,对它们在糖尿病治疗中的作用和机制进行了综述。但各类石斛多糖在糖尿病模型中降低血糖水平和改善糖尿病并发症方面的药理作用,及其在糖尿病防治中药理活性的影响因素及作用机制仍研究较少,本文就以上方面进行综述,以期为石斛多糖在糖尿病及并发症治疗方面的进一步开发利用提供参考。
1 石斛多糖在糖尿病中的药理作用
石斛属为兰科植物,品系众多,目前药用广泛的有铁皮石斛(Dendrobium officinale)、霍山石斛(D.huoshanense)、金钗石斛(D.nobile)、鼓槌石斛(D.chrysotoxum)、齿瓣石斛(D.devonianum)等[5]。由于生物碱、香豆素[6]、倍半萜[7]等具有降血糖功能活性的成分在石斛中的含量较低,提取和分离难度相对较大,因此近年来关于石斛降血糖功能及改善糖尿病并发症的研究主要集中于各类石斛多糖。
1.1 石斛多糖的降血糖作用
高血糖是糖尿病最重要的临床表现,而从霍山石斛、金钗石斛、铁皮石斛、迭鞘石斛、细茎石斛、鼓槌石斛中提取得到的多糖,近年来均被证明可以有效降低糖尿病模型的血糖水平[8-14]。糖尿病最主要有2种类型:其中Ⅰ型糖尿病通常是由于胰岛β细胞被破坏引起的,在对石斛降血糖功能特性研究中,最常采用的是由化学药物诱导建立的动物模型,如四氧嘧啶或链脲佐菌素诱导的糖尿病小鼠/大鼠模型;Ⅱ型糖尿病是最为常见的糖尿病的类型(超过90%),其特征是胰岛素抵抗和胰岛素分泌相对不足,常用的动物模型一般为长期高糖高脂饮食诱导的糖尿病小鼠/大鼠模型。在上述动物模型中,多种石斛多糖均被证实能够有效降低模型动物的空腹血糖值、餐后血糖值,且不会使正常小鼠的血糖值发生明显变化。同时,石斛多糖也能通过各种复杂的机制,降低动物模型体内糖化血红蛋白和糖化血清蛋白(glycated serum protein,GSP)的含量[8,11],修复胰岛细胞损伤[8],提高血清胰岛素水平[11-13],改善胰岛素抵抗等[9],有效改善机体对血糖水平的调节。不同石斛多糖的降糖作用见表1。
表1 不同石斛多糖降血糖作用研究
Table 1 The hypoglycemic effect of Dendrobium polysaccharides
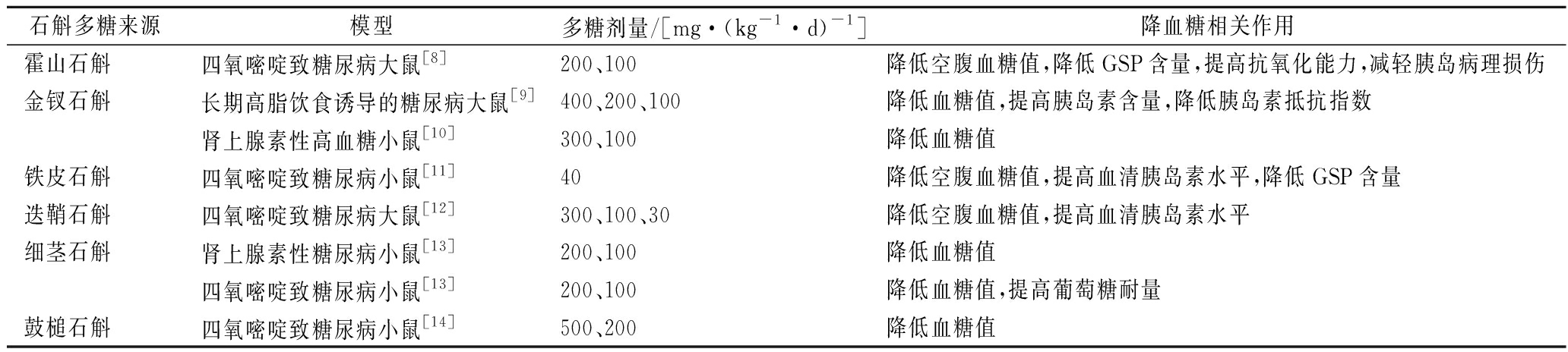
石斛多糖来源模型多糖剂量/[mg·(kg-1·d)-1]降血糖相关作用霍山石斛四氧嘧啶致糖尿病大鼠[8]200、100降低空腹血糖值,降低GSP含量,提高抗氧化能力,减轻胰岛病理损伤金钗石斛长期高脂饮食诱导的糖尿病大鼠[9]400、200、100降低血糖值,提高胰岛素含量,降低胰岛素抵抗指数肾上腺素性高血糖小鼠[10]300、100降低血糖值铁皮石斛四氧嘧啶致糖尿病小鼠[11]40降低空腹血糖值,提高血清胰岛素水平,降低GSP含量迭鞘石斛四氧嘧啶致糖尿病大鼠[12]300、100、30降低空腹血糖值,提高血清胰岛素水平细茎石斛肾上腺素性糖尿病小鼠[13]200、100降低血糖值 四氧嘧啶致糖尿病小鼠[13]200、100降低血糖值,提高葡萄糖耐量鼓槌石斛四氧嘧啶致糖尿病小鼠[14]500、200降低血糖值
1.2 石斛多糖防治糖尿病并发症的作用
研究证实,石斛多糖除直接的降血糖作用外,还对常见的多种并发症有明显的改善作用[15-21],例如糖尿病肾病、糖尿病性视网膜损伤、糖尿病性白内障、糖尿病性心血管病变。糖尿病的并发症是由于机体长期处于高糖状态下,体内的糖、蛋白质、脂肪、电解质等化学因子代谢紊乱引起细胞损伤,导致神经、血管发生病变,从而引起的各类可能危及患者生命的疾病。据美国糖尿病协会2010年统计,糖尿病并发症的发病率非常高,5年以上的病人其并发症的发病率高达61%,且并发症一旦产生将很难通过药物治疗将其逆转。近期针对糖尿病模型动物的大量研究证实,体内氧化应激、炎症反应能直接或间接地造成细胞和组织损坏,在糖尿病并发症的发生发展中起着重要作用。石斛多糖可降低糖尿病患者血糖、血脂水平,并令血压恢复正常;抑制细胞凋亡[18,21];减少体内氧化应激反应[15,18];降低机体炎症水平[16],从而有效预防或改善糖尿病并发症。不同石斛多糖对糖尿病并发症的改善作用见表2。
表2 不同石斛多糖对糖尿病并发症的改善作用
Table 2 The treatment for diabetes complications with Dendrobium polysaccharides
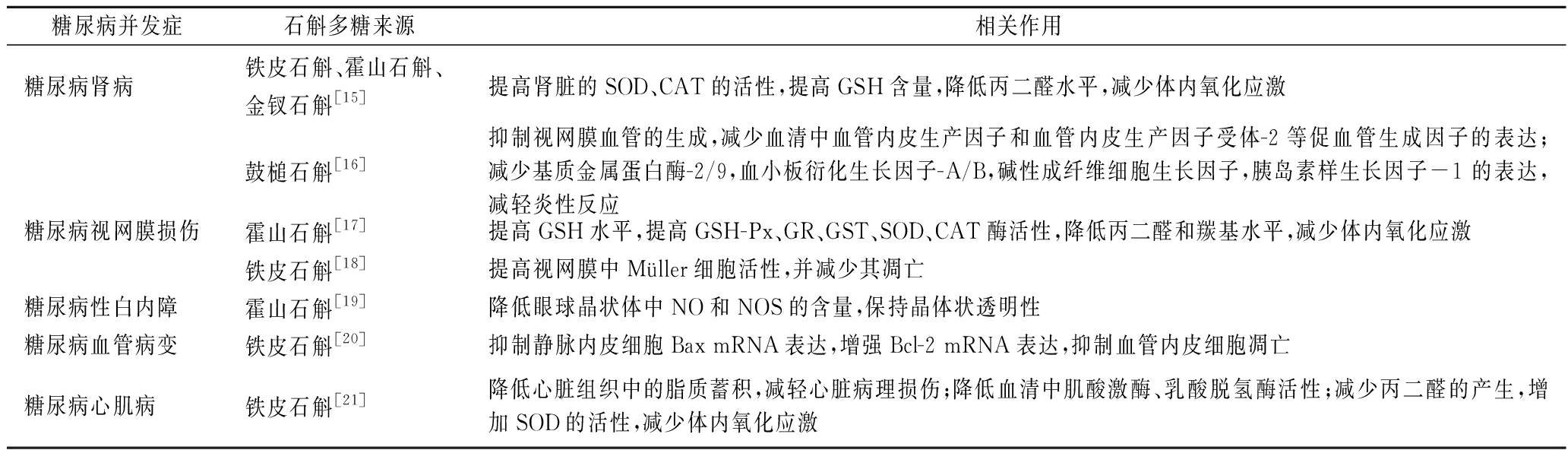
糖尿病并发症石斛多糖来源相关作用糖尿病肾病铁皮石斛、霍山石斛、金钗石斛[15]提高肾脏的SOD、CAT的活性,提高GSH含量,降低丙二醛水平,减少体内氧化应激鼓槌石斛[16]抑制视网膜血管的生成,减少血清中血管内皮生产因子和血管内皮生产因子受体-2等促血管生成因子的表达;减少基质金属蛋白酶-2/9,血小板衍化生长因子-A/B,碱性成纤维细胞生长因子,胰岛素样生长因子-1 的表达,减轻炎性反应糖尿病视网膜损伤霍山石斛[17]提高GSH水平,提高GSH-Px、GR、GST、SOD、CAT酶活性,降低丙二醛和羰基水平,减少体内氧化应激铁皮石斛[18]提高视网膜中Müller细胞活性,并减少其凋亡糖尿病性白内障霍山石斛[19]降低眼球晶状体中NO和NOS的含量,保持晶体状透明性糖尿病血管病变铁皮石斛[20]抑制静脉内皮细胞Bax mRNA表达,增强Bcl-2 mRNA表达,抑制血管内皮细胞凋亡糖尿病心肌病铁皮石斛[21]降低心脏组织中的脂质蓄积,减轻心脏病理损伤;降低血清中肌酸激酶、乳酸脱氢酶活性;减少丙二醛的产生,增加SOD的活性,减少体内氧化应激
2 防治糖尿病中石斛多糖药理活性的影响因素
相关研究表明石斛多糖具有降血糖和改善糖尿病并发症的活性,有作为治疗糖尿病的药物和功能性食品的价值。但石斛多糖的种类[23,25-27]、使用的剂量[14-15]、提取纯化方式[31-32]以及多糖改性[34-36]等均会导致其活性差异,因此研究影响石斛多糖活性的因素具有重要意义。
2.1 石斛种类的影响
口服的石斛多糖可迅速被胃酸降解产生稳定的片段[22],随后被小肠吸收进入全身循环。不同种类的石斛因其多糖成分存在差异,因而糖苷键裂解后产生的多糖片段不同,在改善糖尿病方面也会有不同的表现。李秀芳[23]采用水提醇沉法,从5种常见药用石斛中得到它们的粗多糖,并以相同剂量对糖尿病小鼠模型进行降血糖的活性研究,发现霍山石斛中的多糖活性优于其他石斛,金钗石斛多糖的降血糖活性略强于铁皮石斛,而流苏石斛和鼓槌石斛并没有明显的降糖功能。石斛中的葡聚糖以直接通过肠道上皮细胞的内在化过程被吸收到血液中[24]。WANG等[25]以铁皮石斛、兜唇石斛中的葡聚糖为研究对象,结果表明,这2类石斛中的葡聚糖均能显著减缓葡萄糖的扩散速率,但石斛多糖分支度的增加会减小其对α-淀粉酶的抑制作用。因此,需根据不同石斛的多糖成分和含量有针对性地在防治糖尿病方面开展生产和应用。
2.2 石斛单一多糖类型的影响
目前关于石斛多糖的研究,逐渐由探究石斛粗多糖对糖尿病的影响,变为分离提纯后单一多糖的组成及结构特征,并考察不同分离多糖的降血糖活性差异。大量研究表明,即使是从同一石斛中分离得到的多糖,它们的降血糖活性也会有明显的差异。汤志远等[11]从铁皮石斛的茎中分离获得4种硫酸多糖,分别以相同的剂量对四氧嘧啶诱发小鼠糖尿病模型进行给药。21 d后发现,其中含量最高的分离多糖DOP1的降血糖、提高血清胰岛素水平以及降低GSP含量的作用最强,其单糖组成和物质的量比为阿拉伯糖:葡萄糖∶半乳糖∶甘露糖=3.5∶1.5∶1.2∶1.0。近几年,国内外对石斛的研究不再局限于茎,石斛叶和根[26-27]也被证实具有降血糖及抗糖尿病相关功效。但即使是同一种石斛,不同部位所含的多糖种类也并不会完全相同。LIU等[28]从霍山石斛的茎、根、叶和花中分离得到的多糖的相对分子质量分别为2.59×105、1.41×104、2.09×105和4.78×105 Da,且它们单糖组成、糖苷键类型、序列以及乙酰化位点间也都存在显著差异。它们结构的差异预示着不同的生物活性,未来在防治糖尿病及并发症的相关应用中应该对此加以区别,但目前仍鲜有此方面报道。因此从石斛的不同部位分离纯化得到单一多糖,并阐明其结构特征也有利于对石斛多糖降血糖方面的研究。
2.3 石斛多糖剂量的影响
科学的用药剂量是保障石斛多糖安全有效的关键。2010年《中华人民共和国药典》推荐每人每日的铁皮石斛用量为6~12 g,通常在实验中也会参考与之相当的石斛多糖剂量,对动物模型进行给药[29],一般设置在500 mg/(kg·d)内。研究表明,在此范围内石斛多糖的降血糖作用为剂量依赖型[8-14],相对高剂量(>200 mg/(kg·d))的石斛多糖[8-9,13]的降血糖效果更为明显,而低剂量[30 mg/(kg·d)]的石斛多糖[12]并不能使血糖降至正常水平。另外,剂量的选择也关系到能否正确评价石斛多糖降血糖效果。PAN等[15]发现四氧嘧啶诱导的小鼠,以50~200 mg/kg的剂量喂食鼓槌石斛多糖12 d后,没有降低血糖作用,而ZHAO等[14]报道在同一小鼠模型中,使用剂量为200~500 mg/(kg·d)具有显著降低血糖水平的作用。因此,了解石斛多糖在胃肠道内的消化,设置有效合理的石斛多糖口服剂量也是需要研究解决的问题。
2.4 石斛多糖制备工艺的影响
石斛多糖的提取工艺也可能会改变其理化性质,从而影响其防治糖尿病相关药理作用的发挥。超声和微波[30]常被用于促进多糖的浸出,但在处理过程中可能会使部分多糖发生解聚。提取时,加入碱性溶液也可能会使石斛多糖复杂的网状结构裂解[31],导致其生物活性改变。谭青云等[32],选用传统热水提取法、酶提取法、闪式提取法、超声波提取法、冻融提取法这5种常用方式提取铁皮石斛多糖,并对所得粗多糖进行体外降血糖活性的测定。研究发现,冻融提取法对铁皮石斛多糖的结构影响较小,得率和所得多糖的平均分子质量最高,体外降血糖活性也相对最强。另外,石斛多糖的纯度也会影响它生物活性的发挥,通常研究多糖的化学结构与糖尿病药理作用的关系也需要较高的纯度,因此纯化过程也是制备多糖的重要步骤。然而,目前分离纯化石斛多糖主要采用的是耗时多、产量低的柱层析方法,为满足工业化大生产的需求,分级醇沉、盐析及超滤等更高效的分离提纯方式有望得到应用,但它们对石斛多糖相关药理作用的影响仍有待进一步确认。
2.5 石斛多糖改性的影响
一般多糖的生物活性取决于其结构特征,例如单糖组成的类型、分子质量、取代度、糖苷键的连接类型以及分支的类型和位置[33]。通过适当的处理改变多糖的结构,可能会提高石斛多糖在治疗糖尿病方面的生物活性。ZHA等[34]报道了使用果胶酶水解霍山石斛多糖,可以降低霍山石斛多糖的分子质量,并能加强其对蛋白质非酶糖基化的抑制作用。王丹等[35]研究发现,经红曲霉发酵后的铁皮石斛多糖液对α-葡萄糖苷酶和α-淀粉酶的抑制活性相对未发酵的对照组分别提高了78.9%和 86.8%。近期,对多糖的分子修饰以改善其生物活性的研究也引起了广泛的关注。LI等[36],对霍山石斛多糖DHPD1中多糖残基的C-2和C-6进行硫酸化,发现硫酸化可以增强石斛多糖的抗糖基化活性,且硫酸基团的取代度越高,抗糖基化作用越强。目前虽有较多石斛多糖防治糖尿病效果的研究,但具体哪些结构会影响石斛多糖的降血糖作用效果还未明确。
3 石斛多糖对糖尿病治疗作用的主要机制研究
在明确石斛多糖对糖尿病治疗效果的基础上,探明其改善糖尿病作用机制将有利于促进石斛多糖类产品的开发与应用。根据现有研究,石斛多糖降低血糖和防治糖尿病并发症的主要作用机制为:恢复胰腺损伤并促进胰岛素分泌[37-40],抑制肠道α-淀粉酶和α-葡萄糖苷酶活性[40-41],清除自由基和抗脂质过氧化[42-43],抗糖基化[44-45],调节信号通路PI3K/Akt[25,46]和NF-κB[48-50]。
3.1 保护胰岛β细胞,促进胰岛素分泌
胰岛素是目前发现的动物体内唯一的降血糖激素,糖尿病的特征是胰岛β细胞分泌的胰岛素绝对或相对缺乏,导致机体内的血糖水平调节不良。尽管目前糖尿病中β细胞损伤、凋亡的机制是复杂且有争议的,但抑制β细胞损伤和凋亡,并促进胰岛素分泌仍是改善机体对血糖水平控制的关键。大量研究证实,石斛多糖能够通过抗炎、抗氧化等方式修复受损胰岛的结构[37]。陈云龙等[13]研究发现,100、200 mg/kg的细茎石斛多糖能显著减轻四氧嘧啶对胰岛β细胞的损伤,恢复胰岛β细胞的功能,最终起到降血糖的作用。另外有研究认为,胰高血糖素样肽-1(glucagon like pepticle 1,GLP-1)是一类影响糖代谢的重要激素,它可以刺激胰岛素的分泌。而糖尿病患者胃肠道L细胞GLP-1分泌减少,这是造成糖尿病患者餐后血糖异常升高的重要原因。WANG等[25]分离得到了平均分子质量为73 kDa的霍山石斛纯化多糖,其口服可以恢复由高脂饮食和链脲佐菌素诱导破坏的胰岛,并刺激GLP-1的分泌,提高胰岛β细胞分泌胰岛素的水平。由此可知,石斛多糖具有胰内降血糖作用机制,它可以通过恢复胰腺损伤,促进胰岛素的分泌,提高体内胰岛素对血糖的响应水平等方式稳定血糖。
3.2 抑制肠道α-淀粉酶、α-葡萄糖苷酶活性
餐后血糖的异常可能会引起机体对胰岛素敏感性的降低,因此降低餐后血糖峰值是缓解糖尿病患者病情的重要方法。在哺乳动物体内,碳水化合物通常被消化系统中的各类水解酶分解成单糖,在小肠到血液被吸收,餐后血糖水平随之升高。其中,α-淀粉酶是一类分解长链碳水化合物的酶;而α-葡萄糖苷酶可以水解葡萄糖苷键[39],进而释放出葡萄糖。它们都是碳水化合物消化吸收、糖原分解代谢必不可少的酶,因而对它们具有抑制活性的物质常被认为是糖尿病的潜在治疗剂。阿卡波糖、伏格列波糖等口服降糖药就是通过竞争性抑制α-葡萄糖苷酶,达到降低餐后血糖峰值的效果。目前,已有多种石斛多糖被研究证实对α-葡萄糖苷酶有抑制活性[40]。孟映霞[41]对金钗石斛叶多糖的体外研究发现,浓度为10 mg/mL的粗多糖对α-葡萄糖苷酶和α-淀粉酶的抑制率可达45.63%、39.91%,随后的体内动物实验也证实了石斛多糖具有对这2类酶活性较强的抑制作用。石斛多糖能够通过延迟葡萄糖向血糖的转化,从而减少餐后血糖的升高。
3.3 清除自由基及抗脂质过氧化
人体代谢过程中必然会产生自由基,然而当体内自由基产生过量,或自身的抗氧化防御能力不足时,体内细胞、组织器官、酶的损伤和脂质过氧化程度会随之增加。胰岛β细胞对糖尿病患者病情发展有关键作用,然而它表达抗氧化酶的水平相对较低,非常容易受到活性氧和活性氮的攻击而受到损伤。有研究表明,在糖尿病动物模型中,石斛多糖作为一类具有抗氧化和免疫增强功能的化合物,可以提高机体内SOD、CAT和GSH-Px等酶的活性,恢复体内抗氧化酶系统的活力,并降低丙二醛的水平[42],从而改善β细胞功能障碍并减少β细胞凋亡。另外,糖尿病患者体内长期过高的脂质过氧化水平,会导致催化生成谷胱甘肽(GSH)的还原性谷胱甘肽酶的活性大大降低,进而对组织细胞的结构和功能产生损害,诱发各类并发症。LI等[17]研究发现,霍山石斛多糖能增加晶状体内的GSH含量,并提高GSH-Px的活性,阻止糖尿病性白内障的发生。因此,可推测石斛多糖因其较强的清除自由基的能力,可以减少胰岛β细胞的氧化损伤;另一方面,石斛多糖可以增强体内抗氧化酶系统的功能,分解脂质过氧化物,减少组织器官中过氧化物的积累,通过其抗氧化活性和改善机体抗氧化系统能力的机制来改善糖尿病及其并发症。
3.4 抗糖基化
糖基化是一类缓慢而不可逆的非酶促的糖化反应,反应过程中糖的醛基和蛋白质的氨基之间发生复杂的反应,形成高分子酮胺结构。糖基化终末产物(advancend glycation end-products,AGEs)在体内的聚集,会降低内皮型一氧化氮合酶(endothelial nitric oxidesynthase,NOS)的表达,而eNOS调节产生的内皮源性血管舒张因子NO[43],对于维持血管舒缩功能、神经保护作用有着重要作用。同时,AGEs也会降低血栓调节蛋白的表达,破坏机体凝血与抗凝血的平衡,进而引发各种糖尿病并发症。体外实验研究发现,石斛多糖能以剂量和时间依赖的方式抑制糖基化,质量分数为2%的霍山石斛多糖溶液对蛋白质糖基化的抑制率可达28%[44]。动物实验也证实了霍山石斛多糖[19]可以通过减少iNOS基因表达和AGEs的产生,从而抑制糖尿病性白内障的发生。每日喂食200 mg/kg霍山石斛多糖,大鼠模型中晶状体内NO和NOS的含量降低33%以上,晶状体混浊程度显著减轻。由此,可推测石斛多糖改善糖尿病作用的机制可能是抑制体内的糖基化反应,减少糖基化产物的生成,从而改善因机体长期处于高血糖状态下产生的各类器官病变,对糖尿病并发症起到防治作用。
3.5 调节信号通路PI3K/Akt
现代研究普遍认为,PI3K/Akt 信号通路在葡萄糖代谢的调节中起着重要作用。葡萄糖转运体(glucose transportes,GLUT)是细胞膜上的载体蛋白,人体中部分葡萄糖扩散进入细胞的过程就是通过GLUT的转运完成的,因此其分布也对糖尿病的病情有着重要影响。PI3K/Akt信号通路的激活,会促进GLUT4的转位,并促使GLUT2蛋白的表达[45],从而增加各类细胞对葡萄糖的摄取,起到调节糖原合成、糖异生和糖酵解的作用,改善血糖水平。WANG等[25]研究发现,200 mg/(kg·d)的霍山石斛多糖GXG给药显著促进了PI3K和Akt的磷酸化,而FoxO1和GSK3β的磷酸化被明显抑制,从而抑制了肝细胞将多种非糖物质转变成葡萄糖或糖原,同时也能够减弱肝的脂多糖促炎症反应。WANG等[46]实验证实了铁皮石斛多糖可以促使糖尿病小鼠体内胰岛素受体底物IRS1与IRS-β的结合,上调PI3K蛋白的表达,通过调节肝或肌肉中的糖原合酶、糖原合酶激酶,增加GLUT4的表达,最终发挥调节糖代谢紊乱的作用。因此可推测,石斛多糖可以通过调节PI3K/Akt信号通路,影响各类组织细胞对葡萄糖的摄取,进而调节糖尿病患者体内的糖代谢,发挥改善胰岛素抵抗和降血糖的作用。
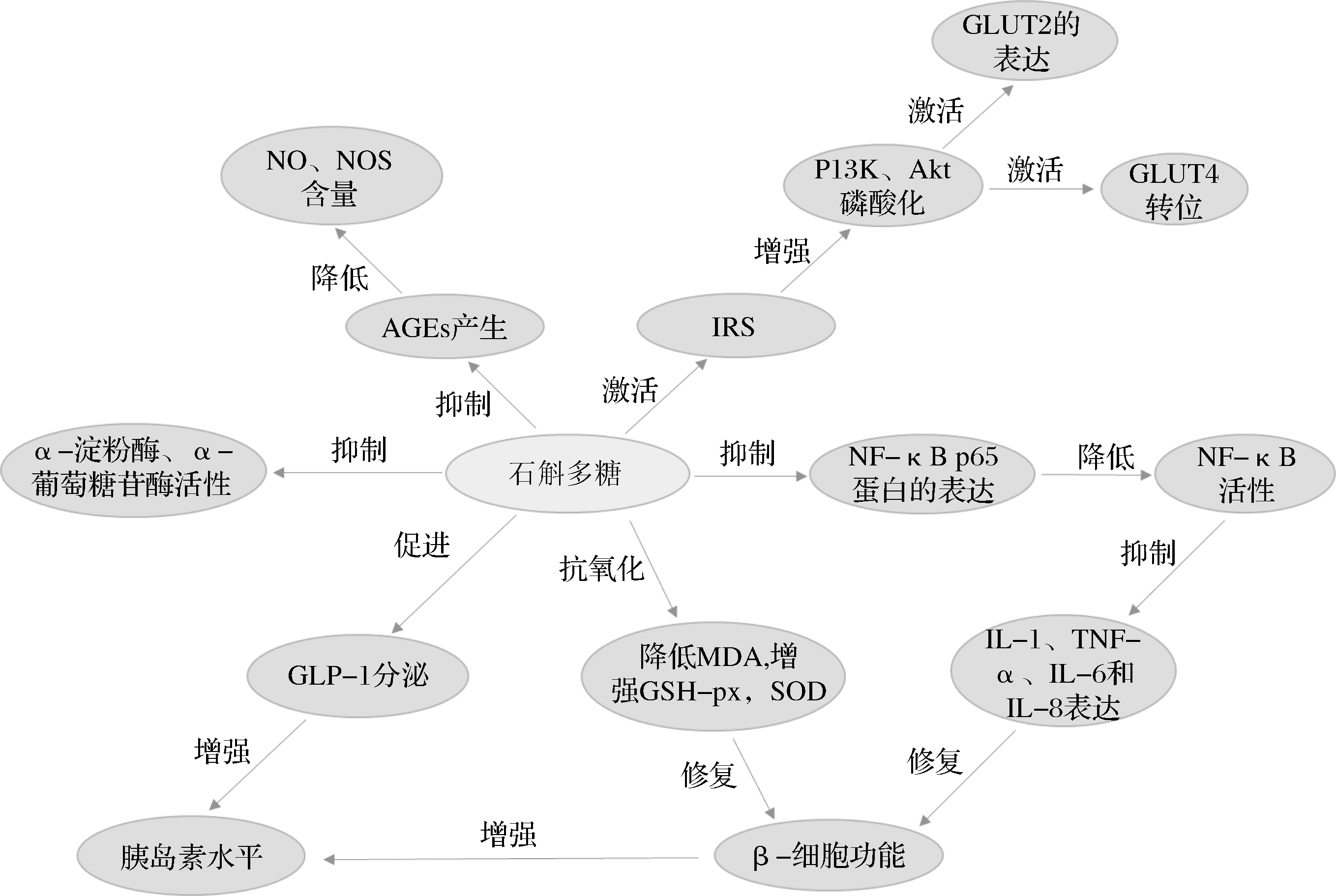
图1 石斛多糖降糖作用机制
Fig.1 Hypoglycemic mechanism of Dendrobium polysaccharide
3.6 调节信号通路NF-κB
近年来,国内外多项研究发现,糖尿病性视网膜病变、肾病等的动物模型中NF-κB通路被激活[47-48]。其中,核转录因子κB(nuclear factor κB,NF-κB)的激活会导致一系列靶基因的激活,导致各种炎症细胞因子如IL-1、IL-6、IL-8和TNF-α的过量表达,由此引发的炎症过程不仅会破坏胰岛β细胞,也会使各类组织器官产生一定的生理变化。LI等[48]研究发现,石斛多糖可以有效抑制NF-κB的表达,喂食铁皮石斛多糖的糖尿病性视网膜病变大鼠体内NF-κB的表达明显低于糖尿病组,而正常组的大鼠无阳性表达。胰岛素抵抗通常会引发血管内皮的损伤,最终导致动脉粥样硬化。高糖诱导的大鼠实验模型中,血管内皮依赖性舒张功能会受到抑制,钟惠娟等[49]发现铁皮石斛多糖对其具有改善作用,作用机制也可能与NF-κB 信号通路有关。由此可知,石斛多糖可以有效抑制患者体内NF-κB的过量表达,这可能是它控制机体正常血糖水平,以及对糖尿病并发症的早期干预和保护的机制。
4 结论与展望
相比于常规口服抗糖尿病药物,石斛多糖的优势突出,开发前景广阔:虽然影响石斛多糖药理活性的因素众多,但其安全性高,保健功能确切且可长期服用;石斛多糖改善糖尿病及其并发症的机制多样,相比于靶点明确的化学药物,它对糖尿病的防治更偏向于综合改善,作用更加全面,其作用机制见图1;石斛传统的药用部位为茎,但随着开发的深入,其他部位提取的多糖也被证实具有改善血糖水平的作用,综合利用开发前景广阔。
尽管石斛多糖的降血糖的药理活性已被大量实验证实,但相比于常规的糖尿病治疗药物,未来还有许多问题需要进一步深入研究:
1)最合适的石斛种类以及石斛多糖的制取方法目前尚无定论。我国目前主要的药用石斛约有20余种,临床上石斛的种类和产地多样,且目前单一多糖样品的制备较困难,多数研究仍只是对粗提物的功能进行评估。因此需要进一步的工作来研究各类石斛多糖的糖尿病相关药理活性,从而选择合适的石斛多糖以开发功能性产品。
2)多糖的结构与降血糖功能之间的关系尚不清楚。目前,对于石斛多糖结构的研究还处在单糖组成及分子质量大小等一级结构的阶段,对于高级结构的研究,以及生物活性所需的特定的寡糖片段的探索仍不足。进一步揭示石斛多糖的结构与其特定功能、作用机制的关系,仍是目前需要深入探索的方面。
3)糖尿病的发病机制复杂,临床上不同降糖药有各自不同的作用机制和相应的适应症。要开发符合临床需求的石斛多糖制剂和相关保健品,需对其机制进行更加深入的探究。目前对石斛多糖的代谢机理、胃肠道消化的研究也仍处于初级阶段,在实际临床中的治疗效果也需要进行确认。另外,石斛与其他药物或成分联用的疗效及机制也有待进一步研究。
[1] POUYA S,INGA P,PARASKEVI S,et al.Global and regional diabetes prevalence estimates for 2019 and projections for 2030 and 2045: Results from the International Diabetes Federation Diabetes Atlas,9th edition[J]. Diabetes Research and Clinical Practice,2019,12(157):107 843.
[2] BAILEY C J,TAHRANI A A,BARNETT A H,et al.Future glucose-lowering drugs for type 2 diabetes[J].The Lancet Diabetes & Endocrinology,2016,4(4):350-359.
[3] 马忠宾.铁皮石斛降血糖作用的研究概况[J].首都食品与医药,2018,25(5):101-102.
MA Z B.Research on hypoglycemic effect of Dendrobium candidum (in Chinese)[J].Capital Food Medicine,2018,25(5):101-102.
[4] 颜美秋,杨志远,施秋秋,等.石斛在糖尿病等代谢性疾病中的作用及机制研究进展[J].中草药,2019,50(10):2 491-2 497.
YAN M Q,YANG Z Y,SHI Q Q,et al.Research progress on protective effects and mechanism of Dendrobii caulis on metabolic disturbances[J].Chinese Traditional and Herbal Drugs,2019,50(10):2 491-2 497.
[5] 国家药典委员会. 中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015.
National Pharmacopoeia Committee.Pharmacopoeia of the People’s Republic of China.Part 1[M].Beijing:China Medical Science and Technology Press,2015.
[6] 李旻,刘友平,范婧娴,等.川产迭鞘石斛中香豆素的分离鉴定及药材质量标准研究[J].中国药房,2010,21(7):624-625.
LI M,LIU Y P,FAN J X,et al.Isolation and identification of coumarin in Dendrobium denneanum cultivated in Sichuan and its quality standard study[J].China Pharmacy,2010,21(7):624-625.
[7] 张雪, 高昊,韩慧英,等.金钗石斛中的倍半萜类化合物[J].中草药,2007,38(12):1 771-1 774.
ZHANG X,GAO H,HAN H Y,et al.Sesquiterpenes from Dendrobium nobile[J].Chinese Traditional and Herbal Drugs,2007,38(12):1 771-1 774.
[8] 邓媛元.霍山石斛多糖抗糖尿病性白内障的研究[D].合肥:合肥工业大学,2007.
DENG Y Y. Studies on the anti.diabetic cataract of polysaccharides from Dendrobium huoshanense[D]. Hefei:Hefei University of Technology,2007.
[9] LIU Y,WU J,LI W,et al.Effect of RIP3 expression in myocardial tissue of type 2 diabetic rats by treating with Dendrobium nobile polysaccharide[J].Journal of Liaoning University of Traditional Chinese Medicine,2017,19(12):44-48.
[10] 李菲, 黄琦,李向阳,等.金钗石斛提取物对肾上腺素所致血糖升高的影响[J].遵义医学院学报,2008,31(1):11-12.
LI F,HUANG Q,LI X Y,et al.Effects of the extracts from Dendrobium nobile lindl on bloodsugar in normal and hyperglycemic mice[J].Acta Academiae Medicinae Zunyi,2008,31(1):11-12.
[11] 汤志远, 周晓宇,冯健,等.铁皮石斛多糖降血糖作用研究[J].南京中医药大学学报,2016,32(6):566-570.
TANG Z Y,ZHOU X Y,FENG J,et al.The hypoglycemic activity of homogeneous polysaccharides from Dendrobium officinale[J].Journal of Nanjing University of Traditional Chinese Medicine,2016,32(6):566-570.
[12] 罗傲霜. 迭鞘石斛多糖降血糖作用研究[D].成都:四川大学,2006.
LUO A S.Effect of Dendrobium denneanum polysaccharide reducing blood glucose in vivo[D].Chengdu:Sichuan University,2006.
[13] 陈云龙, 何国庆,张铭,等.细茎石斛多糖的降血糖活性作用[J].浙江大学学报(理学版),2003,30(6):693-696.
CHEN Y L,HE G Q,ZHANG M,et al.Hypoglycemic effect of the polysaccharide from Dendrobium moniliforme[J].Journal of Zhejiang University (Science Edition),2003,30(6):693-696.
[14] ZHAO Y P,SON Y O,KIM S S,et al.Antioxidant and anti-hyperglycemic activity of polysaccharide isolated from Dendrobium chrysotoxum Lindl[J].International Journal of Biological Macromolecules,2007,40(5):670-677.
[15] PAN L,LI X,WANG M,et al.Comparison of hypoglycemic and antioxidative effects of polysaccharides from four different Dendrobium species[J].International Journal of Biological Macromolecules,2014,64:420-427.
[16] GONG C Y,YU Z Y,LU B,et al.Ethanol extract of Dendrobium chrysotoxum Lindl ameliorates diabetic retinopathy and its mechanism[J].Vascular Pharmaceutical Biology,2014,62(3):134-142.
[17] 李秀芳,邓媛元,潘利华,等.霍山石斛多糖对糖尿病性白内障大鼠眼球晶状体组织抗氧化作用的研究[J].中成药,2012,34(3):418-421.
LI X F,DENG Y Y,PAN L H,et al.Antioxidant effect of polysaccharide from Dendrobium huoshanense on lens tissue of diabetic cataract rats[J].Chinese Traditional Patent Medicine,2012,34(3):418-421.
[18] 李雅嘉, 王华,李强翔.铁皮石斛多糖对高糖状态下视网膜Müller 细胞活力及凋亡的调控[J].中国老年学杂志,2014,34(23):6 683-6 685.
LI Y J,WANG H,LI X Q.Regulation of polysaccharide of Dendrobium on cell viability and the rates of apoptosis in rats retinal M üller cells cultured with high glucose[J].Chinese Journal of Gerontology,2014,34(23):6 683-6 685.
[19] LUO J,DENG Y,ZHA X.Mechanism of polysaccharides from Dendrobium huoshanense on streptozotocin-induced diabetic cataract[J].Pharmaceutical Biology,2008,46(4):243-249.
[20] 张贝贝, 刘文洪,李俊峰,等.铁皮石斛多糖对高糖诱导的血管内皮细胞Bax、Bcl-2表达的影响[J].中国药理学通报,2015,31(1):64-70.
ZHANG B B,LIU W H,LI J F,et al,Effects of polysaccharides from Dendrobium officinale on expression of Bax and Bcl-2 in vascular endothelial cells induced by high sugar[J].Chinese Pharmacological Bulletin,2015,31(1):64-70.
[21] ZHANG Z,ZHANG D,DOU M,et al.Dendrobium officinale Kimura et Migo attenuates diabetic cardiomyopathy through inhibiting oxidative stress,inflammation and fibrosis in streptozotocin-induced mice[J].Biomed Pharmacother,2016,84:1 350-1 358.
[22] XIE S Z,GE J C,LI F,et al.Digestive behavior of Dendrobium huoshanense polysaccharides in the gastrointestinal tracts of mice[J].International Journal of Biological Macromolecules,2018(107):825-832.
[23] 李秀芳. 霍山石斛和四种药典石斛多糖降血糖活性比较研究[D].合肥:合肥工业大学,2012.
LI X F.Comparison of hypoglycemic activities of polysaccharides from Dendrobium huoshanense and four Dendrobium species cited in Pharmacopoeia[D].Hefei:Hefei University of Technology,2012.
[24] PETER J R,ELIZABETH L A,TAMMY O S,et al.Oral delivery and gastrointestinal absorption of soluble glucans stimulate increased resistance to infectious challenge[J].Journal of Pharmaceutical biology and Experimental Therapeutics,2005,314(3):1 079-1 086.
[25] WANG H Y,LI Q M,YU N J,et al.Dendrobium huoshanense polysaccharide regulates hepatic glucose homeostasis and pancreatic β-cell function in type 2 diabetic mice[J].Cabohydr Polym,2019,211:39-48.
[26] YANG K,LU T,ZHAN L,et al.Physicochemical characterization of polysaccharide from the leaf of Dendrobium officinale and effect on LPS induced damage in GES-1 cell[J].International Journal of Biological Macromolecules,2020,149(1):320-330.
[27] 宓文佳, 陈素红,吕圭源,等.铁皮石斛根提取物对2型糖尿病模型小鼠的降糖作用研究[J].中药药理与临床,2015,31(1):125-129.
MI W J,CHEN S H,LV G Y,et al.Hypoglycemic effect of extracts from Dendrobium officinale roots on type 2 diabetic model mice[J].Pharmacy and Clinics of Chinese Materia Medica,2015,31(1):125-129.
[28] YANG K,LU T T,ZHAN L H,et al.Physicochemical characterization of polysaccharide from the leaf of Dendrobium officinale and effect on LPS induced damage in GES-1 cell[J].International Journal of Biological Macromolecules,2020,149(1):320-330.
[29] LIU B,SHANG Z Z,LI Q M,et al.Structural features and anti-gastric cancer activity of polysaccharides from stem,root,leaf and flower of cultivated Dendrobium huoshanense[J].International Journal of Biological Macromolecules,2020(143):651-664.
[30] 黄晓君,聂少平,王玉婷,等.铁皮石斛多糖提取工艺优化及其成分分析[J].食品科学,2013,34(22):21-26.
HUANG S J,NIE S P,WANG Y T,et al.Optimized extraction and compositional analysis of polysaccharides from dried stems of Dendrobium officinale [J].Food Science,2013,34(22):21-26.
[31] 陈盛余, 赵丹丹,谢瑜,等.铁皮石斛多糖的微波辅助提取工艺研究[J].食品研究与开发,2017,38(6):49-52.
CHEN S Y,ZHAO D D,XIE Y,et al.Study on the technology of extracting polysaccharides from dried stems of Dendrobium officinale kimuraet migo by microwave method[J].Food Research And Development,2017,38(6):49-52.
[32] 敖娇, 鲍家科,夏玉吉,等.不同提取方法对金钗石斛多糖形貌结构的影响[J].中成药,2018,40(7):1 648-1 652.
AO J,BAO J K,XIA Y J,et al.Effects of different extraction methods on morphology and structure of polysaccharides from Dendrobium nobile [J].Chinese Traditional Patent Medicine,2018,40(7):1 648-1 652.
[33] 谭青云, 袁永俊,王丹,等.不同提取方式对铁皮石斛多糖及体外降血糖的影响[J].食品科技,2019,44(6):202-206.
TAN Q Y,YUAN Y J,WANG D,et al.Effects of different extraction methods on polysaccharide from Dendrobium candidum and hypoglycemic effect in vitro[J].Food Science and Technology,2019,44(6):202-206.
[34] ZHANG Y L,LU X Y,ZHANG Y N,et al.Sulfated modification and mmunomodulatory activity of water-soluble polysaccharides derived from fresh Chinese persimmon fruit[J].International Journal of Biological Macromolecules,2010,46(1):67-71.
[35] ZHA X Q,LI X L,ZHANG H L,et al.Pectinase hydrolysis of Dendrobium huoshanense polysaccharide and its effect on protein nonenzymatic glycation[J].International Journal of Biological Macromolecules,2013,61(1):439-447.
[36] 王丹, 袁永俊,谭青云,等.不同菌种发酵对铁皮石斛多糖及其生物活性的影响[J].中国调味品,2019,44(9):39-43.
WANG D,YUAN Y J,TAN Q Y,et al.Effects of different strains fermentation on polysaccharide and biological activity of Dendrobium candidum[J].China Condiment,2019,44 (9):39-43.
[37] LI X L,XIAO J J,ZHA X Q,et al.Structural identification and sulfated modification of an antiglycation Dendrobium huoshanense polysaccharide[J].Carbohydrate Polymers,2014,106(15):247-254.
[38] 赵亨, 昌智平,张艳磊,等.金钗石斛多糖对高糖诱导的大鼠INS-1细胞胰岛素分泌的影响[J].中国保健营养,2014,24(4):2 456-2 457.
ZHAO H,CHANG Z P,ZHANG Y L,et al.Effect of Dendrobium nobile polysaccharides on insulin secretion by rat INS-1 cells cultured in high glucose[J].China Health Care & Nutrition,2014,24(4):2 456-2 457.
[39] MEERA S,MARCELLO C L,CHIARA D M,et al.Contribution of endogenous glucagon-like peptide-1 to changes in glucose metabolism and islet function in people with type 2 diabetes four weeks after Roux-en-Y gastric bypass (RYGB)[J].Metabolism,2019,93(1):10-17.
[40] LIU Z,MA S.Recent advances in synthetic α-glucosidase inhibitors[J].Chemmedchem,2017,12(11):31-44.
[41] 马荣锋, 唐川,汪雯瀚,等.霍山石斛与铁皮石斛的体外生物活性比较[J].食品工业科技,2019,40(12):26-30;37.
MA R F,TANG C,WANG W H,et al.Comparison of biological activities in vitro of Dendrobium huoshanense and Dendrobium officinale[J].Science and Technology of Food Industry,2019,40(12):26-30;37.
[42] 孟映霞. 金钗石斛叶水溶性多糖的提取分离纯化及体外生物活性研究[D].无锡:江南大学,2017.
MENG Y X,Studies on extraction,isolation,purification and in vitro bioactivity of water-soluble polysaccharides from Dendrobium nobile Lindl.leaves[D].Wuxi:Jiangnan University,2017.
[43] 周琪.铁皮石斛水提物对糖尿病小鼠血糖和肠道菌群的影响[D].大连:大连医科大学,2017.
ZHOU Q,The influence of Dendrobium candidum extract on blood glucose and the intestinal microflora in diabetic mice[D].Dalian:Dalian Medical University,2017.
[44] GUO Z,ZHOU Y,YANG J,et al.Dendrobium candidum extract inhibits proliferation and induces apoptosis of liver cancer cells by inactivating Wnt/β-catenin signaling pathway[J].Biomedicine & Pharmacotherapy,2019,12(110):371-379.
[45] PAN L,FENG B,WANG J,et al.Structural characterization and anti-glycation activity in vitro of a water-soluble polysaccharide from Dendrobium huoshanense[J].Journal of Food Biochemistry,2013,37(3):313-321.
[46] GARABADU D,KRISHNAMURTHY S.Metformin attenuates hepatic insulin resistance in type-2 diabetic rats through PI3K/Akt/GLUT-4 signalling independent to bicuculline-sensitive GABAA receptor stimulation[J].Pharmaceutical Biology,2017,55(1):722-728.
[47] WANG K,WANG H,LIU Y,et al.Dendrobium officinale polysaccharide attenuates type 2 diabetes mellitus via the regulation of PI3K/Akt-mediated glycogen synthesis and glucose metabolism[J].Journal of Functional Foods,2018(40):261-271.
[48] GUAN T,FANG F,SU X,et al.Silencing PEG3 inhibits renal fibrosis in a rat model of diabetic nephropathy by suppressing the NF-κB pathway[J].Molecular and Cellular Endocrinology,2020,513:110 823.
[49] LI J,LI G,YU Q.Effects of polysaccharides of Dendrobium candidum on overexpression of inflammatory factors in diabetic rats with retinopathy[J].Chin J Chin Ophthalmol,2016,26(1):7-11.
[50] 钟惠娟, 陈璐,周洁,等.铁皮石斛多糖对高糖诱导的血管内皮依赖性舒张功能的影响[J].中国新药杂志,2017(12):103-109.
ZHONG H J,CHEN L,ZHOU J,et al.Effect of Dendrobium polysaccharides on injury of endothelium-dependent relaxation induced by high glucose[J].Chinese Journal of New Drugs,2017(12):103-109.