如今老龄化愈来愈严重,已成为人类发展中面临的一大挑战。老年人随着身体机能变得迟缓,各项生理功能减弱,尤其是伴随各种病症的情况,会引起吞咽能力下降,表现为吞咽功能障碍[1]。吞咽障碍患者可能有吸入性肺炎和其他呼吸系统疾病的风险[2],甚至危及生命。研究表明,以黄原胶为胶基制备的食品增稠剂,具备较高的黏度,可以延缓吞咽流体食品的速度,对患有吞咽障碍的病人有一定治疗作用,从而避免一系列可能发生的危险[3]。
黄原胶(xanthan gum,XG)作为一种食品添加剂,已广泛应用于增稠、悬浮、乳化等方面[4]。但黄原胶在溶解过程中,由于颗粒表面快速溶胀形成有黏度的胶层,容易导致结块,降低了整体的溶解速度,在应用领域上受到一定限制,因此对黄原胶进行改性成为重要的研究方向。物理改性方法相对化学改性更安全,化学改性往往会引入新的物质而难以去除,且工艺比较复杂。目前对黄原胶物理改性方法,如造粒[5]、与小分子多糖复配[6]、添加分散剂[7]等,分别有设备需求高、用量大等问题;干热改性是一种操作简单、安全健康的物理改性方法[8],目前黄原胶多用于与淀粉混合进行干热处理来提高淀粉的黏度、抑制糊化、热稳定性等理化性质[9-11],包括木薯淀粉[12]、玉米淀粉[13]、马铃薯淀粉[14]等与黄原胶干热处理,淀粉分子的羟基与黄原胶分子的羧基发生交联从而引起理化性质的改变,而鲜有报导黄原胶单独干热改性的变化。
黄原胶与其他胶体如瓜尔胶[15]、魔芋胶[16]、刺槐豆胶[17]等复配,有增稠协同的效果。预糊化淀粉冷热水皆可溶,具有增稠稳定作用,麦芽糊精作为一种小分子多糖,经常用作食品配料,改善食品品质[18],因其良好的水溶性,与黄原胶复配可增加黄原胶与水的接触面积,提高黄原胶的分散性能[19-20]。因此本实验选择预糊化淀粉和麦芽糊精与改性黄原胶复配。
本研究对黄原胶进行干热改性,探讨其改性后的速溶性和黏度变化机理,并与预糊化淀粉和麦芽糊精复配,应用于吞咽造影,探讨其应用效果。
1 材料与方法
1.1 材料与仪器
黄原胶(水分含量11%,食品级),山东阜丰集团有限公司;预糊化淀粉(食品级),嘉兴欣欣食品科技有限公司;麦芽糊精(食品级),河南百里溪食品配料有限公司;硫酸钡(Ⅱ型)干混悬剂,青岛红蝶新材料有限公司;奥特顺咽,市售国产增稠剂,广州奥迪特生物科技有限公司;鹤鸿春,市售国产增稠剂,青岛思博瑞恩实业有限公司;莎罗雅牌市售增稠剂,日本。
NDJ-5S型旋转黏度计,上海昌吉地质仪器有限公司;Nicolet is10型傅里叶红外光谱仪,美国;DAWN 多角度激光光散射仪,美国Wyatt公司;Maetersizer 200型激光粒度分析仪、XRD-6100型X-射线衍射仪,日本岛津;PQ001型低场核磁共振分析仪,上海纽迈电子科技有限公司;Lumions Fusion FD 型X 线机,西门子医疗系统有限公司。
1.2 实验方法
1.2.1 干热改性工艺
黄原胶粉末均匀平铺于培养皿中,烘箱75 ℃处理成2%的水分含量,控制质量为1.5 g。将培养皿密封放入水浴锅中,90 ℃恒温加热3 h后取出,研碎过筛,恢复水分含量至11%。
1.2.2 黏度和溶解时间的测定
取0.2 g改性黄原胶粉末加入约100 mL蒸馏水中,800 r/min磁力搅拌至完全溶解,记录溶解时间。静置1 h后使用旋转黏度计测定黏度,单位mPa·s。
1.2.3 干热改性黄原胶的结构表征
1.2.3.1 傅里叶红外光谱测定
取2 mg样品加100 mg KBr研磨,压片制样,使用Nicolet is10型傅里叶红外光谱仪进行波段扫描,扫描波数为4 000~400 cm-1[21]。
1.2.3.2 粒度测定
使用Maetersizer 200型激光粒度分析仪进行样品粒度分布和平均粒度的测定和分析,样品重复3次。将微量样品洒入分散介质中,启动循环泵将样品充分分散并进行测试,光源照射样品颗粒发生折射,将信号转化成数据输出。分散介质为无水乙醇,折射率为1.36;样品折射率设定为1.52,吸收率0.01;遮光度10%左右。
1.2.3.3 分子质量测定
使用美国Wyatt公司的DAWN型多角度激光光散射仪进行测定。将样品用流动相配制成0.2 mg/mL浓度的溶液,搅拌溶解,静置过夜,过0.22 μm滤膜后进样200 μL,每个样品测3次,进样前用流动相洗针,使用ASTRA进行数据处理。测定条件:色谱柱Shodex OHpak SB-805HQ型;流动相0.1 mol/L NaNO3溶液;柱温40 ℃;流速0.6 mL/min[22]。
1.2.3.4 结晶度测定
将样品压片,采用XRD-6100型X-射线衍射仪进行扫描测定[23]。测定条件:Cu靶,管压40 kV,管流30 mA,扫描步长0.02°,扫描角速度6°/min,2°角范围10~80,温度25 ℃。
1.2.4 干热改性黄原胶(dry heat modified xanthan gum,DXG)的复配方法
将不同组合的DXG和预糊化淀粉与麦芽糊精粉末混合复配,使复配总量为2.2 g,加入100 mL蒸馏水手动搅拌溶解,记录溶解时间和表观黏度(30 r/min,3号转子,25 ℃下测定)。从多组复配物中选出3组,利用低场核磁共振分析仪通过水分分布分析找出最适的复配方案。
1.2.5 复配增稠剂的吞咽造影分析
将黄原胶、预糊化淀粉和麦芽糊精最适复配物(1份为2.2 g)加入100 mL钡餐溶液(钡餐浓度为35%)中,分为3个不同梯度浓度:稀薄型(0.7份)、花蜜型(1份)和蜂蜜型(1.3份)[24],搅拌溶解均匀,形成黏稠型钡餐。在X线透视下,患者依次食用3种黏稠度液体,观察患者在进食时会厌及梨状窝是否有残留、误吸等症状。
2 结果与分析
2.1 干热改性黄原胶的黏度和溶解时间
经90 ℃恒温加热3 h得到干热改性黄原胶,对其黏度和溶解速度进行了测定,结果如表1所示。
表1 质量浓度为2 g/L的XG与DXG的黏度和溶解时间
Table 1 2 g/L concentration of XG and DXG viscosity and dissolution time

样品溶解时间/min黏度/(mPa·s)XG12±1.13220±5.51DXG3.5±0.25510±5.03倍数3.4倍2.3倍
由表1可知,质量浓度为2 g/L的DXG溶液,其黏度为510 mPa·s,溶解时间约为3.5 min, 与质量浓度为2 g/L XG溶液相比,DXG的黏度和溶解速度分别提高了2.3倍和3.4倍,该结果显示改性后黄原胶的黏度和速溶性均得到明显提高。
2.2 干热改性黄原胶结构表征
2.2.1 傅里叶红外光谱分析
干热改性黄原胶与黄原胶的红外光谱图如图1所示。
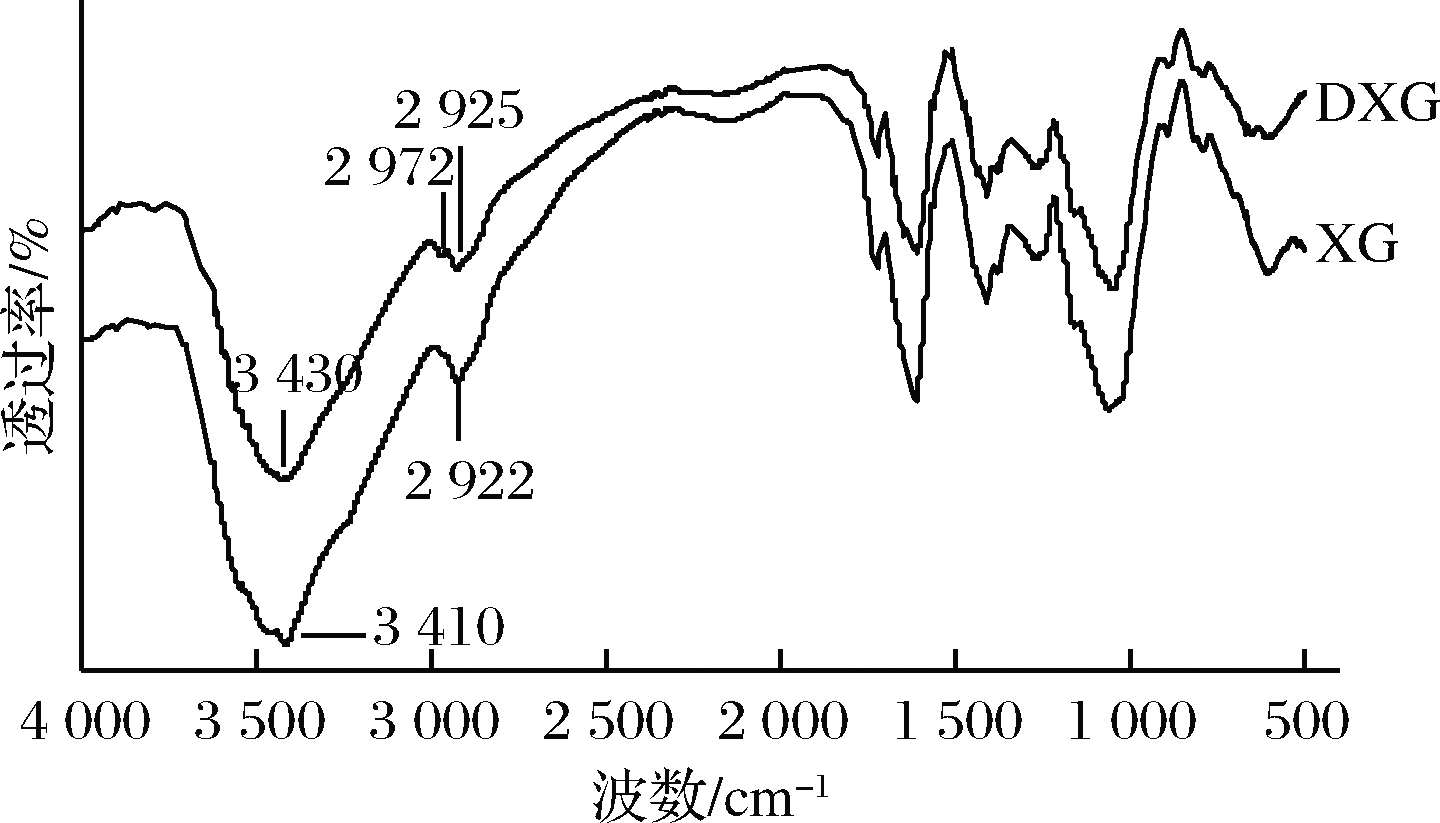
图1 XG与DXG的红外光谱图
Fig.1 XG and DXG infrared spectrum
由图1可知,3 410 cm-1为XG的—OH伸缩振动吸收峰,而DXG对应的峰在3 430 cm-1处,根据AHUJA等[25]的报导,吸收峰向高波数位移说明分子间氢键作用力减弱,氢键等分子间作用力越小,说明聚合物的溶解能力越好[26],该结果与文献[27]研究结果相似。XG在2 922 cm-1处为分子中—C—H的伸缩振动吸收峰,DXG对应的吸收峰在2 925 cm-1处,且DXG在2 972 cm-1处增加了一段短而宽的小峰,此处为烷基的吸收峰,推测高温使黄原胶分子链上的羟基与羧基发生交联反应;文献表明[28-29],淀粉与黄原胶在干热过程中发生交联,本研究中,黄原胶本身含有羟基和羧基,说明发生交联反应。
2.2.2 粒度分析
如图2所示, XG和DXG的粒度曲线图相似,粒度均在100 μm左右。XG的粒度为d(0.1)=26.617 μm,d(0.5)=93.708 μm,d(0.9)=199.354 μm,黄原胶的粒度与LEE测定的粒度相似[30],DXG的粒度为d(0.1)=29.575 μm,d(0.5)=96.043 μm,d(0.9)=214.427 μm,DXG的粒度比XG的粒度增大,DXG的平均粒度比XG增大了2.335 μm,LI等[31]发现淀粉与黄原胶混合干热后的粒度增大,说明两者发生了交联。通过粒度分析验证干热条件可以使黄原胶发生交联,但DXG比XG的粒度增加不到3 μm,反应程度较小。
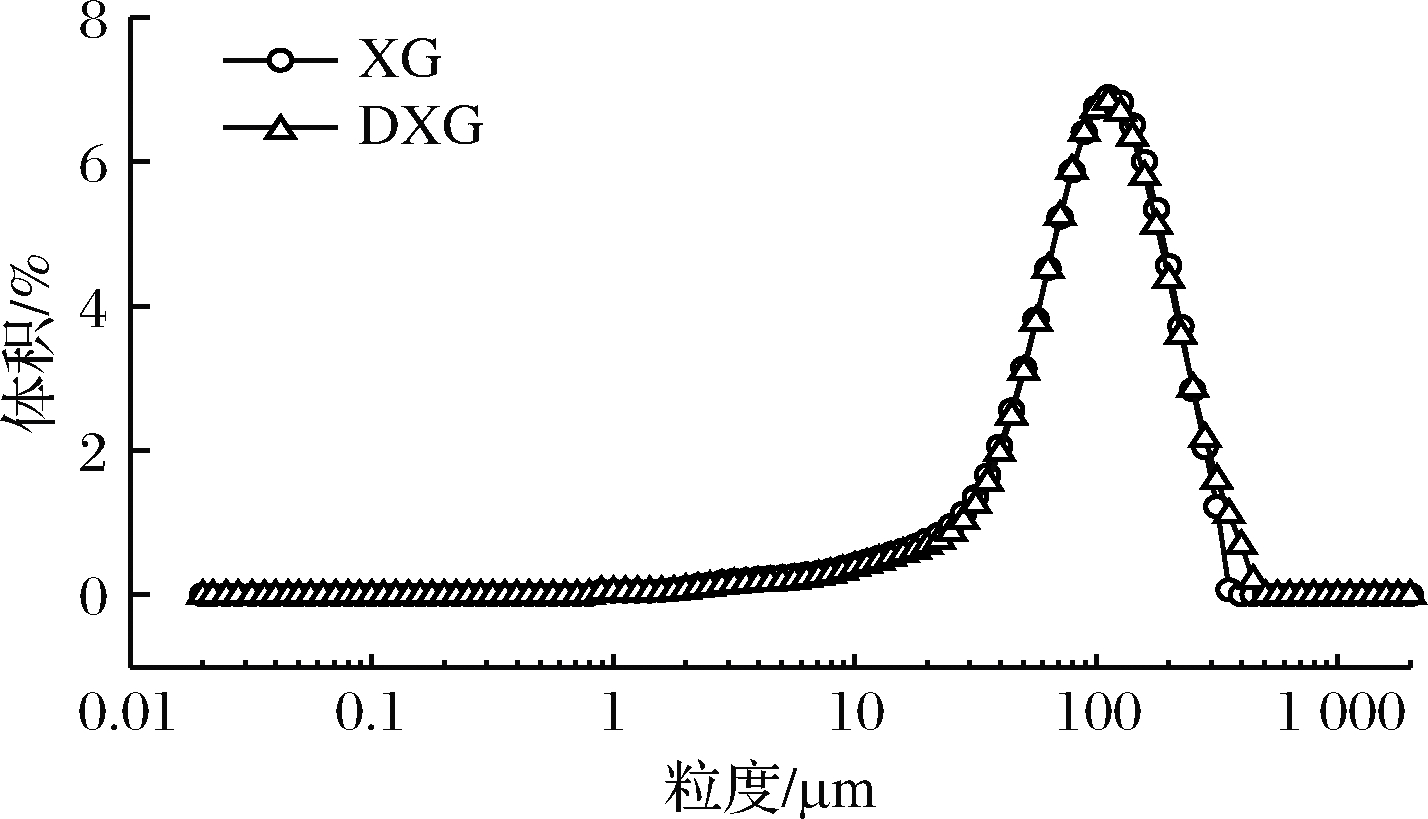
图2 XG与DXG的粒度
Fig.2 Granularity of XG and DXG
2.2.3 分子质量分析
运用尺寸排阻色谱结合多角度激光光散射法测定的黄原胶及干热改性黄原胶的重均分子质量Mw和分子质量分布的图谱和数据如图3和表2所示。由图3可知,XG和DXG的分子质量分布都较窄,没有明显的杂峰,说明分子质量分布较小;保留时间越小,代表样品的分子质量越大,保留时间在17 min左右XG和DXG都出现分子质量的吸收峰,说明XG和DXG的分子质量较大。由图3不能明显看出两者的区别,结合表2中的数据可知,XG的分子质量为5.725×106,DXG的分子质量为6.403×106,改性黄原胶的分子质量相比黄原胶增大,但两者相差不大,主要原因为黄原胶的干热反应并没有加入其他反应物质,黄原胶分子之间只发生了少量的交联,该结果与粒度分析结果相呼应。Mw/Mn为聚合物的分子质量分布,据文献[32]表明,分子质量分布越小,聚合物具有的不同分子质量片段越少,DXG的分子质量分布降低,说明该最优条件下的干热反应并没有发生较大程度的降解;Rg/Rh为均方回转半径与流体力学半径的比值,它随着链段密度的增大而减小[33],DXG的Rg/Rh减小,即改性后的黄原胶发生一定程度的聚合,密度增大,结构紧凑。黄原胶分子质量的增大以及更紧密的网络结构,使其在溶液中具有更长的分子链和更多分子链缠结点,溶液流动性变差,因此溶液黏度增大。

a-XG;b-DXG
图3 XG和DXG的分子质量图谱
Fig.3 Molecular weight profile of XG and DXG
表2 分子质量测定结果
Table 2 Molecular weight determination results

样品Mw×10-6/(g·mol-1)Mw/MnRg/nmRh/nmRg/RhXG5.725±0.081.269±0.1196.2±0.01112.556±0.031.743DXG6.403±0.061.046±0.09186.9±0.02125.283±0.021.492
2.2.4 结晶度分析
由图4可知,黄原胶与干热改性黄原胶的衍射特征峰相似,在2θ=20.4°处都有明显的特征峰,整体表现为非晶态物质[34],改性后的黄原胶没有发生较大的变化。XG有少量结晶区,如2θ=31.46°和75.14°,而在DXG的衍射曲线中这2个峰消失。有文献表明[35],结晶区的分子结构比较紧密,溶剂分子难以渗入,溶解缓慢,而无定型区溶解较快。对比XG和DXG的无定型区和结晶区,DXG的结晶区较少,计算两者的结晶度,XG为26.17%,DXG为19.97%,XG的结晶度较大,所以DXG相较XG具有较好的溶解能力。
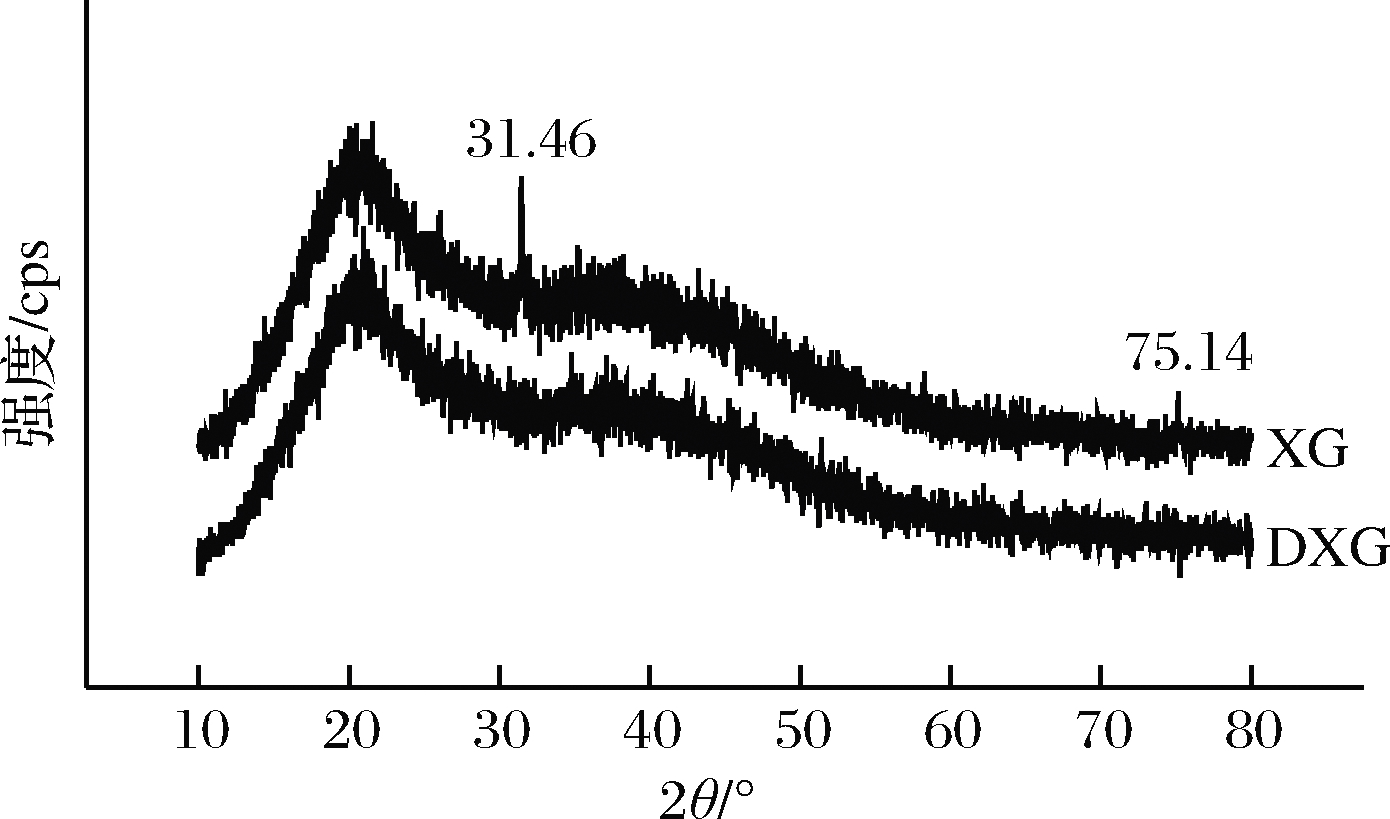
图4 XG和DXG的X-射线衍射图谱
Fig.4 XG and DXG X-ray diffraction patterns
多数文献表明,淀粉与黄原胶共同干热处理,淀粉分子上的羟基可与黄原胶分子上的羧基发生交联,从而提高淀粉的理化性质,获得更广泛的应用领域。黄原胶分子链上有较多羟基基团和羧基基团,在适当的干热条件下,黄原胶分子链上的羟基和羧基间也可发生交联反应,使粒径增大,傅里叶红外光谱和粒径分析证明了这一点;尺寸排阻色谱结合多角度激光光散射法说明多个黄原胶分子链相互连接,分子质量增大,且网络结构更紧密,引起黏度的增大;干热改性后黄原胶结晶区减弱,更容易在水中溶解。综合以上验证说明干热改性黄原胶可以改善其理化性质。
2.3 干热改性黄原胶的复配
患有吞咽障碍的老年人不仅正常饮食有困难,还极有可能引发肺炎等呼吸系统疾病,甚至危及生命,进食增稠流体食品是治疗吞咽障碍的重要方法。根据老年吞咽障碍患者对增稠饮品的要求,黏度需要达到花蜜型[36],溶解时间越快越好。
本实验中2 g/L的干热改性黄原胶手动搅拌需要15 min左右溶解,黏度只有500 mPa·s(25 ℃,30 r/min),干热改性黄原胶作为增稠剂还不足以达到速食的需求,因此需要对其进行复配。
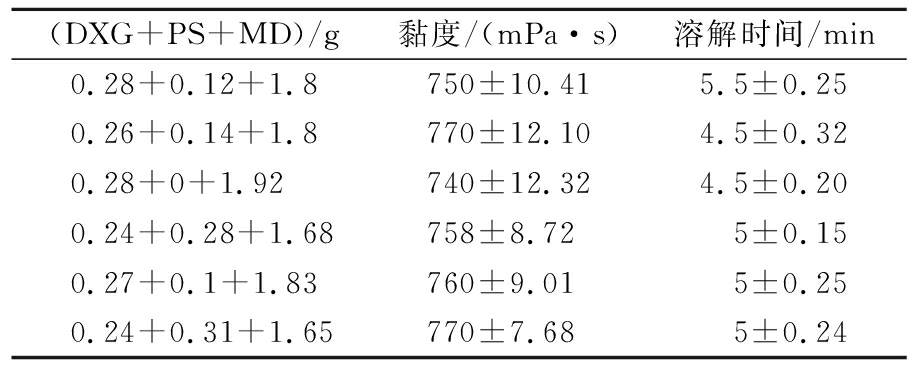
将DXG与预糊化淀粉(pre-gelatinized starch,PS)和麦芽糊精(maltodextrin,MD)复配,如表3所示,以总复配物2.2 g为共同点,选出6组不同组合的复配物加入100 mL水中,手动搅拌溶解,25 ℃ 下测定黏度(30 r/min),所有复配物的溶解时间都在5 min 左右,黏度在750 mPa·s左右。
从表3中选出3种较好的复配组合,为0.24 g DXG+0.31 g PS+1.65 g MD、0.26 g DXG+0.14 g PS+1.8 g MD和0.27 g DXG+0.1 g PS+1.83 g MD,分别加入100 mL吞咽造影剂钡餐中,进行低场核磁共振检测,分析其水分分布情况,判断哪一种复配组合的溶液更稳定(以不添加复配增稠剂的钡餐为空白组),如图5所示。通过弛豫时间T2的大小判断溶液体系中的物质与水分子的结合程度,反映溶液的稳定性,T2越小,代表结合越紧密,溶液的稳定性越好[37]。如图5所示,T2在1 000 ms附近的一段区域对应游离水的弛豫时间,3组加复配物的钡餐溶液都比空白组的T2小,且信号强度降低,说明溶液中的一部分游离水被大分子束缚,流动性降低。在100 ms附近为结合水与游离水的混合区域;信号在20 ms左右对应的是结合水,该信号中没有空白组,且以0.26 g DXG+0.14 g PS+1.8 g MD复配组合的弛豫时间最短,说明加入复配物的溶液与水分子形成了氢键等作用力。综合考虑,0.26 g DXG+0.14 g PS+1.8 g MD组合最好,复配比为m(干热改性黄原胶)∶m(预糊化淀粉)∶m(麦芽糊精)=1.86∶1∶12.86,加入100 mL钡餐溶液中,手动搅拌溶解时间为5 min,黏度为720 mPa·s。
表3 不同复配组合的黏度和溶解时间
Table 3 Viscosity and dissolution time of different compounding combinations
(DXG+PS+MD)/g黏度/(mPa·s)溶解时间/min0.28+0.12+1.8750±10.415.5±0.250.26+0.14+1.8770±12.104.5±0.320.28+0+1.92740±12.324.5±0.200.24+0.28+1.68758±8.72 5±0.150.27+0.1+1.83760±9.01 5±0.250.24+0.31+1.65770±7.68 5±0.24
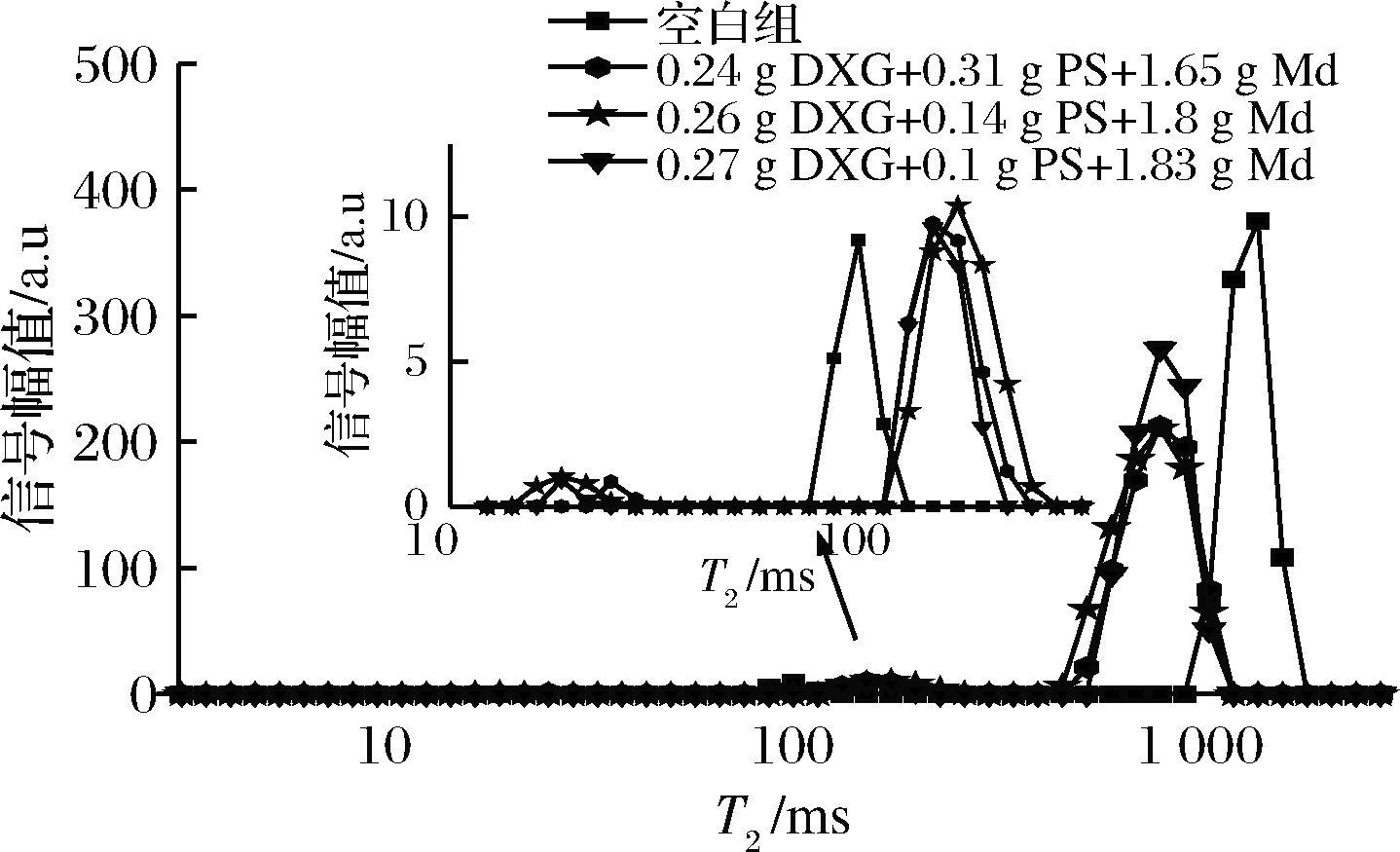
图5 复配增稠溶液的低场核磁共振图
Fig.5 Low-field nuclear magnetic resonance diagram of the compound thickened solution
以花蜜型黏度为准,将最佳复配组合配方与市售的国产奥特顺咽、鹤鸿春以及日产莎罗雅牌增稠剂进行速溶性、黏度以及价格对比,结果如表4所示。将增稠剂加入100 mL钡餐溶液中,手动搅拌溶解,黏度测定温度25 ℃,转速30 r/min。
表4 不同增稠剂性能对比
Table 4 Performance comparison of different thickeners

品牌黏度/(mPa·s)溶解时间/min价格/(元·份-1)奥特顺咽680±18.5628±1.152.80鹤鸿春 532±15.3332±2.302.00莎罗雅 795±9.31 6±0.753.13最佳配方720±10.12 5±0.361.00
如表4所示,本实验得到的最佳配方溶解性最优,价格最低,且黏度并不逊色于其他国产品牌,各方面性能较好,在复配增稠产品中有一定潜在使用价值。
2.4 吞咽造影分析
吞咽造影剂钡餐在造影图像中可呈现黑色影像,有利于观察吞咽过程是否产生误吸或残留。误吸即流体在被吞咽时经口吞入,由食道咽下时发生少量流入气管的现象[38];误吸易导致气管阻塞及剧烈咳呛,食物残留不利于下一次吞咽,易引起咽部发生病变等。将最优复配比为m(干热改性黄原胶)∶m(预糊化淀粉)∶m(麦芽糊精)=1.86∶1∶12.86的组合用于吞咽造影。
在X线机透视下观察病人吞咽造影剂的情况,并通过从侧位或前后正位成像对吞咽的不同阶段进行评估,判断在吞咽过程中有无误吸等情况。
图6-a和图6-b分别为吞咽时的正面与侧向造影图像,两图可观察到在会厌和梨状窝处造影剂残留;图6-c和图6-d分别表示添加食品增稠剂与未添加食品增稠剂的吞咽过程,图6-c显示吞咽比较顺畅,而图6-d表明发生明显误吸现象,说明伴有食品增稠剂的钡餐比较黏稠,大多自由水被束缚在溶液中,在吞咽时流体内物质相互牵引,不容易分散,从而能够直接由食道吞入,而没有添加增稠剂的钡餐为稀薄型流体,黏度很小,由食道往下吞咽过程中流体易分散,难以正常吞咽,容易误吸入气管;图6-e和图6-f分别为添加增稠剂和未添加增稠剂的钡餐吞咽后残留状况,未添加增稠剂的钡餐吞咽后会厌有较多残留,而添加了增稠剂的钡餐因溶液具有凝胶特性(弹性),增稠剂具有润滑作用,吞咽时不易残留物质[39]。

a~b-分别为正面和侧面会厌和梨状窝位置;c~d-分别为添加增稠剂和未添加增稠剂的吞咽状况;e~f:分别为添加增稠剂和未添加增稠剂的吞咽后钡餐残留状况
图6 添加复配增稠剂与不添加增稠剂的吞咽造影图像
Fig.6 Swallowing contrast images with and without added thickener
3 结论
(1)质量浓度为2 g/L的干热改性黄原胶溶液的黏度为510 mPa·s,溶解时间约3.5 min,比黄原胶黏度高290 mPa·s,溶解时间缩短8.5 min,黏度和速溶性明显提高。
(2)红外光谱、粒度、分子质量和X-射线衍射等结构表征验证了干热改性黄原胶发生交联,粒径和分子质量增大,黏度提高,干热改性后黄原胶结晶区减弱,速溶性提高。
(3)将改性黄原胶与预糊化淀粉和麦芽糊精以质量比1.86∶1∶12.86进行复配,于100 mL吞咽造影剂钡餐中,黏度达720 mPa·s,且手动搅拌5 min即可溶解,相比其他市售增稠剂其黏度和速溶性都占优势。吞咽造影结果显示添加复配增稠的造影剂,吞咽更顺畅,不易发生误吸,可有效减缓吞咽功能障碍的问题。
(4)本改性复配产品有望成为一种价格低、安全健康、制备工艺简单的可替代型吞咽辅助剂和增稠剂。
[1] 陈建设, 吕治宏.老年饮食障碍与老年食品:食品工业的挑战与机遇[J].食品科学,2015,36(21):310-315.
CHEN J S, LYU Z H, Eating disorders of elderly:Challenges and opportunities of food industry[J].Food Science, 2015,36 (21):310-315.
[2] 韩维嘉, 孙建琴, 易青, 等.上海地区养护机构老年人吞咽障碍及营养风险调查研究[J].老年医学与保健, 2012, 18(3):170-172.
HAN W J, SUN J Q, YI Q, et al.Investigation of dysphagia and nutrition risk in the elderly from nursing home in Shanghai[J].Geriatrics & Health Care, 2012, 18(3):170-172.
[3] MACKLEY M R, TOCK C, ANTHONY R, et al.The rheology and processing behavior of starch and gum-based dysphagia thickeners[J].Journal of Rheology, 2013, 57(6):1 533.
[4] JANG H Y, ZHANG K, CHON B H, et al.Enhanced oil recovery performance and viscosity characteristics of polysaccharide xanthan gum solution[J].Journal of Industrial and Engineering Chemistry, 2015, 21:741-745.
[5] IMAD A F, SANDRA E H, JOHN R M, et al.Water-dispersible xanthan gum containing composition:EP 1833904 B1[P].2010-04-21.
[6] 旷勇, 汪和平, 张世寅, 等.一种油水两溶型迷迭香抗氧化剂的制备方法:中国, CN201510830192.3[P].2016-04-20.
KUANG Y, WANG H P, ZHANG S Y, et al.Preparation method of oil-soluble water-soluble type rosemary antioxidant:China, CN201510830192.3[P].2016-04-20.
[7] BERNARD V.Readily dispersed/dissolved porous biopolymer granules:US, 5003060[P].1991-03-26.
[8] LIU K, HAO Y C, CHEN Y, et al.Effects of dry heat treatment on the structure and physicochemical properties of waxy potato starch[J].International Journal of Biological Macromolecules, 2019, 132:1 044-1 050.
[9] YZA B, MLA B, XYA B, et al. Impacts of guar and xanthan gums on pasting and gel properties of high-amylose corn starches[J]. International Journal of Biological Macromolecules, 2020, 146:1 060-1 068.
[10] 汝远, 王蕾, 周君, 等.干热处理对玉米淀粉性质的影响[J].食品工业科技, 2015(16):140-143.
RU Y, WANG L, ZHOU J, et al.Effect of dry heating on properties of corn starch[J].Science and Technology of Food Industry, 2015(16):140-143.
[11] 李敏. 魔芋葡甘露聚糖结肠靶向给药系统的构建及体外释放研究[D].南宁:广西大学, 2013.
LI M.The construction of konjac glucomannan colon specific drug delivery system and in vitro evaluation[D].Nanning:Guangxi University, 2013.
[12] 王凯.淀粉与黄原胶、果胶共混干热改性研究[D].广州:华南理工大学, 2011.
WANG K.Study on dry heating treatment of starch and xanthan gum/pectin blends[D].Guangzhou:South China University of Technology, 2011.
[13] SUN Q, SI F, XIONG L, et al.Effect of dry heating with ionic gums on physicochemical properties of starch[J].Food Chemistry, 2013, 136(3-4):1 421-1 425.
[14] 邱超, 姬娜, 李晓静,等.干热处理对马铃薯淀粉—离子胶混合物理化性质的影响[J].粮油食品科技, 2015(3):11-15.
QIU C, JI N, LI X J, et al.Effect of dry heating on physicochemical properties of potato starch-ionic gum mixture[J].Science and Technology of Cereals, Oils and Foods, 2015(3):11-15.
[15] BAK J H, YOO B.Intrinsic viscosity of binary gum mixtures with xanthan gum and guar gum:Effect of NaCl, sucrose, and pH[J].International Journal of Biological Macromolecules, 2018, 111:77-81.
[16] ABBASZADEH A, MACNAUGHTAN W, SWORN G, et al.New insights into xanthan synergistic interactions with konjac glucomannan:A novel interaction mechanism proposal[J].Carbohydrate Polymers, 2016, 144:168-177.
[17] KURT A, TOKER O S, TORNUK F.Effect of xanthan and locust bean gum synergistic interaction on characteristics of biodegradable edible film[J].International Journal of Biological Macromolecules, 2017, 102:1 035-1 044.
[18] 张隋鑫,曹勇,许秀颖,等.预糊化淀粉的制备、性质及应用[J].食品科技, 2019, 44(3):257-260.
ZHANG S X, CAO Y, XU X Y, et al.Production, properties and applications of pre-gelatinazed starch[J].Food Science and Technology, 2019, 44(3):257-260.
[19] 张晶,刘亚伟,方宏兵.修饰麦芽糊精在食品工业中的应用[J].食品工业科技, 2010, 31(10):426-429.
ZHANG J, LIU Y W, FANG H B.Application of modified maltdextrin in food industry[J].Science and Technology of Food Industry, 2010, 31(10):426-429
[20] MASUM A K M, CHANDRAPALA J, ADHIKARI B, et al.Effect of lactose-to-maltodextrin ratio on emulsion stability and physicochemical properties of spray-dried infant milk formula powders[J].Journal of Food Engineering, 2019, 254:34-41.
[21] YAHOUM M M, MOULAI-MOSTEFA N, CERF D L.Synthesis, physicochemical, structural and rheological characterizations of carboxymethyl xanthan derivatives[J].Carbohydrate Polymers, 2016:267-275.
[22] CHE Y J, TAN Y, CAO J, et al.A study of aggregation behavior of a sulfobetaine copolymer in dilute solution[J].Journal of Polymer Research, 2010, 17(4):557-566.
[23] LI Y, ZHANG H, SHOEMAKER C F, et al.Effect of dry heat treatment with xanthan on waxy rice starch[J].Carbohydr Polym, 2013, 92(2):1 647-1 652.
[24] 钟磊, 吴柳拿, 周烈,等. 吞咽障碍者增稠流体食品流变学研究进展[J]. 食品科学, 2018, 39(1):313-319.
ZHONG L, WU L N, ZHOU L, et al. Progress in rheology of thickened liquid foods for dysphagic patients[J]. Food science, 2018, 39(1): 313-319.
[25] AHUJA M, KUMAR A, SINGH K.Synthesis, characterization and in vitro release behavior of carboxymethyl xanthan[J].International Journal of Biological Macromolecules, 2012, 51:1 086-1 090.
[26] 李煜,付晓婷,许加超,等.干热处理不同时间对琼胶与β-环糊精复配物理化性质的影响[J].食品工业科技, 2018, 39(19):40-45.
LI Y, FU X T, XU J C, et al.Effect of different dry-heating time on physicochemical properties of agar/β-cyclodextrin mixture[J].Science and Technology of Food Industry, 2018, 39(19):40-45.
[27] 汝远.热处理对玉米淀粉结构和性质的影响[D].泰安:山东农业大学,2015:36-37.
RU Y.Effect of heat treatment on structure and properties of corn starch[D].Taian:Shandong Agricultural University, 2015:36-37.
[28] 王凯, 高群玉.木薯淀粉与黄原胶共混干热改性研究[J].食品工业科技, 2011, 32(7):75-78.
WANG K, GAO Q Y.Study on dry heating treatment of starch and xanthan blend[J].Science and Technology of Food Industry, 2011, 32(7):75-78.
[29] LIM H S, BEMILLER J N, LIM S T.Effect of dry heating with ionic gums at controlled pH on starch paste viscosity[J].Cereal Chemistry, 2003, 80(2):198-202.
[30] LEE H, YOO B.Agglomerated xanthan gum powder used as a food thickener:Effect of sugar binders on physical, microstructural, and rheological properties[J].Powder Technology, 2020, 362:301-306.
[31] LI Y, ZHANG H, SHOEMAKER C F, et al.Effect of dry heat treatment with xanthan on waxy rice starch[J].Carbohydrate Polymers, 2013, 92(2):1 647-1 652.
[32] 李彦杰.黄原胶分子的辐射修饰、产物特征及功能特性研究[D].北京:中国农业科学院,2011:23-24.
LI Y J.Study on radiation modification of xanthan gum molecularand its product features and functional characteristics[D].Beijing:Chinese Academy of Agricultural Sciences, 2011:23-24.
[33] 王小金.黄原胶的化学改性与性能研究[D].济南:山东大学,2012:22-23.
WANG X J.Synthesis and properties of modified xanthan gum[D].Jinan:Shandong University, 2012:22-23.
[34] PANDEY S, MISHRA S B.Graft copolymerization of ethylacrylate onto xanthan gum, using potassium peroxydisulfate as an initiator[J].International Journal of Biological Macromolecules, 2011, 49(4):530-535.
[35] SU L, JI W K, LAN W Z, et al.Chemical modification of xanthan gum to increase dissolution rate[J].Carbohydrate Polymers, 2003, 53:497-499.
[36] 吴君波,王珂,杨光,等.改善吞咽功能食品增稠剂的研究[J].工业微生物, 2019,49(3):38-45.
WU J B, WANG K, YANG G, et al.Food thickener for improving swallowing function[J].Industrial Microbiology, 2019, 49(3):38-45.
[37] 姚晶, 孟祥晨.大豆水溶性多糖对酸性乳饮料稳定作用的研究[J].中国乳品工业, 2009,37(6):54-61.
YAO J, MENG X C.Stabilization of soybean soluble polysaccharide on acidified milk drinks[J].China Dairy Industry, 2009, 37(6):54-61.
[38] 丁辉. 咽动态造影检查在脑卒中后吞咽障碍的临床应用价值[D].太原:山西医科大学, 2016.
DING H.Clinical application value of video fluoroscopy swallowing study in post-stroke dysphagia[D].Taiyuan:Shanxi Medical University, 2016.
[39] 金挺剑, 邱纪方, 孙炳照.食团黏稠度对连续吞咽过程中舌肌运动的影响[J].神经损伤与功能重建, 2006, 1(3):190-192.
JIN T J, QIU J F, SUN B Z.Influence of bolus consistency on lingual behaviors in sequential swallowing[J].Neural Injury and Functional Reconstruction, 2006, 1(3):190-192.