食品是人类赖以生存的最基本的物质基础,除应具备安全性和营养性外,还应具备色、香、味。当食品中存在对人体有害因素时,人摄入后将导致某些疾病的发生,严重时可能丧命,因此,近年来,食品的质量安全倍受关注。食品合成色素酒石黄和日落黄常用于各类食品中,尤其是饮料中常加入了合成色素,以提高感官、增进食欲。但着色剂并非越多越好,着色剂添加过量时,会对人体产生某些副作用或甚至导致中毒、致癌、死亡。因此,对夏日大量使用的饮料,我国国家标准 GB 2760—2014《食品安全国家标准 食品添加剂使用标准》严格规定,饮料中酒石黄和日落黄的添加量均不得超过 0.10 g/kg。为保障人类的身体健康和生命安全,对饮料中着色剂含量进行研究有着重要意义。近年,国内外对酒石黄和日落黄的检测方法主要有:高效液相色谱法[1-7]、电化学法[8-15]、荧光法[16-17] 及分光光度法[18-21]等。这些方法在酒石黄和日落黄共存时,需采取某些特殊处理方式,如需吸附和分离处理后才能进行各色素的测定。分光光度分析中,当两色素共存时,若吸收峰出现较大重叠(即存在相互干扰)时,也不能进行单一物质的测定,常需采用分离操作或根据吸光度的加和性,采用较繁琐的解联立方程组的办法来求得混合色素的含量[20-21]。本研究中的方法既不采用操作复杂的吸附、分离处理,也不采用复杂的数学处理模式,只需通过控制溶液酸度,便可达到用吸收光谱法同时测定共存的酒石黄和日落黄含量的目的,方法简便、快速,并且迄今未见文献报道。
1 材料与方法
1.1 材料与试剂
酒石黄(tartrazine, TAR)标准物质(纯度 ≥98%,lot:A3J6L1)、日落黄(sunset yellow,SUN)标准物质(纯度 ≥98%,lot:JN1103RA14),北京盛世康普化工技术研究院,北京普析科技有限公司;甲基绿(methyl green, MET)(纯度 99%),上海如吉生物科技发展有限公司;氨丁三醇(Tris,纯度 99%),河南天孚化工有限公司;盐酸(分析纯),重庆川东化工有限公司;超纯水,成都优普超纯水仪制。
饮料样品:佳得乐柠檬味(1#)、美年达香蕉味(2#)、佳得乐橙味(3#)、纤颜苹果味(4#)、芬达橙味(5#),均购自当地超市。
1.2 仪器与设备
U-3010 型紫外-可见分光光度计,日本日立公司;KQ-200VDE 型超声波清洗机,昆山市超声仪器有限公司;pHS-3C型酸度计,上海理达仪器厂。
1.3 标准溶液与试剂溶液的配制
酒石黄标准溶液:准确称取酒石黄标准物质(±0.000 1 g),加水溶解并定容至容量瓶中,配制成534.4 mg/L贮备液,操作液为53.44 mg/L,存于4 ℃冰箱中。日落黄标准溶液:准确称取日落黄标准物质(±0.000 1 g),加水溶解并定容至容量瓶中,配制成452.4 mg/L贮备液,操作液为45.24 mg/L,存于4 ℃冰箱中。甲基绿溶液:653.2 mg/L 水溶液。Tris-HCl 溶液:采用0.20 mol/L Tris 溶液与0.10 mol/L HCl 溶液配制,pH 3.5~9.8。
1.4 样品处理
准确移取各饮料样品30.0 mL,分别置于小烧杯中,在天平上准确称取其质量(±0.000 1 g),45 ℃ 超声处理20 min,加适量水后,再超声10 min,用NH3·H2O 调至中性,再于45 ℃ 超声处理10~15 min,冷至室温后,用水定容至100 mL,即为待测液。
1.5 实验方法
准确移取酒石黄和日落黄标准操作液适量,分别置于10 mL 比色管中,加入pH 9.43 Tris-HCl 溶液1.00 mL,再加653.2 mg/L 甲基绿溶液2.00 mL,用水定容,摇匀,待充分反应15 min 后,在紫外-可见分光光度计上,以各体系的试剂空白作参比,扫描各溶液的吸收光谱,在574 nm 处测定酒石黄-甲基绿体系溶液的吸光度(A),在488 nm 处测定日落黄-甲基绿体系溶液的吸光度(A),最终求得各饮料样品中共存色素——酒石黄和日落黄的含量。
2 结果与分析
2.1 酒石黄体系与日落黄体系的吸收光谱特征
从酒石黄和日落黄的结构式可知,两者均可与甲基绿(三苯甲烷碱性染料)以静电作用生成离子缔合物。
从图1可知,单独的酒石黄溶液和日落黄溶液在可见光区均有较大吸收,最大吸收峰分别位于426 nm(酒石黄)和480 nm(日落黄),曲线1 和曲线4 表明,它们的吸收谱线有一定的重叠,当两色素共存时,因谱线的叠加,互相间有干扰,不能单独进行某一色素的测定。但当加入甲基绿溶液和pH 9.43 Tris-HCl 溶液后,酒石黄与甲基绿反应生成的缔合物在可见光区产生2 个明显的负吸收峰和1 个明显的正吸收峰(曲线3),日落黄与甲基绿反应生成的缔合物在可见光区产生2 个明显的正吸收峰(曲线5)。曲线3 与曲线5 和曲线2比较,均有波移现象,说明酒石黄和日落黄均可与甲基绿反应生成新物质。从曲线3 与曲线5 的比较可知,在Tris-HCl 溶液酸度相同(均为pH 9.43)和甲基绿浓度、用量相同的情况下,酒石黄-甲基绿体系的测定波长为574 nm时,共存物质日落黄不干扰测定,而在652和450 nm处测定,日落黄会有严重干扰;对于日落黄-甲基绿体系,当测定波长为488 nm 时,溶液中共存的酒石黄对其测定无干扰,当测定波长为648 nm 时,酒石黄对其测定存在严重干扰。酒石黄体系和日落黄体系的线性图见图2,吸收光谱特征见表1。可知,当溶液酸度为pH 9.43 时,可在574 nm 测定酒石黄(日落黄不干扰),在488 nm 测定日落黄(酒石黄不干扰)。该方法与已报道的文献[18-21]比较,不需吸附、分离操作,也不用解复杂的方程组,只需控制好溶液酸度,便可在不同波长下分别测定共存色素的含量。
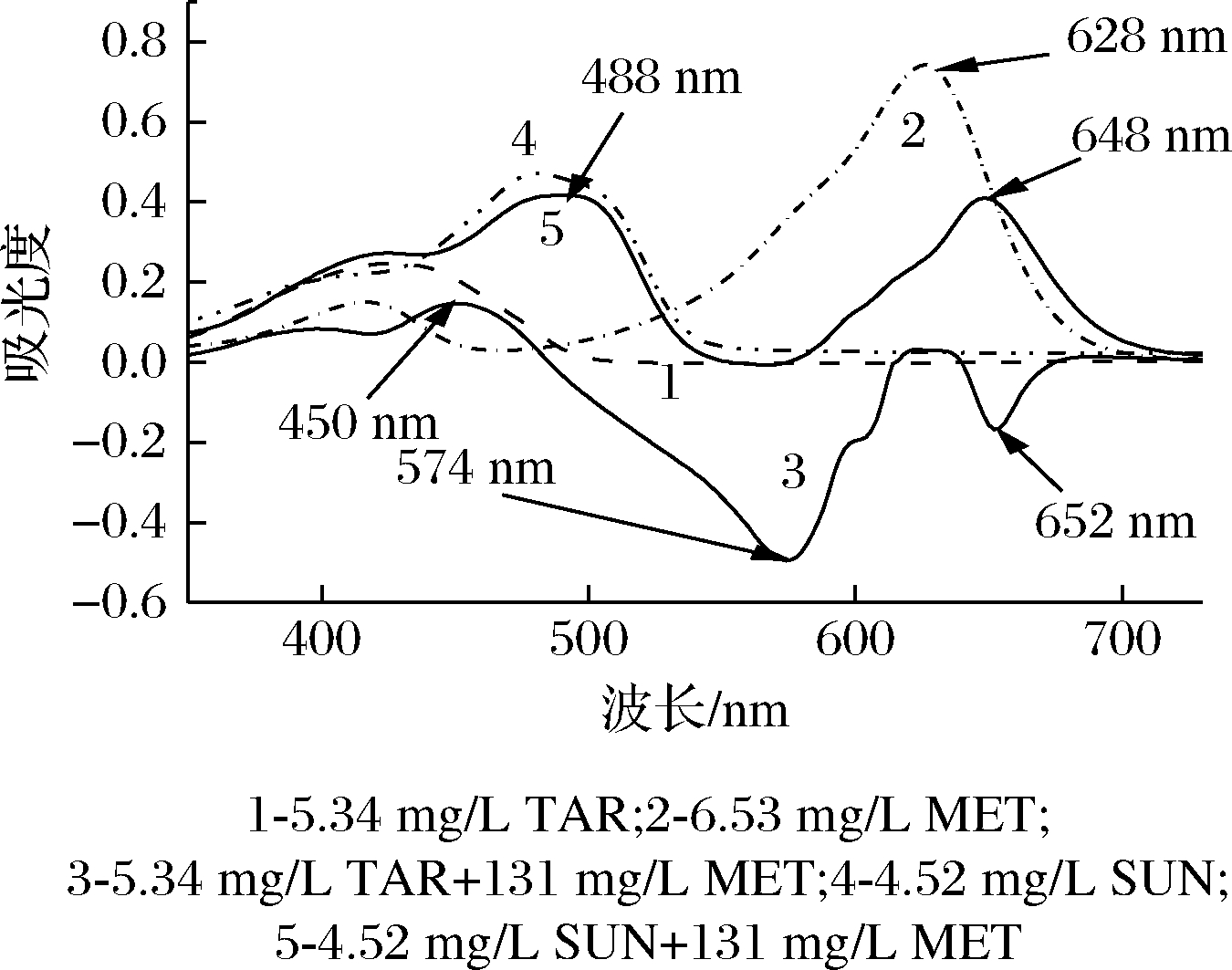
图1 酒石黄和日落黄与甲基绿反应的吸收光谱
Fig.1 Absorption spectra of tartrazine and sunset
yellow reacted with methyl green
表1 酒石黄-甲基绿体系与日落黄-甲基绿体系的
吸收光谱特征
Table 1 Characteristics of absorption spectrum of
tartrazine-methyl green system and sunset
yellow-methyl green system

物质A574A488λAb/nmλF/nm酒石黄--426 (A=0.247)-日落黄--480(A=0.472)-酒石黄+甲基绿(pH 9.43)-0.495-0.018450652,304,242,222日落黄+甲基绿(pH 9.43)-0.0010.417648,490,312,234-
注:λAb为吸光度为正时峰值对应波长;λF为吸光度为负时峰值对应波长
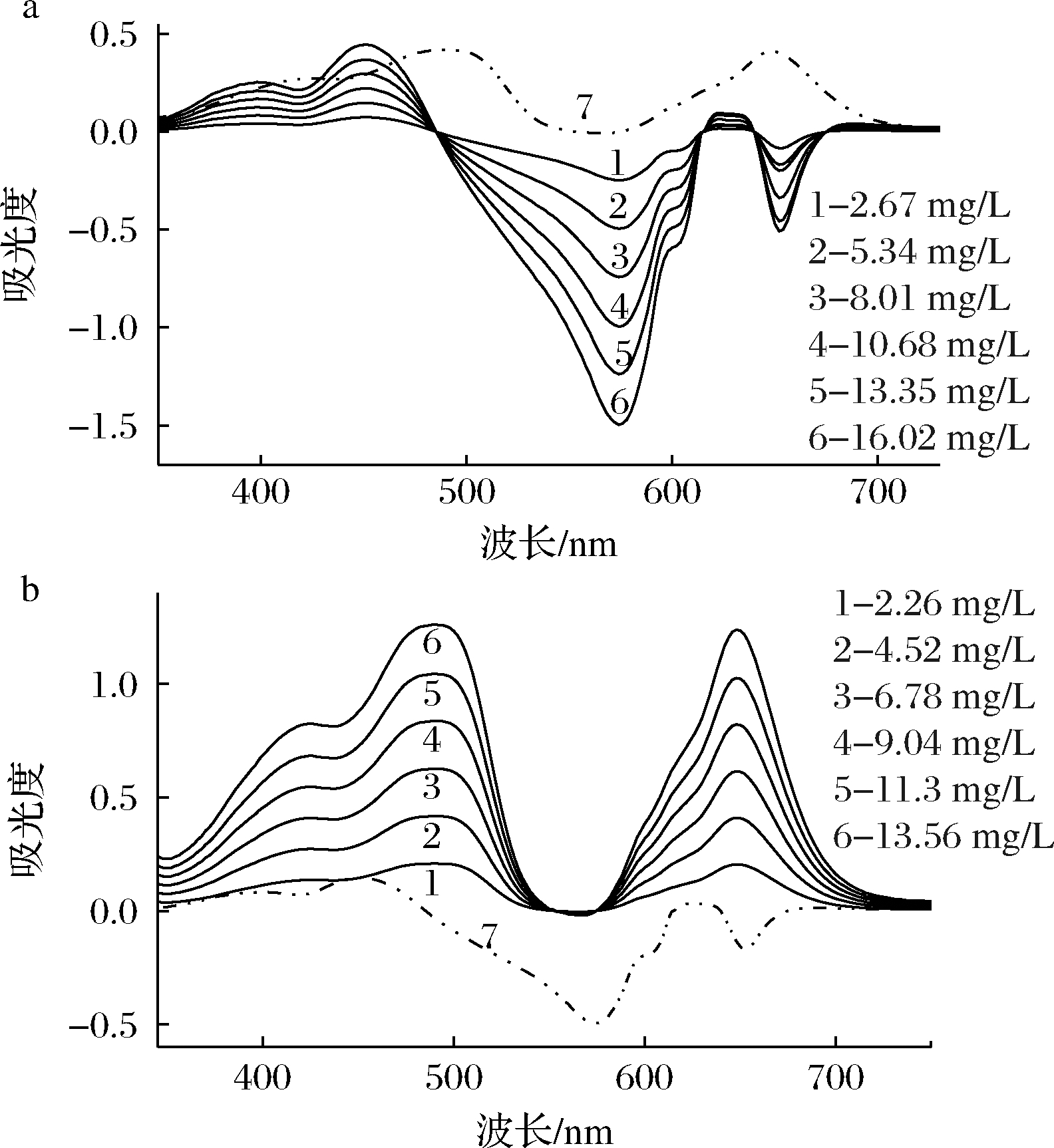
a-酒石黄;b-日落黄
图2 酒石黄、日落黄和甲基绿体系的线性吸收光谱
Fig.2 Linear absorption spectrum of tartrazine and sunset
yellow reacted withd methyl green
注:甲基绿131 mg/L;试剂空白参比
2.2 反应条件
2.2.1 溶液pH 及用量的选择
取酒石黄、日落黄标准操作液1.00 mL,甲基绿溶液2.00 mL,考察了酒石黄-甲基绿体系与日落黄-甲基绿体系pH 3.5~9.8 的Tris-HCl 溶液对吸光度的影响,结果见图3。从图3-a可知,当测定波长为574 nm 时,酒石黄-甲基绿体系pH 4.42~9.43时,随着溶液pH 的增大,体系溶液吸光度绝对值(|A|)逐渐增强,当pH 9.43 时,|A| 达最大,之后逐渐减弱;而日落黄-甲基绿体系随着pH 的增大,|A| 逐渐降低,当pH 9.43 时,|A|= 0.001。
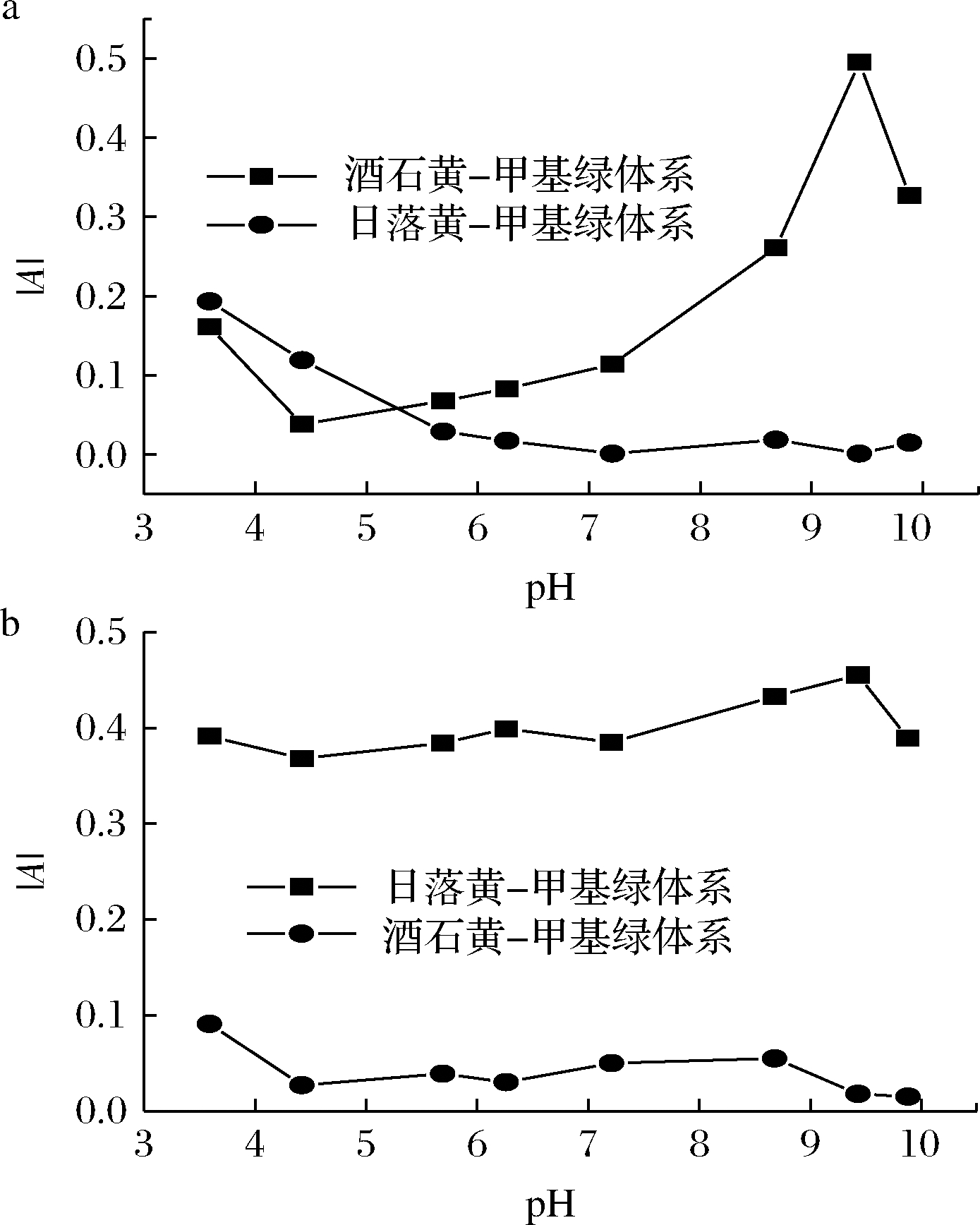
a-574 nm;b-488 nm
图3 溶液pH对不同测定波长下|A|的影响
Fig.3 Effect of solution pH on |A| under different wave length
从图3-b可知,当测定波长为488 nm 时,日落黄-甲基绿体系pH 3.59~9.43时,对|A|的影响均较大,当pH 9.43 时,|A| 达最大,之后有所降低;而酒石黄-甲基绿体系除pH 3.59 外,其余pH 对|A| 影响均不大,当pH 9.43 时,|A|= 0.018。可见,选用pH 9.43 的Tris-HCl 溶液,不仅灵敏度相对最大,而且在574 nm 波长处测定酒石黄,日落黄不干扰;在488 nm 波长处测定日落黄,酒石黄不干扰。故可用控制溶液酸度的办法来消除共存色素-酒石黄和日落黄间的相互干扰,达到分别测定的目的。
同时考察了pH 9.43 Tris-HCl 用量对|A| 的影响,结果见图4,用量为1.00 mL 时,无论在574 nm 测定酒石黄,还是在488 nm 测定日落黄,均有较大灵敏度。实验选择在最佳条件下进行各项试验。
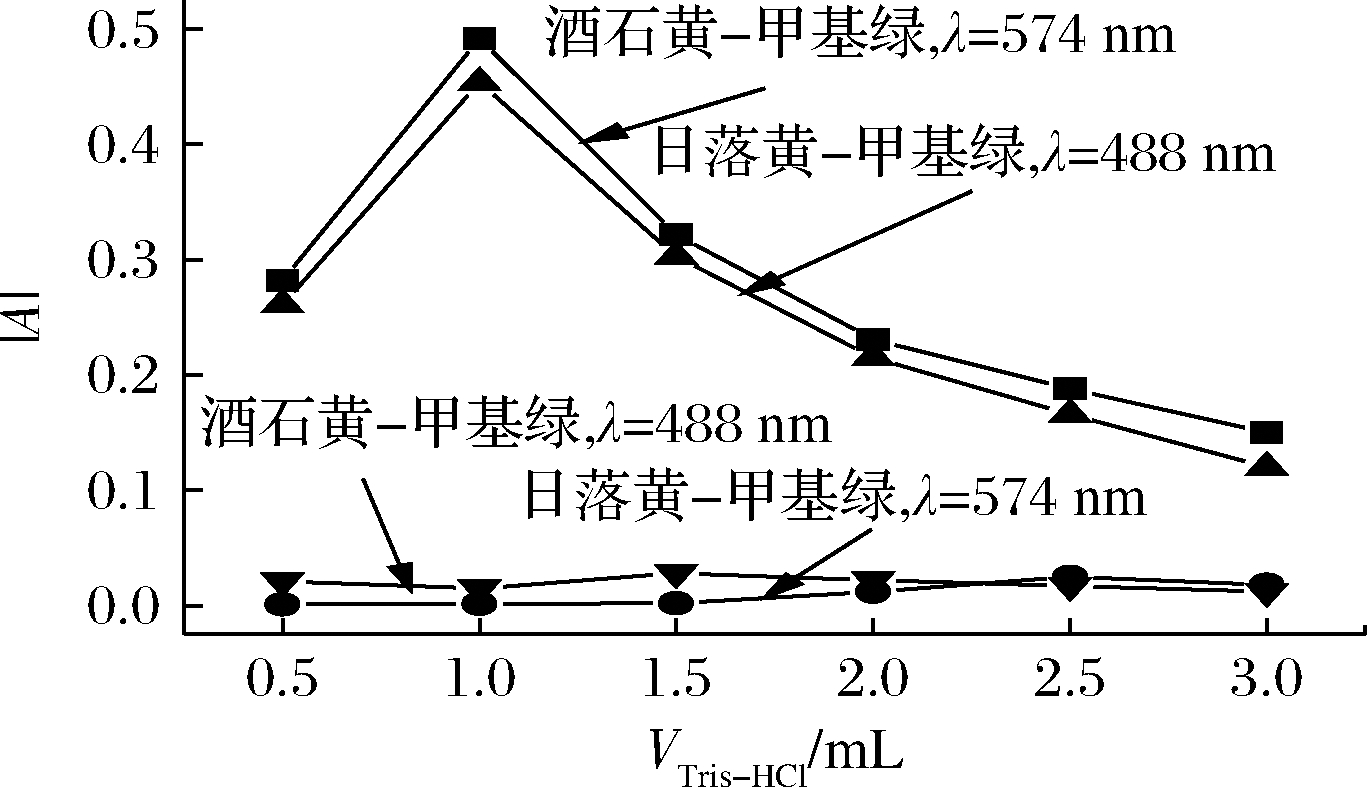
图4 Tris-HCl溶液用量对|A| 的影响
Fig.4 Effect of Tris-HCl buffer on|A|
2.2.2 甲基绿溶液用量的选择
取酒石黄、日落黄标准操作液1.00 mL,pH 9.43 Tris-HCl 溶液1.00 mL,考察了甲基绿溶液(653.2 mg/L)用量对酒石黄体系和日落黄体系|A| 的影响,结果见图5。当测定波长为574 nm 时,甲基绿用量对酒石黄-甲基绿体系的|A| 有较大影响,而对日落黄-甲基绿体系的|A| 基本无影响。当测定波长为488 nm 时,甲基绿用量对日落黄-甲基绿体系的|A| 有较大影响,而对酒石黄-甲基绿体系的|A| 基本无影响。可见,无论在574 nm波长处测定酒石黄还是在488 nm波长处测定日落黄,甲基绿用量为2.00 mL 时,它们均有相对较大的灵敏度,且互不干扰。实验选用甲基绿溶液2.00 mL。
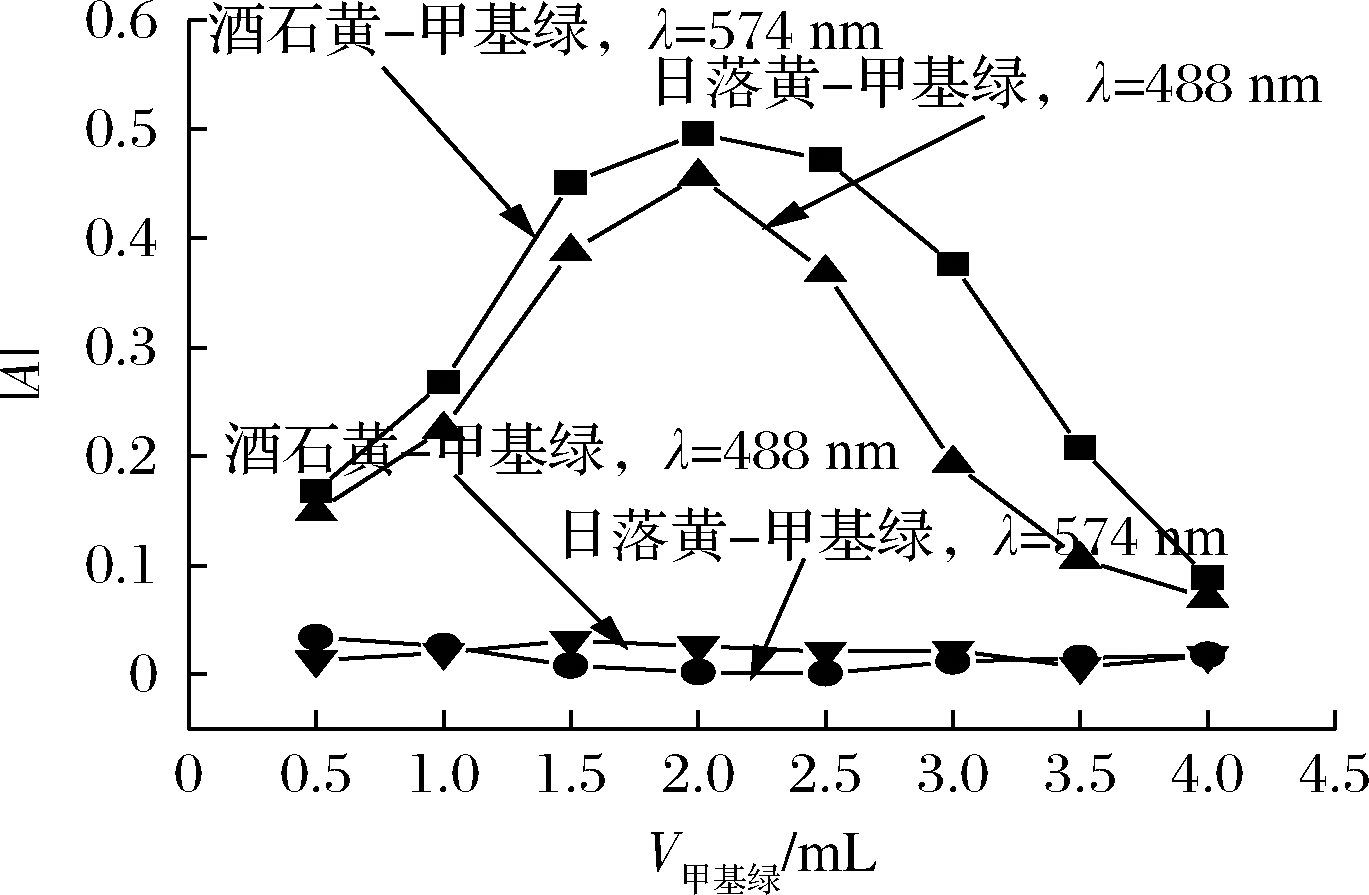
图5 甲基绿用量对|A| 的影响
Fig.5 Effect of methyl green dosage on|A|
2.2.3 反应时间的选择
在前述选定的最佳条件下,考察了酒石黄、日落黄与甲基绿的反应时间对|A| 的影响。结果表明,酒石黄-甲基绿体系与日落黄-甲基绿体系在15 min 内均可反应完全,稳定时间约50 min。两体系均选在15 min 后测定。
2.3 方法学考察
2.3.1 酒石黄和日落黄的标准曲线及灵敏度
分别准确移取酒石黄和日落黄标准操作液0.00、0.50、1.00、1.50、2.00、2.50、3.00 mL,分别置于10 mL 比色管中,加入选定条件的pH 9.43 Tris-HCl 溶液1.00 mL 和甲基绿溶液2.00 mL,用水定容、摇匀,15 min 后,各体系以试剂空白作参比,测定各溶液的吸光度A,作574 nm 处酒石黄的A-ρ 标准曲线和488 nm 处日落黄的A-ρ 标准曲线。标准曲线相关参数见表2可知,该方法有较高灵敏度和较宽线性范围。
表2 酒石黄和日落黄标准曲线相关参数
Table 2 Related parameters of standard curves of tartrazine and sunset yellow

体系测定波长λ/nm线性范围ρ/(mg·L-1)回归方程相关系数r表观摩尔吸光系数κ/[L·(mol·cm)-1]检出限ρ/(mg·L-1)定量限ρ/(mg·kg-1)酒石黄-甲基绿5740.04~16.0A574=0.000 597 8-0.093 35 ρ 0.999 94.90×1040.0331.80日落黄-甲基绿4880.04~13.6A488=-0.000 461 1+0.092 47 ρ0.999 94.19×1040.0281.51
2.3.2 方法的选择性
按实验方法,考察了酒石黄-甲基绿体系在574 nm 处测定5.34 mg/L 酒石黄,考察了日落黄-甲基绿体系在488 nm 处测定4.52 mg/L 日落黄,相对误差≤±5%,共存物的影响见表3。结果表明该方法有良好的选择性。
2.3.3 样品测定、准确度及精密度
取1.4中制备好的待测液2.00 mL,按实验方法分析其含量并计算原始饮料中酒石黄和日落黄的含量,同时参考文献方法[21]进行对照试验,见表4。
按样液的配制方法,准确移取30 mL 各饮料样品分别置于各小烧杯中,并称其准确质量(±0.000 1 g),再分别加入一定量的酒石黄或日落黄标准贮备液,并于45 ℃ 超声20 min,后续操作同1.4中样品处理,最后用水定容至100 mL。取该液2.00 mL,按实验方法测定各加标回收量,如表4所示。
表3 共存物质的影响
Table 3 Effect of coexistent substance

共存物质相对误差/%允许倍数TAR体系SUN体系TAR体系SUN体系共存物质相对误差/%允许倍数TAR体系TAR体系SUN体系TAR体系蔗糖1.81.6100100Mg2+3.53.0100100葡萄糖1.5-1.2100100Sr2+3.03.4100100麦芽糖-2.32.8100100Pb2+4.3-3.8100100D-果糖4.23.8100100Ba2+3.6-2.8100100L-亮氨酸3.53.8100100Fe2+-2.53.2100100L-白氨酸-2.8-2.5100100NH+4-3.53.0100100L-赖氨酸3.23.3100100Cl-2.62.3100100L-组氨酸4.44.0100100柠檬酸三钠-3.8-3.25050D-色氨酸-3.63.0100100尿素4.23.55050L-谷氨酸4.24.3100100抗坏血酸3.53.55050D-苏氨酸3.5-3.8100100淀粉4.04.25050甘氨酸4.04.2100100CO2-3-3.22.85050甜蜜素4.3-3.2100100C2O2-44.0-3.35050安赛蜜3.62.8100100苯甲酸4.03.53030K+1.21.6100100山梨酸3.83.83030Na+2.01.8100100Fe3+4.64.21010Ca2+3.0-3.3100100Al3+4.54.41010
表4 市售饮料样品分析结果及回收试验(n=5)
Table 4 Analysis results and recovery test of commercial beverage samples (n=5)
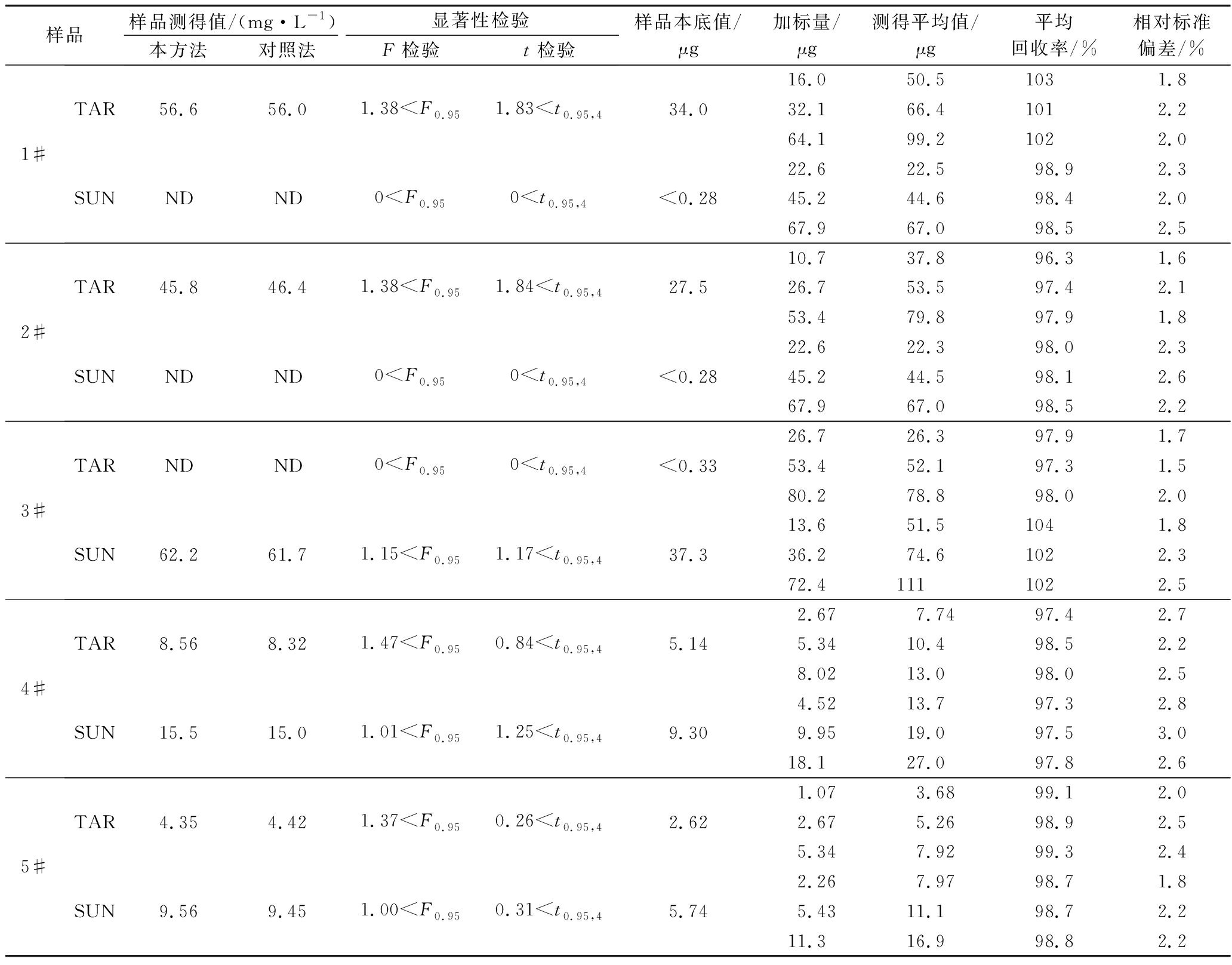
样品样品测得值/(mg·L-1)显著性检验本方法对照法F检验t检验样品本底值/μg加标量/μg测得平均值/μg平均回收率/%相对标准偏差/%1#16.050.5103 1.8TAR56.656.01.38 注:ND 为未检出;样品含量<检出限的按检出限的1/2 计算回收率
3 结论
共存色素酒石黄和日落黄含量的测定,可以用甲基绿作探针,通过控制溶液酸度,选择不同测定波长,达到分别测定共存物中两色素的目的。该方法简便,不需吸附、分离操作,也不用复杂的数学求解,快速,样品处理简单,准确度和精密度满足定量分析要求,并有较高灵敏度和较宽的线性范围,适用于饮料中共存酒石黄和日落黄含量的测定。
[1] LI R,WANG Y,TAN J,et al.Simultaneous determination of synthetic edible pigments in beverages by titania-based RP-HPLC[J].Arabian Journal of Chemistry,2020,13(2):3 875-3 881.
[2] CHEN D M,WU M R,XIE S Y,et al.Determination of tartrazine,lutein,capsanthin,canthaxanthin and β-carotene in animal-derived foods and feeds by HPLC method[J].Journal of Chromatographic Science,2019,57(5):462-468.
[3] 刘剑波,余莲芳,朱明扬,等.固相萃取-高效液相色谱法同时测定蔬菜制品中11种合成着色剂[J].食品研究与开发,2018,39(23):141-146.
LIU J B,YU L F,ZHU M Y,et al.Simultaneous determination of 11 synthetic colorants in vegetable products by solid phase extraction-high performance liquid chromatography[J].Food Research and Development,2018,39(23):141-146.
[4] LI Q,LIU W,ZHU X S.Green choline amino acid lonic liquid aqueous two-phase extraction coupled with HPLC for analysis sunset yellow in beverages[J].Food Analytical Methods,2019,12(11):2 527-2 534.
[5] HOSSEININIA S A R,KAMANI M H,RANI S.Quantitative determination of sunset yellow concentration in soft drinks via digital image processing[J].Journal of Food Measurement and Characterization,2017,11(3):1 065-1 070.
[6] 高家敏,钮正睿,李红霞,等.高效液相色谱法测定饮料中 12 种水溶性合成着色剂[J].食品安全质量检测学报,2019,10(1):135-140.
GAO J M,NIU Z R,LI H X,et al.Determination of 12 kinds of water-soluble synthetic colorants in drinks by high performance liquid chromatography[J].Journal of Food Safety and Quality,2019,10(1):135-140.
[7] 戴玉婷,杨晋青,葛淑丽,等.固相萃取-高效液相色谱法测定饮料中的9种合成着色剂[J].食品与发酵科技,2019,55(2):81-84.
DAI Y T,YANG J Q,GE S L,et al.Simultaneous determination of nine synthetic colorants in beverages by high performance liquid chromatography with solid phase extraction[J].Food and Fermentation Sciences & Technology,2019,55(2):81-84.
[8] TAHTAISLEYEN S,GORDUK O,SAHIN Y.Electrochemical determination of tartrazine using a graphene/poly(L-phenylalanine) modified pencil graphite electrode[J].Analytical Letters,2020,53(11):1 683-1 703.
[9] BAYTAK A K,AKBA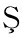 E,ASLANOGLU M.A novel voltammetric platform based on dysprosium oxide for the sensitive determination of sunset yellow in the presence of tartrazine[J].Analytica Chimica acta,2019,1087:93-103.
E,ASLANOGLU M.A novel voltammetric platform based on dysprosium oxide for the sensitive determination of sunset yellow in the presence of tartrazine[J].Analytica Chimica acta,2019,1087:93-103.
[10] CHEBOTAREV A,KOICHEVA A,BEVZIUK K,et al.Simultaneous determination of sunset yellow and tartrazine in soft drinks on carbon-paste electrode modified by silica impregnated with cetylpyridinium chloride[J].Journal of Food Measurement and Characterization,2019,13(3):1 964-1 972.
[11] NOVIANDRI I,RAMINAS A.The effect of tartrazine in voltammetric determination of rhodamin B with molecularly imprinted poly(3-aminophenol) modified carbon electrode[J].Key Engineering Materials,2019,4 902:107-112.
[12] ARVAND M,ZEINOLABEDINPOUR G.Determination of sunset yellow in foodstuffs by surface modification of nonconductive polyester of polyvinyl alcohol sheet used as overhead projector film[J].Food Analytical Methods,2019,12(8):1 858-1 870.
[13] DEROCO P B,MEDEIROS P R A,ROCHA-FILHO P R C,et al.Simple flow injection analysis system coupled to multiple-pulse amperometry and a boron-doped diamond electrode for the simultaneous determination of sunset yellow and aspartame[J].Chem Electro Chem,2020,7(8):1 943-1 950.
[14] TRAN Q T,PHUNG T T,NGUYEN Q T,et al.Highly sensitive and rapid determination of sunset yellow in drinks using a low-cost carbon material-based electrochemical sensor[J].Analytical and Bioanalytical Chemistry,2019,411(28):7 539-7 549.
[15] GHANBARI K,ROUSHANI M,FARZADFAR F,et al.Developing a four-dimensional voltammetry as a powerful electroanalytical methodology for simultaneous determination of three colorants in the presence of an uncalibrated interference[J].Chemometrics and Intelligent Laboratory Systems,2019,189:27-38.
[16] YANG X P,LUO N,TAN Z J,et al.A fluorescence probe for tartrazine detection in foodstuff samples based on fluorescence resonance energy transfer[J].Food Analytical Methods,2017,10(5):1 308-1 316.
[17] 杨彩玲,赵国虎,张鸣,等.氮掺杂碳量子点荧光猝灭法测定柠檬黄[J].化学研究与应用,2019,31(7):1 293-1 298.
YANG C L,ZHAO G H,ZHANG M,et al.Determination of tartrazine based on fluorescent quenching of nitrogen doped carbon quantum dot[J].Chemical Research and Application,2019,31(7):1 293-1 298.
[18] TÜLAY O,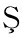 ERIFE T,
ERIFE T, AFAK C,et al.Determination of color additive tartrazine (E102) in food samples after dispersive solid phase extraction with a zirconium-based metal-organic framework (UiO-66(Zr)-(COOH)2)[J].Food Additives & Contaminants:Part A,2020,37(5):731-741.
AFAK C,et al.Determination of color additive tartrazine (E102) in food samples after dispersive solid phase extraction with a zirconium-based metal-organic framework (UiO-66(Zr)-(COOH)2)[J].Food Additives & Contaminants:Part A,2020,37(5):731-741.
[19] DUDKINA A A,VOLGINA T N,SARANCHINA N V,et al.Colorimetric determination of food colourants using solid phase extraction into polymethacrylate matrix[J].Talanta,2019,202:186-189.
[20] 孙延春,敬铭.分光光度法测定饮料中色素含量[J].四川理工学院学报(自然科学版),2012,25(5):25-28.
SUN Y C,JING M.Determination of pigments in beverage by ultraviolet spectrophotometry[J].Journal of Sichuan University of Science & Engineering(Natural Science Edition),2012,25(5):25-28.
[21] 李紫薇,袁阳,贾风勤.分光光度法同时测定饮料中的苋菜红和柠檬黄[J].伊犁师范学院学报(自然科学版),2010(4):30-32.
LI Z W,YUAN Y,JIA F Q.Spectrophotometric determination of amaranth and tartrazine in drinks[J].Journal of Yili Normal University (Natural Science Edition),2010(4):30-32.