鱼类作为重要的水产食品原料,因其体内富含蛋白质、无机盐以及不饱和脂肪酸等营养成分,而深受人们的重视。而鱼肉作为鱼类主要的食用部分,含有丰富的肌原纤维蛋白和肌浆蛋白,其溶解性、凝胶特性、乳化特性、起泡特性等功能特性是决定鱼糜制品、水产功能饮料以及水产分解型调味品品质的重要因素。对鱼肉蛋白进行改性处理,改善蛋白的功能特性,有利于提高鱼肉蛋白利用率,实现鱼肉蛋白高质化应用。
常见的动、植物蛋白改性方法按照原理可分为物理改性、化学改性、酶改性和基因工程[1]。其中,物理改性通过温度变化、压力差、机械力、电磁场、射线等作用形式,改变蛋白质的高级结构和分子间的聚集[2],相比于其他改性方法,物理改性操作便捷,对产品营养性能影响较小[1]。传统的物理改性方法包括热加工、冻融、挤压等,但是改性效果一般、操作时间较长[3],而新兴物理改性技术能克服传统方法的不足,具有操作时间短、耗能低等优点。此外,消费者对新技术应用的开放性态度以及对食品质量的高要求,使其对创新型传统食品有较高的支付意愿,这更利于新兴物理改性技术的应用[4]。因此,新兴物理改性方法在鱼肉蛋白产品的加工中具有较好的应用前景。
目前,物理改性研究多集中在改性植物蛋白或改性乳蛋白方面,且已应用于面制品以及肉类加工产品,而鱼肉蛋白改性仍处于研究中。因此,该文对鱼肉蛋白的物理改性研究进行综述,以期为鱼类深加工产品的工艺优化、鱼肉蛋白产品的研发、鱼糜加工副产物资源有效利用和蛋白改性新方法的探索提供参考。
1 超声波技术
1.1 改性机理
超声波被定义为超过人类听觉阈值(>16 kHz)的声波,其中多选用低频高强度超声波(high intensity ultrasound,HIU)改变食物理化性质[5]。声波产生空化效应和机械效应,破坏氢键和疏水键等非共价键,使蛋白质解聚[6],蛋白结构展开,暴露出结构内部的巯基和疏水基团,二级结构(α-螺旋、β-折叠、无规则卷曲)发生变化。除此之外,超声波通过改变蛋白结构,增加蛋白间的静电排斥作用,抑制肌球蛋白自组装,利于提高蛋白质溶解度[7]。但进一步提高超声强度或超声时间,蛋白质分子会因疏水相互作用而发生聚集,相应的功能特性降低;凝胶结构的孔隙度增加,致使网状结构中的水分子向外释放。
超声波会引起蛋白质分子质量的变化,随着超声强度以及超声时间的增加,肌球蛋白重链会发生降解[7];而在更高的超声强度下,肌球蛋白含量减少更加明显,降解蛋白在自由基的作用下发生氧化重排,产生大分子物质[8]。肌球蛋白可以影响蛋白凝胶的形成,但大分子物质的产生反而不利于蛋白胶凝。目前,很多研究认为超声不会引起蛋白的降解或聚集,研究结果的不一致性可能与超声强度、超声频率以及蛋白质种类等因素有关。超声强度以及超声频率较高、或者超声时间较长都可能导致蛋白质降解,使分子质量发生变化。动、植物蛋白改性一般选择20 kHz单频超声波进行处理,空化冲击力大,但空化气泡数量较少,对蛋白结构处理不能达到均匀改性效果,可能使部分蛋白过度超声而发生凝聚,而其他蛋白未受超声影响。在鲢鱼肌原纤维蛋白[9]、蛋清蛋白[10]、乳清蛋白[11]研究中发现,多频超声波空化强度高,可以缩短超声处理时间,增强蛋白改性效果,但对改性的均匀性需要进一步研究。
超声波具有较强的改性效果,但也有一定的局限性。首先,在非最佳超声条件下,特别是经过高功率或长时间超声,会导致水分子(H2O→H+·OH)分解形成高度活性自由基,增加破坏性氧化过程的发生[12]。海水鱼的脂肪含量丰富,在自由基的作用下,会加速脂肪的氧化,影响鱼糜凝胶制品的品质特性。其次,超声波主要通过空化作用改变蛋白质结构,但实际蛋白所受空化强度不均匀,使得蛋白质的变化不一,从而影响对结果的分析。因此,对超声技术的研究不能仅局限于超声强度和超声时间对蛋白的影响,更应关注均匀改性以使蛋白获得更好的功能特性。
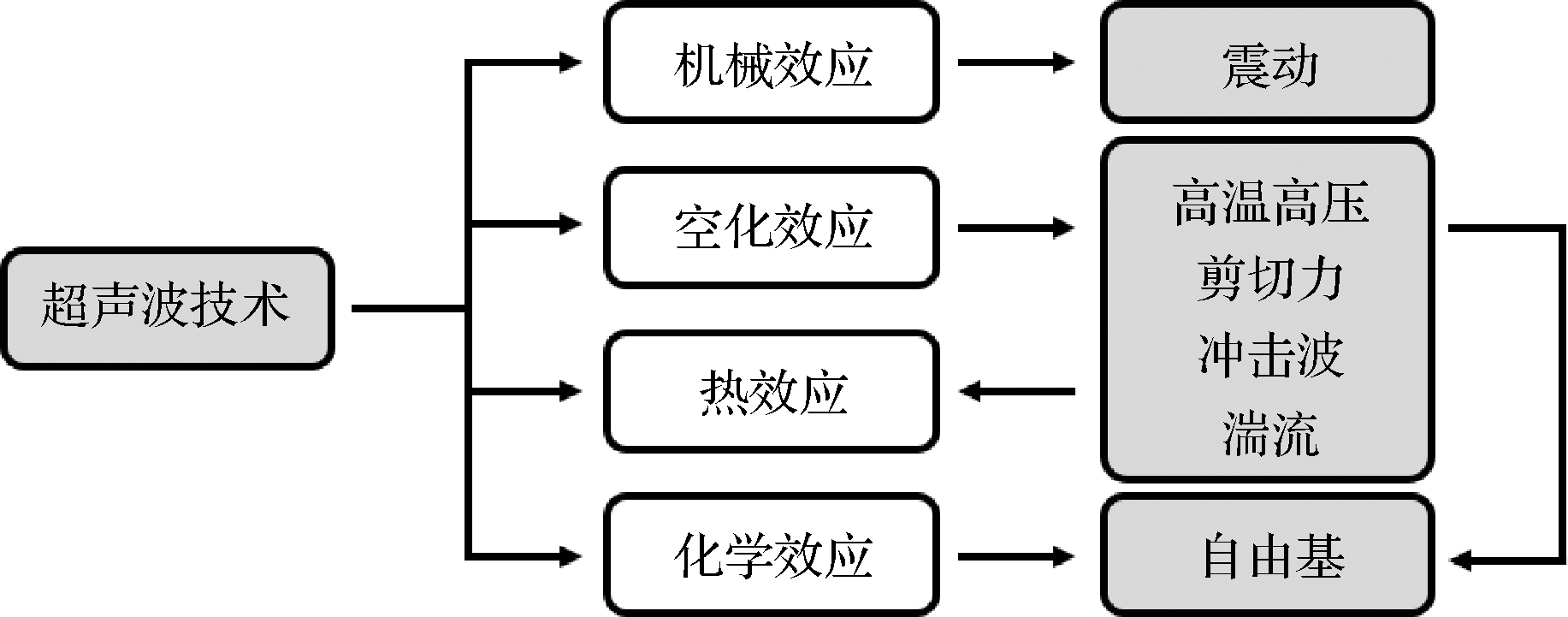
图1 超声波技术对蛋白的改性机制
Fig.1 Mechanism of protein modification by
ultrasound technology
1.2 功能特性的变化
溶解性是蛋白质的水合特性,蛋白质溶解度是指在水中的分散程度。肌原纤维蛋白通常在水溶液中溶解度很低,在较高浓度的盐溶液(>0.3 mol/L)中才能溶出[13]。表1为应用低频高强度超声波改性鱼肉蛋白的部分实例。通过测定蛋白溶解度探索蛋白的分散程度,也可通过测定蛋白粒径、比表面积、浊度间接了解蛋白的溶解程度,而电位、表面疏水基团含量、巯基含量、内源性荧光强度以及二级结构变化可以解释上述指标的变化。超声波处理可以提高盐溶性蛋白的溶解度,其改性原因可总结为以下4个因素:(1)蛋白质的构象发生改变,使亲水基团暴露;(2)空化使蛋白凝聚体解聚,粒径减少;(3)改变蛋白表面电位,阻碍蛋白质聚集;(4)经过超声处理后,适当温度升高有助于增加溶解度。但是要注意的是,如果蛋白质超声处理时间过长,产热过多会使蛋白质发生凝聚,不利于提高蛋白质溶解度。
凝胶特性的变化与蛋白结构改变以及蛋白质分子之间的相互作用有关[14]。凝胶特性的变化通过凝胶强度、质构特性、持水性、水分分布以及微观结构等进行表征。经过超声处理,肌原纤维蛋白以及肌球蛋白凝胶的凝胶特性也会发生相应的变化。在一定的超声条件下,凝胶形成能力、持水性增加,微观结构更紧密,固定化水含量增加,可知蛋白凝胶的凝胶特性增强与蛋白质粒径、共价键以及疏水相互作用有关。
蛋白质乳化特性以及起泡特性主要与蛋白表面活性有关(表面疏水性、亲水性、净电荷或电荷分布等),此外还受溶解性、离子强度、pH以及温度的影响。乳化特性和起泡特性通常选用乳化活性指数和乳化稳定性、起泡能力和起泡稳定性进行评价。根据表1可知,在适当超声条件下,空化作用以及机械作用减少蛋白分子尺寸并使蛋白分散均匀,使其乳化特性以及起泡特性增强。但在鱿鱼蛋白[15]以及大豆蛋白[16]的研究中发现超声处理会降低起泡稳定性,其原因可能与蛋白黏度降低有关,黏度降低不利于空中网络结构的形成,从而不利于起泡稳定性的增强。
表1 应用低频高强度超声波改性鱼肉蛋白举例
Table 1 Examples of fish protein modified by HIU

蛋白来源蛋白类型超声方式超声条件a改性效果参考文献Katsuwonus pelamis肌原纤维蛋白超声探针Ⅰ-20 kHz,Ⅲ-40%,Ⅳ-3 min,Ⅴ-4~10 ℃溶解性增强[17]Katsuwonus pelamis肌原纤维蛋白超声探针Ⅰ-20 kHz,Ⅲ-40%,Ⅳ-0~12 min,Ⅴ-4~10 ℃溶解性和乳化活性指数增强[18]Ctenopharyngodon idellus肌原纤维蛋白超声探针Ⅰ-20 kHz,Ⅱ-0~800 W,Ⅳ-20 min凝胶特性增强[19]Nemipterus virgatus肌原纤维蛋白超声水浴Ⅰ-28 kHz,Ⅱ-0~400 W,Ⅴ-25→51 ℃(51 ℃停留8 min)溶解性增强[20]Hypophthalmichthys molitrix肌原纤维蛋白超声探针Ⅱ-0~400 W,Ⅳ-30 min,Ⅴ-≤8 ℃乳化特性和起泡特性增强[21]Hypophthalmichthys molitrix肌球蛋白超声探针Ⅰ-20 kHz,Ⅱ-100~250 W,Ⅳ-0~12 min凝胶特性增强[22]Hypophthalmichthys molitrix肌球蛋白超声探针Ⅰ-20 kHz,Ⅱ-150 fW,Ⅳ-3、9 min凝胶特性增强[23]
注:Ⅰ-超声频率;Ⅱ-超声功率;Ⅲ-超声波振幅;Ⅳ-超声时间;Ⅴ-温度
2 超高压技术
2.1 改性机理
超高压(ultra-high pressure,UHP)技术是指在100 MPa以上的压力条件下处理食品,从而改变其空间结构以及所含成分的生物活性[3]。经过UHP处理,蛋白发生变化:在较低压力强度下,非共价键断裂,蛋白解聚,粒径降低[1];蛋白结构共价键被破坏,结构展开,疏水基团暴露,蛋白表面电位发生改变;大量暴露的巯基氧化生成二硫键(压强≥200 MPa)[24];二级结构α-螺旋减少,蛋白由有序向无序转变[25]。随着压力强度以及保压时间增加,蛋白质受疏水相互作用和静电相互作用发生凝聚,而当蛋白质处于更高压力条件下,则会发生不可逆的变性。
UHP技术应用广泛,在改性处理过程中一般不会促进脂肪氧化,但也有研究发现UHP会加快鱼肉脂肪氧化,这可能与高强度压力或长时间处理有关[26]。脂肪氧化过程中产生的中间产物会与蛋白质进一步反应形成更多的羰基和巯基,从而影响蛋白质的功能特性,但适当的氧化会提高蛋白的凝胶特性[27]。因此,在UHP处理过程中,针对不同原料应选择适宜的压力强度和保压时间,控制环境温度来避免蛋白功能特性降低。
2.2 功能特性的变化
UHP处理鱼肉蛋白,其变性程度主要与压力强度和保压时间有关,表2为应用UHP改性鱼肉蛋白的典型例子。不同压力条件下蛋白溶解度变化不一,这是由于在适宜的处理条件下,加压可以减小蛋白质粒径,从而改变蛋白质溶解状态,非适宜压力强度和保压时间下,蛋白质分子内部的疏水基团结构展开而数量增加,有利于蛋白质分子间疏水相互作用的产生,导致蛋白质凝聚,溶解度下降。因此,UHP技术虽然可以提高盐溶性蛋白的溶解度,但如果反应强度过高会不利于控制蛋白的变化,基于蛋白结构的复杂性,改性处理条件还需要进一步研究。
超声对凝胶特性及乳化特性的影响比较明显,在适宜的压力强度和保压时间下,超声对两者均起到提高作用。疏水基团以及巯基的暴露,为疏水相互作用的产生和二硫键的形成提供了条件,而这有利于鱼糜三维微观结构的形成,提高蛋白的凝胶特性。乳化性与溶解度和表面疏水性有关,加压减少了蛋白粒径、暴露疏水基团,利于提高蛋白的乳化性,但随着进一步加压,蛋白聚集,疏水基团被包埋,乳化性降低。目前尚无UHP技术对鱼肉蛋白质发泡性能影响的研究,但依据机理,蛋白质经过UHP处理,蛋白结构展开、溶解度增加,更利于提高蛋白的吸附率,改善蛋白质的发泡特性。
表2 应用超高压改性鱼肉蛋白
Table 2 Examples of fish protein modified by UHP

蛋白来源蛋白类型超高压条件改性效果参考文献Katsuwonus pela-mis肌原纤维蛋白Ⅰ-100~500 MPa,Ⅱ-10 min,Ⅲ-(23±2) ℃溶解性和乳化特性增强[18]Nemipterus spp.肌动球蛋白Ⅰ-200~600 MPa,Ⅱ-10~50 min溶解性降低[24]Nemipterus virga-tus肌球蛋白Ⅰ-150~600 MPa,Ⅱ-5 min凝胶特性增强[28]Nemipterus virga-tus肌球蛋白Ⅰ-100~500 MPa,Ⅱ-3 min,Ⅲ-25 ℃凝胶特性增强[29]Merluccius merluc-cius肌浆蛋白Ⅰ-200~600 MPa,Ⅱ-6 min,Ⅲ-20 ℃溶解性降低,乳化稳定性增强[30]
注:Ⅰ-压力强度;Ⅱ-保压时间;Ⅲ-温度
3 微波技术
3.1 改性机理
微波是指频率为300 MHz~300 GHz的电磁波,可以使食品中的极性分子在高频电场作用下发生摩擦和碰撞,将磁场能转化为热能,使食品温度升高,可作为灭菌、干燥和解冻的传统方法[3]。在蛋白改性上,微波通过电磁和热的作用使蛋白空间结构发生伸展、疏水基团暴露出来,产生分子间的相互作用,从而改变蛋白质空间构象,理化性质和功能特性也随之发生改变[31]。对于肌球蛋白等极性分子,微波会影响蛋白质之间的静电相互作用。但是进一步提高微波强度或者处理时间,功能特性会出现先增加后逐渐降低的趋势。这是由于大量疏水基团的暴露使得蛋白质聚集,疏水基团内陷,表面疏水性降低。此外,在电场的作用下更容易形成二硫键,其表面疏水性高于水浴加热后的蛋白质[32]。
3.2 功能特性的变化
微波处理鱼肉蛋白,其强度大小会影响溶解度的变化。CAI等[33]发现高强度微波处理(300~900 W)草鱼鱼肉中的肌原纤维蛋白和肌浆蛋白溶解度均降低,这可能因为微波引起极性分子的旋转和碰撞,压缩了蛋白质表面亲水残基周围的水化层,增加了蛋白质表面静电相互作用;此外,随着反应时间的延长,疏水基团暴露在蛋白质表面,表现出疏水相互作用,使蛋白聚集,致使溶解度降低。但在较低微波强度(100 W)条件下,蛋白经过微波处理粒径降低,亚基数量增加,使得溶解度有所改善[34]。除此之外,由于电磁效应可通过破坏稳定的蛋白质-蛋白质结构,辅助其他改性技术提高蛋白溶解性。LI等[20]发现超声与微波联合(超声300 W,微波100 W)不仅可以提高蛋白溶解度,还可以改善pH变化对蛋白溶解性的影响,使蛋白质在等电点附近仍可达到较高的溶解度。
通过微波处理可以提高蛋白的凝胶特性、乳化特性以及起泡特性。适当微波处理可以推动巯基氧化生成二硫键,促使蛋白质交联、凝胶化的产生,提高鱼糜凝胶的保水性和凝胶强度,使鱼糜凝胶呈现致密的微观三维网络结构[35]。依据ZHENG等[34]对植物蛋白乳化性的探究,可以推测在较低微波强度下(50~100 W),微波可以提高蛋白乳液的乳化能力、乳化稳定性和流动性,并且可以减少油滴尺寸,这是疏水基团暴露及二级结构变化导致的。同时,适量热处理以及电磁作用促进蛋白展开,使表面疏水基团暴露,有利于提高蛋白起泡性。但也有人认为蛋白质通过非共价键形成更大聚集体,水-空气界面膜的稳定性下降,起泡特性降低[36]。因此,微波改性对蛋白起泡特性的影响还需进一步研究。
4 辐照技术
4.1 改性机理
辐照通常作为减少微生物污染、延迟食品货架期的非热处理技术。目前,辐照技术常借助60Co放射性同位数衰变时产生的γ-射线,或是电子加速器产生的电子束进行蛋白改性。经过辐照改性,蛋白肽链在空间的排列更加舒展,暴露了部分包埋在蛋白分子内部的活性基团。继续增加辐照剂量,辐照产生的自由基会加速蛋白质氧化,但适度氧化会促进交联产生并会暴露更多的疏水基团,对鱼肉蛋白的功能特性影响较小[37]。
辐照对蛋白质分子质量的变化仍存在争议。部分学者发现,肌球蛋白在高剂量(6~9 kGy)的电子束以及γ-射线辐照下,肌球蛋白重链及肌动蛋白会发生交联,形成较大分子质量的多聚体,肌球蛋白重链含量降低[38-39]。部分学者认为肌原纤维蛋白中的肌球蛋白易受高剂量(9 kGy)电子束辐照发生降解[40],这可能是由于自由基氧化造成的,但电泳图谱中并未出现小分子物质数量的增加。因此,高剂量辐照蛋白含量的变化仍需深入研究。
高辐照剂量可能会使氨基酸残基发生氧化、断裂,改变蛋白一级结构[14],在允许剂量范围下辐照改性食品,其氨基酸含量无明显变化,不会造成太大损失。此外,在对畜肉产品进行辐照处理时发现反式脂肪酸含量增加,但在草鱼鱼糜电子束辐照过程中,反式脂肪酸含量无显著性变化(P>0.05)[41],可能是由蛋白来源的差异性导致的。因此,还需要严格控制辐照剂量和辐照时间,在提高蛋白的功能特性的同时,保证食品的安全性。
4.2 功能特性的变化
辐照处理可以提高肌原纤维蛋白的溶解度,且经过研究发现溶解度的增加与自由基促进蛋白降解也有一定关系,但是随着辐照剂量的增加,肌浆蛋白的溶解度呈下降趋势,这与蛋白构象的变化以及蛋白交联和聚集有关[42]。此外,辐照还可以改善鱼糜的凝胶特性。LIN等[38]对带鱼鱼糜进行电子束辐照预处理,发现在7~9 kGy剂量下的凝胶表层结构致密,基本形成凝胶网络;吕梁玉等[43]用电子束辐照梅鱼鱼糜,发现5 kGy辐照剂量下的鱼糜所形成凝胶的持水性、质构等性能优于其他剂量组。蛋白结构的变化有利于交联网络的形成,使得凝胶特性有所改善[44]:辐照产生自由基促进二硫键的形成;蛋白结构展开,蛋白表现较高的疏水相互作用;α-螺旋结构含量降低、β-折叠增加。
由于辐照促使蛋白展开,表现出较高表面疏水性,可推测在适宜辐照剂量下可改善鱼肉蛋白的乳化特性及起泡特性,这在大米蛋白[45]、芝麻籽蛋白[46]和猪肌原纤维蛋白[47]的研究中得到证实。此外,根据蛋白种类的不同,适宜的辐照剂量差异较大。但有研究认为辐照引起蛋白交联降低了鱼肌原纤维蛋白的乳化活性指标及乳化稳定性[39]。因此,在对蛋白功能特性进行研究的同时,还需要对蛋白内部结构进行解析,这样才能更好解释蛋白特性的变化。
5 低温等离子体技术
5.1 改性机理
等离子体是由处于气态的离子、自由基、自由电子和中性物质组成的部分电离混合物,具有极高的化学反应活性,在食品行业中多作为一种新兴的杀菌方法进行应用,等离子体系统见图2[48]。在低温等离子体体系中,带电粒子持续不断地获得能量,会与样品发生碰撞和蚀刻,诱导蛋白结构由致密变松散,大量活性基团暴露[49],但气态粒子仍能保持较低的温度,因此可作为一种蛋白改性技术,改变蛋白的功能特性[50]。目前,食品领域中,低温等离子体技术常用的放电方式有介质阻挡放电、辉光放电和电晕放电[51]。
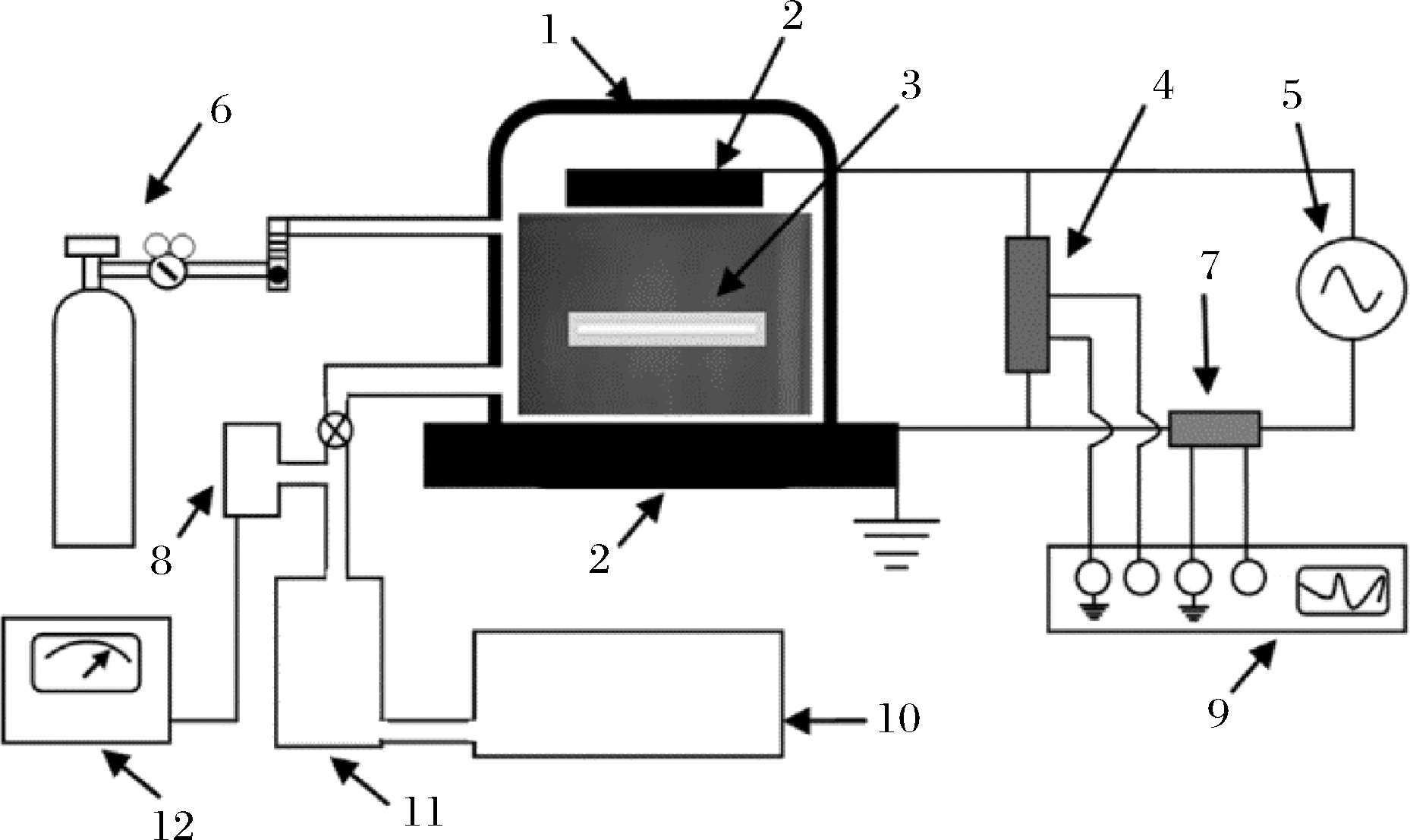
图2 等离子体系统原理图
Fig.2 Schematic diagram of plasma system
注:1-等离子体真空室;2-电极;3-薄膜样品;4-高压探针;5-电源
(0~15 kV,60 Hz);6-干式气缸;7-并联电阻(电流测量);8-真空计;
9-示波器;10-机械真空泵;11-涡轮分子真空泵;12-真空计
5.2 功能特性的变化
等离子体技术可以改变蛋白质的凝胶特性。MIAO等[52]研究了等离子体对阿拉斯加狭鳕肌肉肌原纤维蛋白的理化特性的影响,发现等离子体技术(40 kV)可以增强肌原纤维蛋白凝胶性以及热稳定性,使肌原纤维蛋白功能特性增强;随着处理电压的升高,游离巯基含量明显降低,蛋白凝聚,肌原纤维蛋白的浊度和表面疏水性增加。
目前尚无等离子体技术对鱼肉蛋白质溶解性、乳化特性、起泡特性影响的研究,但可依据其他蛋白的研究进行推测。适宜的低温等离子体处理条件下,高能粒子轰击蛋白质分子,使亲水位点暴露结合大量水,提高蛋白溶解性;随着进一步的轰击,疏水基团的暴露有利于乳化性能和起泡性能的提高[49]。但也有研究认为溶解度随处理时间增加而降低,且其原因归结于疏水性基团的暴露[53]。结果的差异性可能与不同种类蛋白结构的差异性及蛋白内部活性基团所处位置有关,鱼肉蛋白的研究可参考对虾肌原纤维蛋白[53]。
作为一种新型技术,低温等离子体技术在蛋白质改性,尤其是鱼肉蛋白改性方面的研究较少,但目前研究认为低温等离子体对商品化包装鱼片脂质的氧化指标、脂肪酸组成及营养质量无显著影响(P>0.05),但对较为敏感的鱼肉蛋白还需要进一步探究[54]。
6 其他因素在改性过程中对蛋白的影响
6.1 离子强度
在物理改性过程中,除了技术处理条件对蛋白功能特性有一定影响,环境条件对其也有一定影响。离子强度对肌原纤维蛋白等盐溶性蛋白影响较大。在鱼肉蛋白改性过程中,通常添加NaCl来提高离子强度,促进盐溶性蛋白溶出,增加蛋白质-蛋白质之间的相互作用,改善蛋白质溶解性、凝胶特性、乳化特征和起泡特性[55];而在低盐浓度下,蛋白不易展开、静电斥力较弱,使得蛋白易发生凝聚,不利于蛋白产品的加工[56-57]。但随着消费者对健康饮食的青睐,低盐蛋白产品的开发是蛋白类食品研究的重要方向。
目前,可以降低鱼肉制品中NaCl含量但仍能保证蛋白功能水平的方法有:蛋白质改性、钠替代和添加活性肽。蛋白质改性技术可以促进蛋白结构展开,使更多的活性基团(亲水基团、疏水基团、巯基等)暴露,从而改善低盐环境下蛋白的功能特性。钠替代是选择CaCl2、KCl、MgCl2部分替代NaCl,在提高离子强度的同时,对蛋白结构也会有相应的影响,这种方法多辅助蛋白改性技术对蛋白进行处理。添加活性肽可以提高蛋白的凝胶特性[58],但相比于前2种方法成本较高,不适于实际生产。
6.2 温度
温度会影响蛋白结构变化和产品品质。为了排除温度对蛋白的消极影响,通常在0~4 ℃环境下存放蛋白或进行蛋白改性;但由于部分改性设备的局限性,使得温度不能保持较低的恒温状态,如UHP改性过程中通常处于常温条件下。在常温环境中,鱼肉的盐溶性蛋白会随着时间增加损失增大,且温度越高损失率越大[59]。温度对鱼糜制品的凝胶形成能力也有一定的影响,ZHU等[60]发现阿拉斯加鳕鱼鱼糜在5 ℃UHP处理下的凝胶比25 ℃具有更强的凝胶强度,这可能是由于蛋白酶在不同温度下对蛋白的影响所致。因此,在蛋白改性过程中需依据不同的改性目的控制温度的变化、设定所需温度。
6.3 pH
pH不仅可以影响蛋白表面电荷,还会影响蛋白质结构的变化。目前,蛋白改性过程中多借助pH偏移法辅助修饰蛋白,pH偏移法使处于极端pH条件下的蛋白质内部氢键断裂、结构展开,随着pH逐渐调节至中性后,蛋白可发生重新折叠[61]。相比于中性环境,蛋白疏水基团在酸碱条件下含量较高,且碱性环境下与中性相比巯基含量差异更大,这与蛋白结构的展开有关。此外,在酸性条件下蛋白巯基更易产生二硫键,而在碱性条件下二硫键容易发生断裂,这可能与改性过程中产生的自由基有关,有研究表明在酸性情况下更易产生自由基,所以在酸碱环境下二硫键的含量有一定差异性[62-63]。因此,可通过调节pH来辅助蛋白改性,提高蛋白的功能特性。
不同改性技术在处理过程中也会对蛋白样品pH产生影响。如蛋白溶液经过超声处理后pH增加、经过长时间低温等离子体技术pH会降低,但是多数改性过程时间短、强度低,对pH影响不显著(P>0.05)。
7 展望
蛋白质改性的应用前景十分广阔,而物理改性相比于其他改性方法更温和、无污染,对产品营养性能影响较小,更适用于蛋白加工生产。但是鱼肉蛋白物理改性研究仍还存在一些问题值得进一步思考:(1)目前蛋白改性研究多以技术为主题,探索蛋白的不同功能特性变化,但以实际生产为目的,需要从蛋白功能特性角度出发,选择适宜物理改性方法,并探索实施应用的可能性;(2)对于不同鱼肉原料,其营养成分差异性大,部分技术的化学效应会影响脂肪以及蛋白的变化,可能对功能特性起到提升/降低的作用,因此,在探究改性蛋白特性的同时,也需要对其他营养成分的变化进行探讨,以确保鱼类加工产品品质;(3)利用不同改性原理,将物理改性方法与化学方法或酶法联用,能更好地实现对蛋白功能特性的修饰,但联合改性技术中不可控因素较多且步骤繁琐,因此还需要对其改性效果和投入成本进行比较;(4)目前物理改性蛋白研究多局限于植物蛋白和乳清蛋白,很多新兴物理改性技术,如超临界流体挤压、机械旋磨活化技术,对鱼肉蛋白功能特性的影响还有待进一步研究。
[1] 郭超凡, 王云阳.蛋白质物理改性的研究进展[J].食品安全质量检测学报,2017,8(2):428-433.
GUO F C,WANG Y Y.Research progress on physical modification methods of protein[J].Journal of Food Safety and Quality,2017,8(2):428-433.
[2] 张晶晶, 郑惠娜,章超桦,等.水产蛋白的提取及其改性研究进展[J].安徽农业科学,2014,42(11):3 401-3 403;3 422.
ZHANG J J,ZHENG H N,ZHANG C H,et al.Research progress of extraction and modification of aquatic protein[J].Journal of Anhui Agricultural Sciences,2014,42(11):3 401-3 403;3 422.
[3] MIRMOGHTADAIE L,ALIABADI S S,HOSSEINI S M.Recent approaches in physical modification of protein functionality[J].Food Chemistry,2016,199:619-627.
[4] ROSELLI L,CICIA G,CAVALLO C,et al.Consumers’ willingness to buy innovative traditional food products:the case of extra-virgin olive oil extracted by ultrasound[J].Food Research International,2018,108:482-490.
[5] O’SULLIVAN J J,PARK M,BEEVERS J,et al.Applications of ultrasound for the functional modification of proteins and nanoemulsion formation:A review[J].Food Hydrocolloids,2017,71:299-310.
[6] MA W C,WANG J M,XU X B,et al.Ultrasound treatment improved the physicochemical characteristics of cod protein and enhanced the stability of oil-in-water emulsion[J].Food Research International,2019,121:247-256.
[7] LIU R,LIU Q,XIONG S B,et al.Effects of high intensity unltrasound on structural and physicochemical properties of myosin from silver carp[J].Ultrasonics Sonochemistry,2016,37:150-157.
[8] LIU H T,ZHANG H,LIU Q,et al.Solubilization and stable dispersion of myofibrillar proteins in water through the destruction and inhibition of the assembly of filaments using high-intensity ultrasound[J].Ultrasonics Sonochemistry,2020,67:105160.
[9] 胡爱军,卢秀丽,郑捷,等.不同频率超声对鲢鱼肌原纤维蛋白结构的影响[J].现代食品科技,2014,30(3):23-27.
HU A J,LU X L,ZHENG J,et al.Effect of different frequency ultrasonic treatments on the structures of silver carp myofibrillar protein[J].Modern Food Science and Technology,2014,30(3):23-27.
[10] SUN J,MU Y Y,JING H,et al.Effects of single-and dual-frequency ultrasound on the functionality of egg white protein[J].Journal of Food Engineering,2020,277:109 902.
[11] CHENG Y,DONKOR P O,REN X F,et al.Effect of ultrasound pretreatment with mono-frequency and simultaneous dual frequency on the mechanical properties and microstructure of whey protein emulsion gels[J].Food Hydrocolloids,2019,89:434-442.
[12] GHARIBZAHEDI S M T,SMITH B.The functional modification of legume proteins by ultrasonication:A review[J].Trends in Food Science and Technology,2020,98:107-116.
[13] CHEN X,XU X L,LIU D M,et al.Rheological behavior,conformational changes and interactions of water-soluble myofibrillar protein during heating[J].Food Hydrocolloids,2018,77:524-533.
[14] 王盼盼. 食品中蛋白质的功能特性综述[J].肉类研究,2010(5):62-71.
WANG P P.Functionality of food protein[J].Meat Research,2010(5):62-71.
[15] ARREDONDO-PARADA I,TORRES-ARREOLA W,SUAREZ-JIMENEZ G M,et al.Effect of ultrasound on physicochemical and foaming properties of a protein concentrate from giant squid (Dosidicus gigas) mantle[J].LWT-Food Science and Technology,2020,121:108 954.
[16] REN X E,LI C,YANG F,et al.Comparison of hydrodynamic and ultrasonic cavitation effects on soy protein isolate functionality[J].Journal of Food Engineering,2020,265:109 697.
[17] 李长乐, 武雅琴,王莉莎,等.超声波及超声波结合酸处理优化鲣鱼肌原纤维蛋白功能特性[J].食品与发酵工业,2019,45(3):119-123.
LI C L,WU Y Q,WANG L S,et al.Study on the optimization of gelling properties of skipjack myofibrillar protein by ultrasonic and ultrasonic combined with acid treatment[J].Food and Fermentation Industries,2019,45(3):119-123.
[18] 李长乐, 王琛,郭全友,等.超声波、超高压处理对鲣鱼肌原纤维蛋白功能性质的影响[J].食品与发酵工业,2018,44(7):96-101.
LI C L,WANG C,GUO Q Y,et al.Effect of ultrasonic and ultrahigh pressure on the functional properties of skipjack myofibrillar protein[J].Food and Fermentation Industries,2018,44(7):96-101.
[19] WEN Q H,TU Z C,ZHANG L,et al.Effect of high intensity ultrasound on the gel and structural properties of Ctenopharyngodon idellus myofibrillar protein[J].Journal of Food Biochemistry,2017,41(1).
[20] LI Z Y,WANG J Y,ZHENG B D,et al.Impact of combined ultrasound-microwave treatment on structural and functional properties of golden threadfin bream (Nemipterus virgatus) myofibrillar proteins and hydrolysates[J].Ultrasonics Sonochemistry,2020,65:105 063.
[21] 尹艺霖,刘学军.不同超声功率处理对鲢鱼肌原纤维蛋白理化特性及凝胶品质的影响[J].肉类研究,2019,33(3):14-19.
YIN Y L,LIU X J.Effects of ultrasonic power on physicochemical properties and gel quality of myo brillar protein from silver carp[J].Meat Research,2019,33(3):14-19.
brillar protein from silver carp[J].Meat Research,2019,33(3):14-19.
[22] 谢亚如, 刘庆,熊善柏,等.高强度超声作用下鲢鱼肌球蛋白的结构及流变学特性变化[J].食品科学,2019,40(5):77-84.
XIE Y R,LIU Q,XIONG S B,et al.Effect of high intensity ultrasound on structural and rheological properties of myosin from silver carp[J].Food Science,2019,40(5):77-84.
[23] AN Y Q,LIU Q,XIE Y R,et al.Aggregation and conformational changes of silver carp myosin as affected by the ultrasound-calcium combination system[J].Journal of the Science of Food and Agriculture,2018,98(14):5 335-5 343.
[24] ZHOU A,LIN L,LIANG Y,et al.Physicochemical properties of natural actomyosin from threadfin bream (Nemipterus spp.) induced by high hydrostatic pressure[J].Food Chemistry,2014,156:402-407.
[25] 曹莹莹, 张亮,王鹏,等.超高压结合热处理对肌球蛋白凝胶特性及蛋白二级结构的影响[J].肉类研究,2013,27(1):1-7.
CAO Y Y,ZHANG L,WANG P,et al.Combined effect of ultra high pressure and heating on gel properties and secondary structure of myosin[J].Meat Research,2013,27(1):1-7.
[26] MEDINA-MEZA L G,BARNABA C,BARBOSA-CANOVAS G V.Effects of high pressure processing on lipid oxidation:A review[J].Innovative Food Science and Emerging Technologies,2014,22:1-10.
[27] YU D W,WU L Y,REGENSTEIN J M,et al.Recent advances in quality retention of non-frozen fish and fishery products:a review[J].Critical Reviews in Food Science and Nutrition,2020,60(10):1 747-1 759.
[28] WANG J,LI Z,ZHENG B,et al.Effect of ultra-high pressure on the structure and gelling properties of low salt golden threadfin bream (Nemipterus virgatus) myosin[J].LWT-Food Science and Technology,2019,100:381-390.
[29] GUO Z B,LI Z Y,WANG J Y,et al.Gelation properties and thermal gelling mechanism of golden threadfin bream myosin containing CaCl2 induced by high pressure processing[J].Food Hydrocolloids,2019,95:43-52.
[30] VILLAMONTE G,POTTIER L,DE LAMBALLERIE M.Influence of high-pressure processing on the physicochemical and the emulsifying properties of sarcoplasmic proteins from hake (Merluccius merluccius)[J].European Food Research and Technology,2016,242(5):667-675.
[31] 冯建慧, 曹爱玲,陈小强,等.微波对食品蛋白凝胶性和结构影响研究进展[J].食品工业科技,2017,38(18):317-322.
FENG J H,CAO A L,CHEN X Q,et al.Research progress of effect of microwave heating on gelation properties and structure of food protein[J].Science and Technology of Food Industry,2017,38(18):317-322.
[32] CAO H W,JIAO X D,FAN D M,et al.Microwave irradiation promotes aggregation behavior of myosin through conformation changes[J].Food Hydrocolloids,2019,96:11-19.
[33] CAI L Y,FENG J H,CAO A L,et al.Denaturation kinetics and aggregation mechanism of the sarcoplasmic and myofibril proteins from grass carp during microwave processing[J].Food and Bioprocess Technology,2018,11(2):417-426.
[34] ZHENG Y M,LI Z Y,ZHANG C,et al.Effects of microwave-vacuum pre-treatment with different power levels on the structural and emulsifying properties of lotus seed protein isolates[J].Food Chemistry,2020,311:125 932.
[35] LIU X Y,FENG D D,JI L,et al.Effects of microwave heating on the gelation properties of heat-induced Alaska pollock (Theragra chalcogramma) surimi[J].Food Science and Technology International,2018,24(6):497-506.
[36] 赵维高, 刘文营,黄丽燕,等.食品加工中蛋白质起泡性的研究[J].农产品加工(学刊),2012(11):69-72.
ZHAO W G,LIU W Y,HUANG L Y,et al.Review of the research on protein foaming ability in food processing[J].Academic Periodical of Farm Products Processing,2012(11):69-72.
[37] 张晗, 高星,宣仕芬,等.电子束辐照对鲈鱼肉肌原纤维蛋白生化特性及其构象的影响[J].食品科学,2019,40(13):81-86.
ZHANG H,GAO X,XUAN S F,et al.Effect of electron beam irradiation on biochemical properties and structure of myofibrillar protein from Lateolabrax japonicus meat[J].Food Science,2019,40(13):81-86.
[38] LIN X P,YANG W G,XU D L,et al.Improving gel properties of hairtail surimi by electron irradiation[J].Radiation Physics and Chemistry,2015,110:1-5.
[39] SHI Y,LI R Y,TU Z C,et al.Effect of gamma-irradiation on the physicochemical properties and structure of fish myofibrillar proteins[J].Radiation Physics and Chemistry,2015,109:70-72.
[40] LV M C,MEI K L,ZHANG H,et al.Effects of electron beam irradiation on the biochemical properties and structure of myofibrillar protein from Tegillarca granosa meat[J].Food Chemistry,2018,254:64-69.
[41] ZHANG H F,WANG W,WANG H Y,et al.Effect of e-beam irradiation and microwave heating on the fatty acid composition and volatile compound profile of grass carp surimi[J].Radiation Physics and Chemistry,2017,130:436-441.
[42] LI C L,HE L C,MA S M,et al.Effect of irradiation modification on conformation and gelation properties of pork myofibrillar and sarcoplasmic protein[J].Food Hydrocolloids,2018,84:181-192.
[43] 吕梁玉, 罗华彬,吕鸣春,等.电子束辐照对梅鱼鱼糜化学作用力、流变及其凝胶特性的影响[J].食品科学,2018,39(19):7-12.
LV L Y,LUO H B,LV M C,et al.Effect of electron beam irradiation on chemical interactions,rheological and gel properties of Collichthys lucidus surimi[J].Food Science,2018,39(19):7-12.
[44] LIN X P,YANG W G,XU D L,et al.Effect of electron irradiation and heat on the structure of hairtail surimi[J].Radiation Physics and Chemistry,2015,114:50-54.
[45] ZHANG X X,WANG L,CHEN Z X,et al.Effect of electron beam irradiation on the structural characteristics and functional properties of rice proteins[J].Rsc Advances,2019,9(24):13 550-13 560.
[46] HASSAN A B,MAHMOUD N S,ELMAMOUN K,et al.Effects of gamma irradiation on the protein characteristics and functional properties of sesame (Sesamum indicum L.) seeds[J].Radiation Physics and Chemistry,2018,144:85-91.
[47] KWANG-HWAN K,SAM PIN L,KEY W.Effects of electron beam irradiation on functional and other associated properties of pork myofibrillar salt-soluble proteins[J].Journal of Food Science and Nutrition,2006,11(1):73-77.
[48] ROMANI V P,OLSEN B,COLLARES M P,et al.Improvement of fish protein films properties for food packaging through glow discharge plasma application[J].Food Hydrocolloids,2019,87:970-976.
[49] 季慧, 于娇娇,张金,等.介质阻挡低温等离子处理对花生蛋白持水性及溶解性的影响[J].农业工程学报,2019,35(4):299-304.
JI H,YU J J,ZHANG J,et al.Effects of dielectric barrier discharge cold plasma treatment on solubility and water holding capacity of peanut protein[J].Transactions of the Chinese Society of Agricultural Engineering,2019,35(4):299-304.
[50] 杨新文,牛文俊,成军虎,等.低温等离子技术及其对食品品质与微生物的影响[J].食品与机械,2019,35(9):199-203;215.
YANG X W,NIU W J,CHENG J H,et al.Cold plasma technology and its effect on the food quality and microorganism[J].Food and Machinery,2019,35(9):199-203;215.
[51] 燕杰. 低温等离子体处理技术及装置[D].北京:中国石油大学,2011.
YAN J.Technology and device of low-temperature plasma[D].Beijing:China University of Petroleum,2011.
[52] MIAO W H,NYAISABA B M,KODDY J K,et al.Effect of cold atmospheric plasma on the physicochemical and functional properties of myofibrillar protein from Alaska pollock (Theragra chalcogramma)[J].International Journal of Food Science and Technology,2020,55(2):517-525.
[53] EKEZIE F G C,CHENG J H,SUN D W.Effects of atmospheric pressure plasma jet on the conformation and physicochemical properties of myofibrillar proteins from king prawn (Litopenaeus vannamei)[J].Food Chemistry,2019,276:147-156.
[54] PEREZ-ANDRES J M,DE ALBA M,HARRISON S M,et al.Effects of cold atmospheric plasma on mackerel lipid and protein oxidation during storage[J].LWT-Food Science and Technology,2020,118:108 697.
[55] DACHMANN E,NOBIS V,KULOZIK U,et al.Surface and foaming properties of potato proteins:Impact of protein concentration,pH value and ionic strength[J].Food Hydrocolloids,2020,107:105 981.
[56] GE G,HAN Y R,ZHENG J B,et al.Physicochemical characteristics and gel-forming properties of myofibrillar protein in an oxidative system affected by partial substitution of NaCl with KCl,MgCl2 or CaCl2[J].Food Chemistry,2020,309:114 537.
[57] 朱一丹, 谢国锦,高岭,等.不同pH和离子强度条件下青鱼(Mylopharyngodon piceus)肌浆蛋白IgG/IgE结合能力的变化[J].食品与发酵工业,2020,46(14):34-39.
ZHU Y D,XIE G J,GAO L,et al.Effect of different pH and ion strength on IgG/IgE binding capacity of sarcoplasmic protein of black carp (Mylopharyngodon piceus)[J].Food and Fermentation Industries,2020,46(14):34-39.
[58] ZHANG L T,LI Q,HONG H,et al.Prevention of protein oxidation and enhancement of gel properties of silver carp (Hypophthalmichthys molitrix) surimi by addition of protein hydrolysates derived from surimi processing by-products[J].Food Chemistry,2020,316:126 343.
[59] 周国艳, 郭堂鹏.鲢鱼鱼糜在储藏过程中新鲜度和盐溶性蛋白质变化研究[J].食品科技,2008,29(8):240-243.
ZHOU G Y,GUO T P.Study on the change of silver carp surimi freshness and salt-soluble protein during the storage[J].Food Science and Technology,2008,29(8):240-243.
[60] ZHU Z W,LANIER T C,FARKAS B E,et al.Transglutaminase and high pressure effects on heat-induced gelation of Alaska pollock (Theragra chalcogramma) surimi[J].Journal of Food Engineering,2014,131:154-160.
[61] 周向军, 董瑞红,高义霞.pH偏移结合温和热处理对蚕豆分离蛋白结构和功能的影响[J].食品与发酵工业,2019,45(1):100-108.
ZHOU X J,DONG R H,GAO Y X.Effects of pH-shifting combined with mild heating processes on structural and functional properties of broad bean protein isolates[J].Food and Fermentation Industries,2019,45(1):100-108.
[62] GAO H,MA L,LI T Q,et al.Impact of ultrasonic power on the structure and emulsifying properties of whey protein isolate under various pH conditions[J].Process Biochemistry,2019,81:113-122.
[63] BREWER M S.Irradiation effects on meat flavor:A review[J].Meat Science,2009,81(1):1-14.