天冬(asparagi radix)为百合科植物天冬[Asparagus cochinchinensis(Lour) Merr.]的干燥块根,别名天门冬、天棘、万岁藤,是一味传统中草药,是国家卫生部公布的第三批药食两用资源之一[1]。天冬生长面积广,资源丰富,主产于中国中西部地区,如贵州、广西、云南、湖南、四川等地,在韩国等国家亦有分布[2]。天冬性寒、味甘、微苦、归肺、肾经,具有养阴润燥,清肺生津的功效,其对肺燥干咳、顿咳痰黏、腰膝酸痛、内热消渴、热病津伤等均有一定的作用[3]。目前使用的天冬以野生为主,由于天冬抗肿瘤、抗氧化、抗炎症和免疫调节等活性显著,人们开始深入研究天冬的药理活性[4-5]。随着人们保健意识和生活水平的提高,天冬的需求量也在逐年增加,为提升天冬药材资源的有效利用率,保护天冬的药材资源,提取分离并深入研究其化学成分,如黄酮、甾体皂苷等,已经成为热点[6-7]。
多糖及其复合物是自然界含量丰富的天然大分子物质之一,广泛存在于动物细胞膜、高等植物和微生物细胞壁中,其中植物多糖通常包含许多具有不同结构和生物学活性的单糖成分[8]。天冬多糖作为天冬中重要有效成分之一,引起研究者广泛关注。天冬多糖具有增强机体免疫活性的功能[9-10]。ZHANG等[9]发现,天冬多糖可以通过TLR4/NF-MDSCB途径促进髓源性抑制细胞凋亡,从而选择性地降低肿瘤小鼠脾脏中髓源性抑制细胞的比例,表明其在癌症治疗中的潜在应用。大量研究表明天冬多糖有显著抗癌效果[11-13]。翁苓苓等[11]发现体外低氧环境下天冬多糖显著抑制人肝癌细胞增殖,且呈剂量依赖性,可能通过抑制HIF-1α/VEGF表达和促进肝癌细胞凋亡达到抗肝癌的作用。李志孝等[13]从天冬中热提得到半乳葡聚糖对人乳腺癌(MCF-7)、人口腔上皮癌(KB)及Lewis肺癌具有抑制作用。但是目前对天冬多糖的理化性质和流变学性质方面的系统性研究还鲜有报道。
因此,本文针对野生天冬进行提取,得到多糖组分,并对其理化性质和溶液的流变学特性进行了研究,为未来天冬多糖的开发利用提供理论依据。
1 材料与方法
1.1 材料与试剂
本研究选用的是自然干燥的天冬,购自云南省昆明市某批发市场,经鉴定为Asparagus cochinchinensis(Lour) Merr.的干燥块根;试剂均为国产分析纯。
1.2 仪器与设备
RE-52AA旋转蒸发仪,上海亚荣;Aglient 1200高效液相色谱仪,美国Aglient;UV-2550 PC紫外可见分光光度计、DSC-60plus差式扫描量热仪,日本岛津;ICS-5000+离子色谱仪,美国Dionex;SU1510扫描电镜,日本日立;multimode8原子力显微镜,美国Bruker;Ultima IV X射线衍射仪,日本理学株式会社;Q50热重分析仪,美国TA;MARS 60动态流变仪,德国HAAKE。
1.3 试验方法
1.3.1 天冬多糖的制备
向适量脱脂干燥天冬粉末中加入蒸馏水,料液比1∶20(g∶mL),搅拌后80 ℃水浴浸提2 h。待浸提液冷却后,6 000 r/min离心10 min得上清液。上清液旋蒸浓缩至原体积的1/3,按1∶1.5的体积比向上清液中加入无水乙醇使乙醇终体积分数达60%,4 ℃醇沉过夜,离心(6 000 r/min,10 min)取沉淀。沉淀溶解后使用Sevage试剂[V(氯仿)∶V(正丁醇)=4∶1]去除蛋白质[8]。使用100 kDa透析袋透析,真空冷冻干燥得到天冬多糖[25 ℃下溶解度(112.26±3.80) mg/mL],将其命名为ARP。
1.3.2 ARP相对分子质量测定
采用高效液相色谱法测定ARP的相对分子质量。配制葡聚糖标准品(T3、T10、T40、T70、T100、T2000)溶液,得到分子质量的对数对出峰时间的回归方程,将ARP溶液的出峰时间代入方程即得ARP重均分子量。
1.3.3 ARP紫外全波长扫描
用去离子水配制质量浓度为1 mg/mL的ARP溶液,以蒸馏水作为空白对照,使用紫外分光光度计在190~400 nm范围内扫描。
1.3.4 ARP总糖含量测定
总糖含量测定采用苯酚-硫酸法[14]。
1.3.5 ARP糖醛酸含量测定
糖醛酸测定采用间羟基联苯法[15]。
1.3.6 酯化度测定
酯化度测定采用滴定法[16]。
1.3.7 ARP单糖组成测定
采用离子色谱测定ARP单糖组成。5 mg ARP中加入1 mL 2 mol/L三氟乙酸,在具塞试管中于110 ℃下水解3 h,氮吹除三氟乙酸,用超纯水配制成10 mg/L溶液,用脉冲安培检测器和Dionex Carbopac PA20柱(150 mm×3 mm)高效阴离子交换柱检测。以D-鼠李糖、L-阿拉伯糖、D-半乳糖、D-葡萄糖、L-木糖、D-甘露糖、D-半乳糖醛酸、D-葡萄糖醛酸为标准品。
1.3.8 ARP微观形态观察
1.3.8.1 扫描电镜(scanning electron microscope,SEM)观察
取少量干燥的ARP样品平贴在0.5 cm×0.5 cm导电胶上,喷金后使用SEM观察表面形态。
1.3.8.2 原子力显微镜(atomic force microscope,AFM)观察
将质量浓度为0.1 μg/mL的ARP溶液少量滴于洁净的云母片上。待液滴晾干后,在显微镜下观察。原子力显微镜的成像力为0.05~3.0 nN,共振频率为2 kHz。
1.3.9 X射线衍射(X ray diffraction,XRD)分析
采用XRD测定样品的结晶性能。衍射条件为:波长为1.541 8 A,电压为40 kV,电流为40 mA,2θ范围为5~80°。
1.3.10 热重分析
精确称取3.0 mg ARP放入坩埚中进行热重分析,以N2为加热气氛,防止空气与样品发生氧化影响实验结果(温度设置:25~600 ℃,升温速率:10 ℃/min),得到热重曲线(thermogravimetric,TG)和微商热重曲线(derivative thermogravimetric,DTG)。
1.3.11 差示扫描量热分析
采用差示扫描量热法(differential scanning calorimetry,DSC)对相变过程进行表征。精确称取3.0 mg干燥的ARP样品密封于坩埚中,以空白坩埚作为参比样品。温度设置为25~200 ℃,升温速率为10 ℃/min。
1.3.12 ARP流变性质的测定
采用流变仪对ARP溶液进行动静态流变性质的测定。测定参数设置为:平板直径60 mm,间距1 mm,温度25 ℃。
1.3.12.1 温度对ARP溶液流体性能的影响
配制质量浓度为30 g/L的ARP溶液,在不同温度下(5、15、25、45、80 ℃)进行表观黏度的测定,剪切速率分别设定为0.1、50、100 s-1。使用Arrhenius方程[17]拟合黏度与温度的关系以表征溶液流体学行为,如公式(1)所示。
(1)
式中:η,溶液表观黏度,Pa·s;A,预指数因子;Ea,活化能,J/mol;R,摩尔系数,J/(mol·K);T,绝对温度,K。
1.3.12.2 质量浓度及剪切速率对ARP溶液黏度的影响
分别配制质量浓度为10、20、40、50和80 g/L的ARP溶液,进行静态稳剪切扫描,温度控制在25 ℃,测定剪切速率0.1~100 s-1下表观黏度的变化。使用幂律牛顿方程[18]拟合表观黏度与剪切速率的关系,如公式(2)所示。
η=K×γn-1
(2)
式中:η,溶液表观黏度,Pa·s;K,稠度系数,Pa·sn;γ,剪切速率,s-1;n,流动指数。
1.3.12.3 盐离子浓度对ARP溶液流体行为的影响
用去离子水分别配制质量浓度为30 g/L的ARP溶液,分别加入NaCl和CaCl2,调节Na+、Ca2+质量浓度为0、1、10和20 g/L,混匀后上机测定剪切应力和表观黏度。
1.3.12.4 ARP浓度对黏弹性行为的影响
采用流变仪振荡模式对10、20和40 g/L样品动态扫描,测定温度25 ℃,测定频率0.1~10 Hz。
1.4 数据处理与统计分析
实验数据使用Origin 8.0软件作图,并用SPSS statistics 19软件进行数据分析和处理。
2 结果与分析
2.1 ARP重均分子量(Mw)测定
如图1-b所示,ARP的高效液相色谱图中仅有一个对称性好的主峰,响应值高,出峰时间为9.787 min。根据葡聚糖标准品在HPLC上的保留时间绘制logMw对保留时间的标准曲线(图1-a),得到回归方程为y=-0.358 2x+9.368 8,R2=0.996 1,由此测得ARP相对分子质量Mw为730 kDa。
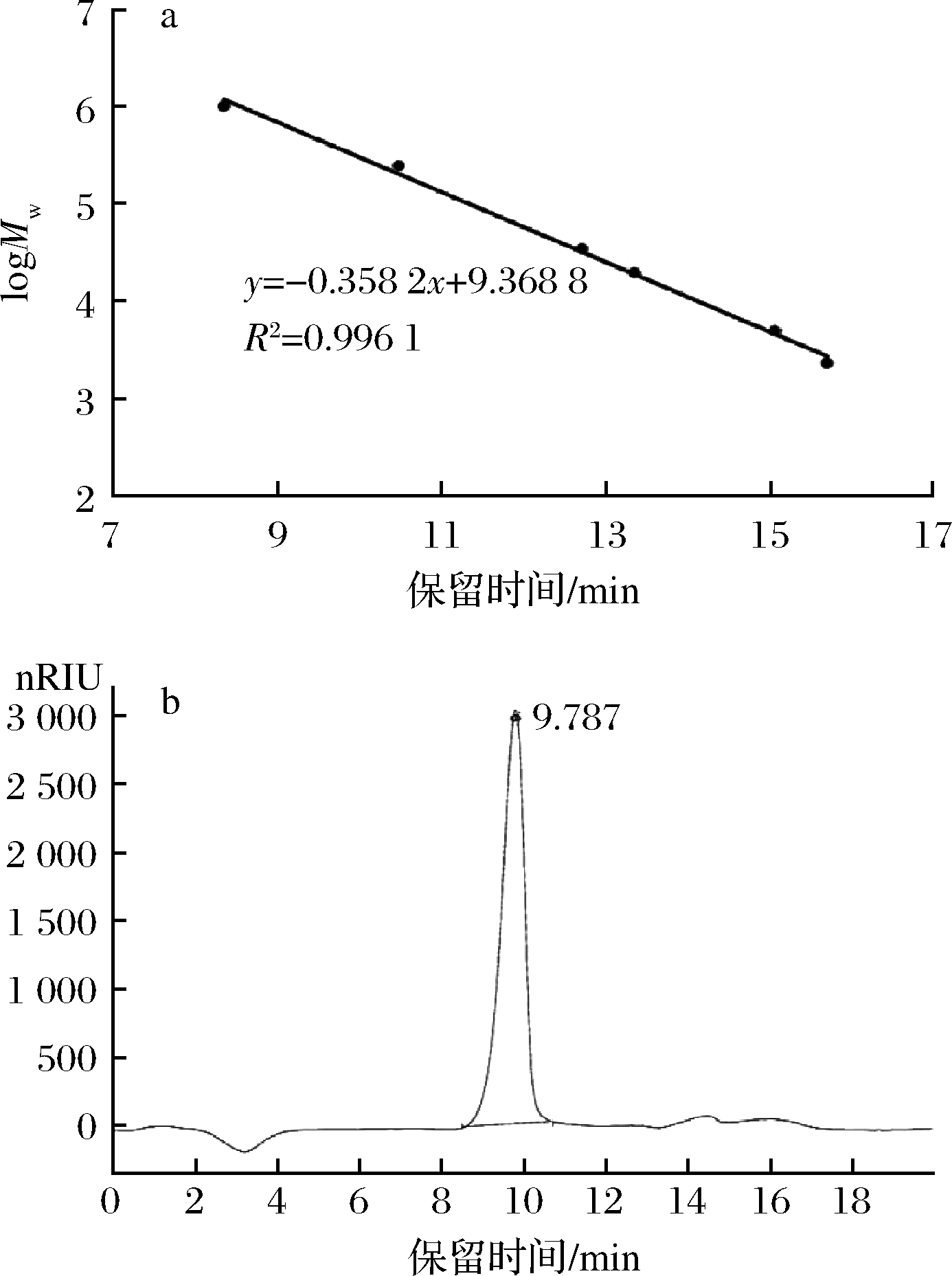
a-不同分子质量葡聚糖标准曲线;b-ARP高效液相色谱图
图1 葡聚糖标准曲线和ARP高效液相色谱图
Fig.1 Dextran standard curve and high performance liquid
chromatography of ARP
2.2 ARP纯度鉴定和化学组成
ARP紫外扫描光谱如图2所示,ARP在260和280 nm处均无明显的吸收峰,说明ARP不含蛋白质、核酸等杂质。
以葡萄糖作为标准品的回归方程y=5.828 2x-0.036 6,R2=0.999 6,测得ARP总糖含量为(93.75±1.68)%。经半乳糖醛酸标准曲线比对和回归方程y=5.167 6x-0.001 9,R2=0.997 6,计算出ARP总糖醛酸含量为(26.99±0.97)%。由滴定法测得ARP的酯化度为(38.2±0.14)%。综上表明采用传统的水提醇沉法得到的天冬多糖为总糖含量高、低甲氧基的酸性多糖。
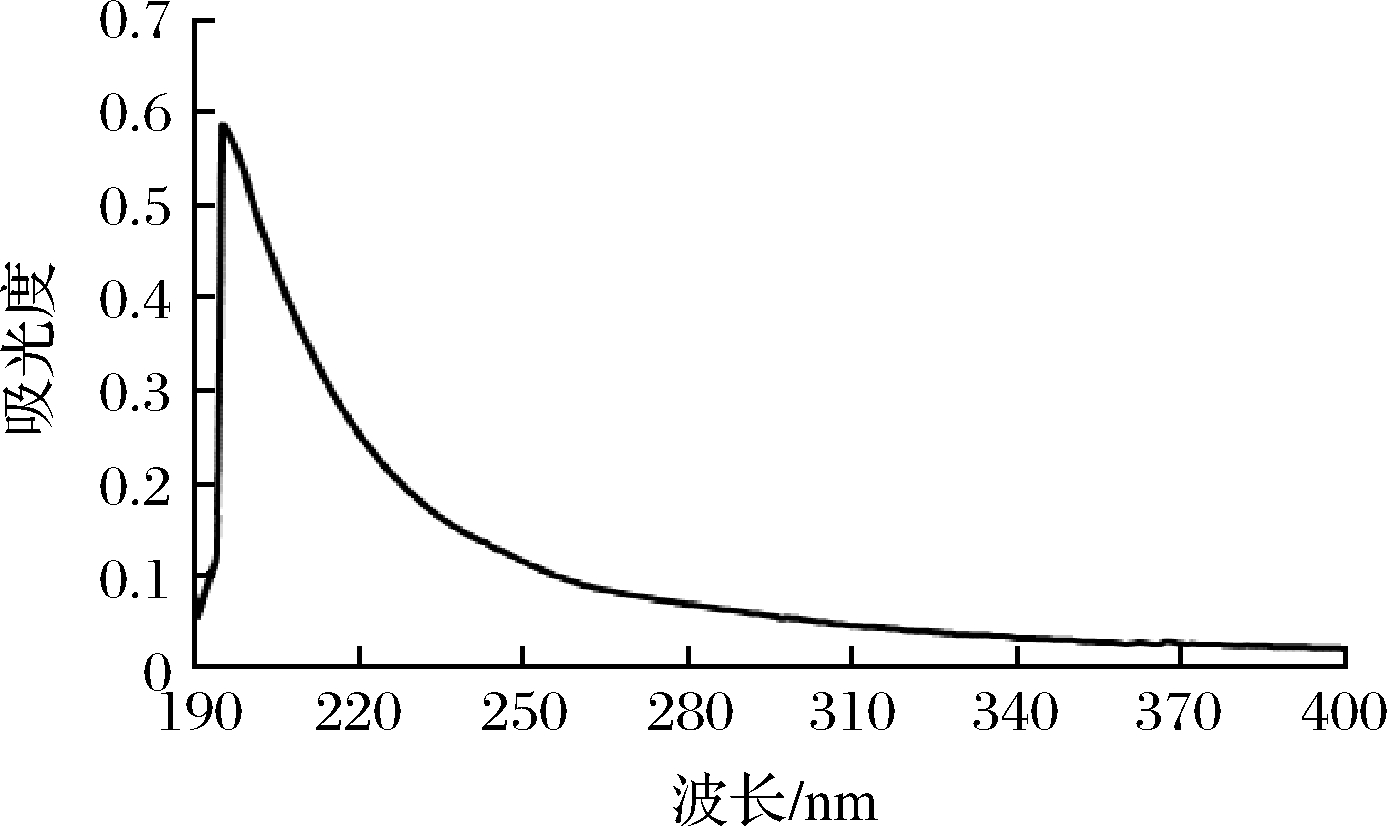
图2 ARP紫外光谱扫描图
Fig.2 UV scanning spectrum of ARP
2.3 ARP单糖组成分析
离子色谱结果表明(图3),ARP由鼠李糖(Rha)、阿拉伯糖(Ara)、半乳糖(Gal)、葡萄糖(Glc)、木糖(Xyl)、甘露糖(Man)6种单糖和半乳糖醛酸(GalA)、葡萄糖醛酸(GlcA)2种糖醛酸组成,物质的量比是0.27∶1.39∶4.42∶12.66∶1∶0.50∶4.83∶0.29,表明ARP是一种酸性杂多糖,主要由葡萄糖、半乳糖和半乳糖醛酸组成。研究结果表明,ARP与其他天冬多糖组分相比具有不同的单糖组成[13],进一步证明ARP是一种新的多糖。
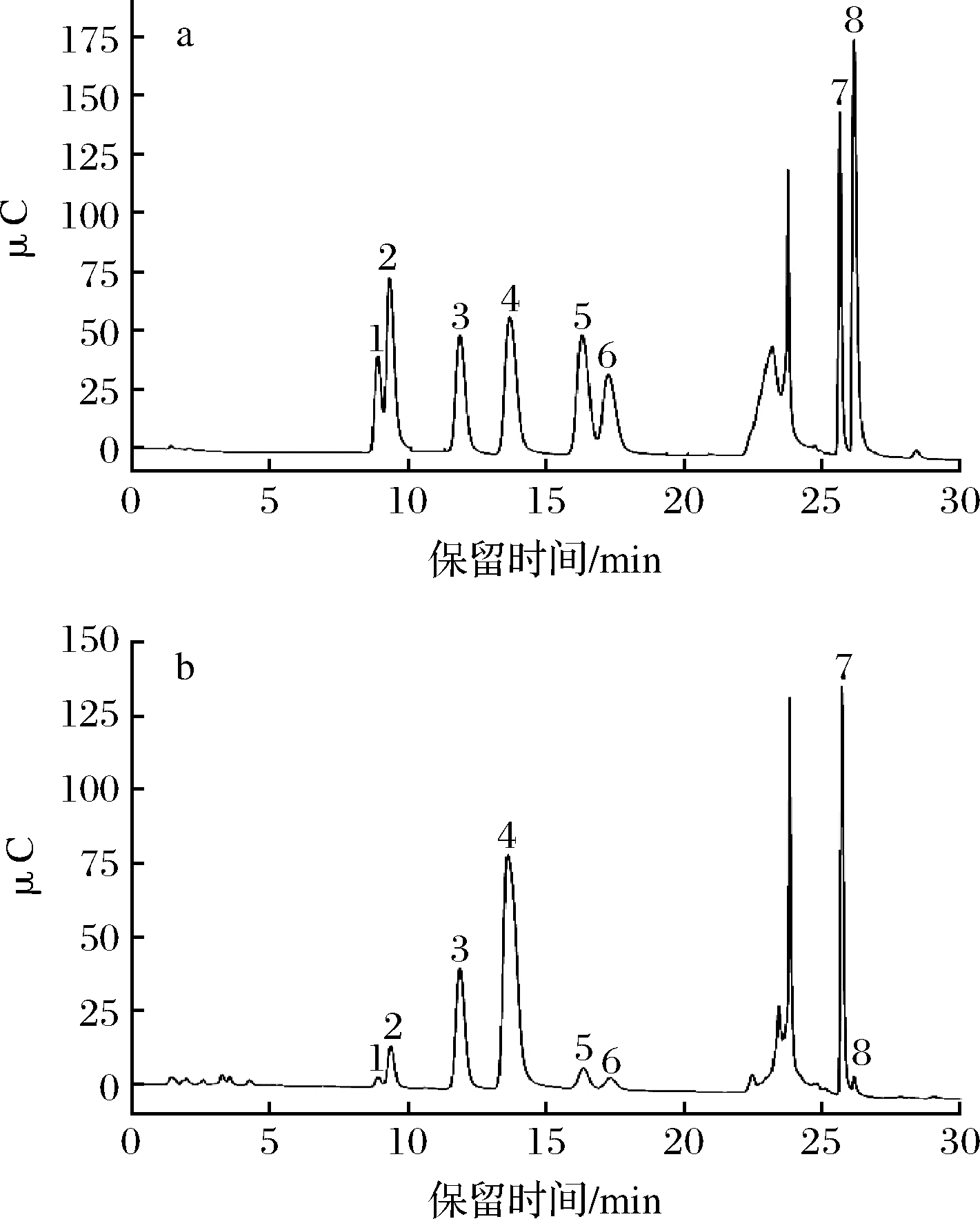
a-单糖标准品离子色谱图;b-ARP离子色谱图
图3 单糖标准品与ARP单糖组成离子色谱对比图
1-Rha;2-Ara;3-Gal;4-Glc;5-Xyl;6-Man;7-GalA;8-GlcA
Fig.3 Ion chromatogram of monosaccharide standards and
monosaccharide compositions of ARP
2.4 SEM和AFM观察
使用SEM观察ARP表面微观结构。图4-a中ARP呈网状结构,相互交叉连接;放大至500倍时(图4-b),可以观察到网状结构表面紧密较平滑,丝状物相互交织。
AFM是一种适用于观察多糖构象的有效工具,可以在亚纳米级上表征大分子聚合物[19]。图4-c,图4-d分别为在二维和三维角度观察ARP分子构象的扫描图。分散在极稀溶液中的ARP表现为球状聚集状态,部分区域团聚状更为显著。这可能是多糖高分子在水溶液中由于分子间相互作用产生交互缠结。多糖中氢键和半乳糖醛酸的含量对其大分子构象至关重要,而天冬多糖中较高的糖醛酸含量对其形态的聚集行为影响较大[20]。

a-SEM(×100倍);b-SEM(×500倍);c-AFM 2D图;d-AFM 3D图
图4 SEM和AFM观察ARP表面形态与构象
Fig.4 Observation of surface morphology and conformation
of ARP by SEM and AFM
2.5 XRD分析
XRD检测分析多糖结晶度,一般而言,晶体表现为尖而窄的特征峰,而非晶态物质表现为宽而弥散的衍射峰[21]。如图5所示,在20.7°(2θ)有一较宽的衍射峰,峰宽且弥散,此为ARP主要的结晶反射区。结晶不完整的晶体内部存在位错等缺陷,晶粒细小会导致衍射峰宽化现象[22]。由此表明ARP存在部分结晶现象,但结晶性较弱,属于无定型结构。
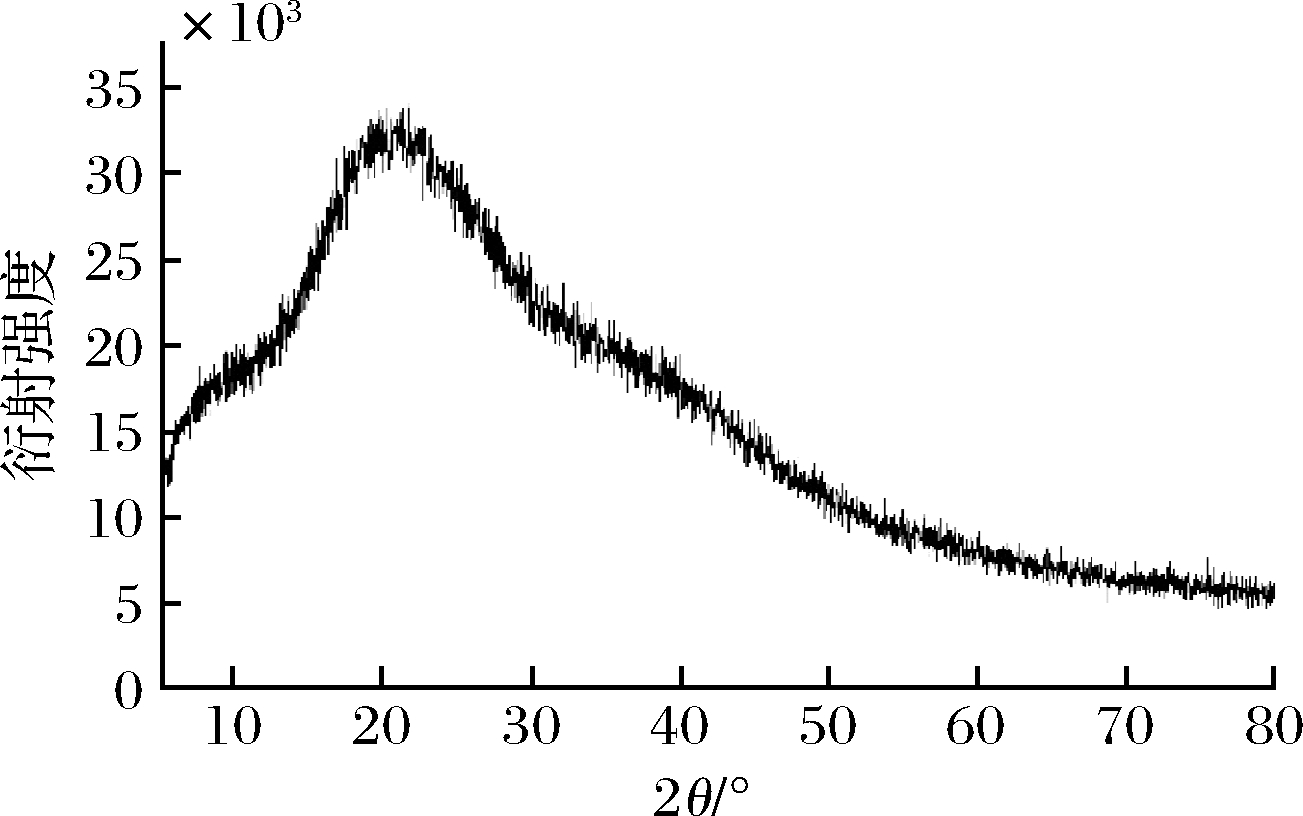
图5 ARP的X-衍射图谱
Fig.5 X-ray diffraction patterns of ARP
2.6 TG分析
图6中2条曲线即TG和DTG曲线,二者直观反映出多糖样品质量和失重率与温度变化之间的关系。从失重率曲线上可以看出,ARP的热降解过程经历了4个阶段,总失重率为93.35%。在25~100 ℃范围,ARP质量缓慢减少,损失率为9.45%,归因于多糖样品中自由水和结合水的失去。当温度从200 ℃升至357.01 ℃时,ARP样品质量出现显著损失,出现2个失重峰,失重率最高。这主要是因为多糖分子发生了剧烈的解聚和分解,大量多糖分子在高温作用下降解为具有挥发性的小分子量物质,如裂解产生CO2、水蒸气等[23]。随着温度的继续攀升,质量缓慢减小,失重趋势渐缓,此时大部分多糖被碳化为灰分和无机成分。
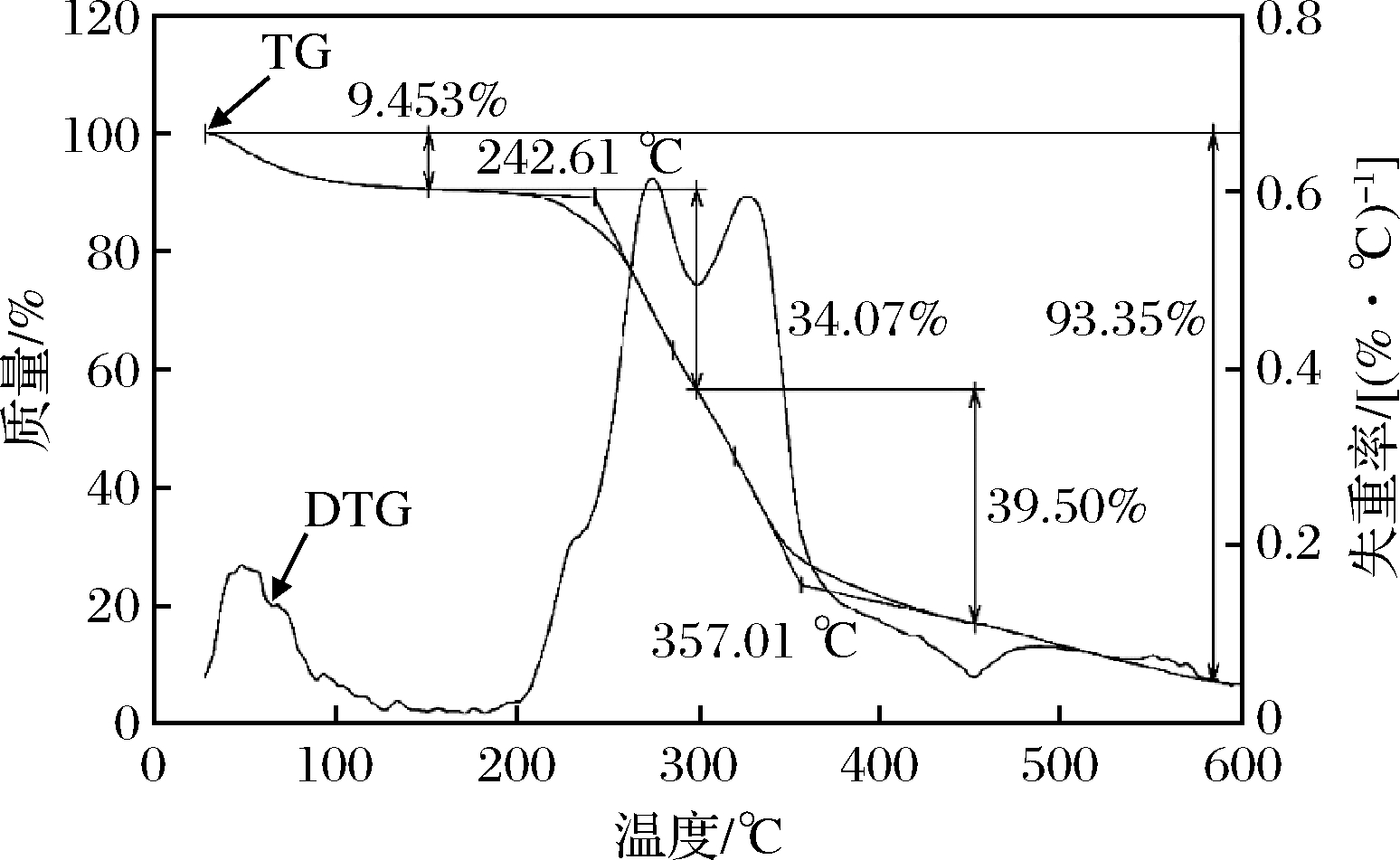
图6 ARP的热重分析
Fig.6 Thermogravimetric analysis of ARP
2.7 DSC分析
DSC是一种用于研究高分子热学性能及稳定性的重要热力学技术,以反映干燥样品在不同温度溶胀过程中由于聚合物链的重组而产生的热作用[24]。多糖由于分子间相互作用,有形成多糖链凝聚缠结、相互交联的趋向。当达到玻璃化转变温度(Tg)时,聚合链重组而产生热作用,即在DSC升温曲线中体现为吸热峰。如图7所示,ARP在82.3 ℃处有强吸热峰(-1.661 mW/mg),这归因于在Tg条件下,多糖中水分的蒸发所致。继续升温至200 ℃未出现新的吸热峰,表明在25~200 ℃范围内ARP未发生由于糖苷键断裂而引发的解聚反应,该阶段多糖结构稳定,未发生熔化分解。此结果与从决明子中分离出的半乳甘露聚糖结果一致,其转变温度为80 ℃[25]。此外,样品曲线呈现明显对称吸热峰,说明实验所提取的多糖纯度较高[26]。
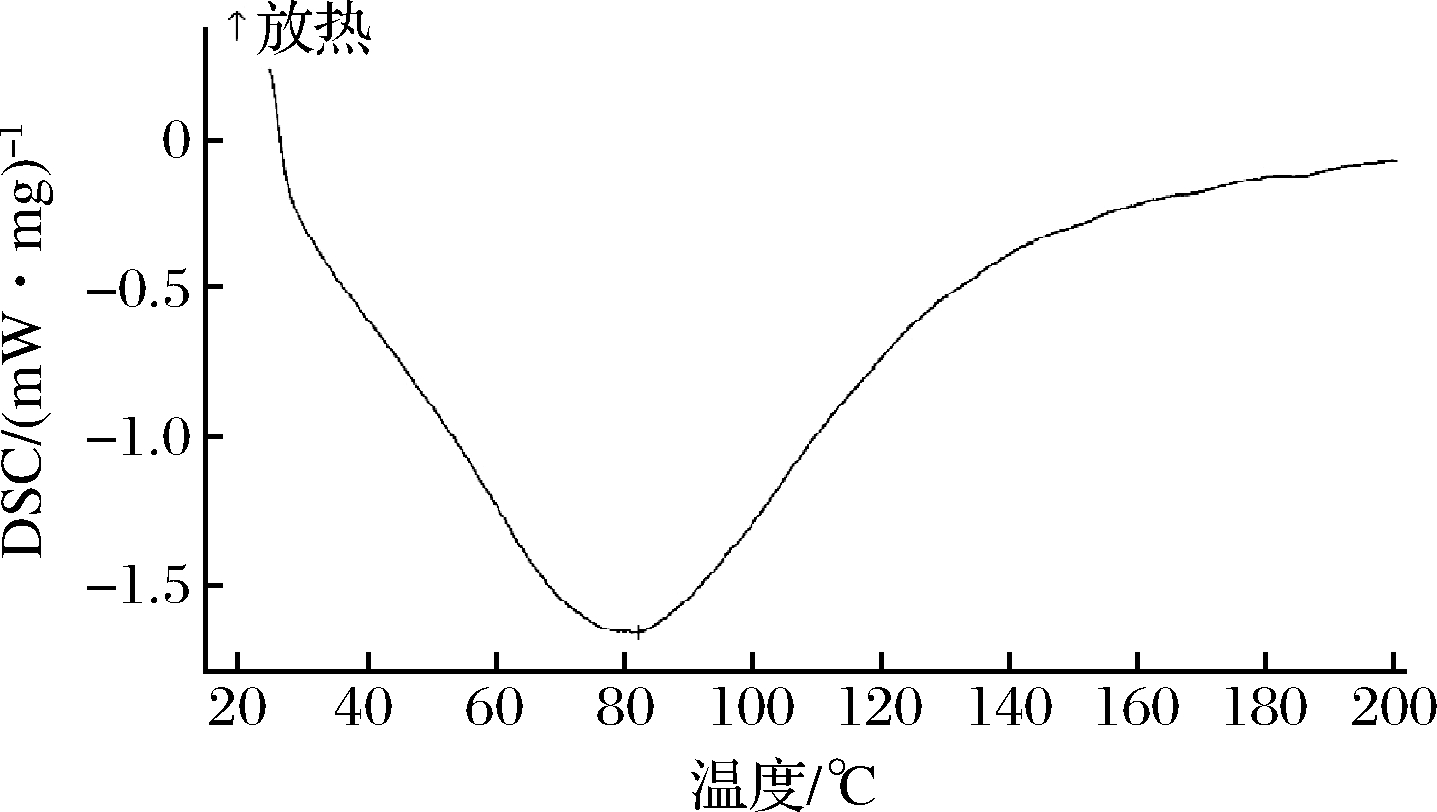
图7 ARP的DSC曲线
Fig.7 DSC curve of ARP
2.8 流变性质分析
2.8.1 温度对ARP溶液流体性能的影响
ARP溶液的表观黏度随温度变化的曲线如图8所示。对ARP黏度η和温度T关系进行Arrhenius方程拟合,得到ln η与1/T的Arrhenius方程关系式和相关参数,结果如表1所示,R2在0.965~0.982之间变化,表明流动曲线符合Arrhenius模型。
在低剪切速率γ(0.01 s-1)下,ARP溶液黏度η受T影响较大,随温度升高η先增大后急剧下降。黏度增大可能是由于在极微弱的外力和低温条件下,链间缔合作用占优势,高分子链间的缔合、缠结使分子链的运动受阻,导致溶液的黏度增大。温度升高加速了分子链的热运动,溶液中的多糖分子无规则运动加剧,分子间距离增大,相互作用力减弱,流动阻力降低致使溶液黏度下降[26]。同时,由热运动引起的聚合物链的解缠可能导致黏度降低。样品的黏度曲线也可以利用Arrhenius方程进行解释(R2=0.965),表明此时溶液η的变化与T的相关性较大。Ea反映了聚合物流动的难易程度,与聚合物的链柔性和大分子相互作用相关,Ea越大,分子间相互作用越显著,黏度随温度的变化就越大[27]。在15~80 ℃时,活化能Ea为28.320 kJ/mol,此时样品流动性能较差。
在高剪切速率(50和100 s-1)下,ARP溶液的η随着T的升高而缓慢下降,基本符合Arrhenius方程,表现出轻微的温度依赖性。随着剪切速率加剧,多糖溶液η变化的温度敏感性降低。因为高速剪切破坏多糖分子的聚集状态,分子间作用力大大减弱,溶液流动过程中需要克服的活化能减小。同时,在相同温度高剪切速率下的黏度明显低于低剪切速率。当剪切速率从50 s-1增至100 s-1时,Ea略有下降,黏度减小,但变化不显著,表明当施予较高的剪切速率时,黏度不再受剪切速率的影响。

图8 温度对ARP表观黏度的影响
Fig.8 Effect of temperature on apparent viscosity of ARP
表1 不同剪切速率下ARP溶液的Arrhenius方程和参数
Table 1 Arrhenius equations and parameters of ARP

剪切速率/s-1温度/℃Arrhenius方程活化能Ea/(kJ·mol-1)频率因子A相关系数R20.0115~80lnη0.01=3 407.89(1/T)-11.265 6328.3200.000 012 810.96550.005~80lnη50=1 485.01(1/T)-7.887 3812.3400.000 375 450.975100.005~80lnη100=1 332.708(1/T)-7.536 0811.0750.000 533 480.982
2.8.2 质量浓度及剪切速率对ARP溶液黏度的影响
ARP溶液质量浓度对其表观黏度的影响如图9所示。对ARP黏度η和剪切速率γ关系进行幂律方程拟合,得到log η与log γ的幂律方程和相关参数,该模型可以很好地描述聚合物在不同剪切速率下的剪切稀化行为,结果如表2所示。由图9可知,各浓度下的ARP均表现出典型的剪切稀化行为。同一剪切速率下,随着多糖浓度的增大,η显著升高,其表观黏度以浓度依赖的方式增加,溶液抗剪切性能提升,这种现象是由于多糖分子间距离减少,单位体积分子数量增加,致使分子间交联和相互作用增强。同一质量浓度下,随着剪切速率的增加,ARP黏度急剧降低,出现剪切稀化现象,之后黏度不再发生显著变化。
理论上,稠度系数K值和流动指数n值共同影响黏度的变化,且K值与n值之间呈负相关[16]。当ARP质量浓度为10~50 g/L时,在低剪切速率下(<1 s-1),R2为0.985~0.998,表明此时流动曲线与幂律模型拟合较优,流动指数n<1,呈现出假塑性流体性质。而在较高剪切速率下(1~100 s-1),溶液的n值接近于1,趋近于牛顿流体的性质,表现为流体η与γ相关性低。该现象推测一方面是由于在高分子稀溶液中,高分子因为布朗运动而趋于无规则分布状态,当施以外力时,高分子处于流动场中,多糖分子由无序状态开始趋于流动场的速度方向运动,增大流动性。另一方面可能与溶液中分子链的缠结有关,由于外界给予分子间摆脱相互缠结的外力,较高的剪切速率破坏分子链间的缔合作用,体系中多糖长链解离,分子链形成相对稳定有序的结构,使溶液黏度降低[27]。
随着多糖浓度的增加,剪切变稀现象的持续范围更加广泛。当ARP质量浓度增大至80 g/L时,黏度随着剪切速率的增大而持续降低。此时溶液浓度大,黏度大小取决于分子间作用力和流动场外力的相对大小,由于分子间相互折叠缠结等助力分子间的强作用力,需要更大的剪切速率破坏分子间作用力,所以剪切稀化的范围较其他质量浓度组大。
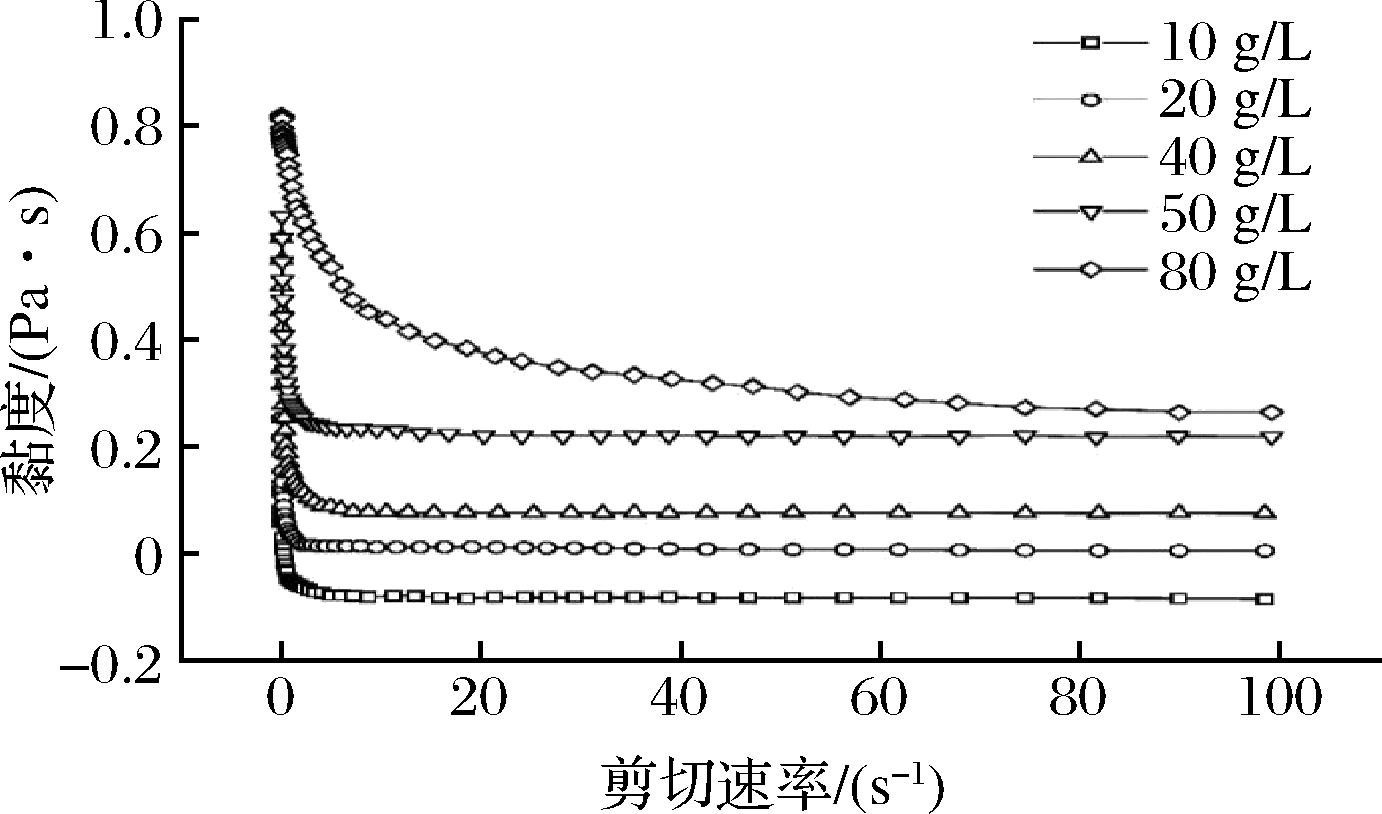
图9 剪切速率对不同质量浓度ARP溶液表观黏度的影响
Fig.9 Effect of shear rate on apparent viscosity of
ARP at different concentration
表2 不同质量浓度下ARP溶液的幂律方程和参数
Table 2 Power-law equations and parameters of
ARP at different concentration
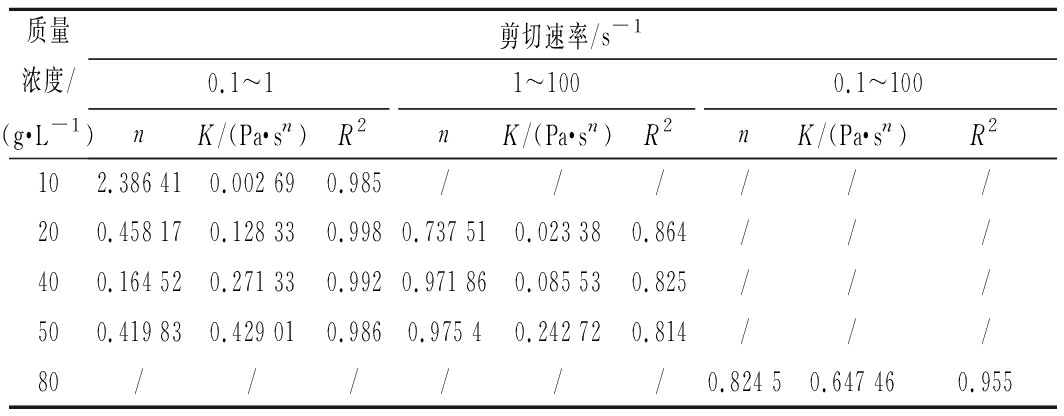
质量浓度/(g·L-1)剪切速率/s-10.1~11~1000.1~100nK/(Pa·sn)R2nK/(Pa·sn)R2nK/(Pa·sn)R2102.386 410.002 690.985//////200.458 170.128 330.9980.737 510.023 380.864///400.164 520.271 330.9920.971 860.085 530.825///500.419 830.429 010.9860.975 40.242 720.814///80//////0.824 50.647 460.955
2.8.3 盐离子浓度对ARP溶液流体行为的影响
如图10-a所示,空白组的黏度随剪切速率提高逐渐降低。随着在溶液中加入盐离子,ARP的黏度均出现不同程度的增加,呈剂量依赖性,但ARP溶液仍保持假塑性流体的特性。1 g/L的Na+对ARP黏度影响较小,当添加相同浓度的盐离子时,Ca2+对ARP溶液的增稠程度显著优于Na+。高浓度的Ca2+使ARP的η呈现出先剪切稠化的膨胀性流体行为,后剪切稀化的假塑性流体行为。剪切稠化原因是ARP作为低酯化度的酸性多糖,结构中少量羧酸基团被酯化,但大多数仍属于具有高Ca2+结合活性的羧酸基团。大量的Ca2+结合位点有助于形成二聚体,进而横向聚集形成多聚体构成egg-box网络结构[28],改善凝胶的流变特性。蛋盒模型本身致密的网格结构赋予其高黏度的特点[29]。添加Na+可以降低多糖链间静电作用,形成一定数量的氢键,交联度增加,使体系形成网格结构,从而提高了溶液的黏度。而在相同浓度无机盐条件下,价态更高的Ca2+能提供更多的电荷,架桥能力显著优于Na+,从而增稠能力更优。
空白组剪切应力τ随剪切速率增加呈直线上升趋势(图10-b)。盐离子添加组的τ随着γ的增加呈现分段上升趋势,前段(0.01~0.1 s-1)上升幅度较后段(0.1~100 s-1)更大。添加Ca2+后显著提升τ且在低γ处有一“馒头峰”,η也在相同速率处出现鼓包,同时η和τ的峰值与Ca2+添加量呈正相关,说明ARP的黏度和剪切应力的增加对CaCl2更为敏感。
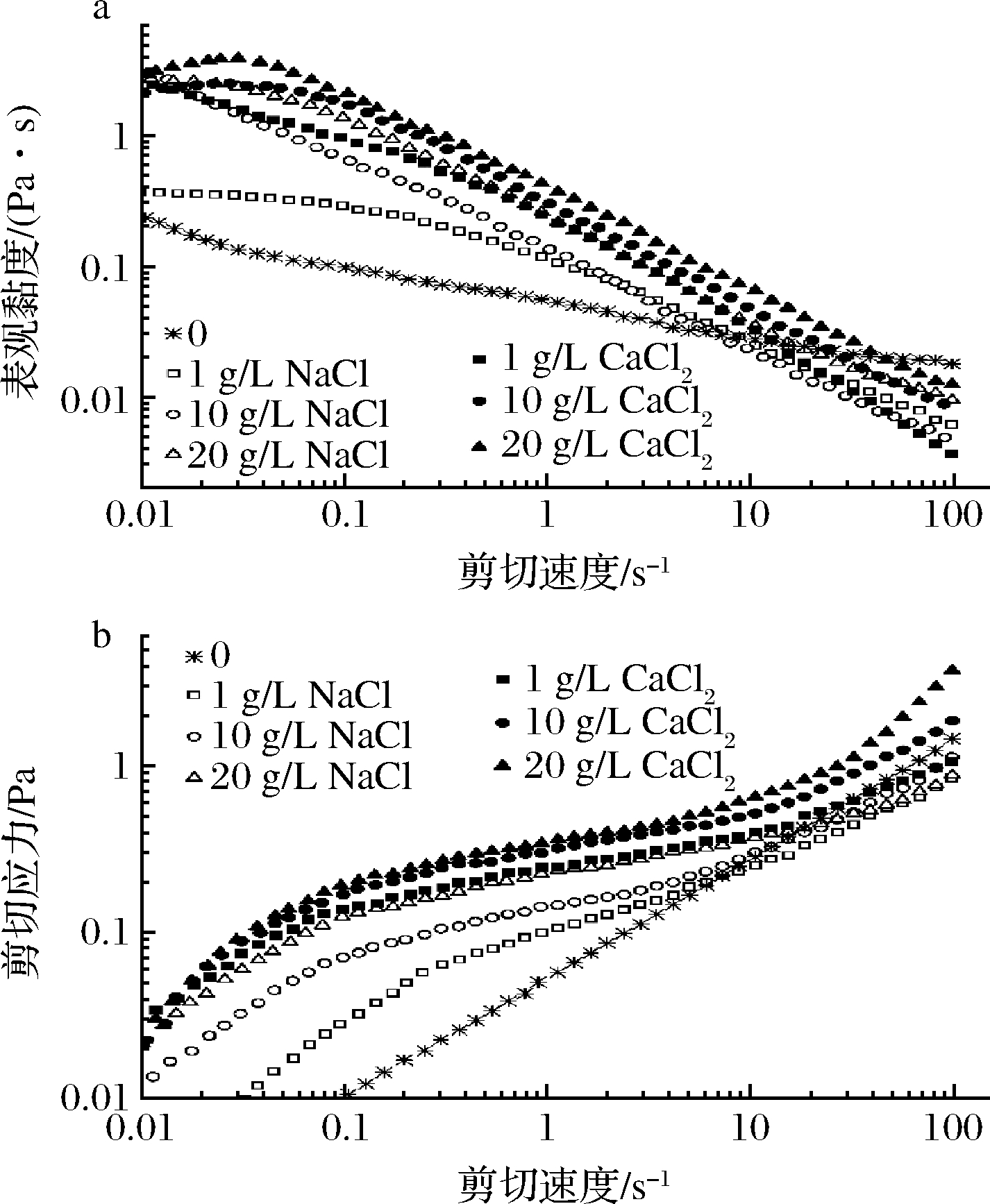
a-表观黏度;b-剪切应力
图10 Na+和Ca2+浓度对ARP溶液(30 g/L)表观黏度和
剪切应力的影响
Fig.10 Effects of Na+and Ca2+ concentration on apparent
viscosities and shear stresses of ARP solutions (30 g/L)
2.8.4 ARP质量浓度对黏弹性行为的影响
多糖是黏弹性材料,同时具有固、液特性,其特性可通过动态流变测量。图11显示了质量浓度对ARP的储能模量(G′)和损耗模量(G″)随频率的影响。G′表征高聚物溶液抵抗形变的能力即类固体属性,G″表征高聚物溶液的黏性特征即类液体属性[30]。图11表明在所有浓度下G′和G″均随频率的增加而增加,表现出频率依赖性。在低f时,两者关系为G′>G″,此时ARP溶液表现出类似于固体的弹性行为即弱凝胶的典型特征;随着f提高,交叉点出现,此时G′<G″,ARP溶液呈现黏稠液体性质[31]。G′与G″相交的f即为多糖溶液体系发生改变的临界频率,两者的交集很好地反映了聚合物的黏弹性行为,定义了黏性行为的开始或接近于黏稠液体状态。交叉点越早出现,黏性的贡献就越大。随着质量浓度的增大,体系中的G′与G″均显著升高,差异以浓度依赖的方式扩大,交叉点随着质量浓度的增加向低频区域移动。交叉点的变化可能归因于ARP高Mw加剧了分子缠结,而长时间的低频振荡会使多糖链解缠和重排,导致交叉点发生变化。同时,ARP黏弹性行为与浓度亦相关,G′和G″均随之增加。质量浓度越高,相互连接的链越多,网络越密。这表明质量浓度对ARP成胶性能影响极显著,增加质量浓度可提升ARP成胶趋势和黏弹特性。
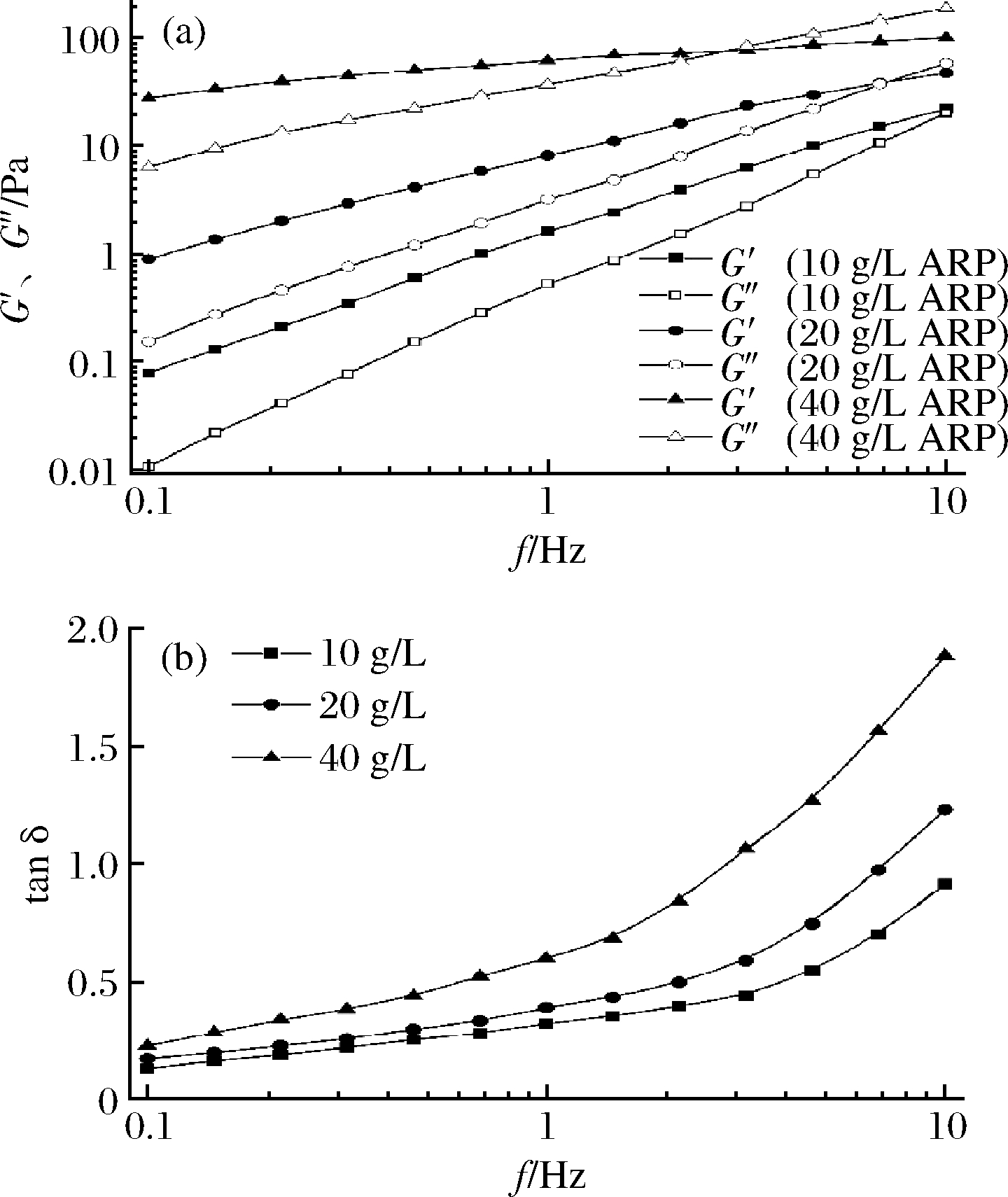
a-G′和G″;b-tanδ
图11 不同质量浓度ARP溶液的G′、G″和tanδ
随振荡频率的变化趋势
Fig.11 Variation trend of G′,G″ and tan δ of ARP solution
with different mass concentration with oscillation frequency
当质量浓度为10 g/L时,G′与G″具有明显的频率依赖性,G′>G″,阻尼tanδ(G″与G′的比值)始终<1,多糖呈现弱凝胶结构,体现弹性行为[32];随着浓度提高,G′与G″的频率依赖性逐渐降低,G′与G″开始出现交集,tanδ值显著增加且逐渐>1,tanδ呈现浓度依赖性,此时ARP具有黏性行为。
3 结论
本研究以水提醇沉法制得天冬多糖ARP,总糖含量(93.75±1.68)%,糖醛酸含量(26.99±0.97)%,酯化度为(38.2±0.14)%,Mw为730 kDa,属于纯度较高的酸性多糖。ARP由Rha、Ara、Gal、Glc、Xyl、Man六种单糖和GalA、GlcA两种糖醛酸组成,物质的量比是0.27∶1.39∶4.42∶12.66∶1∶0.50∶4.83∶0.29。ARP呈表面紧密平滑的网状结构,在极稀溶液中的ARP表现为球形聚集状。ARP结晶性较弱但具有良好的热稳定性(高达200 ℃),适用于高温处理与加工,多糖的热稳定性也是其在食品应用中选择适当生产条件的重要依据。
ARP流变特性的研究结果主要体现在4个方面。(1)ARP溶液流体行为受T和γ的影响。在低γ下,黏度随温度的变化发生波动;在高γ时,η随T的升高缓慢下降,基本符合Arrhenius方程。(2)ARP溶液的η随溶液质量浓度上升而增加。随着γ的增大,ARP溶液η下降,出现剪切稀化现象。流动指数n均小于1,符合幂律方程对非牛顿流体特征的解释。(3)盐离子对ARP溶液具有增稠、提高剪切应力作用,且Ca2+增稠程度显著优于Na+。国家卫健委公布天冬可用于保健食品,由此ARP-Ca2+系统具有应用于保健型流质食品的潜力,并有营养补充矿物质Ca2+的好处。(4)动态流变学特性研究分析表明,随着多糖浓度的增大,体系中的储能模量G′、损耗模量G″和tanδ均显著升高,即多糖的黏弹性都随之增加,且黏性性能的增大速率明显高于弹性性能的增大速率。综上,ARP具有高黏度、强剪切稀释性、良好的胶凝性和耐热性能,可作为一种新型的水胶体应用于食品等行业。
[1] 国家药典委员会. 中华人民共和国药典 3部 [M].北京:中国医药科技出版社,2010.
Chinese Pharmacopoeia Commission.Pharmacopoeia of the People’s Republic of China (Edition 3) [M].Beijing:China Medical Science and Technology Press,2010.
[2] CHOI J Y,KIM J E,PARK J J,et al.The Anti-inflammatory effects of fermented herbal roots of asparagus cochinchinensis in an ovalbumin-induced asthma model[J].Journal of Clinical Medicine,2018,7(10):377.
[3] 宫兆燕, 张君利.天冬活性化合物的提取及其药理活性研究进展[J].医学综述,2018,24(24):4 938-4 942.
GONG Z Y,ZHANG J L.Research progress of active compounds extraction in asparagus and its pharmacological activity[J].Medical Recapitulate,2018,24(24):4 938-4 942.
[4] JIAN R,ZENG K W,LI J,et al.Anti-neuroinflammatory constituents from Asparagus cochinchinensis[J].Fitoterapia,2013,84:80-84.
[5] SUN Q,ZHU L,LI Y,et al.A novel inulin-type fructan from Asparagus cochinchinensis and its beneficial impact on human intestinal microbiota[J].Carbohydrate Polymers,2020,247:116 761.
[6] ZHU G L,HAO Q,LI R T,et al.Steroidal saponins from the roots of Asparagus cochinchinensis[J].Chinese Journal of Natural Medicines,2014,12(3):213-217.
[7] JALSRAI A,NUMAKAWA T,KUNUGI H,et al.The neuroprotective effects and possible mechanism of action of a methanol extract from asparagus cochinchinensis:In vitro and in vivo studies[J].Neuroscience,2016,322:452-463.
[8] CHEN Y J,JIANG X,XIE H Q,et al.Structural characterization and antitumor activity of a polysaccharide from Ramulus mori[J].Carbohydrate Polymers,2018,190:232-239.
[9] ZHANG W S,HE W Z,SHI X D,et al.An Asparagus polysaccharide fraction inhibits MDSCs by inducing apoptosis through toll-like receptor 4[J].Phytotherapy Research,2018,32(7):1 297-1 303.
[10] 汤小蕾. 天冬多糖对小鼠免疫功能影响的实验研究[J].中医药导报,2014,20(10):83-84.
TANG X L.Study on the effects of Asparagus cochinchinensis polysaccharide on immunity function in mice[J].Guiding Journal of Traditional Chinese Medicine and Pharmacy,2014,20(10):83-84.
[11] 翁苓苓, 高玲,张闽光.天冬多糖低氧下抑制肝癌作用的体外实验研究[J].现代中西医结合杂志,2019,28(24):2 623-2 628.
WENG L L,GAO L,ZHANG M G.Anticancer effects of deproteinized asparagus polysaccharide on hepatocellular carcinoma cells in hypoxia in vitro[J].Modern Journal of Integrated Traditional Chinese and Western Medicine,2019,28(24):2 623-2 628.
[12] 程伟, 程紫薇,邢东炜,等.天冬多糖逆转缺氧诱导的上皮间质转换抑制人肝癌细胞迁移[J].辽宁中医杂志,2019,46(10):2 127-2 130.
CHENG W,CHENG Z W,XING D W,et al.Asparagus polysaccharides suppress migration of human hepatocellular carcinoma cells by reversing epithelial-mesenchymal[J].Liaoning Journal of Traditional Chinese Medicine,2019,46(10):2 127-2 130.
[13] 李志孝, 黄成钢,陈谦,等.天门冬半乳葡聚糖的化学结构及其抑瘤活性的研究[J].兰州大学学报,2000,36(5):77-81.
LI Z X,HUANG C G,CHEN Q,et al.Studies on chemical constitution and antitumor activity of galacto-glucan from Asparagus cochinchinensis[J].Journal of Lanzhou University(Natural Sciences),2000,36(5):77-81.
[14] DUBOIS M,GILLES K A,HAMILTON J K,et al.Colorimetric method for determination of sugars and related substances[J].Analytical Chemistry,1956,28(3):350-356.
[15] BLUMENKRANTZ N,ASBOE-HANSEN G.New method for quantitative determination of uronic acids[J].Analytical Biochemistry,1973,54(2):484-489.
[16] BAI L L,ZHU P L,WANG W B,et al.The influence of extraction pH on the chemical compositions,macromolecular characteristics,and rheological properties of polysaccharide:The case of okra polysaccharide[J].Food Hydrocolloids,2020,102:105 586.
[17] XIAO Q,TONG Q,LIM L-T.Pullulan-sodium alginate based edible films:Rheological properties of film forming solutions[J].Carbohydrate Polymers,2012,87(2):1 689-1 695.
[18] RAO M A.Rheology of fluid and semisolid foods-principle and applications[M].2nd Ed.New York:Springer Science+Business Media,2007.
[19] WANG J Q,NIE S P.Application of atomic force microscopy in microscopic analysis of polysaccharide[J].Trends in Food Science & Technology,2018,87:35-46.
[20] LIU W,WANG H,YU J P,et al.Structure,chain conformation,and immunomodulatory activity of the polysaccharide purified from Bacillus calmette Guerin formulation[J].Carbohydrate Polymers,2016,150:149-158.
[21] JEDDOU K B,CHAARI F,MAKTOUF S,et al.Structural,functional,and antioxidant properties of water-soluble polysaccharides from potatoes peels[J].Food Chemistry,2016,205:97-105.
[22] QIAN J Y,CHEN W,ZHANG W M,et al.Adulteration identification of some fungal polysaccharides with SEM,XRD,IR and optical rotation:A primary approach[J].Carbohydrate Polymers,2009,78(3):620-625.
[23] SHEHATA M G,DARWISH A M G,EL-SOHAIMY S A.Physicochemical,structural and functional properties of water-soluble polysaccharides extracted from Egyptian agricultural by-products[J].Annals of Agricultural Sciences,2020,65(1):21-27.
[24] CHIU M H,BEREZOWSKI N S,PRENNER E J.7-DSC applications:Macromolecules[J].Drug-Biomembrane Interaction Studies,2013:237-263.DOI:10.1533/9781908818348.237
[25] PAWAR H A,LALITHA K G.Isolation,purification and characterization of galactomannans as an excipient from Senna tora seeds[J].International Journal of Biological Macromolecules,2014,65:167-175.
[26] KTARI N,BKHAIRIA I,NASRI M,et al.Structure and biological activities of polysaccharide purified from Senegrain seed[J].International Journal of Biological Macromolecules,2020,144:190-197.
[27] YE J F,HUA X,ZHAO Q Y,et al.Chain conformation and rheological properties of an acid-extracted polysaccharide from peanut sediment of aqueous extraction process[J].Carbohydrate Polymers,2020,228:115 410.
[28] KRONGSIN J,GAMONPILAS C,METHACANON P,et al.On the stabilisation of calcium-fortified acidified soy milks by pomelo pectin[J].Food Hydrocolloids,2015,50:128-136.
[29] CAO L,LU W,MATA A,et al.Egg-box model-based gelation of alginate and pectin:A review[J].Carbohydrate Polymers,2020,242:116 389.
[30] CHOI Y,LEE Y,CHANG Y H.Structural and rheological properties of pectic polysaccharide extracted from Ulmus davidiana esterified by succinic acid[J].International Journal of Biological Macromolecules,2018,120:245-254.
[31] NIE X R,LI H Y,DU G,et al.Structural characteristics,rheological properties,and biological activities of polysaccharides from different cultivars of okra (Abelmoschus esculentus) collected in China[J].International Journal of Biological Macromolecules,2019,139:459-467.
[32] LEE Y K,JUNG S K,CHANG Y H.Rheological properties of a neutral polysaccharide extracted from maca (Lepidium meyenii Walp.) roots with prebiotic and anti-inflammatory activities[J].International Journal of Biological Macromolecules,2020,152:757-765.