果胶是一种具有复杂结构的水溶性膳食纤维,可作为增稠剂、稳定剂、乳化剂广泛应用于食品、医药及化妆品行业。根据其酯化度可将果胶分为低酯果胶和高酯果胶。在制备凝胶时,低酯果胶需要的糖含量大大低于高酯果胶,因可用于减肥产品及特殊人群食品的制备而倍受关注。天然来源的低酯果胶极少,往往需要通过高酯果胶脱酯获得。豆腐柴(Premna microphylla Turcz),又名“臭黄荆”,广泛分布于我国长江以南地区,是一种药食兼用野生植物。豆腐柴叶含有丰富的果胶、蛋白质及10多种氨基酸、粗纤维、β-胡萝卜素、黄酮类等营养成分,具有热量低、抗炎、抗衰老、降胆固醇、增强免疫力和排毒等功效,营养价值极高[1]。研究表明,豆腐柴叶中果胶含量达35%,可成为低酯果胶的潜在来源[2]。对豆腐柴低酯果胶进行探究不仅有助于大力开发豆腐柴资源,还可为我国果胶工业的发展提供新方向。
超声破碎提取技术是基于超声波的空化效应发挥作用,超声波促使提取液产生若干气泡,在气泡破裂的瞬间产生巨大的能量致使果胶溶出。超声破碎技术不仅能大幅提升产物得率,还能有效节省提取时间,如WANG等[3]对传统法、超声法提取柑橘果胶的效率进行比较,研究表明超声法在温度降低13.3 ℃,时间缩短37.78%的前提下,果胶得率提高了16.34%。酶法提取果胶可通过降解植物细胞壁,促进果胶基质溶出速率。在工业生产中,酶法提取可使用温和的提取剂,有效避免传统法提取中工业废水带来的污染[4]。因此,将超声破碎技术同酶法提取相结合,可有效提高豆腐柴果胶得率,缩短提取时间。目前,豆腐柴果胶研究主要集中于提取工艺的优化以及如半乳糖醛酸、酯化度等基本理化性质的测定。尚未见到探究超声-酶两步法提取的豆腐柴果胶理化特性及结构表征的研究。
因此,本研究以豆腐柴为原料,采取超声-酶两步法提取果胶,对其半乳糖醛酸、酯化度、色度等基本性质进行检测,通过高效液相色谱法测定其分子质量及单糖组成,采用傅里叶红外扫描(Fourier transform infrared spectroscopy,FTIR)、差示量热扫描 (differential scanning calorimeter,DSC)、热重扫描(Thermogravimetry,TG)、扫描电镜(scanning electron microscope,SEM)、X射线(X-ray diffraction,XRD)等对其结构进行表征,并对其流变特性、抗氧化活性进行探究,以期为豆腐柴低酯果胶的开发及综合利用提供理论依据。
1 材料与方法
1.1 材料与试剂
豆腐柴叶,由巫山县天煜奇叶农业开发有限公司提供。将豆腐柴叶清洗,晾干,微波灭酶,粉碎过60目筛后保存于干燥器中备用。
柠檬酸、柠檬酸钠、草酸铵、乙醇(均为分析纯),成都科龙化工试剂有限公司。
1.2 仪器与设备
SCIENTZ-1500F超声波分散仪,宁波新芝生物科技股份有限公司;LGJ-10真空冷冻干燥机,北京松原华兴科技有限公司;UltraScan Pro测色仪,美国Hunter Lab公司;Phenom Pro扫描电子显微镜,荷兰Phenom World公司;X′Pert PRO X射线衍射仪,荷兰帕纳科公司;TG209F1热重分析仪,德国耐驰公司;Spectrun100傅里叶红外光谱仪、DSC 4000差示扫描量热仪,美国Perkin Elmer公司;MCR302流变仪,奥地利安东帕公司。
1.3 实验方法
1.3.1 豆腐柴果胶的制备
取6 g豆腐柴叶粉末于烧杯中,以1∶60(g∶mL)的料液比加入6 g/L草酸铵溶液。经前期预实验优化,设置超声功率为525 W,超声时间为8 min。将处理后的样液离心(4 000 r/min,15 min),抽滤分离上清液与豆腐柴渣。取豆腐柴渣于烧杯中,加入2%(质量分数)的纤维素酶,以1∶60(g∶mL)的料液比加入0.05 mol/L的柠檬酸-柠檬酸钠缓冲液。在50 ℃下搅拌15 min后,沸水浴灭酶5 min。将样液离心(4 000 r/min,15 min),抽滤,将其上清液与超声处理得到的上清液混合浓缩后,加入浓缩液同体积的乙醇,4 ℃下静置过夜。用少量乙醇、纯水先后洗涤果胶后,冷冻干燥,于干燥器中保存备用。
1.3.2 豆腐柴果胶一般营养成分
采用间羟基联苯法测定豆腐柴果胶中总糖醛酸含量,根据ZOUAMBIA等[5]的方法略做修改;Folin-酚法测定豆腐柴果胶中的总酚含量[6];考马斯亮蓝法测定豆腐柴果胶中蛋白质含量[7];苯酚-硫酸法测定豆腐柴果胶中总糖含量[7];滴定法测定豆腐柴果胶酯化度[8]。
1.3.3 单糖组成分析
参考刘瑶等[9]的方法并略作修改,采用高效液相色谱法测定豆腐柴果胶单糖组成。
取样品于安瓿瓶中,加入三氟乙酸,于110 ℃下酸解8 h,冷却后用氮吹仪吹干,调样品至中性,用超纯水定容。
分别精密称取各标准单糖,将其等摩尔混合,配制成标准单糖混合溶液。分别吸取400 μL标准单糖混合溶液、水解后样品于离心管中,加入乳糖溶液作为内标,接着加入NaOH溶液和1-苯基-3-甲基-5-吡唑啉酮(3-Methyl-1-phenyl-2-pyrazolin-5-one,PMP)溶液,涡旋振荡,70 ℃水浴反应30 min。加入HCl溶液,再加入1 mL 氯仿反复萃取3次,取水层过0.22 μm水系滤膜,待用。
使用C18色谱柱,采用紫外检测器(波长250 nm),以不同体积分数乙腈分别与0.05 mol/L磷酸盐缓冲溶液作为流动相的A相[φ(乙腈)=15%]、B相[φ(乙腈)=40%],流速为0.7 mL/min,进样体积20 μL。
1.3.4 分子质量测定
参考杨文丽等[10]的方法并略作修改。采用高效体积排阻色谱法测定豆腐柴果胶分子质量,取不同分子质量的葡聚糖标准品及果胶样品0.5 mg,分别溶于1 mL超纯水中,过0.45 μm水膜备用。
使用7.8×300 mm i.d.TSK G4000 PWXL-SEC色谱柱、示差检测器,以体积分数为0.02% NaN3溶液为流动相,设置流速为0.6 mL/min,进样量为20 μL,检测时间为30 min,柱温为40 ℃。
1.3.5 色度测定
参考LIEW等[11]的方法,以白板作为参考,使用测色仪测定果胶样品亮度值CIELab坐标(L*、a*、b*),根据公式(1)和公式(2)计算色相角H及色度C。
(1)
(2)
1.3.6 傅里叶红外光谱扫描
参考OGUTU等[12]的方法。取1~2 mg样品于玛瑙研钵中,按质量比1∶50加入干燥的溴化钾粉末,研细后加入压膜器内制片,扫描范围4 000~400 cm-1,扫描次数32次,分辨率4 cm-1。
1.3.7 差示量热扫描
参考EINHORN-STOLL等[13]的方法并略作修改。取1~5 mg样品于铝盘中,用空铝盘作为参考进行DSC检测。在氮气环境下以10 ℃/min速率升温,检测温度范围为20~300 ℃。
1.3.8 热重分析
参考EINHORN-STOLL等[13]的方法并略作修改。取1~5 mg果胶样品,在氮气环境下进行热重检测,以10 ℃/min速率升温,检测温度为50~600 ℃。
1.3.9 扫描电镜分析[14]
取少量豆腐柴果胶样品,使用导电胶将样品黏于样品台上,清理黏附不牢固的样品粉末。将样品置于离子溅射仪中进行喷金处理后,在10 kV加速电压条件下放大观察样品形态特征并拍照。
1.3.10 X射线衍射
参考KAZEMI等[15]的方法并略作修改,将豆腐柴果胶研磨至粉末状后过200目筛。取少量粉状豆腐柴果胶于承载框内,通过压样使其表面平整紧密。X射线检测条件:衍射角为10°~80°,扫描速率为5°/min。
1.3.11 流变特性测定
参考JIANG等[16]的方法并略作修改。将果胶样品溶于去离子水中配成质量浓度为2.5、5、10、15 g/L的溶液。使用平板探头(直径60 mm),在25 ℃下测量剪切速率(0.1~100 s-1)变化下的表观黏度曲线。
选取质量浓度为10 g/L的果胶溶液为样品,使用平板探头(直径60 mm)在25 ℃下进行动态振荡扫描实验,测定频率在0.1~10 Hz的储能模量(G′)与损耗模量(G″)。
1.3.12 抗氧化性活性测定
(1)DPPH自由基清除率[17]
配制不同浓度的果胶溶液及0.1 mmol/L的DPPH乙醇溶液。将样品与试剂按体积比1:1混合均匀后,避光保存30 min。在517 nm下测定样品吸光值A1及纯水、乙醇混合溶液(1∶1)吸光值A0。按公式(3)计算DPPH自由基清除率:
DPPH自由基清除率![]()
(3)
(2)ABTS阳离子自由基清除率[17]
制备25 mL ABTS储备溶液(7 mmol/L),其中过硫酸钾溶液2.45 mmol/L,常温下避光反应16 h得到ABTS溶液。用PBS缓冲液(10 mol/L,pH 7.4)稀释ABTS溶液,使其在734 nm处吸光度为0.70±0.02,得到ABTS工作液。分别取1 mL不同浓度果胶样品溶液与3 mL ABTS工作液混合,避光反应10 min。在734 nm下测定样品吸光度A1,以纯水作试剂空白,测定吸光度为A0。按公式(4)计算ABTS阳离子自由基清除率:
ABTS阳离子自由基清除率![]()
(4)
1.3.13 数据分析
每个实验重复2次,每个样品平行测定3次,结果以平均值±标准偏差表示,使用Origin Pro 9.6作图。
2 结果与分析
2.1 豆腐柴果胶得率及基本性质
豆腐柴果胶得率、基本性质及单糖组成如表1所示。通过超声-酶两步法对豆腐柴果胶进行提取,其得率较高,达到35.53%。LU等[18]通过传统酸提法优化制备豆腐柴果胶,在最佳条件下(90 ℃,2 h),其果胶得率为18.25%。相比之下,超声-酶法制备豆腐柴果胶不仅大幅提升得率,还能有效缩短提取时间。
豆腐柴果胶的L*、a*、b*、DE值分别为81.22、1.76、5.39、19.71,其亮度值较高,颜色与白板间存在肉眼可见的差异,略微偏向黄色以及极其微弱的红色。根据H值(71.86°)可知,豆腐柴果胶偏向黄色[19]。其饱和度C值为5.67,表明其饱和度较低[20]。色差指标表明,豆腐柴果胶颜色较亮,呈现浅黄色。
豆腐柴果胶的总酚、总蛋白含量分别为2.73%、2.84%。总糖、总糖醛酸分别达到22.25%、81.17%。豆腐柴果胶酯化度为16.80%,为低酯果胶。这与PAN等[21]的研究结果基本一致,其研究通过草酸铵加热提取法提取豆腐柴果胶,测得其酯化度为13.69%。
豆腐柴果胶分子质量的Mw为27.24 kDa,Mn为15.30 kDa,Mw/Mn为1.78,表明豆腐柴果胶分子质量较低,且较为均一。WANG等[22]对经不同提取法获得的芒果皮果胶进行了表征,相比酸提取,超声提取的果胶分子量降低43%。ZHANG等[23]探究了超声对果胶结构的影响,结果表明超声波可促进果胶分子量的降低。
豆腐柴果胶单糖组成中半乳糖醛酸(trigalacturonic acid,GalA)含量最高,为42.34%。葡萄糖(glucose,Glc)、L-鼠李糖(L-rhamnose monohydrate,Rha)、D-半乳糖(D-galactosamine, Gal)、L-阿拉伯糖(L-arabinose,Ara)及岩藻糖(L-fucose,Fuc)等是主要的中性单糖组成。其中Glc含量最高,达30.16%,这可能是由于纤维素酶对细胞壁的降解导致。果胶结构可分为同型半乳糖醛酸聚糖(homogalacturonan,HG)、鼠李半乳糖醛酸聚糖Ⅰ(rhamngalacturonan-Ⅰ,RG-Ⅰ)及鼠李半乳糖醛酸聚糖Ⅱ(rhamngalacturonan-Ⅱ,RG-Ⅱ)。通过计算相关单糖比例可以评价果胶结构的线性关系,Rha/GalA比值可评价RG对果胶结构的贡献。(Ara+Gal)/Rha值越高,RG-Ⅰ型结构中侧链越长。GalA/(Rha+Gal+Ara+Fuc)可评价果胶线性度(值越大,线性度越高)。豆腐柴果胶的Rha/GalA值(0.10)介于0.05~1.00,其结构主要为RG-Ⅰ型[24]。其(Ara+Gal)/Rha、GalA/(Rha+Gal+Ara+Fuc)值分别为0.95、1.57。经超声提取的柑橘果胶的(Ara+Gal)/Rha为3.68[3],商业苹果果胶GalA/(Rha+Gal+Ara+Fuc)为4.22[25]。单糖组成分析结果表明豆腐柴果胶结构线性度较低,以含有较短侧链的RG-Ⅰ型为主要结构[21,26]。
表1 豆腐柴果胶得率、基本性质及组成
Table 1 Yield, basic properties and composition of pectin from Premna microphylla Turcz

评价指标测定结果得率/%35.53±1.65L∗81.22±0.24a∗1.76±0.02b∗5.39±0.05DE19.71±0.23H71.86°±0.17°C5.67±0.05总酚质量分数/%2.73±0.34总糖质量分数/%22.25±0.69总蛋白质量分数/%2.84±0.34总糖醛酸质量分数/%81.17±2.70酯化度16.80±1.58Mw/kDa27.24Mn/kDa15.30Mw/Mn1.78Man/mol%0.33±0.06Rha/mol%3.77±0.78GlcA/mol%0.20±0.03GalA/mol%42.34±4.76Glc/mol%30.16±6.15Gal/mol%2.70±0.67Ara/mol%1.23±0.30Fuc/mol%18.92±1.82Rha/GalA0.10±0.01(Ara+Gal)/Rha0.95±0.05GalA/(Rha+Gal+Ara+Fuc)1.57±0.18
2.2 傅里叶红外光谱分析
豆腐柴果胶的红外光谱如图1-a所示。3 194 cm-1处的宽吸收峰对应于多糖中羟基的O—H伸缩振动,2 936 cm-1处的吸收峰对应于CH、CH2、CH3的C—H的伸缩振动。果胶通常在1 600~1 700 cm-1处及1 700~1 800 cm-1处出现特征峰,分别由游离羧基、酯化羧基的振动引起。豆腐柴果胶在1 642 cm-1处具有高透射率,然而并未出现酯化羧基的吸收峰(1 700~1 800 cm-1处),这可能是由于其酯化度较低的原因,这与PAN等[21]研究结果类似。1 403、1 324 cm-1处的吸收峰表明果胶中存在羧基。1 016~1 145 cm-1处的吸收峰是由糖环中的C—O—C、C—O—H振动引起,1 072 cm-1处的信号值主要是由半乳糖、阿拉伯糖等中性糖引起[27]。950~1 200 cm-1图谱较为复杂,被认为是碳水化合物的“指纹”区域[5,28-29]。上述这些特征峰证实了样品中果胶的存在。
2.3 差示量热扫描及热重分析
豆腐柴果胶的DSC、TG图谱如图1-b所示。图中实线为DSC曲线,记录了升温期间反应焓的变化,虚线为TG曲线,记录升温期间果胶重量的改变。根据TG结果可知,豆腐柴果胶随温度提升发生的变化主要可分为40~150 ℃及150~400 ℃2个阶段。第一个阶段中,果胶中的水分受热蒸发引起质量下降,同时,DSC扫描图谱显示其在此阶段(78.6 ℃左右)出现第1个吸热峰。在第二阶段中,DSC图谱中在259.3 ℃出现一个放热峰,TG图谱中显示其质量降低至37.5%。此阶段中,果胶结构受热降解,发生糖苷键断裂、脱羧反应等现象[30-31]。出现峰值的温度越靠右,表明样品具有更好的热稳定性[13]。JIANG等[32]对商品柑橘果胶及柿皮果胶进行了DSC、TG扫描,其吸热峰分别出现在94.05和72.45 ℃,放热峰分别在241.76 ℃和248.26 ℃。相对柿皮果胶而言,豆腐柴果胶吸热峰及放热峰出现位置都更靠右,这表明豆腐柴果胶具有相对较好的热稳定性。
2.4 X射线衍射图谱
豆腐柴果胶的X衍射图谱(图1-c)中有多个尖锐且强烈的峰,在17.0°、30.8°、31.6°、34.4°、38.6°、41.4°、44.3°、47.2°、55.3°出现了明显的尖峰,这与KAZEMI等[15]的结果类似,表明其具有一定的结晶度。相对无定形态果胶,豆腐柴果胶等结晶度较高的果胶具有更大的分子间力,相对更难溶解[11]。受来源及提取方法影响,果胶结晶度有较大差异[31]。如超声提取法可能会增加果胶的结晶度,用超声法制备的茄皮果胶,其X衍射图谱出现尖锐强烈的峰,具有较好的结晶度[33]。
2.5 扫描电镜图像
SEM分析(图1-d)发现,豆腐柴果胶表面相对粗糙,带有一些褶皱,出现较多孔隙。这可能是由于超声及酶处理导致果胶结构破裂,出现孔隙结构。这与XU等[34]测定的结果类似,传统法与超声法提取的柚皮果胶的SEM图像显示,经超声处理过的果胶表面形态发生了较大变化,组织变的多孔并出现了裂缝。
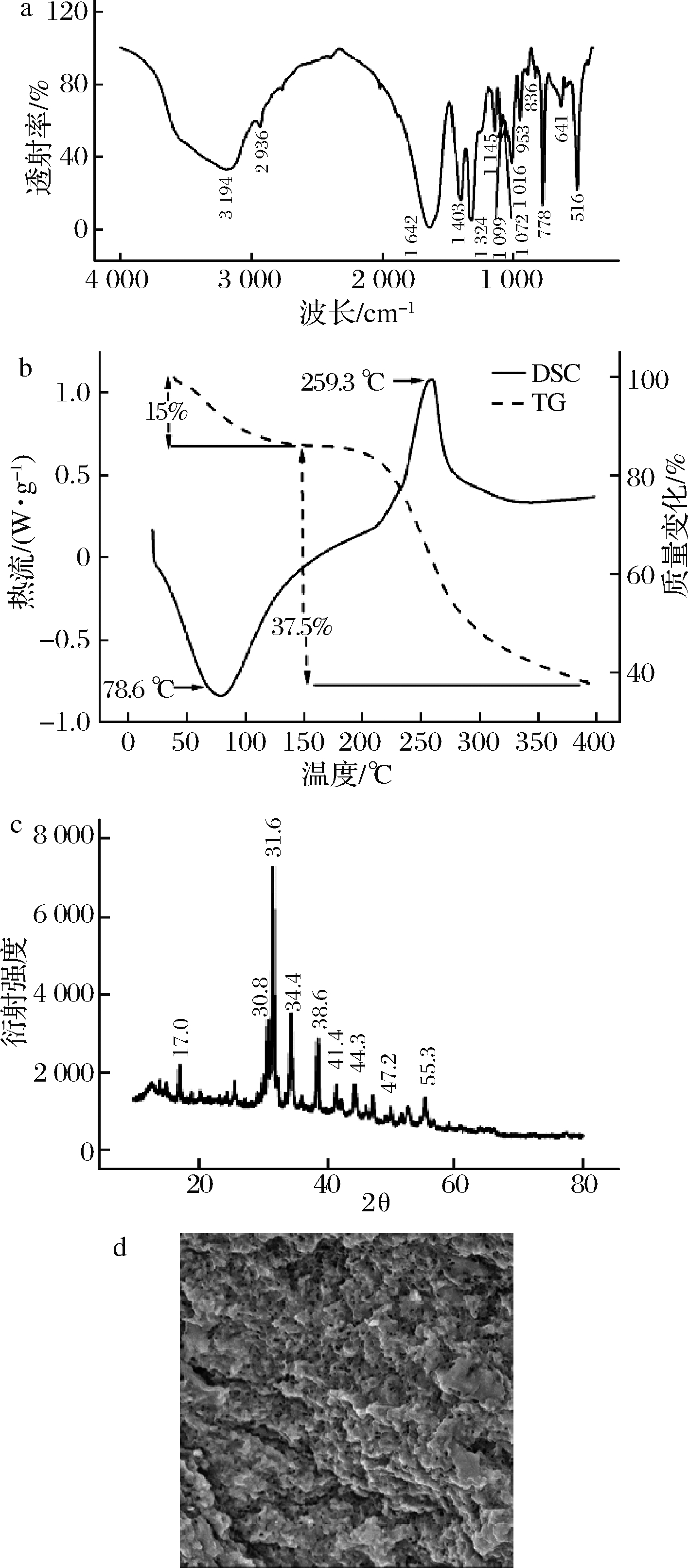
a-FTIR分析;b-DSC、TG图谱;c-XRD图谱;d-SEM图像
图1 豆腐柴果胶的结构表征结果
Fig.1 The structure characterization results of pectin from Premna microphylla Turcz
2.6 流变特性
图2-a、图2-c分别显示了不同浓度豆腐柴果胶、商品苹果果胶溶液黏度随剪切速率变化的过程。随着剪切速率的增加,不同浓度的2种果胶溶液表观黏度均下降,出现剪切变稀现象,具有明显的非牛顿假塑性特征,这主要是因为果胶分子间力受外界力增加而逐渐减弱[35-36]。果胶黏度对浓度具有依赖性,随着果胶浓度的增加,果胶分子间距离缩短,分子间作用力增加,最终果胶的黏度呈现上升的趋势。在低浓度下,果胶分子间相距较远,彼此无法相互作用而难以形成空间网状结构。随着果胶浓度增加,分子间距离缩短进而相互缠结形成网状结构,增加果胶溶液黏度[37]。相对商品苹果果胶,豆腐柴果胶黏度更低。在无金属离子存在下,果胶黏度随其酯化度增加而增加[38]。因此,酯化度可能是导致2种果胶黏度存在差异的原因(前期测得商品苹果果胶酯化度为68.42%)。
选取质量浓度为10 g/L的豆腐柴果胶、商品苹果果胶溶液进行动态振荡扫描流变学研究,测定果胶溶液的储能模量(G′)和损耗模量(G″)如图2-b、图2-d所示。G′、G″分别又被称作弹性模量、黏性模量,反映样品的弹性及黏性。2种果胶溶液的G′均高于G″,机械响应表现为凝胶状,表现出较好的弹性[39]。tanδ为G″与G′的比值,其值越大,表明样品中黏性成分比重更大,样品呈流体状态[40]。豆腐柴果胶tanδ为0.46左右,商品苹果果胶tanδ为0.12~0.23,相比而言,豆腐柴果胶溶液的流体性质更加明显。
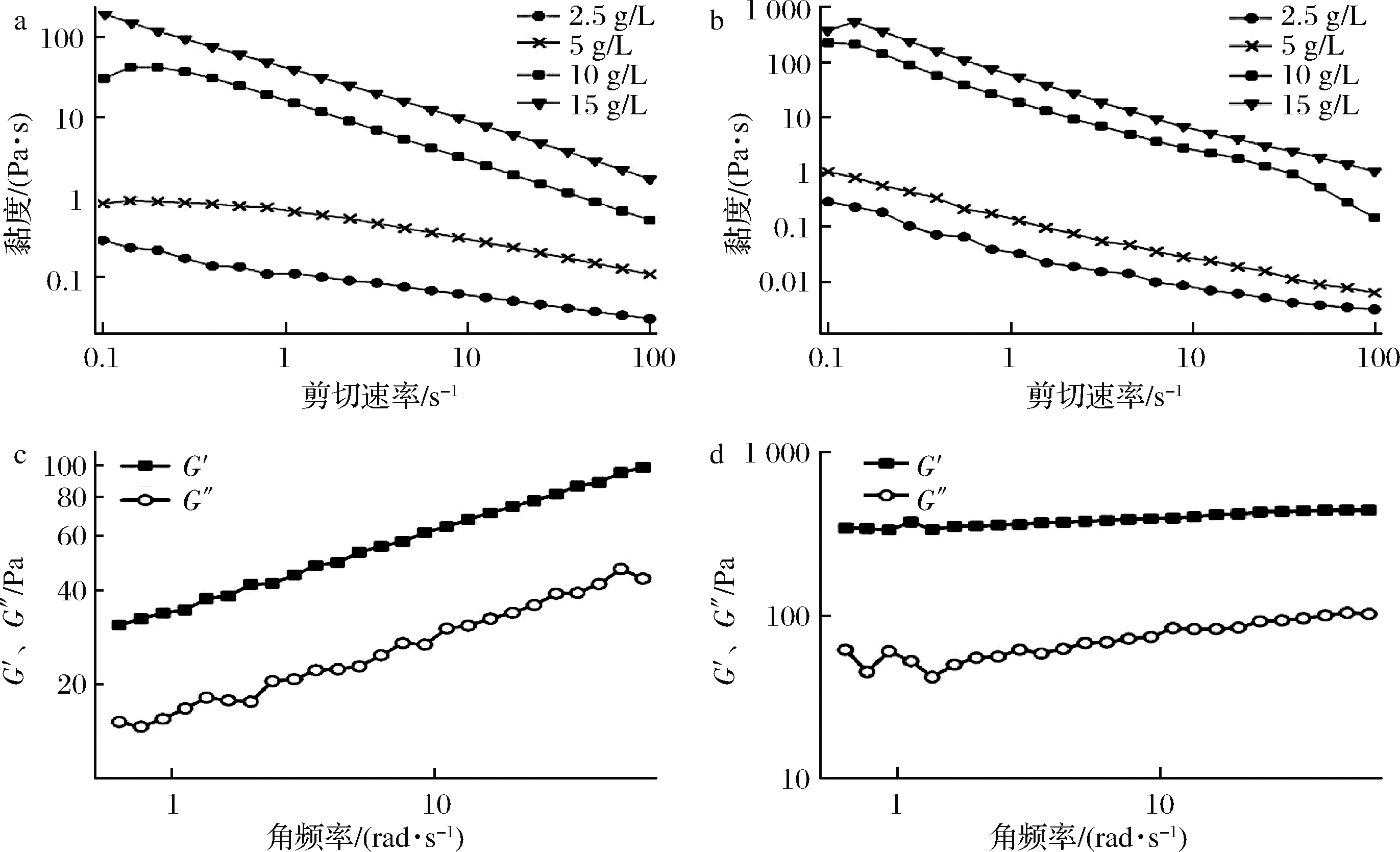
a, c-豆腐柴果胶;b, d-商品苹果果胶
图2 豆腐柴果胶的流变特性
Fig.2 The rheological properties results of pectin from Premna microphylla Turcz
2.7 抗氧化活性
DPPH自由基含有单电子,可稳定地存在于有机溶液中,其乙醇溶液呈现紫色。ABTS与过硫酸钾可生成ABTS阳离子自由基,其溶液呈现深绿色。果胶等多糖具有一定的抗氧化能力,其分子结构中的还原性末端含有半缩醛羟基,可提供质子还原DPPH自由基及ABTS阳离子自由基,将其转换为无色溶液,降低其在最高吸收波长下的吸光值。
选取质量浓度为0.125、0.25、0.50、1.00、2.00 g/L豆腐柴果胶溶液,测定其DPPH自由基及ABTS阳离子自由基清除率,探究其抗氧化能力,结果如图3所示。在0.125~0.50 g/L,豆腐柴果胶抗氧化性表现出强烈的剂量依赖性,浓度越高,其抗氧化能力越好,两者呈现的线性关系较好。在此范围内计算得出豆腐柴果胶溶液DPPH自由基、ABTS阳离子自由基清除率IC50值分别为0.37、0.34 g/L。IC50值越低证明其抗氧化效果越好。巫永华等[41]测定了牛蒡多糖不同组分的DPPH自由基清除率的IC50值为0.62 g/L。郑恒光等[42]提取的杏鲍菇多糖ABTS阳离子自由基清除率IC50超过3 g/L。
在0.50~2.00 g/L,果胶的自由基清除率增加的趋势减缓。在果胶质量浓度达到2.00 g/L时,豆腐柴果胶的DPPH自由基、ABTS阳离子自由基清除率分别达到87.01%、96.08%。MZOUGHI等[43]测定了一种碱蓬属植物(Suaeda fruticosa)果胶的抗氧化活性,其质量浓度为10 g/L时,DPPH自由基、ABTS阳离子自由基清除率分别为69.5%、69%。因此,通过比较可知,豆腐柴果胶具有相对较好的抗氧化活性。

a-DPPH自由基;b-ABTS阳离子自由基
图3 豆腐柴果胶的抗氧化性
Fig.3 The antioxidant activity results of pectin from Premna microphylla Turcz
3 结论
通过超声-酶法提取豆腐柴果胶得率达到35.53%,证明超声-酶法可有效提高得率,缩短提取时间。获得的豆腐柴低酯果胶呈浅黄色,其表面粗糙,含有较多孔隙。就组成成分而言,豆腐柴果胶杂质含量较低,糖醛酸含量高,GalA、Glc、Rha、Gal、Ara及Fuc是其主要的单糖组成。豆腐柴果胶为较均一的低分子质量果胶,以短侧链的RG-Ⅰ型为主要结构,线性度较低,具有一定的结晶度。超声-酶法提取的豆腐柴果胶分子质量较低,可避免大分子质量果胶难以吸收、溶解度低的问题,具有更优异的生理活性。此外,豆腐柴果胶具有相对较好的热稳定性、流变特性及抗氧化能力。
综上所述,豆腐柴果胶可成为商品低酯果胶的良好来源。未来可将研究重点专注于豆腐柴果胶的生理活性,为豆腐柴果胶产品的开发提供新的方向。
[1] 李刚凤, 罗家兴, 李洪艳,等.豆腐柴叶营养成分分析与评价[J].食品研究与开发, 2019, 40(21):62-65.
LI G F, LUO J X, LI H Y, et al.Analysis and evaluation on nutritional composition of Premna microphylla Turcz leaves[J].Food Research and Development, 2019, 40(21):62-65.
[2] 宁海凤. 豆腐柴叶中果胶的提取工艺及其性质研究[D].无锡:江南大学, 2010.
NING H F.Study on extraction technology and properties of pectin from leaves of Premna microphylla Turcz[D].Wuxi:Jiangnan University, 2010.
[3] WANG W J, MA X B, XU Y T, et al.Ultrasound-assisted heating extraction of pectin from grapefruit peel:Optimization and comparison with the conventional method[J].Food Chemistry, 2015, 178:106-114.
[4] ADETUNJI L R, ADEKUNLE A, ORSAT V, et al.Advances in the pectin production process using novel extraction techniques:A review[J].Food Hydrocolloids, 2017, 62:239-250.
[5] ZOUAMBIA Y, ETTOUMI K Y, KREA M, et al.A new approach for pectin extraction:Electromagnetic induction heating[J].Arabian Journal of Chemistry, 2017, 10(4):480-487.
[6] 唐宇, 张小利, 何晓琴, 等.体外模拟胃肠消化过程中蒸汽爆破处理的苦荞麸皮的抗氧化及抗增殖活性[J].食品与发酵工业, 2019, 45(3):107-115.
TANG Y, ZHANG X L, HE X Q, et al.Antioxidantive and anti-proliferative activities of steam exploded tartary buckwheat bran during simulated gastrointestinal digestion in vitro[J].Food and Fermentation Industries, 2019, 45(3):107-115.
[7] 陈光静. 方竹笋的加工废笋渣中多糖的分离纯化和结构解析及其生物活性研究[D].重庆:西南大学, 2019.
CHEN G J.Isolation, purification, structural identification and bioactivity of polysaccharides from bamboo shoots (Chimonobambusa quadrangularis) processing by-products[D].Chongqing:Southwest University, 2019.
[8] 袁敏. 南酸枣果胶的提取及性质的研究[D].广州:华南理工大学, 2016.
YUAN M.Study on extraction and characterization of Choerospondias axillaries pectin[D].Guangzhou:South China University of Technology, 2016.
[9] 刘瑶, 王新然, 赵悦, 等.荞麦皮多糖组成及其抗氧化特性分析[J].食品与发酵工业, 2019, 45(13):134-140.
LIU Y, WANG X R, ZHAO Y, et al.Composition and antioxidant activity of polysaccharides extracted from buckwheat husk[J].Food and Fermentation Industries, 2019, 45(13):134-140.
[10] 杨文丽, 杨波, 杨光.纳豆多糖的理化性质及结构分析[J].食品与发酵工业, 2019, 45(20):132-137.
YANG W L, YANG B, YANG G.Physicochemical properties and structural analysis of natto polysaccharides[J].Food and Fermentation Industries, 2019, 45(20):132-137.
[11] LIEW S Q, TEOH W H, YUSOFF R, et al.Comparisons of process intensifying methods in the extraction of pectin from pomelo peel[J].Chemical Engineering and Processing-Process Intensification, 2019, 143:107 586.
[12] OGUTU F O, MU T H.Ultrasonic degradation of sweet potato pectin and its antioxidant activity[J].Ultrasonics Sonochemistry, 2017, 38:726-734.
[13] EINHORN-STOLL U, KUNZEK H, DONGOWSKI G.Thermal analysis of chemically and mechanically modified pectins[J].Food Hydrocolloids, 2007, 21(7):1 101-1 112.
[14] CHEN X W, QI Y J, ZHU C H, et al.Effect of ultrasound on the properties and antioxidant activity of hawthorn pectin[J].International Journal of Biological Macromolecules, 2019, 131(5):273-281.
[15] KAZEMI M, KHODAIYAN F, LABBAFI M, et al.Pistachio green hull pectin:Optimization of microwave-assisted extraction and evaluation of its physicochemical, structural and functional properties[J].Food Chemistry, 2019, 271:663-672.
[16] JIANG Y, DU J H, ZHANG L G, et al.Properties of pectin extracted from fermented and steeped hawthorn wine pomace:A comparison[J].Carbohydrate Polymers, 2018, 197:174-182.
[17] ROJAS R, ALVAREZ-PÉREZ O B, CONTRERAS-ESQUIVEL J C, et al.Valorisation of mango peels:Extraction of pectin and antioxidant and antifungal polyphenols[J].Waste and Biomass Valorization, 2020, 11(1):89-98.
[18] LU J K, LI J J, JIN R C, et al.Extraction and characterization of pectin from Premna microphylla Turcz leaves[J].International Journal of Biological Macromolecules, 2019, 131:323-328.
[19] SCHIEBER A, HILT P, STREKER P, et al.A new process for the combined recovery of pectin and phenolic compounds from apple pomace[J].Innovative Food Science & Emerging Technologies, 2003, 4(1):99-107.
[20] BERARDINI N, KNÖDLER M, SCHIEBER A, et al.Utilization of mango peels as a source of pectin and polyphenolics[J].Innovative Food Science & Emerging Technologies, 2005, 6(4):442-452.
[21] PAN M K, ZHOU F F, SHI R H, et al.Characterizations of a pectin extracted from Premna microphylla Turcz and its cold gelation with whey protein concentrate at different pHs[J].International Journal of Biological Macromolecules, 2019, 139:818-826.
[22] WANG M M, HUANG B H, FAN C H, et al.Characterization and functional properties of mango peel pectin extracted by ultrasound assisted citric acid[J].International Journal of Biological Macromolecules, 2016, 91:794-803.
[23] ZHANG L F, YE X Q, DING T, et al.Ultrasound effects on the degradation kinetics, structure and rheological properties of apple pectin[J].Ultrasonics Sonochemistry, 2013, 20(1):222-231.
[24] WANG B, DIAO Q Y, ZHANG Z Y, et al.Antitumor activity of bee pollen polysaccharides from Rosa rugosa[J].Molecular Medicine Reports, 2013, 7(5):1 555-1 558.
[25] 任佳琦, 刘昕, 雷琳, 等.苹果中有机酸-果胶复合体系的理化特性及稳定性[J].食品与发酵工业, 2019, 46(12):29-36.
REN J Q, LIU X, LEI L, et al.Physicochemical properties and stability of organic acids/pectin composite system in apple[J].Food and Fermentation Industries, 2019, 46(12):29-36.
[26] RAHMANI Z, KHODAIYAN F, KAZEMI M, et al.Optimization of microwave-assisted extraction and structural characterization of pectin from sweet lemon peel[J].International Journal of Biological Macromolecules, 2020, 147:1 107-1 115.
[27] BAUM A, DOMINIAK M, VIDAL-MELGOSA S, et al.Prediction of pectin yield and quality by FTIR and carbohydrate microarray analysis[J].Food and Bioprocess Technology, 2017, 10(1):143-154.
[28] SHIVAMATHI C S, MOORTHY I G, KUMAR R V, et al.Optimization of ultrasound assisted extraction of pectin from custard apple peel:Potential and new source[J].Carbohydrate Polymers, 2019, 225:115 240.
[29] CHEN R Z, JIN C G, TONG Z G, et al.Optimization extraction, characterization and antioxidant activities of pectic polysaccharide from tangerine peels[J].Carbohydrate Polymers, 2016, 136:187-197.
[30] WANG X, CHEN Q R, LYU X.Pectin extracted from apple pomace and citrus peel by subcritical water[J].Food Hydrocolloids, 2014, 38:129-137.
[31] 王文骏. 柑橘皮果胶超声辅助提取的作用机制研究[D].杭州:浙江大学, 2018.
WANG W J.The research on the mechanism of ultrasound-assisted extraction of pectin from citrus peel[D].Hangzhou:Zhejiang University, 2018.
[32] JIANG Y, XU Y H, LI F, et al.Pectin extracted from persimmon peel:A physicochemical characterization and emulsifying properties evaluation[J].Food Hydrocolloids, 2020, 101:105 561.
[33] KAZEMI M, KHODAIYAN F, HOSSEINI S S.Eggplant peel as a high potential source of high methylated pectin:Ultrasonic extraction optimization and characterization[J].LWT - Food Science and Technology, 2019, 105:182-189.
[34] XU Y T, ZHANG L F, BAILINA Y, et al.Effects of ultrasound and/or heating on the extraction of pectin from grapefruit peel[J].Journal of Food Engineering, 2014, 126:72-81.
[35] HUA X, WANG K, YANG R J, et al.Rheological properties of natural low-methoxyl pectin extracted from sunflower head[J].Food Hydrocolloids, 2015, 44:122-128.
[36] RODSAMRAN P, SOTHORNVIT R.Microwave heating extraction of pectin from lime peel:Characterization and properties compared with the conventional heating method[J].Food Chemistry, 2019, 278:364-372.
[37] LIRA-ORTIZ A L, RESÉNDIZ-VEGA F, R OS-LEAL E, et al.Pectins from waste of prickly pear fruits (Opuntia albicarpa Scheinvar ‘Reyna’):Chemical and rheological properties[J].Food Hydrocolloids, 2014, 37:93-99.
OS-LEAL E, et al.Pectins from waste of prickly pear fruits (Opuntia albicarpa Scheinvar ‘Reyna’):Chemical and rheological properties[J].Food Hydrocolloids, 2014, 37:93-99.
[38] COLODEL C, VRIESMANN L C, DE OLIVEIRA PETKOWICZ C L.Rheological characterization of a pectin extracted from ponkan (Citrus reticulata blanco cv. ponkan) peel[J].Food Hydrocolloids, 2019, 94:326-332.
[39] CHEN Y, ZHANG J G, SUN H J, et al.Pectin from Abelmoschus esculentus:Optimization of extraction and rheological properties[J].International Journal of Biological Macromolecules, 2014, 70:498-505.
[40] 任剑豪, 甘增鹏, 詹浩通, 等.荸荠淀粉糊流变性质的研究[J].中国粮油学报, 2019, 34(11):29-37.
REN J H, GAN Z P, ZHAN H T, et al.et al.Rheological properties of chufa starch paste[J].Journal of the Chinese Cereals and Oils Association, 2019, 34(11):29-37.
[41] 巫永华, 陆文静, 刘梦虎, 等.响应面优化超声波辅助双水相提取牛蒡多糖及抗氧化分析[J].食品与发酵工业, 2020, 46(5):215-223.
WU Y H, LU W J, LIU M H, et al.Optimization of ultrasonic-assisted aqueous two-phase extraction of burdock polysaccharide by response surface design and its antioxidant activities[J].Food and Fermentation Industries, 2020, 46(5):215-223.
[42] 郑恒光, 沈恒胜, 杨道富, 等.杏鲍菇菇头多糖的结构鉴定及生物活性评价[J].食品科学, 2019, 40(22):7-13.
ZHENG H G, SHEN H S, YANG D F, et al.Structural characterization and antitumor activity of crude polysaccharide extracted from the stalk residue of Pleurotus eryngii[J].Food Science, 2019, 40(22):7-13.
[43] MZOUGHI Z, ABDELHAMID A, RIHOUEY C, et al.Optimized extraction of pectin-like polysaccharide from Suaeda fruticosa leaves:Characterization, antioxidant, anti-inflammatory and analgesic activities[J].Carbohydrate Polymers, 2018, 185:127-137.