黑果腺肋花楸 (Aornia melanocarpa) 原产于北美东部和加拿大东部,为蔷薇科腺肋花楸属多年生落叶灌木,又名不老莓、野樱莓等。研究表明,黑果腺肋花楸果实营养物质丰富,如酚类化合物、膳食纤维、糖类、维生素等,其果实中最丰富的次级代谢产物酚类的含量显著高于迄今为止研究的大多数其他浆果和果实,且多酚的组成主要为原花青素聚合物及花青素。在抗癌、抗炎、降血脂及防治心血管疾病等方面有良好的活性[1-3]。目前,国内对其的研究主要集中在繁殖、栽培技术以及生物活性成分研究上,相关产品研究包括果酒、果醋、面条、复合饮料等等[4-7]。作为一种具有极高营养价值与经济价值的新兴小浆果,随着黑果腺肋花楸的推广、产量的逐年递增和人们对功能性食品的重视,果实深加工的价值逐渐被人们所重视,其加工产品会越来越被消费者看好,在我国具有广阔的市场前景。
黑果腺肋花楸成熟为浆果状,故出汁率较高,但同时因为含有大量单宁而味道酸涩,口感较差,因此可以将黑果腺肋花楸果实制成果汁,较好地保留水果原有风味、生物活性和营养物质的同时,口感更好。然而黑果腺肋花楸汁中富含未破碎的植物细胞、果胶、纤维素、半纤维素等大分子,体系成分复杂极易絮凝、下沉出现分层现象,进而影响果汁色泽、风味、口感等,严重影响商品价值,因此在加工过程中必须进行澄清处理。果汁澄清多采用明胶、壳聚糖、果胶酶、纤维素酶等澄清剂来处理。其中壳聚糖能和果汁中带负电荷的胶体相互作用,具有优良的絮凝性能,对蛋白质、果胶、多酚都有一定的作用,可用于果汁澄清,具有快速、简便、易操作等特点,风味、营养成分基本不受影响,且生物稳定性良好[8]。本文旨在通过响应面法研究确定壳聚糖澄清黑果腺肋花楸汁的最佳条件以及黑果腺肋花楸原汁及清汁的品质、抗氧化活性的变化,以期为开发我国丰富的黑果腺肋花楸资源提供技术支撑。
1 材料与方法
1.1 材料与试剂
黑果腺肋花楸,新疆种植基地;壳聚糖(食品级),河南万邦实业有限公司;DPPH自由基,美国Sigma公司;其余试剂均为国产(分析纯),成都市科龙化工试剂厂。
1.2 仪器与设备
MJ-WBL2531H打浆机,广东美的生活电器制造有限公司;PAL-1数显糖度仪,上海上天紧密仪器有限公司;WFJ7200可见分光光度计,尤尼柯(上海)仪器有限公司;PHS-3C酸度计,上海仪电科学仪器股份有限公司;UltraScan PRO 全自动色差仪,美国Hunter Lab公司;HWS-26电热恒温水浴锅,上海齐欣科学仪器有限公司;SYQ-DSX-280B高压灭菌锅,上海申安医疗器械厂。
1.3 实验方法
1.3.1 黑果腺肋花楸汁的制备
黑果腺肋花楸汁的制备工艺如下:
原料挑选→去梗、清洗→胶体磨→粗滤(200目纱布)→原汁→澄清剂澄清→离心→清汁
1.3.2 壳聚糖澄清工艺单因素试验
1.3.2.1 壳聚糖添加量对黑果腺肋花楸汁透光率的影响
取黑果腺肋花楸原汁50 mL于100mL锥形瓶中,分别添加质量浓度0.00、0.10、0.25、0.50、0.75、1.00 g/100mL壳聚糖的量,在40 ℃下澄清60 min,4 000 r/min转速离心10 min,700 nm处测定上清液的透光率。
1.3.2.2 壳聚糖澄清温度对黑果腺肋花楸汁透光率的影响
取黑果腺肋花楸原汁50 mL于100mL锥形瓶中,添加0.5 g/100mL壳聚糖的量,分别在20、30、40、50、60 ℃温度条件下澄清60 min,4 000 r/min转速离心10 min,700 nm处测定上清液的透光率。
1.3.2.3 壳聚糖澄清时间对黑果腺肋花楸汁透光率的影响
取黑果腺肋花楸原汁50 mL于100 mL锥形瓶中,添加0.5 g/100mL壳聚糖的量,在40 ℃温度条件下分别澄清30、60、90、120、150 min,4 000 r/min转速离心10 min,700 nm处测定上清液的透光率。
1.3.3 壳聚糖澄清工艺的响应面优化
在单因素试验的基础上,以透光率(R)为响应值, 以对透光率影响显著的3个因素添加量 (A)、温度 (B) 和时间 (C) 为考察因素, 设计实验,Box-Behnken试验因素与水平见表1。
表1 Box-Behnken试验因素与水平
Table 1 Factors and levels of Box-Behnken experiments design

水平因素添加量(A)/[g·(100mL)-1]温度(B)/℃时间(C)/min-10.25403010.5506000.756090
1.3.4 指标的测定
1.3.4.1 营养成分的测定
色泽:采用全自动色差仪测定;可溶性固形物:采用手持式折光仪测定;总酸:GB/T 12456—2008 《食品中总酸的测定》,pH电位法;单宁:采用Folin-Denis法测定[9];还原糖:采用 3,5-二硝基水杨酸比色法测定[10];总酚:采用 Folin-Ciocalteus 法测定[11];总黄酮:采用硝酸铝络合法测定[12];花色苷:采用pH示差法测定[13];VC:采用分光光度法测定[14]。
1.3.4.2 体外抗氧化活性的测定
DPPH自由基清除率的测定参考文献[15];羟自由基清除率的测定参考文献[16];Fe3+还原能力的测定参考文献[17];总抗氧化能力的测定参考文献[18]。
1.4 数据处理
利用Excel 2010进行数据整理及计算,SPSS 18.0进行数据统计分析,Origin 8.5进行作图。取3次平行实验的平均值作为实验结果。
2 结果与分析
2.1 黑果腺肋花楸汁单因素澄清实验结果
2.1.1 壳聚糖添加量对黑果腺肋花楸汁澄清度的影响
图1表示在40 ℃下不同壳聚糖添加量澄清60 min 透光率的变化。由图1可知,在添加量为0~0.5 g/100mL时,黑果腺肋花楸汁的透光率随着壳聚糖添加量的增加而逐渐增大,当壳聚糖浓度为0.5 g/100mL时透光率达到最大值为92.10%,之后随着壳聚糖用量的增加,透光率呈现下降趋势,这是因为壳聚糖与带负电的可溶性蛋白质、纤维素、果胶、悬浮微粒等物质结合,发生很强的凝聚作用。当壳聚糖过少时,不能使果汁中所有果胶、纤维素等物质被完全絮凝沉淀,澄清效果不明显;而当壳聚糖过多时会导致壳聚糖本身形成一种胶体溶解悬浮在果汁中使透光率下降[19-20]。
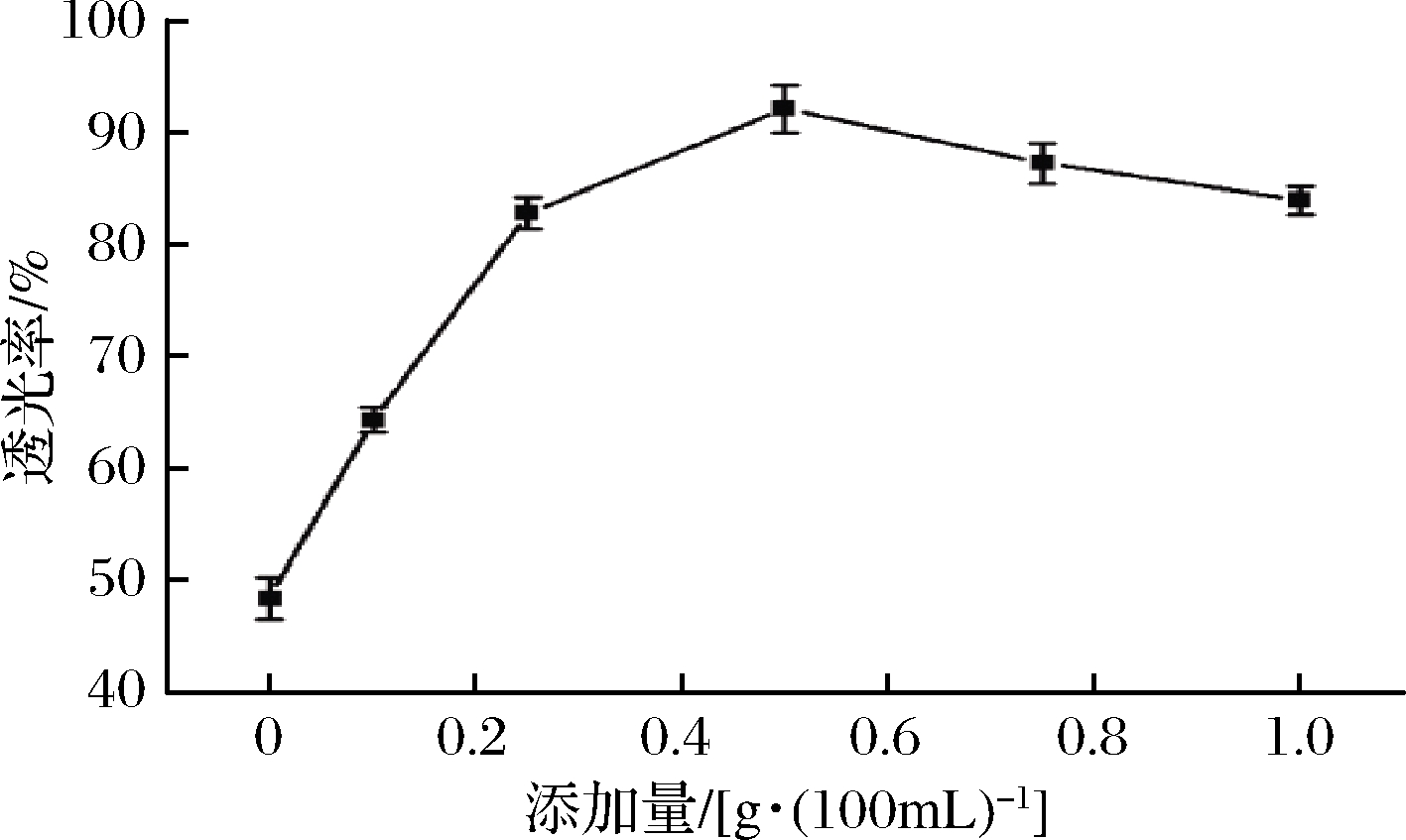
图1 壳聚糖添加量对黑果腺肋花楸汁澄清度的影响
Fig.1 Effect of chitosan addition on transmittance of Aornia melanocarpa juice
2.1.2 壳聚糖澄清温度对黑果腺肋花楸汁澄清度的影响
图2表示在不同澄清温度下壳聚糖添加量为0.5 g/100mL澄清60 min透光率的变化。由图2可知,随着温度的升高,黑果腺肋花楸汁的透光率呈现逐渐增大的趋势,在温度为50 ℃ 时,黑果腺肋花楸汁的透光率达到最大值为 93.73%;此后随着温度的上升透光率略有减小。这是因为壳聚糖为直链多糖,高温可能导致壳聚糖分解,降低了壳聚糖溶液的絮凝效果,从而影响到壳聚糖的澄清效果[21]。
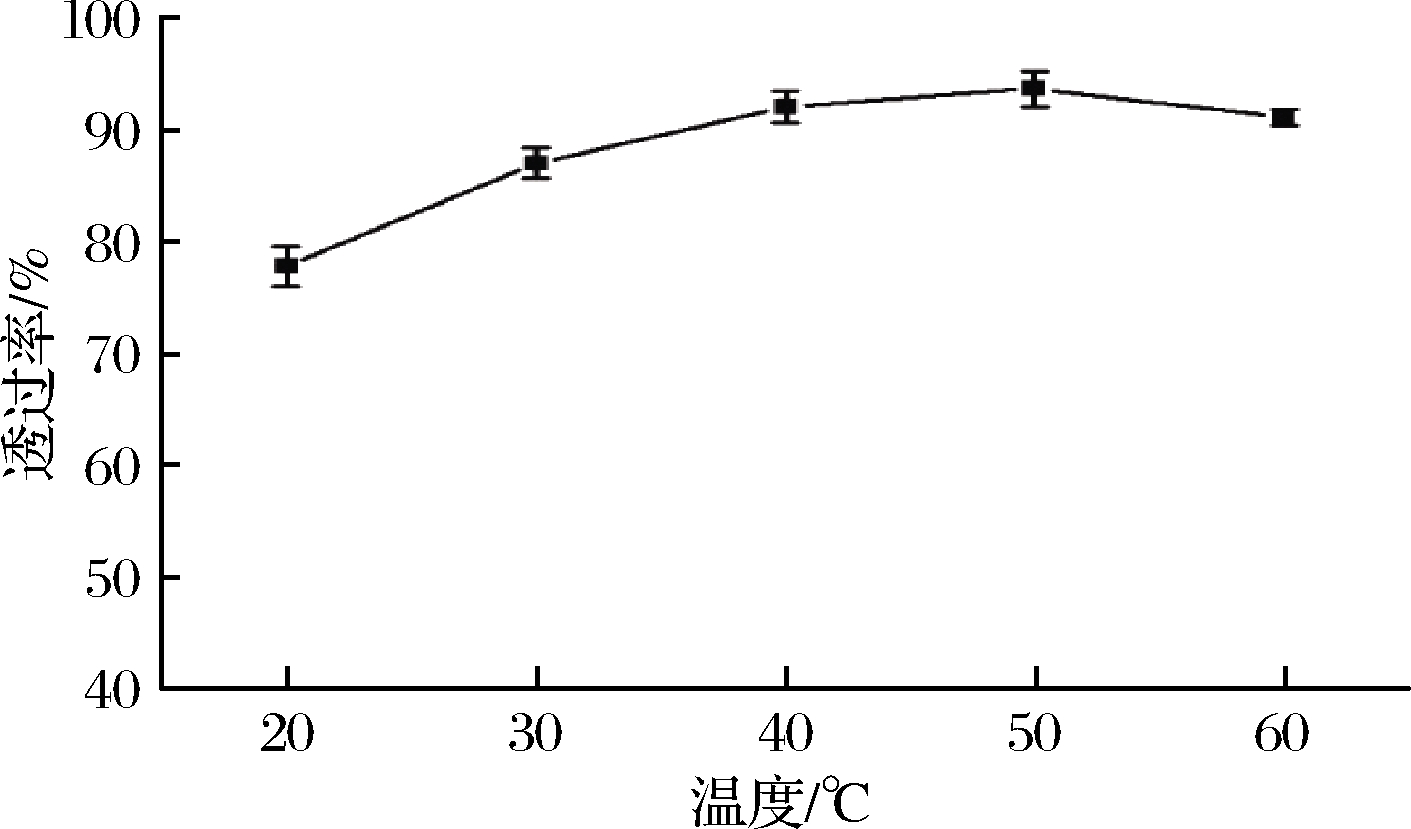
图2 澄清温度对黑果腺肋花楸汁澄清度的影响
Fig.2 Effect of clarification temperature on transmittance of Aornia melanocarpa juice
2.1.3 壳聚糖澄清时间对黑果腺肋花楸汁澄清度的影响
图3表示不同澄清时间0.5 g/100mL壳聚糖浓度40 ℃澄清温度下透光率的变化。如图3所示,在0~60 min时,随着澄清时间的延长,黑果腺肋花楸汁的透光率显著增大,最大达到91.07%,此后随时间的延长透光率反而减小,表明过度延长澄清时间对黑果腺肋花楸清汁澄清效果并无促进作用,反而会对澄清产生抑制作用。其原因是壳聚糖与果汁中果胶等带负电荷物质相互作用,产生絮凝沉淀物的沉降速度有限,沉降需要一定的时间。若絮凝沉淀物在果汁中停留时间过长,进一步积累并形成胶体悬浮液,导致澄清效果下降[20]。
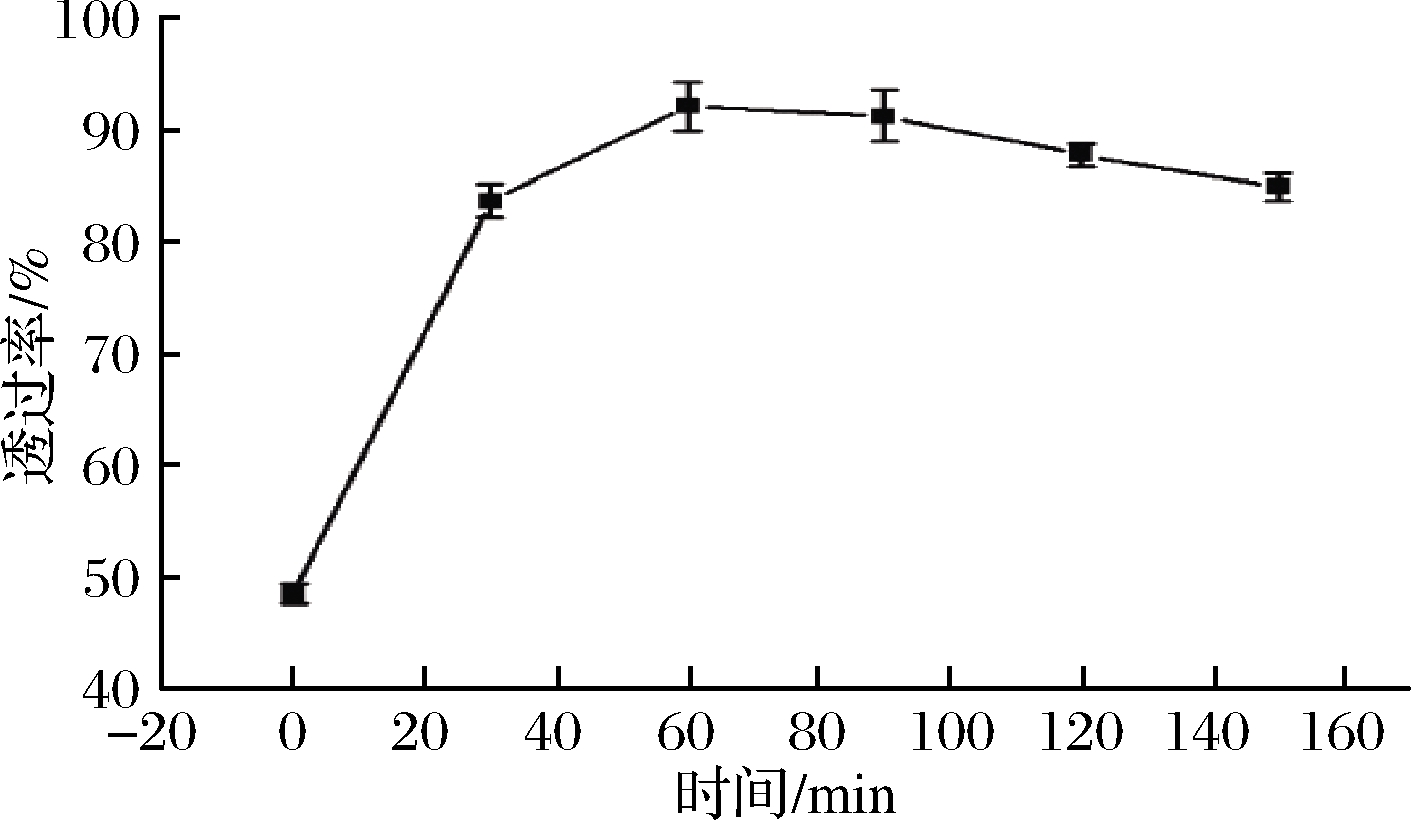
图3 澄清温度对黑果腺肋花楸汁澄清度的影响
Fig.3 Effect of clarification time on transmittance of Aornia melanocarpa juice
2.2 响应面法优化与分析
基于单因素实验结果,并通过设计试验得到响应面结果,所得试验设计及结果见表2。
表2 响应面设计与结果
Table 2 Response surface Box-Behnken design arrangement and experimental results
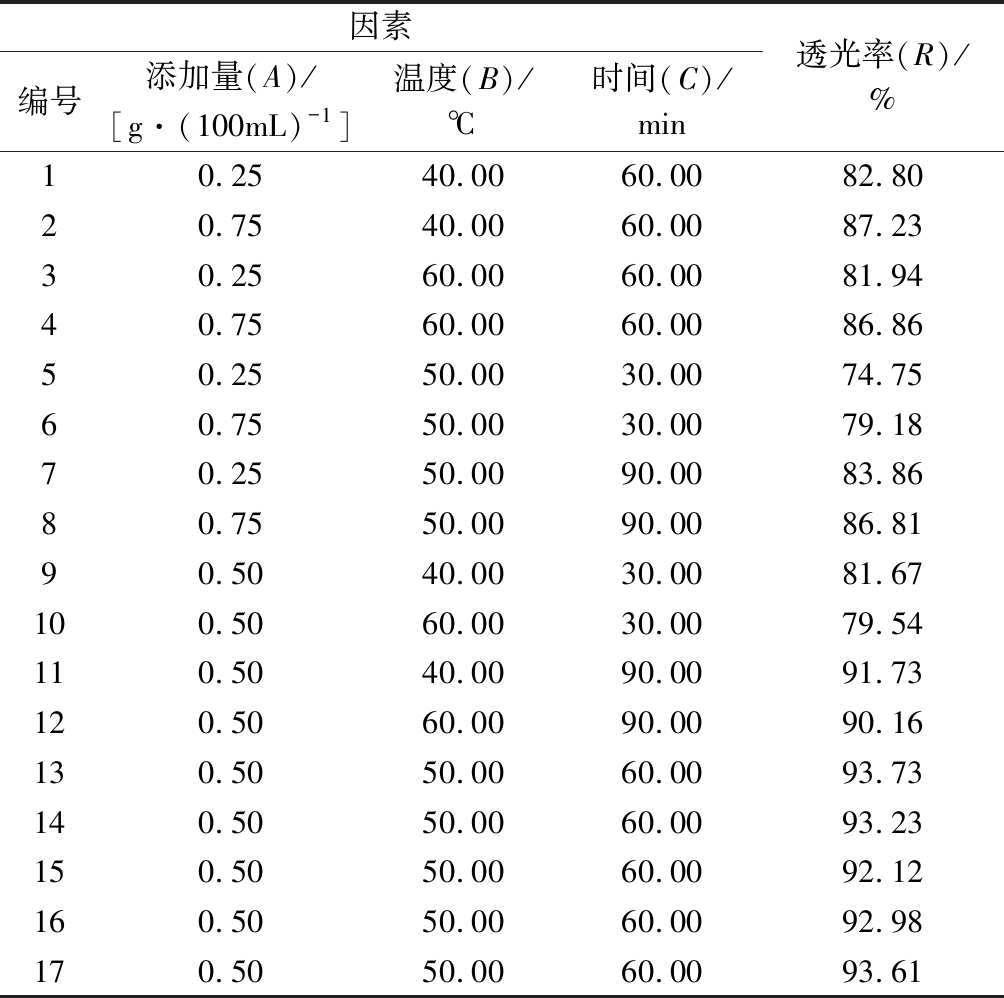
因素编号添加量(A)/[g·(100mL)-1]温度(B)/℃时间(C)/min透光率(R)/%10.2540.0060.0082.8020.7540.0060.0087.2330.2560.0060.0081.9440.7560.0060.0086.8650.2550.0030.0074.7560.7550.0030.0079.1870.2550.0090.0083.8680.7550.0090.0086.8190.5040.0030.0081.67100.5060.0030.0079.54110.5040.0090.0091.73120.5060.0090.0090.16130.5050.0060.0093.73140.5050.0060.0093.23150.5050.0060.0092.12160.5050.0060.0092.98170.5050.0060.0093.61
2.2.1 回归模型的建立及显著性分析
对表中的数据进行多元回归拟合,得到黑果腺肋花楸汁澄清工艺参数的二次回归方程:
R=-13.53+115.89A+1.85B+0.878 35C+0.009AB-0.049AC+0.000 47BC-105.212A2-0.019 5B2-0.006 1C2
对上述模型进行方差分析及回归模型系数显著性检验,结果见表3。结果显示模型P值小于0.000 1,表明该模型达到极显著水平;同时失拟项P=0.223 6>0.05不显著,表明在试验参数范围内,模型合理,实验方法准确可行,可用来推测与分析壳聚糖澄清黑果腺肋花楸汁的试验结果。回归模型的负相关系数R2=0.982 2,说明该模型能预测98.22%的实验数据;方程决定系数![]() 变异系数<3%,表明响应值透光率的实际值与预测值之间具有良好一致性,模型可靠。
变异系数<3%,表明响应值透光率的实际值与预测值之间具有良好一致性,模型可靠。
通过比较F值的大小可知影响黑果腺肋花楸汁透光率的3个因素大小顺序为C(时间)> A(添加量) >B(温度)。用P值来检验回归系数的显著性,其中一次项A、B、C、平方项A2、B2、C2对响应值影响显著(P<0.05),其他因素组合对透光率无显著影响(P>0.05)。
表3 回归方程方差分析表
Table 3 Analysis of variance for the regression equation
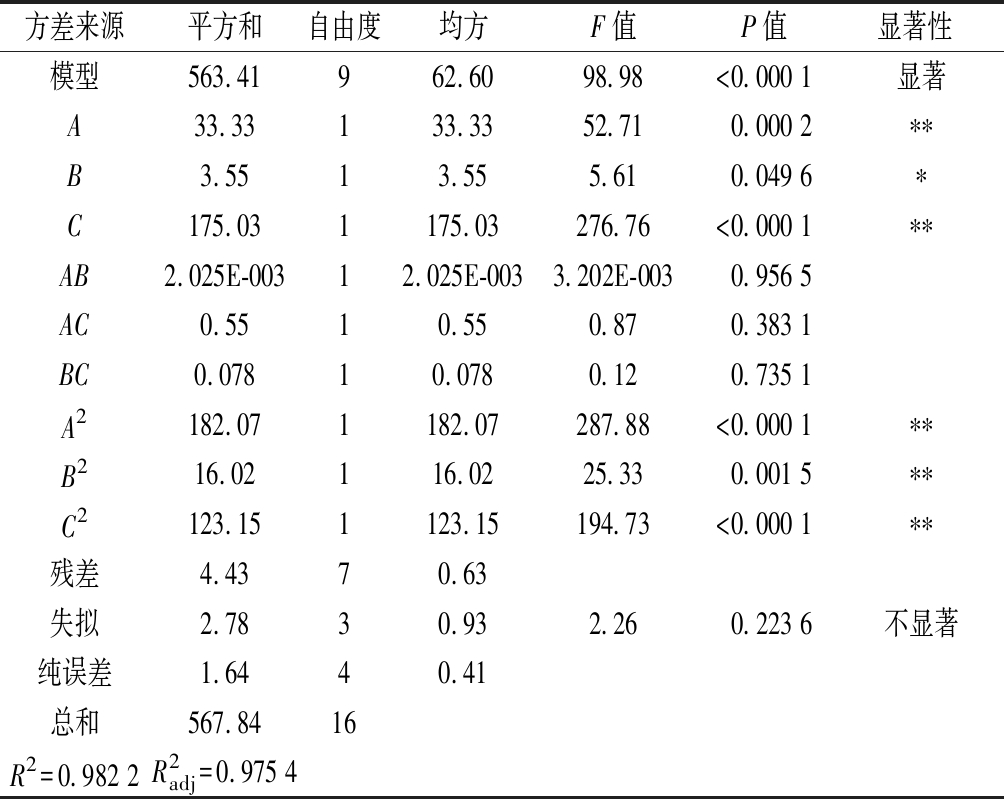
方差来源平方和自由度均方F值P值显著性模型563.41962.6098.98<0.000 1显著A33.33133.3352.710.000 2∗∗B3.5513.555.610.049 6∗C175.031175.03276.76<0.000 1∗∗AB2.025E-00312.025E-0033.202E-0030.956 5AC0.5510.550.870.383 1BC0.07810.0780.120.735 1A2182.071182.07287.88<0.000 1∗∗B216.02116.0225.330.001 5∗∗C2123.151123.15194.73<0.000 1∗∗残差4.4370.63失拟2.7830.932.260.223 6不显著纯误差1.6440.41总和567.8416R2 =0.982 2R2adj=0.975 4
注:P>0.05(不显著);P<0.05(显著,*);P<0.01(极显著,**)
2.2.2 响应曲面分析及最佳工艺研究
由响应面图可以分析出单一自变量或者2个自变量之间的交互作用对响应值的影响,因素之间的交互作用越强,则等高线椭圆形越明显。添加量、澄清时间、澄清温度之间的交互作用的响应面如图4所示,与表3中交互相P值的分析结果一致。
经过响应面法优化,得到壳聚糖澄清黑果腺肋花楸汁的最优条件为添加量0.56 g/100mL,澄清温度48.67 ℃,澄清时间66.67 min,预测透光率为94.06%。根据实际操作的方便性,调整工艺条件为添加量0.56 g/100mL,澄清温度49 ℃,澄清时间67 min。在上述条件下,进行3次验证性试验,得到透光率为93.89%,与模型预测值相差较小,误差为0.17%。说明该模型可靠,能够较好预测壳聚糖澄清黑果腺肋花楸汁的条件与透光率的关系。

a-添加量与温度;b-添加量与时间;c-温度与时间
图4 壳聚糖添加量、澄清温度及时间交互作用对黑果腺肋花楸汁透光率影响的响应面及等高线
Fig.4 Response surface plots and contour lines of effects of interaction between chitosan addition, clarification temperature and time on transmittance of Aornia melanocarpa juice
2.3 黑果腺肋花楸汁可溶性固形物、色泽变化
由表4可知,经过澄清处理得到的黑果腺肋花楸清汁与原汁相比在透光率、可溶性固形物和色泽上都发生了显著变化(P<0.05)。透光率由41.52%提高到93.89%,增加52.37%。清汁的可溶性固形物含量较原汁明显下降,由13.25%到9.97%,这是因为澄清过程中糖、酸、维生素等物质受到不同程度的破坏所导致[8]。色泽是影响黑果腺肋花楸汁品质的一个重要指标,黑果腺肋花楸清汁与原汁相比,L*值和b*值增大,a*值减小,说明亮度增大,红色变浅,黄色加深。
表4 黑果腺肋花楸汁可溶性固形物、色泽变化
Table 4 Changes of soluble solids and color in Aornia melanocarpa juice

处理方式透光率/%可溶性固形物/°BxL∗a∗b∗原汁41.5213.25±0.9832.56±2.4547.95±3.2634.89±2.15清汁93.89∗∗9.97±0.76∗39.03±3.68∗44.61±3.37∗37.86±3.32∗
注:**表示在 P<0.01 水平上,澄清前后差异极显著;*表示在 P<0.05水平上,澄清前后差异显著(下同)
2.4 黑果腺肋花楸汁营养成分变化
黑果腺肋花楸汁经过澄清工艺处理后的活性成分变化如表5所示,可见澄清处理对黑果腺肋花楸汁中的营养成分有一定的影响。单宁属于多酚类化合物,能与蛋白质发生作用从而引起果汁的后混浊,同时单宁含量过高也会导致果汁涩味过重,口感不佳,因此果汁中的单宁含量成为影响清汁稳定性和口感的重要因素[22]。经过澄清处理后的黑果腺肋花楸清汁单宁含量显著下降(P<0.05),降低了28.46%。同时清汁与原汁相比,清汁中的还原糖、总酸、总酚、总黄酮、花色苷及VC含量均有所下降。总酚、总黄酮及花色苷含量分别依次下降17.29%、15.42%、17.87%,但其含量仍处于较高水平。还原糖、总酸及VC的含量也分别降低了25.27%、25.19%、37.20%。导致各成分含量下降的原因应该是由于添加澄清剂壳聚糖处理黑果腺肋花楸汁时,澄清剂在吸附原汁中的蛋白质、果胶等成分的同时也会吸附酚类物质及类黄酮物质,造成其含量下降。
表5 黑果腺肋花楸清汁营养成分变化
Table 4 Changes of nutritional content in Aornia melanocarpa juice

处理方式单宁/(g·L-1)还原糖含量/[mg·(100mL)-1]总酸含量/(g·kg-1)总酚含量/[mg·(100mL)-1]总黄酮含量/[mg·(100mL)-1]花色苷含量/[mg·(100mL)-1]VC/[mg·(100mL)-1]原汁6.7872.19±4.4622.47±1.861 637±7.531 582±4.17789±2.57126.30±4.48清汁4.85∗53.95±5.62∗∗16.81±1.10∗1 354±5.87∗∗1 338±4.28∗∗648±3.61∗∗79.32±2.74∗∗
2.5 黑果腺肋花楸汁体外抗氧化活性变化
2.5.1 DPPH自由基清除能力分析
DPPH自由基在有机溶剂乙醇中是一种稳定的自由基,其孤对电子在 517 nm 附近有强吸收。自由基清除剂可与孤对电子进行配对,使吸收消失或减弱,测定吸收减弱的程度即可反映自由基清除剂的活性[23]。将黑果腺肋花楸汁按照一定浓度稀释后进行测定,黑果腺肋花楸汁在不同浓度下的DPPH自由基清除率见图5。如图5所示,随着样品浓度的升高,DPPH自由基的清除率线性升高后逐渐趋于平缓。但是黑果腺肋花楸原汁的清除率总体上一直高于黑果腺肋花楸清汁。当质量浓度为0.3 mg/mL时,原汁和清汁的清除率均达到最大,分别为99.1%和95.5%。IC50值定义为清除率为50%时所需抗氧化剂的浓度,在体外抗氧化实验中,常用于评价样品清除自由基的能力,所需浓度越低,表明该物质抗氧化性越强。黑果腺肋花楸原汁与清汁DPPH自由基清除率的IC50(mg/mL)分别为0.024、0.027,可见黑果腺肋花楸原汁的清除率强于黑果腺肋花楸清汁。
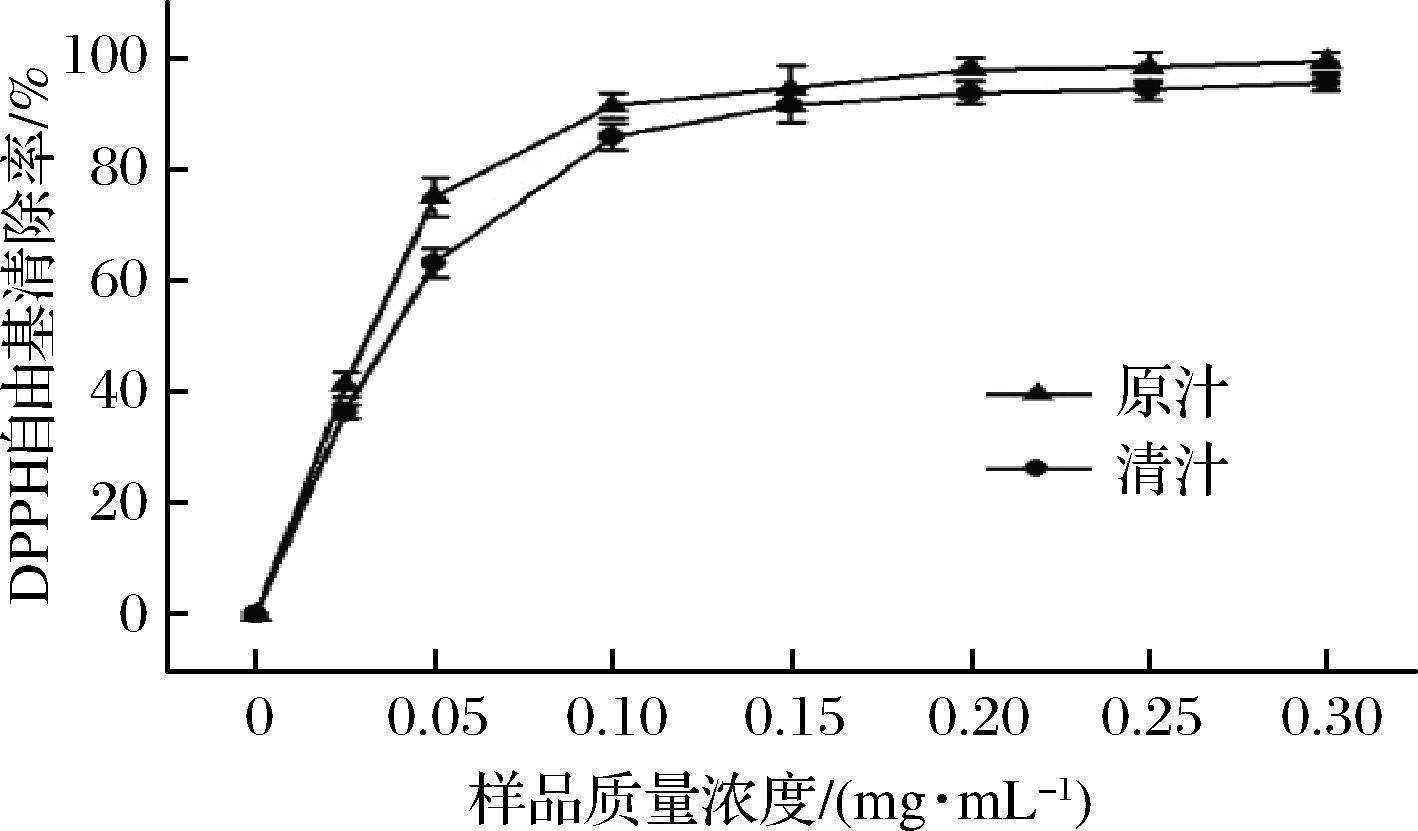
图5 黑果腺肋花楸汁的DPPH自由基清除能力
Fig.5 DPPH自由基 clearance capability of Aornia melanocarpa juice
2.5.2 羟自由基清除能力分析
羟自由基是一类非常活跃的自由基,它能造成糖类、蛋白质、氨基酸、核酸、脂类等物质的氧化性损伤,若待测物能清除羟自由基,则表示其具有抗体内物质氧化的能力[24]。由图6可知,羟自由基清除率与黑果腺肋花楸汁浓度间存在正相关。随着黑果腺肋花楸汁浓度的增加,羟自由基清除率呈先急剧上升,后平缓上升的趋势。当质量浓度为0.2 mg/mL时,黑果腺肋花楸原汁及清汁的羟自由基清除率达到较高水平,分别为82.44%、76.45%。原汁的IC50(mg/mL)值为0.052,显著强于清汁的0.073,说明清汁的羟自由基清除能力弱于原汁。

图6 黑果腺肋花楸汁的羟自由基清除能力
Fig.6 ·OH clearance capability of Aornia melanocarpa juice
2.5.3 Fe3+还原能力分析
铁氰化钾与抗氧化剂发生反应,被还原成亚铁氰化钾,三价铁离子与亚铁氰化钾可以发生作用,产生普鲁士蓝,该物质在700 nm处有特性吸光峰,普鲁士蓝的产量可以被检测出,还原力与抗氧化剂的能力成一定比例,吸光度值越大,说明抗氧化剂的还原力越强[25]。由图7可知,铁离子还原能力随着溶液浓度的增大而增大,呈先急剧上升后缓慢上升趋势。原汁的还原能力始终高于清汁,当质量浓度为0.1 mg/mL时,原汁清除能力为1.809,清汁为1.705。结果表明,黑果腺肋花楸汁具有显著的 Fe3+还原能力和供电子特性,而还原反应的结果通常是终止某些对人体有害的自由基反应,由此可以推断黑果腺肋花楸汁具有益于人体的生物活性。
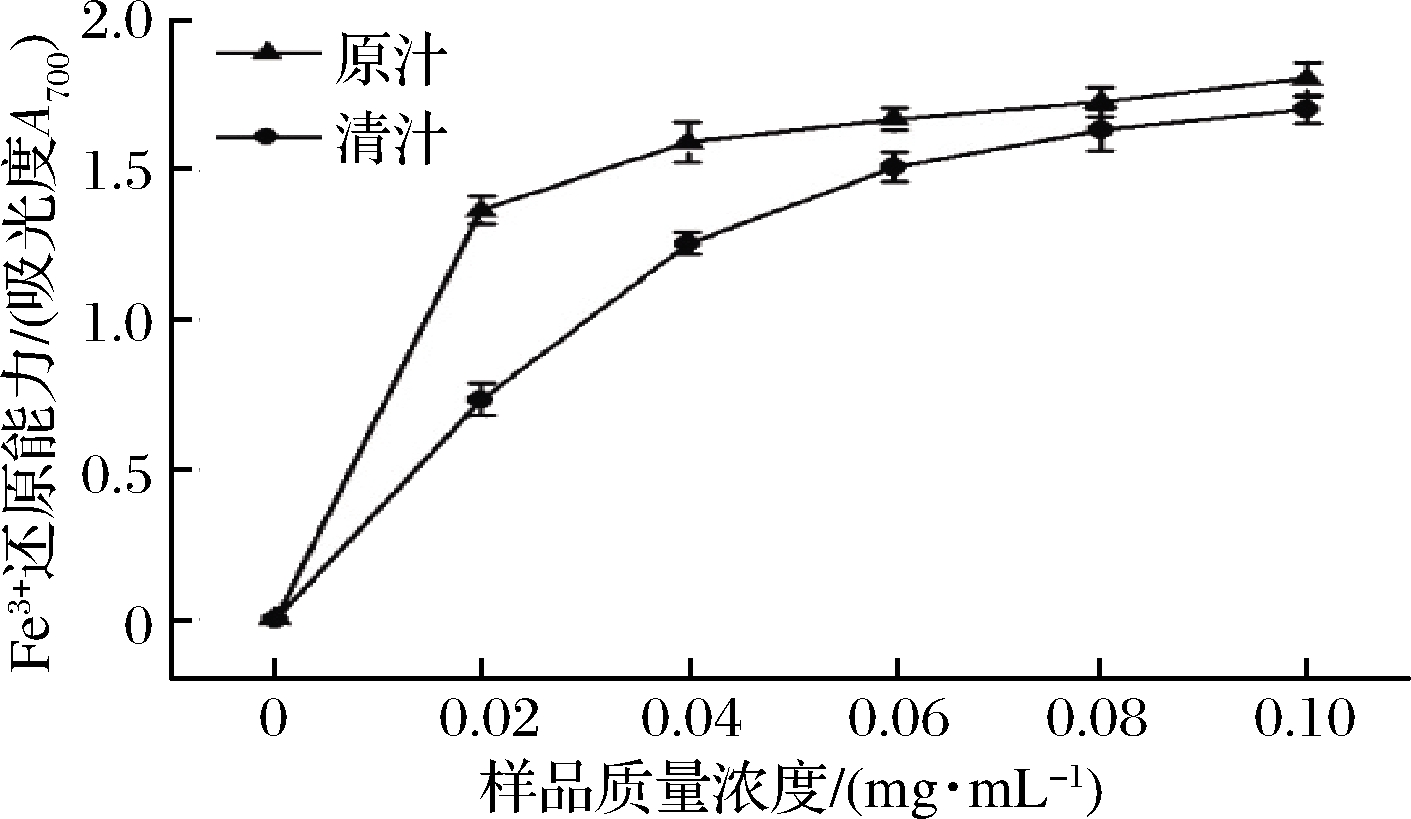
图7 黑果腺肋花楸清汁的Fe3+还原能力
Fig.7 Fe3+reduction ability of Aornia melanocarpa juice
2.5.4 总抗氧化能力分析
试验中用吸光度值来评价各氧化剂的总抗氧化能力,吸光值越高,代表总抗氧化能力越强,试验结果如图8所示。由图8可知,随着样品溶液浓度的增大,总抗氧化活性也均成增加趋势,且黑果腺肋花楸原汁的总抗氧化能力高于清汁。当浓度为0.2 mg/mL时,原汁和清汁的总抗氧化能力分别为2.699和2.142,有显著区别。由此可知黑果腺肋花楸是一种具有开发价值与潜力的抗氧化剂。
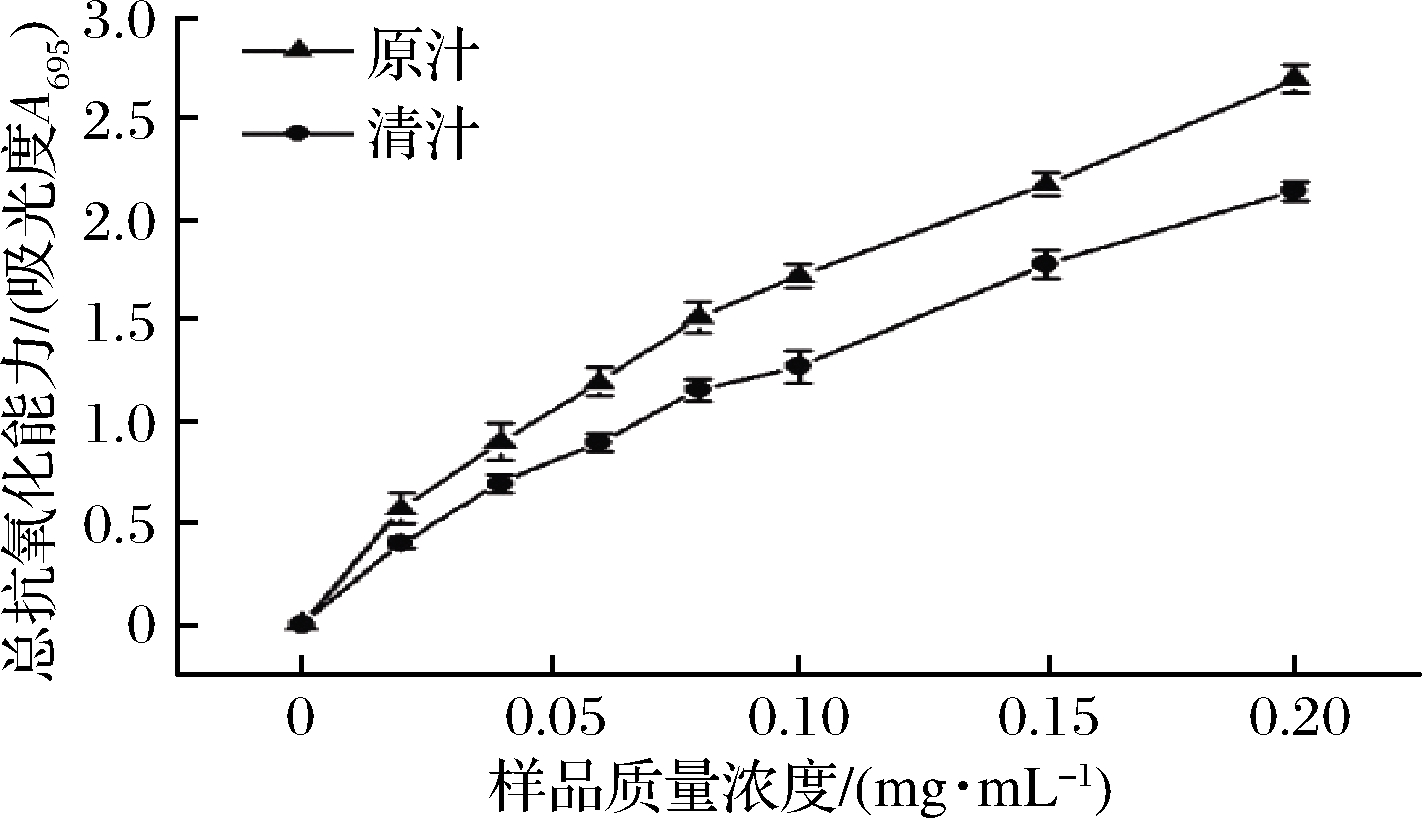
图8 黑果腺肋花楸清汁的总抗氧化能力
Fig.8 Total antioxidant capacity of Aornia melanocarpa juice
2.6 黑果腺肋花楸清汁活性成分与抗氧化能力相关性分析
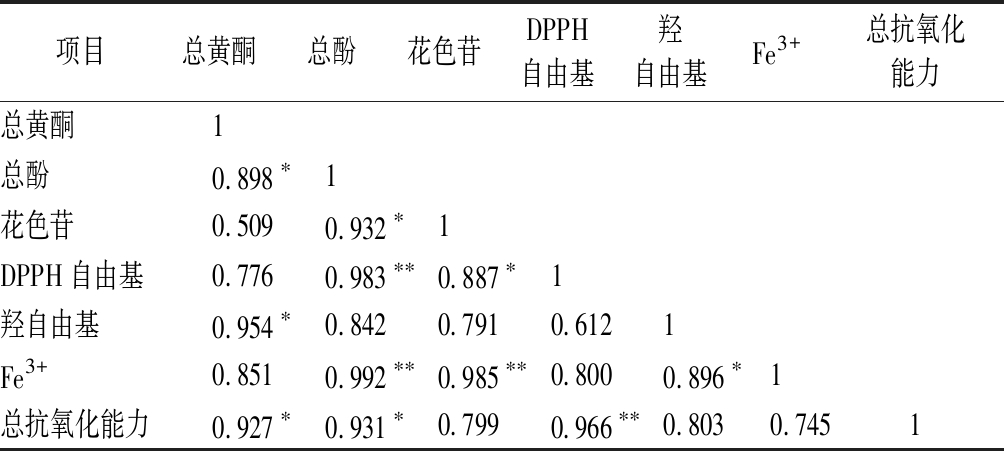
利用SPSS进行Person相关性分析,黑果腺肋花楸清汁主要活性成分与各抗氧化能力评价指标的相关性分析结果如表6所示。可以看出,DPPH自由基清除能力与总酚、花色苷含量显著正相关,相关系数分别为0.983和0.887;羟自由基清除能力与总黄酮含量显著正相关,相关系数为0.954;Fe3+还原能力与总酚、花色苷含量呈现极显著正相关,相关系数分别为0.992和0.985;总抗氧化能力则与总酚、总黄酮含量显著正相关,相关系数分别为0.927和0.931。进一步验证了黑果腺肋花楸清汁的抗氧化能力主要由总酚提供,黄酮、花色苷次之,它们在黑果腺肋花楸清汁自由基清除能力中发挥重要作用。
表6 黑果腺肋花楸清汁的抗氧化能力与主要活性成分的 相关系数
Table 6 Correlation coefficient between antioxidant capacity and main active ingredients of Aornia melanocarpa clear juice
项目总黄酮总酚花色苷DPPH自由基羟自由基Fe3+总抗氧化能力总黄酮1总酚0.898∗1花色苷0.5090.932∗1DPPH自由基0.7760.983∗∗0.887∗1羟自由基0.954∗0.8420.7910.6121Fe3+0.8510.992∗∗0.985∗∗0.8000.896∗1总抗氧化能力0.927∗0.931∗0.7990.966∗∗0.8030.7451
3 小结
本文利用壳聚糖对黑果腺肋花楸汁进行澄清工艺处理,并采用响应面法优化,得到最佳澄清条件为壳聚糖添加量0.56 g/100mL,澄清温度49 ℃,澄清时间67 min,在此条件下黑果腺肋花楸汁透光率可达到93.89%。同时研究表明黑果腺肋花楸清汁与原汁相比各成分含量发生显著变化(P<0.05),总酚、总黄酮和花色苷等活性成分均有所降低,且原汁的抗氧化能力总体上强于清汁。相关性分析表明,黑果腺肋花楸清汁中的总酚含量和黄酮含量与清汁DPPH自由基清除率、羟自由基清除率、Fe3+还原能力和总抗氧化能力呈现较好的相关性。综上,黑果腺肋花楸汁具有较强的抗氧化活性,为以后黑果腺肋花楸汁的实际开发利用提供理论基础。
[1] 焦思桐, 王秋阳, 王超, 等.浆果多酚与黑果腺肋花楸功能作用研究进展[J].现代食品, 2019(12):23-25.
JIAO S T, WANG Q Y, WANG C, et al.Advances in studies on the functional effects of berry polyphenols and aronia melanocarpa[J].Modern food, 2019(12):23-25.
[2] DENEV P, KRATCHANOVA M, PETROVA I, et al.Black chokeberry (Aronia melanocarpa (Michx.) Elliot) fruits and functional drinks differ significantly in their chemical composition and antioxidant activity[J].Journal of Chemistry, 2018, 2018:1-11.
[3] 陈妍竹, 胡文忠, 姜爱丽, 等.黑果腺肋花楸功能作用及食品加工研究进展[J].食品工业科技, 2016, 37(9):397-400.
CHEN Y Z, HU W Z, JIANG A L, et al.Food processing and functional character of Aronia melanocarpa[J].Science and Technology of Food Industry, 2016, 37(9):397-400.
[4] 景安麒, 朱月.基于文献计量的黑果腺肋花楸国内研究现状分析[J].食品工业科技, 2018, 39(23):357-362.
JING A Q, ZHU Y.Analysis of domestic research status of aornia melanocarpa based on literature measurement[J].Science and Technology of Food Industry, 2018, 39(23):357-362.
[5] 刘艳怀, 尹俊涛, 雷勇, 等.黑果腺肋花楸黑枸杞复合饮料工艺研究[J].农产品加工, 2020(10):48-51.
LIU H Y, YIN J T, LEI Y, et al.Processing technology of composite beverage with aronia melanocarpa and Lycium Ruthenicum murr[J].Products Processing, 2020(10):48-51.
[6] 石红艳, 王艳, 商宁, 等.黑果腺肋花楸面条制作工艺研究[J].中国果菜, 2020, 40(5):40-44.
SHI H Y, WANG Y, SHANG N, et al.Study on the processing technology of noodles of Aronia Melanocarpa Elliot[J].China Fruit & Vegetable, 2020,40(5):40-44.
[7] 隋韶奕, 张素敏, 王雪松, 等.黑果腺肋花楸-雪莲果混合型果酒酿造工艺研究[J].农业科技与装备, 2020(2):45-47.
SUI S Y, ZHANG S M, WANG X S, et al.Study on brewing technology for Aronia melanocarpa and Smallanthus sonchifolius mixed win[J].Agricultural Science & Technology and Equipment, 2020(2):45-47.
[8] 许键, 蔡慧农, 倪辉, 等.壳聚糖澄清芦柑果汁工艺条件的优化[J].农业工程学报, 2013, 29(23):268-275.
XU J, CAI H N, NI H, et al.Optimized conditions for clarification of chitosan on ponkan juice[J].Transactions of the Chinese Society of Agricultural Engineering, 2013, 29(23):268-275.
[9] 李静, 聂继云, 李海飞, 等.苹果果实单宁Folin-Denis测定法[J].中国果树, 2006(5):57-59.
LI J, NIE J Y, LI H F, et al.Determination of tannin in apple fruit by Folin Denis method[J].China Fruits, 2006(5):57-59.
[10] SAJID H, AYSHA R, MURTAZA A, et al.Quality assessment of sweet cherry(Prunus avium) juice treated with different chemical preservatives[J].Food Processing & TechnoLogy, 2019, 10(4):1-4.
[11] LAMICHHANE R, KIM S G, POUDEL A,S D, et al.Evaluation of in vitro and in vivo biological activities of Cheilanthes albomarginata Clarke[J].BMC complementary and alternative medicine,2014,14:342.
[12] LUMINITA, D, VIRGIL D, et al.Effects of in vitro gastrointestinal digestion on the antioxidant capacity and anthocyanin content of cornelian cherry fruit extract[J].Antioxidants, 2019, 8(5):114.
[13] 黄晓杰, 田雪瑛, 郭彦玲, 等.桑葚果浆中花色苷及其色泽的热降解动力学[J].食品与发酵工业, 2014, 40(5):77-81.
HUANG X J, TIAN X Y, GUO Y L, et al.Mulberry anthocyanins and its visual colour thermal degradation kinetics[J].Food and Fermentation Industries, 2014, 40(5):77-81.
[14] 马宏飞, 卢生有, 韩秋菊, 等.紫外分光光度法测定五种果蔬中维生素C的含量[J].化学与生物工程, 2012, 29(8):92-94.
MA H F, LU S Y, HAN Q J, et al.Determination of vitamin C content in five kinds of fruits and vegetables by uv spectrophotometry[J].Chemistry Bioengineering, 2012, 29(8):92-94.
[15] 范金波, 蔡茜彤, 冯叙桥, 等.5种天然多酚类化合物抗氧化活性的比较[J].食品与发酵工业, 2014,40(7):77-83.
FAN J B, CAI Q T, FENG X Q, et al.The comparison of five natural phenolic compounds on antioxidant activity in vitro[J].Food and Fermentation Industries, 2014,40(7):77-83.
[16] 綦菁华, 王有年, 于同泉, 等.不同品种桃的酚类活性成分及其抗氧化功能研究[J].食品与发酵工业, 2006, 32(1):103-106.
QI J H, WANG Y N, YU T Q, et al.Study on phenolic active ingredients in various peaches and their antioxidative activities[J].Food and Fermentation Industries, 2006, 32(1):103-106.
[17] RE R, PELLEGRINI N, PROTEGGENTE A, et al.Antioxidant activity applying an improved ABTS radical cation decolorization assay[J].Free Radical Biology and Medicine, 1999, 26(9-10):1 231-1 237.
[18] 潘丽军, 孙潇雅, 姜绍通.紫薯复合饮料的质量指标、营养成分及抗氧化性分析[J].食品科学, 2013, 34(20):165-169.
PAN L J, SUN X Y, JIANG S T.Quality indicators, nutritional composition and antioxidant activities of blended purple sweet potato beverage[J].Food Science, 2013, 34(20):165-169.
[19] 李德燕, 贺红早.不同澄清剂对酥李果酒澄清效果的影响[J].食品研究与开发, 2020, 41(15):62-67.
LI D Y, HE H Z.Effects of different clarifiers on clarification of crisp plum wine[J].Food Research and Development, 2020, 41(15):62-67.
[20] 饶炎炎, 冯建文, 公丽凤, 等.红树莓果汁澄清剂的选择及澄清工艺的优化[J].食品工业科技, 2018, 39(24):209-215;221.
RAO Y Y, FENG J W, GONG L F, et al.Selection of red raspberry juice clarifier and optimization of its clarification process[J].Science and Technology of Food Industry, 2018, 39(24):209-215;221.
[21] 叶清运, 陆玉美, 王鸿祥, 等.壳聚糖对红枣汁澄清效果的影响[J].安徽农业科学, 2016, 44(20):96-98.
YE Q Y, LU Y M, WANG F X, et al.Effects of chitosan on clarification effects of Zizyphus jujube mill juice[J].Journal of Anhui Agricultural Sciences, 2016, 44(20):96-98.
[22] 解利利, 张慜, 孙金才.化学吸附法脱除蓝莓汁中单宁的研究[J].食品与生物技术学报, 2010, 29(6):847-853.
XIE L L, ZHANG M, SUN J C.Syudy on removing tannin in blueberry juice by chimical adsorption[J].Journal of Food Science and Biotechnology, 2010, 29(6):847-853.
[23] 范金波, 蔡茜彤, 冯叙桥, 等.咖啡酸体外抗氧化活性的研究[J].中国食品学报, 2015, 15(3):65-73.
FAN J B, CAI Q T, FENG X Q, et al.Studies on the antioxidant activity in vitro of caffeic acid[J].Journal of Chinese Institute of Food Science and Technology, 2015, 15(3):65-73.
[24] MIRIAM R W, WINTERHALTER P, ESATBEYOGLU T.Phenolic composition, radical scavenging activity and an approach for authentication of aronia melanocarpa berries, juice, and pomace[J].Journal of Food Science, 2019, 84(7).
[25] 张明. 几种体外抗氧化检测方法的评价研究[D].西安:陕西师范大学, 2010.
ZHANG M.Evaluation of several antioxidant detection methods in vitro[D].Xi′an:Shanxi Normal University, 2010.