黑枸杞(Lycium ruthenicum Murr),也称黑果枸杞,茄科枸杞属,为多棘刺灌木,新疆是黑枸杞的主要产区之一,资源丰富,黑枸杞深加工产品主要是黑枸杞干和黑枸杞酒[1-3]。本文研究测定黑枸杞红酒中元素含量的同时进行了主成分分析,确定新疆黑枸杞红酒中的特征微量元素,对新疆黑枸杞红酒地理保护和产地溯源具有重要意义。
微波消解和湿法消解2种前处理方式对元素的检测结果无显著影响。微波消解具有缩短样品制备时间、减少对环境的污染等优点[4-6],本研究前处理采用微波消解作为新疆黑枸杞红酒中多元素检测的前处理方法。目前能满足同时对22种元素进行测定的设备只有电感耦合等离子体质谱仪(inductively coupled plasma mass spectrometry,ICP-MS)[7-9]。ICP-MS具有检出限低、选择性好等优势[10-12],但是其抗干扰能力比较弱,为了提高仪器抗干扰性,本研究在ICP-MS的ICP和碰撞反应池(collision/reaction on cell,CRC)之间附加一级四极杆质量过滤器(the first quadrupole,Q1),与位于CRC后端配置的二级四极杆质量过滤器(the second quadrupole,Q2)组成串联质谱(tandem mass spectrometry,MS/MS),通过Q1和Q2的双重过滤,可以极大提高ICP-MS抗干扰能力和分析灵敏度[13],采用电感耦合等离子体串联质谱(inductively coupled plasma tandem mass spctrometry,ICP-MS/MS)对新疆黑枸杞红酒中多元素进行测定。
主成分分析是一种简化数据集的技术,经常用于减少数据集的维数,同时保持数据集的对方差贡献最大的特征,从而充分反映总体信息[14],主成分分析广泛用于食品的地理保护和产地溯源[15]。本文采用微波消解为前处理,利用ICP-MS/MS检测新疆黑枸杞红酒中22种微量元素含量,采用SPSS 25软件对检测结果进行微量元素主成分分析,确定新疆黑枸杞红酒中的特征微量元素,为新疆黑枸杞红酒的产地溯源保护和地理标志保护提供理论依据。
1 材料与方法
1.1 材料与试剂
市购2017年印象野生黑枸杞红酒187 mL装(原料:黑枸杞、焦亚硫酸钠,类型:干型)、2018年梦凡黑枸杞红酒375 mL装(原料:黑枸杞、焦亚硫酸钠,类型:干型)、2013年中葡黑枸杞红酒187 mL装(原料:黑枸杞焦亚硫酸钠、类型:干型),产地:新疆昌吉,原料产区:新疆昌吉地区种植园。
多元素混合标准物质IV-STOCK-4(含Pb、As、Hg、Cd、Cr、Ni、Al、Cu、Mn、Fe、Sb、Sn、Li、Sr、Zn、Se、Ba、Ag,各元素含量均为1 000 μg/mL),K、Ca、Na、Mg单元素标准物质(1 000 μg/mL),北京标准物质研究中心;硝酸(优级纯)、高氯酸(优级纯),国药集团化学试剂有限公司;实验用水为电导率≤0.08 μS/cm的超纯水;所有玻璃器皿及聚四氟乙烯消解內罐均需用硝酸溶液与水体积比1∶5浸泡过夜,用自来水反复冲洗,再用超纯水冲洗干净。
1.2 仪器与设备
iCAP RQ电感耦合等离子体串联质谱,美国Thermo Scientific公司;TOPEX微波消解仪,上海屹尧仪器科技发展有限公司;GTSONIC-D6超声波清洗仪,广东固特超声股份有限公司;BSA124S-CW分析天平,赛多利斯科学仪器(北京)有限公司;Milli-Q Element纯水器,美国Millipore公司;GT-400赶酸仪,上海屹尧仪器科技发展有限公司;φ180 mm数显可调式电热炉,上海力辰仪器科技有限公司。
1.3 实验方法
1.3.1 样品前处理
用移液枪分别吸取1 mL黑枸杞红酒到聚四氟乙烯消解罐和50 mL三角瓶中,用于微波消解和湿法消解。消解罐中加入5 mL硝酸,三角瓶中加入10 mL硝酸、0.5 mL高氯酸,进行微波消解和湿法消解,微波消解结束后放入赶酸器中进行赶酸,赶酸至0.5 mL左右取出,湿法消解至溶液剩余0.5 mL取下,将消解样品放在通风橱中至室温,用超纯水冲洗3次以上定容至10 mL离心管中,因为新疆黑枸杞红酒中固形物含量较高,为防止固形物堵塞ICP-MS/MS采样锥锥孔,样品过0.45 μm滤膜后备用。同时做好2种前处理方式空白样品。
1.3.2 仪器及工作参数
微波消解参数:控温120~180 ℃、时间45 min、压力<2.0×106 Pa、爬升3 min、保持3 min、最大功率1 600 W、工作功率200 W;电热炉参数:控温120~200 ℃、时间30~40 min、最大功率2 000 W、工作功率100~200 W;ICP-MS/MS参数:KED电压3 V、RF功率1 600 W、等离子体气流量16 L/min、雾化室温度1.25 ℃、雾化器流量1.1 L/min、辅助气流量1.80 L/min、碰撞反应池气流量(O2)、扫描次数3、蠕动泵转速100.0 r/min、离子电压7.75 V、灵敏度7Li:330 000,89Y:380 000。
1.3.3 标准溶液的配制
本次试验根据前期预测试验得到新疆黑枸杞红酒中元素含量数据,决定配制高低2组系列浓度标准曲线,选用K、Ca、Na、Mg单元素标液配制高质量浓度系列混合标液0.0、20.0、40.0、60.0、80.0、100.0 μg/L系列1(STD1),多元素混合标准物质IV-STOCK-4(含Pb、As、Hg、Cd、Cr、Ni、Al、Cu、Mn、Fe、Sb、Sn、Li、Sr、Zn、Se、Ba、Ag)配制低质量浓度混合标液0.0、5.0、10.0、15.0、20.0、30.0 μg/L系列2(STD2)。
1.3.4 黑枸杞红酒元素测定
采用配制的STD1和STD2系列混合标准工作溶液,运用参数条件优化后ICP-MS/MS进行测定,以标准工作液浓度为横坐标,元素响应值为纵坐标,获得各元素校准曲线,在相同分析条件下对样品和空白溶液进行测定。同时通过内标混合T型接头在所有上机测试品中均在线加入20 μg/L的混合内标元素标准溶液对仪器进行在线校正。待测元素较多,质量数差异较大,为了更好地确保仪器的稳定性,消除内差,本次试验选择小、中、大3段质量数元素作为内标[16],选取元素分别为45Sc、51V、89Y、103Rh、186Re、209Bi,内标元素质量浓度为20 μg/L。
1.3.5 数据处理
对混合标准工作溶液检测,检测结果利用ICP-MS/MS的PlasmaLabTM工作站软件(美国Thermo Fisher Scientific公司) 绘制二次线性拟合标准工作曲线。对3种新疆黑枸杞红酒(样品编号1#~3#),每种取5个样品,总计15个样品进行测定,通过绘制二次线性拟合标准工作曲线计算每种微量元素含量。应用SPSS 25软件对检测结果进行主成分分析和确定新疆黑枸杞红酒特征元素分析。
2 结果与分析
2.1 ICP-MS/MS仪器分析
为将本次试验ICP-MS/MS CRC内干扰降到最低,实验采用MS/MS模式,本模式下Q1具有质量过滤功能,仅允许与分析离子具有相同质荷比(m/z)的离子进入CRC,在CRC内通过反应Q2的选择,确保CRC中反应过程和生成产物的一致性。利用分析离子或干扰离子与反应气反应产生的 m/z差异,通过Q2对来自CRC的离子再次过滤消除干扰,能有效实现动态歧视质量筛选,最大程度消除干扰。为评价本次检测新疆黑枸杞红酒多种元素含量的结果准确、稳定,本次试验对每种测定元素进行加标回收实验,计算回收率,同时进行ICP-MS/MS系统稳定性实验。
2.1.1 干扰的消除
ICP-MS工作原理是CRC后连接一个单四级杆,起到了单一质量数筛选功能具有离子导入和通过的作用,在无干扰或者干扰因素较小的时候检测效果比较显著,如Pb、Sn、Ba的检测效果比较好,但是在干扰因素比较强的时候检测灵敏度下降,效果不好。MS/MS检测模式,是在ICP和CRC之间增设一个Q1,与位于CRC后端的Q2构成了双四极杆过滤器。通过Q1实现单一质量数筛选,经过CRC(通入O2、He、H2、NH3等气体)后,再由 Q2做进一步质量数确认,可以消除由多原子离子造成的干扰,从而保证分析结果的准确性。ICP-MS/MS干扰消除工作原理见图1。He池模式下运行的ICP-MS/MS,能有效地测量As和Se的浓度,满足检测要求,但是He模式不适用于带双电荷的离子叠加。镧系元素或稀土元素(rare earth element,REE) 能够形成带双电荷的离子(REE++),这种离子可与As和Se叠加,如,91Zr+叠加到75As16O+,94Mo+叠加到78Se16O+,从而干扰与As和Se的检测。而O2由于其去除干扰能力强,是在ICP-MS/MS检测中用的最广泛的反应气体[21]。在MS/MS质量转移检测模式下,以O2作为反应池气体可避免这些带双电荷的离子发生叠加。在此模式下,分析物以反应产物离子75As16O+和78Se16O+的形式得到测量,其质量数分别移至m/z 91和m/z 94,从而不受初始REE++叠加的影响。MS/MS 模式检测75As+或78Se+时,Q1作为质量过滤器,将其设定为适当的75As+(m/z=75)或78Se+(m/z=78)母离子质量,当75As+和78Se+通过Q1时,Q1有效去除150Nd2+、150Sm2+、151Eu2+和7156Gd2+、156Dy2+、139LaOH2+等多原子离子物质干扰,阻止它们与新的分析物产物离子叠加。进入CRC时通入O2,此时O2与75As+和78Se+目标物质结合生成91AsO+和94SeO+后,设置Q2母离子质量为91AsO+(m/z 91)和94SeO+(m/z 94)再由Q2做进一步质量数确认,消除50Nd2+、150Sm2+、140Ar35Cl+和56Gd2+、156Dy2+、139LaOH2+等多原子离子干扰,从而保证分析结果的准确性。
2.1.2 内标元素选择与稳定性验证实验
根据内标元素(internal standard element,ISTD)的选择是以待测元素与内标元素在等离子体中的行为相似为前提,样品中不含有该元素,且与分析元素质量接近、电离电位相近、化学特征相似的原则[17]选择45Sc、51V、89Y、103Rh、186Re、209Bi为内标元素,5种内标元素涵盖了大、中、小3个元素质量范围,且电离电位和化学特征与待测元素相近。同时在优化实验条件下进行ISTD稳定性实验,连续进样15 h,分析183个样本后查看ISTD信号稳定性。所有样品的ISTD回收率均在初始校准标样值的±20%,这证明实验条件优化后在连续进样15 h后仪器性能稳定。
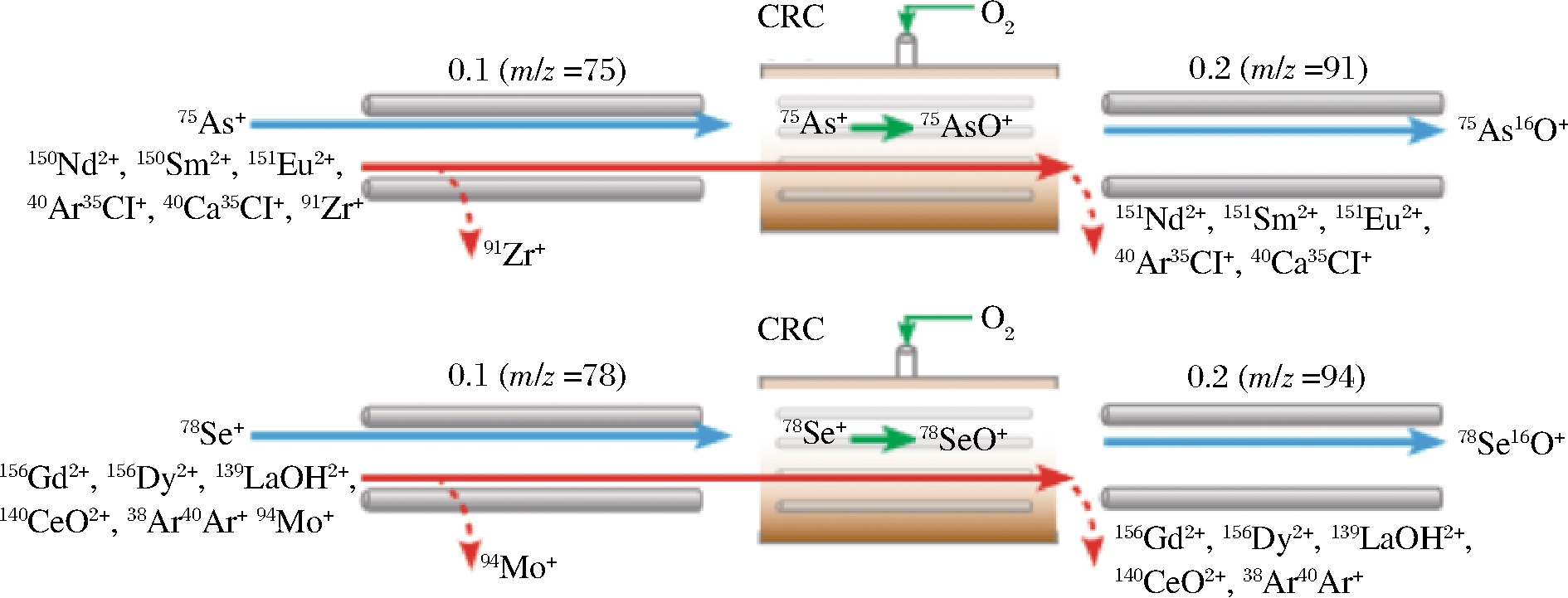
图1 在MS/MS模式下采用ICP-MS/MS消除质谱干扰的 工作原理
Fig.1 Schematic representation of eliminating spectral interference by ICP-MS/MS in the MS/MS mode
2.1.3 线性范围及检出限
本研究在建立起STD1和STD2标准曲线后,分别采用样品加标量STD1为60 μg/L,STD2为10 μg/L考察方法灵敏度。加标样品按上述2种方法进行提取、测定并计算信噪比。以3倍信噪比(S/N=3)对应的添加浓度为检出限,以10倍信噪比(S/N=10)对应的添加浓度为定量下限[18]计算本方法检出限、定量限。结果表明(表1),ICP-MS/MS测得各22种元素R2为0.999 6~1.000、检出限为0.02~0.3 μg/L、定量限为0.1~2.0 μg/L、RSD为1.04%~2.05%,本研究方法检出限、定量限低、精密度,结果稳定,完全满足检验要求。
2.2 黑枸杞红酒中元素含量
2.2.1 两种前处理方式
为确保微波消解和湿法消解2种前处理方式样品来源的唯一性,取3个黑枸杞红酒,每个黑枸杞红酒分成2份(每份处理3个平行样),分别倒入500 mL烧杯中,放在磁力搅拌器上搅拌均匀,分别吸取1 mL样品到微波消解罐和三角瓶中进行微波消解和湿法消解,消解完毕,冷却过0.45 μm滤膜定容到10 mL离心管备用[19]。2种前处理方式检测结果表明(表2),湿法消解和微波消解对检测结果无显著影响(P>0.05)。但是湿法消解过程中加入硝酸和高氯酸混酸污染环境,在消解时容易产生爆炸。微波消解仪具有缩短样品消解时间、减少对环境的污染、改善实验人员的工作环境等优点[20-21],所以本研究采用微波消解作为前处理方法。
表1 分析元素的校准数据、检出限和定量限
Table 1 Calibration data, limits of detection(LODs), and limits of quantification(LOQs) of analytes

元素线性方程相关系数(R2)检出限/(μg·L-1)定量限/(μg·L-1)元素线性方程相关系数(R2)检出限/(μg·L-1)定量限/(μg·L-1) KY=25 327x+1 2231.000 00.31CuY=8 454x+2221.000 00.020.5CaY=22 803x+2 3801.000 00.31MnY=7 871x+1711.000 00.030.1NaY=26 714x+1 7330.999 60.31FeY=12 659x+1 3140.999 80.31MgY=19 283x+2380.999 90.31SbY=19 253x+5790.999 90.030.1PbY=14 906x+1881.000 00.050.2SnY=13 350x+1 2430.999 70.030.1AsY=9 789x+2351.000 00.050.2LiY=18 730x+3641.000 00.20.5HgY=16 013x+2980.999 80.030.1SrY=8 543x+1441.000 00.20.5CdY=17 263x+2431.000 00.050.2ZnY=9 328x+1231.000 00.20.5CrY=8 935x+1 2931.000 00.020.5SeY=8 438x+2431.000 00.030.1NiY=14 898x+1571.000 00.050.2BaY=7 718x+2120.999 90.050.2AlY=2 268x+2 8900.999 80.22AgY=1 1204x+891.000 00.030.1
表2 两种处理方式的检测结果
Table 2 Effect of two sampling pretreatment methods on the analysis
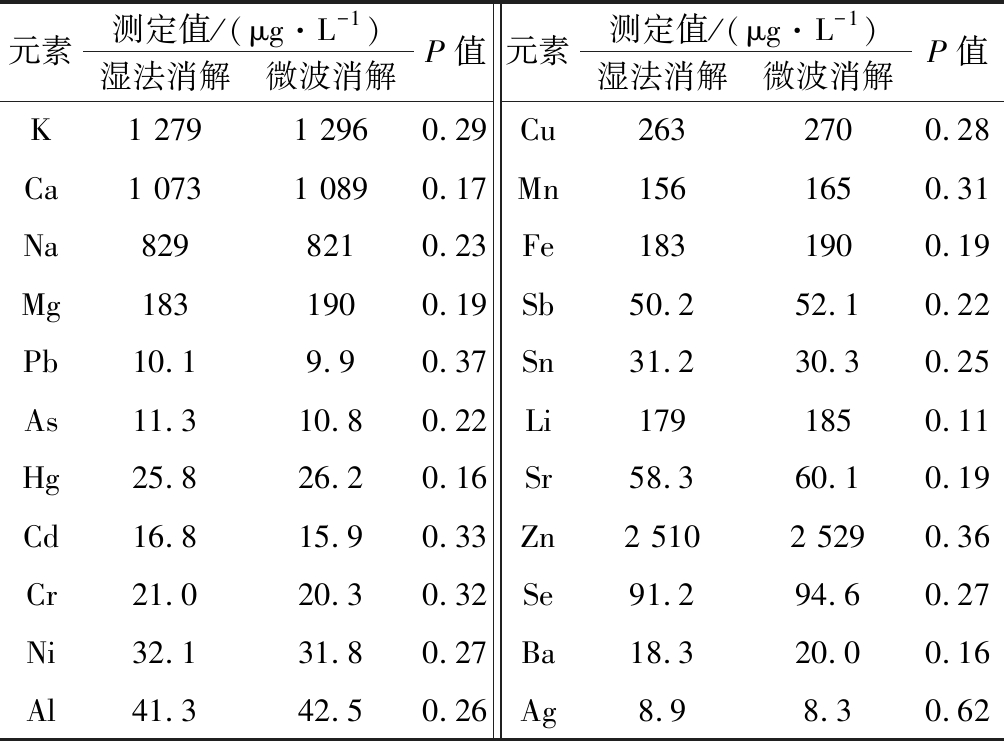
元素测定值/(μg·L-1)湿法消解微波消解P值元素测定值/(μg·L-1)湿法消解微波消解P值K1 2791 2960.29Cu2632700.28Ca1 0731 0890.17Mn1561650.31Na8298210.23Fe1831900.19Mg1831900.19Sb50.252.10.22Pb10.19.90.37Sn31.230.30.25As11.310.80.22Li1791850.11Hg25.826.20.16Sr58.360.10.19Cd16.815.90.33Zn2 5102 5290.36Cr21.020.30.32Se91.294.60.27Ni32.131.80.27Ba18.320.00.16Al41.342.50.26Ag8.98.30.62
2.2.2 方法准确性验证
为保证方法准确性,本研究选取同一黑枸杞红酒样品进行加标实验,对处理好的样品运用参数条件优化,使用ICP-MS/MS方法进行11次平行测定,计算回收率、相对标准偏差(relative standard deviation,RSD),结果表明(表3),样品中各元素加标回收率为89.4%~101.0%,表明方法的准确度好;RSD≤2.02,表明方法的稳定性好,精密度好。
2.2.3 元素含量测定
采用 ICP-MS/MS 对新疆(昌吉)3种(样品种类编号1#~3#)黑枸杞红酒,总计15个样品进行22种微量元素的测定,每个样品重复5次,结果见表4。22种新疆黑枸杞红酒的金属元素中人体所需元素Zn、K、Ca、Na、Mg等含量很高,占所测元素的40.0%。
表3 分析方法的准确度与精密度
Table 3 Accuracy and precision of analytical method
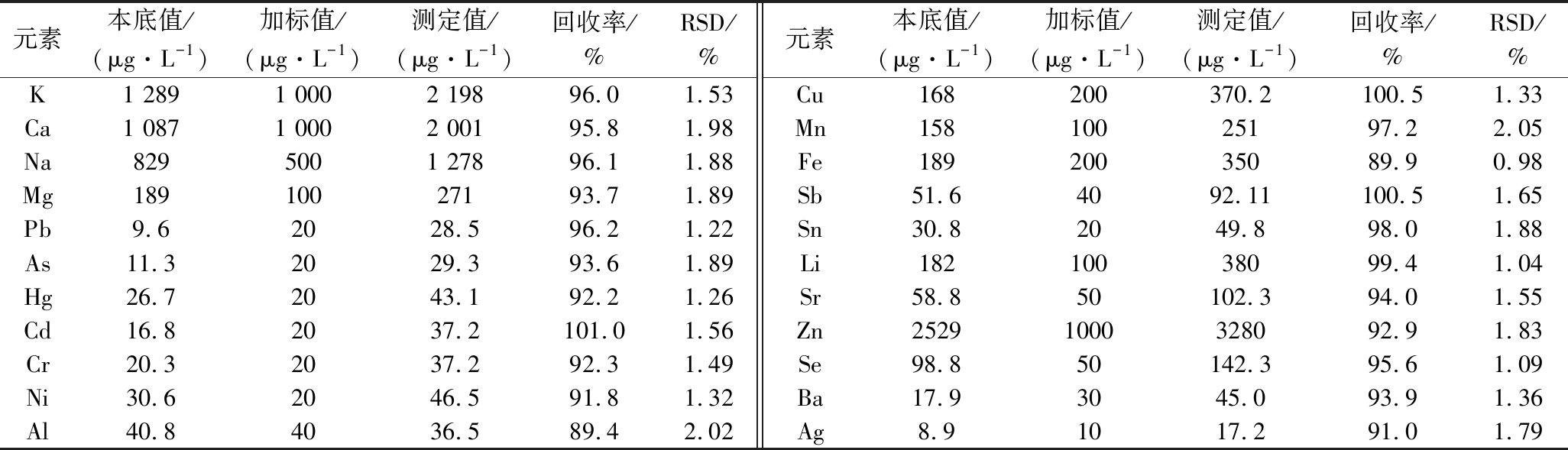
元素本底值/(μg·L-1)加标值/(μg·L-1)测定值/(μg·L-1)回收率/%RSD/%元素本底值/(μg·L-1)加标值/(μg·L-1)测定值/(μg·L-1)回收率/%RSD/%K1 2891 0002 19896.01.53Cu168200370.2100.51.33Ca1 0871 0002 00195.81.98Mn15810025197.22.05Na8295001 27896.11.88Fe18920035089.90.98Mg18910027193.71.89Sb51.64092.11100.51.65Pb9.62028.596.21.22Sn30.82049.898.01.88As11.32029.393.61.89Li18210038099.41.04Hg26.72043.192.21.26Sr58.850102.394.01.55Cd16.82037.2101.01.56Zn25291000328092.91.83Cr20.32037.292.31.49Se98.850142.395.61.09Ni30.62046.591.81.32Ba17.93045.093.91.36Al40.84036.589.42.02Ag8.91017.291.01.79
Hg、Cr、Ag、As、Pb、Ag含量相对较低,对照我国葡萄酒GB/T 15037—2006[22]以及GB 2762—2017《食品安全国家标准 食品中污染物限量》[23],新疆黑枸杞红酒Fe、Cu低于GB/T 15037—2006限量要求,重金属元素的含量远远低于GB 2762—2017中的限量标准。
表4 样品分析结果 单位:μg/L
Table 4 Analytical results of real samples

样品KCaNaMgPbAsHgCdCrNiAlCuMnFeSbSnLiSrZnSeBaAg1#-11 2331 05682921310.211.325.315.321.032.342.816315318050.329.617257.92 50395.323.08.71#-21 2401 08982118111.112.625.916.822.333.643.617216717448.530.718559.32 52290.219.28.31#-31 2391 07381921110.911.524.314.223.630.839.915717218747.332.619058.12 51388.921.17.91#-41 2451 06783319610.312.026.017.019.535.445.317015918349.231.817959.82 53097.619.88.61#-51 2521 05383720810.613.025.815.920.832.741.415117816648.133.519360.32 53793.522.78.02#-11 2831 11683121911.012.123.916.522.234.343.116317317050.830.218858.52 52090.921.88.92#-21 3001 08984519913.213.624.715.124.233.642.318216718649.534.719959.82 53393.220.28.12#-31 2991 09182920712.912.224.914.221.932.140.917717719349.334.619061.22 51995.921.67.22#-41 2791 05583019611.812.025.216.422.233.341.617917018950.834.218362.42 52793.122.88.92#-51 2681 12282221812.613.326.817.921.833.742.417118119650.133.519761.72 53593.322.18.73#-11 2571 17883021811.9129.524.315.323.332.340.817616218848.733.319057.12 53088.623.18.03#-21 2611 15383321812.613.526.915.223.833.139.417915819649.031.518361.22 52289.522.37.43#-31 2891 19984121111.913.225.816.722.632.644.218317320147.330.620063.52 52993.224.07.93#-41 3001 12383222312.712.326.117.923.834.743.717117218950.834.118662.72 54793.121.98.13#-51 2881 17883923111.812.027.016.622.135.043.619215918351.334.220763.42 54089.824.38.4
2.3 主成分分析
2.3.1 黑枸杞红酒的适用性检验
主成分分析是将多个原始变量抽取和压缩成能代表原始变量大量信息的少数综合指标,采用SPSS 25对新疆3种黑枸杞红酒,总计15个样品中22种微量元素的测定结果进行Bartlett′s球状适用性检验,考察原始数据矩阵中各变量是否具有相关性,当原始数据矩阵中各变量具有相关性时适合用于主成分分析研究,反之则不适用[24]。实验结果表明,新疆昌吉产区的3种黑枸杞红酒,总计15个样品中22种微量元素具有线性相关性,能应用于主成分分析研究。
2.3.2 主成分贡献率和选择
对新疆的3种黑枸杞红酒,总计15个样品中22种微量元素的测定结果采用主成分分析法提取公因子,进行特征值和总体方差计算,结果见表5。根据主成分累积方差不低于80%且特征值>1的原则,可以看出累计方差贡献率的80.961%来源于前5个主成分。因此,本实验提取前5个主成分来评判22种微量元素在15个新疆黑枸杞样品中的分布。
表5 主成分分析特征值和总体方差描述
Table 5 Principal component analysis characteristics and total variance explained
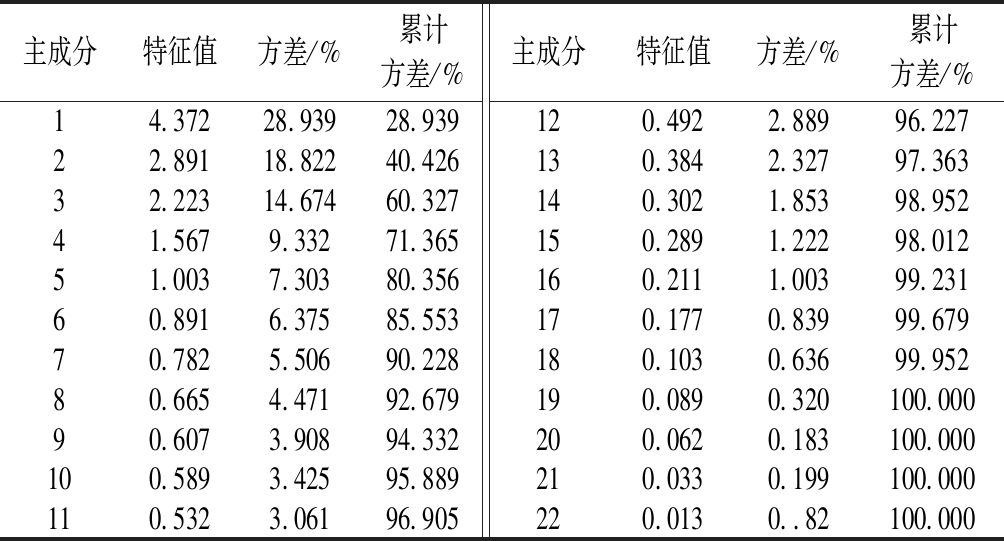
主成分特征值方差/%累计方差/%主成分特征值方差/%累计方差/%14.37228.93928.939120.4922.88996.22722.89118.82240.426130.3842.32797.36332.22314.67460.327140.3021.85398.95241.5679.33271.365150.2891.22298.01251.0037.30380.356160.2111.00399.23160.8916.37585.553170.1770.83999.67970.7825.50690.228180.1030.63699.95280.6654.47192.679190.0890.320100.00090.6073.90894.332200.0620.183100.000100.5893.42595.889210.0330.199100.000110.5323.06196.905220.0130..82100.000
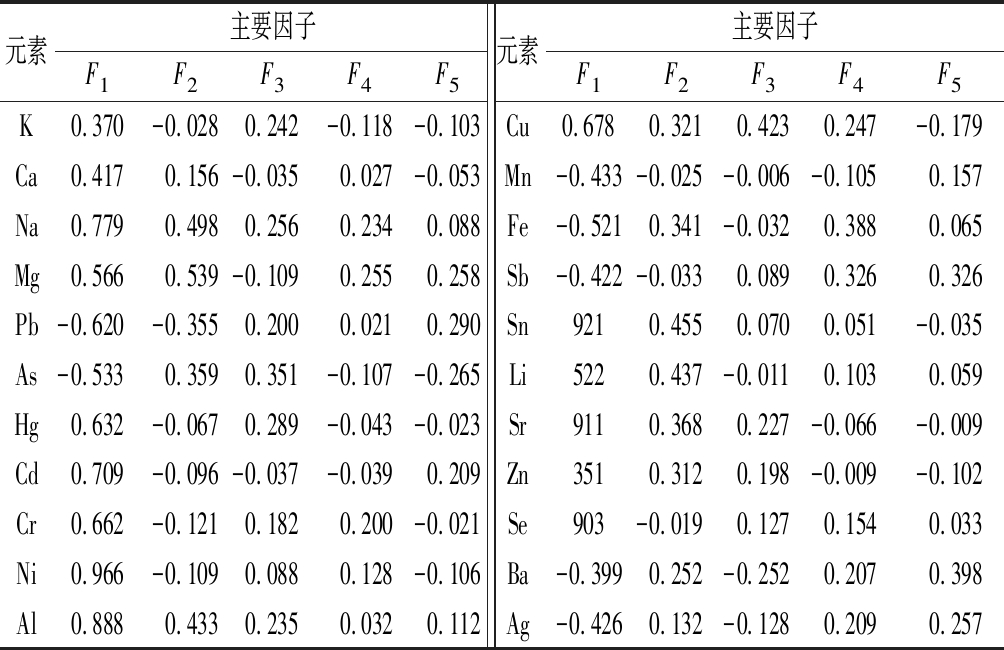
2.3.3 微量元素因子分析
根据新疆黑枸杞红酒微量元素的因子分析结果(表6),分别建立5个主成分因子(F1、F2、F3、F4、F5) 得分模型:
F1=0.370X1+0.417X2+0.779X3+0.566X4-0.620X5-0.533X6+0.632X7+0.709X8+0.662X9+0.966X10+0.888X11+0.678X12-0.433X13-0.521X14-0.422 X15+0.921X16+0.522X17+0.911X18+0.351X19+0.903X20-0.399X21-0.426X22;
F2=-0.028X1+0.156X2+0.498X3+0.539X4-0.355X5+0.359X6-0.067X7-0.096X8-0.121X9-0.109X10+0.433X11+0.321X12-0.025X13+0.341X14-0.033X15+0.455X16+0.437X17+0.368X18+0.312X19-0.019X20+0.252X21+0.132X22;
F3=0.242X1-0.035X2+0.256X3-0.109X4+0.200X5+0.351X6+0.289X7-0.037X8+0.182X9+0.088X10+0.235X11+0.423X12-0.006X13-0.032X14+0.089X15+0.070X16-0.011X17+0.227X18+0.198X19+0.127X20-0.252X21-0.128X22;
F4=-0.118X1+0.027X2+0.234X3+0.255X4+0.021X5-0.107X6-0.043X7-0.039X8+ 0.200X9+0.128X10+0.032X11+0.247X12-0.105X13+0.388X14+0.326 X15+0.051X16+0.103X17-0.066X18-0.009X19+0.154X20+0.207X21+0.209X22;
F5=0.103X1-0.053X2+0.088X3+0.258X4+0.290X5-0.265X6-0.023X7+0.209X8-0.021X9-0.106X10+0.112X11-0.1792X12+0.157X13+0.065X14+0.326X15-0.035X16+0.059X17-0.009X18-0.102X19+0.033X20+0.398X21+0.257X22。
可以看出, F1在 X10、X11、X16、X18、X20,有较大的因子载荷值,分别为0.966,、0.888、0.921、0.903,与对应的 Ni、Al、Sn、Sr、Se有高度正相关性。因此,新疆黑枸杞红酒中所对应的无机特征元素为 Ni、Al、Sn、Sr、Se。
表6 黑枸杞红酒中微量元素的因子分析
Table 6 Factor analysis of trace elements in black wolfberry wine
元素主要因子F1F2F3F4F5元素主要因子F1F2F3F4F5K0.370-0.0280.242-0.118-0.103Cu0.6780.3210.4230.247-0.179Ca0.4170.156-0.0350.027-0.053Mn-0.433-0.025-0.006-0.1050.157Na0.7790.4980.2560.2340.088Fe-0.5210.341-0.0320.3880.065Mg0.5660.539-0.1090.2550.258Sb-0.422-0.0330.0890.3260.326Pb-0.620-0.3550.2000.0210.290Sn9210.4550.0700.051-0.035As-0.5330.3590.351-0.107-0.265Li5220.437-0.0110.1030.059Hg0.632-0.0670.289-0.043-0.023Sr9110.3680.227-0.066-0.009Cd0.709-0.096-0.037-0.0390.209Zn3510.3120.198-0.009-0.102Cr0.662-0.1210.1820.200-0.021Se903-0.0190.1270.1540.033Ni0.966-0.1090.0880.128-0.106Ba-0.3990.252-0.2520.2070.398Al0.8880.4330.2350.0320.112Ag-0.4260.132-0.1280.2090.257
3 结论
以微波消解为前处理,利用ICP-MS/MS测定新疆黑枸杞红酒中 K、Ca、Na、Mg、Pb、As、Hg、Cd、Cr、Ni、Al、Cu、Mn、Fe、Sb、Sn、Li、Sr、Zn、Se、Ba、Ag等22种微量元素,在MS/MS模式下,采用O2作为反应气体,利用质量转移法和原位质量法消除了质谱干扰。该方法检测黑枸杞红酒中Zn、K、Ca、Na、Mg等元素含量很高,占所测元素的40.0%。方法检出限为0.02~0.3 μg/L、样品加标回收率89.4%~101.0%、RSD为1.04%~2.05%,本方法灵敏度高、选择性好、检出限低,结果准确、可靠,完全满足检验要求,适用于新疆黑枸杞红酒中元素含量的测定。采用SPSS 25对3种新疆黑枸杞红酒15个样品测定结果进行主成分分析,提取了5个主成分因子来评判新疆黑枸杞红酒中微量元素的分布,确定了Ni、Al、Sn、Sr、Se为新疆黑枸杞红酒的特征元素。
[1] VETERE A,PRCFROCK D,SCHRADER W, et al.Quantitative and qualitative analysis of three classes of sulfur compounds in crude oil[J].Angew Chem Int Edit, 2017, 56(36):10 933-10 937.
[2] ABEBE G K, BAHN R A, CHALAK A, et al.Drivers for the implementation of market-based food safety management systems:Evidence from Lebanon[J].Food Sci Nutr, 2020, 8(2):1 082-1 092.
[3] NYARUGWE S P, LINNEMANN A R, REN Y, et al.An intercontinental analysis of food safety culture in view of food safety governance and national values[J].Food Control, 2020.DOI:10.1016/j.foodcont.2019.107075.
[4] 焦彧, 冯兰平, 李百蝉, 等.锶同位素在葡萄酒产地溯源中的研究进展[J].中国酿造, 2019, 38(8):9-13.
JIAO Y, FENG L P, LI B C, et al.Advances of strontium isotope in geographical origin trace ability of wine[J].China Brew, 2019, 38(8):9-13.
[5] 贾柳君, 张海红, 王健, 等.采用近红外光谱定量分析葡萄酒发酵液中总酸含量和pH值[J].食品与发酵工业, 2017, 43(2):191-195.
JIA L J, ZHANG H H, WANG J, et al.Determination of total acid and pH in wine fermented liquid by near infrared spectroscopy technology[J].Food and Fermentation Industries, 2017, 43(2):191-195.
[6] 邱会东, 赵波, 张红, 等.食用植物油中重金属分析方法的研究进展[J].中国油脂, 2017, 42(1):76-79.
QIU H D, ZHAO B, ZHANG H, et al.Advance in analysis methods of heavy metals in edible vegetable oils[J].China Oils And Fats, 2017, 42(1):76-79.
[7] 张梦潇, 周文化, 莫华, 等.不同品种紫薯粉鲜湿面条的品质特性及主成分分析[J].食品工业科技, 2020, 41(1):79-85;124.
ZHANG M X, ZHOU W H, MO H, et al.Quality characteristics and principal component analysis of fresh noodles with purple sweet potato flour of different varieties[J].Science and Technology of Food Industry, 2020, 41(1):79-85;124.
[8] 李永娇, 宋川, 张宿义, 等.ICP-MS研究浓香型白酒发酵过程中多种金属元素的变化规律[J].食品工业科技, 2016, 37(17):267-271.
LI Y J, SONG C, ZHANG X Y, et al.Investigation of concentration change of metal elements in the wine lees during fermentation by ICP-MS[J].Science and Technology of Food Industry, 2016, 37(17):267-271.
[9] 马兴, 高健会, 肖亚兵, 等.微波消解-ICP-MS同时测定酒类样品中11种元素[J].食品研究与开发, 2016, 37 (18):155-157.
MA X, GAO J H, XIAO Y B, et al.Determination of 11 elements in wine by ICP-MS with microwave digestion[J].Food Research and Development, 2016, 37(18):155-157.
[10] LIU Z, ZHANG W, ZHANG Y, et al.Assuring food safety and traceability of polished rice from different production regions in China and Southeast Asia using chemometric models[J].Food Control, 2019(99):1-10.
[11] 廖红梅, 覃然, 陈璐, 等.电感耦合等离子体质谱法测定葡萄酒中32种元素的含量[J].食品安全质量检测学报, 2016, 7(12):4 899-4 903.
LIAO H M, QIN R, CHEN L, et al.Determination of 32 kinds of elements in wine by inductively coupled plasma-mass spectrometry[J].Journal of Food Safety and Quality, 2016, 7(12):4 899-4 903.
[12] DOMNG D, XHENG W, WANG W, et al.A new volatiles-based differentiation method of Chinese spirit using longpath gas-phase infrared spectroscopy[J].Food Chemistry, 2014, 155:45-49.
[13] LAO M, COMPANYS E, WENG L, et al.Speciation of Zn, Fe, Ca and Mg in wine with the Donnan membrane technique[J].Food Chemistry, 2018, 239:1 143-1 150.
[14] TARIBA B, PIZENT A, ![]() Z.Determination of lead in Croatian wines by graphite furnace atomic absorption spectrometry[J].Arhiv za Higijenu Rada I Toksikologiju-archives of Industrial Hygiene and Toxicology, 2011,62(1):25-31.
Z.Determination of lead in Croatian wines by graphite furnace atomic absorption spectrometry[J].Arhiv za Higijenu Rada I Toksikologiju-archives of Industrial Hygiene and Toxicology, 2011,62(1):25-31.
[15] SANZ-MEDEL A, MONTES-BAYON M, BETTMER J, et al.ICP-MS forabsolute quantification of proteins forheteroatom tagged, targeted proteomics[J].Trends in Analytical Chemistry, 2012, 40:52-63.
[16] XUE Y, XU X S, YONG L, et al.Optimization of vortex-assisted dispersive liquid-liquid microextraction for the simultaneous quantitation of eleven non-anthocyanin polyphenols in commercial blueberry using the multi-objective response surface methodology and desirability function approach[J].Molecules, 2018, 23(11):2 921.
[17] CAO D, XU X, XUE S, et al.An in situ derivatization combined with magnetic ionic liquid-based fast dispersive liquid-liquid micro extraction for determination of biogenic amines in food samples[J].Talanta, 2019, 199:212-219.
[18] NUR A T, CHE M Y, RAJAR N, et al.Use of principal component analysis for differentiation of gelatin sources based on polypeptide molecular weights[J].Food Chemistry, 2014, 151(5):286-292.
[19] NELSON J, HOPFER H, SILVA F, et al.Evaluation of GC-ICP-MS/MS as a new strategy for specific heteroatom detection of phosphorus, sulfur, and chlorine determination in foods[J].Journal of Agricultural and Food Chemistry, 2015, 63(18):4 478-4 483.
[20] 杨雯懿, 郝静, 田佳于, 等, 利用ICP-MS/MS测定白酒中无机元素的主成分分析及聚类分析[J].食品与发酵工业, 2020, 46(3):257-263.
YANG W Y, HAO J, TIAN J Y, et al.Principal component analysis and cluster analysis of inorganic elements in Baijiu using inductively coupled plasma tandem mass spectrometry[J].Food and Fermentation Industries, 2020, 46(3):257-263.
[21] RANAMUKHAARACHCHI S A,PEIRIS R H,MORESOLI C.Fluorescence spectroscopy and principal component analysis of soy protein hydrolysate fractions and the potential to assess their antioxidant capacity characteristics[J].Food Chemistry, 2017, 217:469-475.
[22] 中华人民共和国国家卫生和计划生育委员会, 国家食品药品监督管理总局.GB 2762—2017 食品安全国家标准 食品中污染物限量[S].北京:中国标准出版社, 2017.
National Health and Family Planning Commission of People′s Republic of China, National medical Products Administration. GB 2762—2017 National food safety standard maximum levels of contaminants in foods[S].Beijing:China Standards Press, 2017.
[23] 中华人民共和国国家质量监督检验检疫局, 中国国家标准化管理委员会.GB 15037—2006 葡萄酒[S].北京:中国标准出版社, 2008.
State Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China, China National Standardization Administration Committee.GB 15037—2006 Wine[S].Beijing:China Standards Press, 2008.
[24] 杨雯懿, 陈林, 周学忠.基于主成分分析和聚类分析的橄榄油中微量元素的统计比较[J].食品与发酵工业, 2020, 46(14):222-227.
YANG W Y, CHEN L, ZHOU X Z, Statistical comparison of trace elements in olive oil based on principal component analysis and cluster analysis[J].Food and Fermentation Industries, 2020, 46(14):222-227.