β-葡萄糖苷酶(β-glucosidase, EC3.2.1.21)又称为苦杏仁苷酶(amygdalase)、龙胆二糖酶(gentiobiose)及纤维二糖酶(cellobiase),能够水解多种葡萄糖缀合物非还原末端的β-D-葡萄糖苷键,释放出β-D-葡萄糖分子和相应的配基分子,该酶广泛分布于微生物、植物、哺乳动物和人体中,在食品、医学、农业及环境等领域具有重要的应用价值[1]。例如,添加β-葡萄糖苷酶能够促进果汁和葡萄酒中重要风味成分的生物转化,增强其口感[2];通过监测人体内的β-葡萄糖苷酶活性可以实现对戈谢病、帕金森、肺动脉高血压及中枢神经系统紊乱等疾病的诊断[3-4];β-葡萄糖苷酶作为纤维素酶系的重要组成成分能够显著促进木质纤维素的完全水解,提高纤维素转化为燃料乙醇的效率[5];土壤中的β-葡萄糖苷酶有助于降解土壤中多种有机质,从而保持土壤质量[6]。与其他物种来源的β-葡萄糖苷酶相比,来自微生物(如细菌、真菌和酵母)的各种β-葡萄糖苷酶表现出更广泛的生化特性、底物特异性和稳定性,大量新型β-葡萄糖苷酶或单独使用、或与其他商业酶制剂联合使用,在食品、香料、酒精饮料、生物燃料和制药领域发挥了巨大的作用。
根据β-葡萄糖苷酶蛋白组成的氨基酸序列相似性和保守结构特征,β-葡萄糖苷酶可划分入GH1、GH2、GH3、GH5、GH9、GH30、GH39和GH116等8个糖基水解酶家族(http://www.cazy.org/),其中GH1家族中的β-葡萄糖苷酶的数量最多[1]。基于X射线衍射和核磁共振图谱数据分析,GH1、GH2、GH5、GH30和GH39家族的β-葡萄糖苷酶具有典型的 (β/α)8桶状催化结构域,GH3家族多呈现 (β/α)8桶状和 (α/β)6三明治状的结构域,而GH9和GH116家族显现出典型的 (α/α)6桶状结构域,当前对于GH1和GH3家族的β-葡萄糖苷酶的结构研究较为广泛[7]。β-葡萄糖苷酶能够催化芳香基或脂肪烃基与糖基之间的β-葡萄糖苷键的断裂,常见的天然水解底物有水杨苷(salicin)、京尼平苷(geniposide)、七叶灵(esculin)、4-甲基伞形酮-β-D-葡萄糖苷(4-methylumbelliferyl-β-D-glucopyranoside,4-MUG)以及纤维二糖(cellobiose)等,人工合成底物有对硝基苯基β-D-吡喃葡萄糖苷(p-nitrophenyl-β-D-glucopyranoside, pNPG)和黄酮醇-β-D-葡萄糖苷(flavonol-β-D-glucoside)等[8]。根据底物酶解后产物的结构类型及特征,测定β-葡萄糖苷酶活性的方法包括多种,主要有分光光度法、荧光法、电化学法以及试剂盒等方法。本文主要综述了近些年各种测定β-葡萄糖苷酶活性方法的原理、优缺点及检测β-葡萄糖苷酶活性的最新应用进展。
1 分光光度法
大多数无机化合物、有机化合物及蛋白质等在紫外或可见光区具有一定的特征光吸收,或者能够转化为某些具有特定吸收的衍生物,因此,分光光度法在生化反应产物的定量分析中应用非常广泛。采用分光光度法测定β-葡萄糖苷酶活性常用的反应底物、工作原理及优缺点如下。
(1)水杨苷法
β-葡萄糖苷酶能够催化水杨苷分解成葡萄糖和水杨醇(saligenin)(图1-a)。第1种显色方法是在碱性、煮沸的条件下,酶解产生的葡萄糖分子与3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)发生氧化还原反应生成棕红色的3-氨基-5-硝基水杨酸(3-amino-5-nitrosalicylic acid),该产物在540 nm处有最大吸收,且其吸光值与酶解产生的葡萄糖量呈线性关系[9];第2种显色方法是在碱性且有铁氰化钾(K3[Fe(CN)6])存在的条件下,水杨苷分解的另一产物水杨醇与4-氨基安替比林(4-aminoantipyrin)反应生成红色的染料安替比林(antipyrine),通过在500~510 nm波长处测定安替比林的吸光值来表征β-葡萄糖苷酶催化水杨苷的水解程度[10]。
DNS显色法仍然是目前最常用的测定酶学活性的经典方法,其操作过程简单、材料试剂廉价易得,仪器设备要求低,并且对于酶解产物为葡萄糖的其它类水解酶也均适用,因此,该方法在高校、科研院所中使用最为普遍;但DNS法显色结果易受反应环境条件的影响,DNS能够与多种还原糖发生显色反应,因此其灵敏度和准确度会受到一定的影响[9]。而4-氨基安替比林具有易潮解、易氧化的性质,其纯度会直接影响空白试验的吸光度值,且显色反应混合物长时间存放不稳定,需要在固定时间内完成样品的测试,否则会导致分析结果的准确性降低,目前,4-氨基安替比林显色法多用于检测土壤、水体中挥发和非挥发性酚类物质含量[11]。
(2)pNPG法
以pNPG作为β-葡萄糖苷酶的酶解底物,其反应产物之一为对硝基苯酚(p-nitrophenol,pNP),通过分光光度计在400~420 nm波长处直接测定pNP的吸光值来评价β-葡萄糖苷酶的水解活性(图1-b)。pNPG和水杨苷均是测定β-葡萄糖苷酶活性的最常用的2种底物,pNPG方法具有操作步骤少、检测条件温和、灵敏度高和重现性较好,水解反应完成后不需额外实验操作就可直接进行定量测定等特点,尤其在微生物和植物中β-葡萄糖苷酶活性的检测应用较为普遍[8, 12]。但pNPG的价格较为昂贵,且在400 nm波长的检测条件下,易受生物混合样品中其它光吸收杂质信号的干扰,一定程度上限制了其应用。
(3)京尼平苷法
梁华正等[13]利用京尼平苷作为β-葡萄糖苷酶的反应底物,其水解产生的京尼平(genipin)与精氨酸能够发生显色反应,通过在590 nm波长处测定反应混合物的吸光度值来评价β-葡萄糖苷酶的活性(图1-c)。该方法与pNPG法相比, 虽然灵敏度较低, 但精密度和准确度均较好,且该显色反应结果能够在宽pH范围(5~9)和长时间内保持稳定(10 h)[13-14]。该方法中使用了精氨酸作为反应的显色底物,但反应环境中的其它氨基酸(甘氨酸、苯丙氨酸、谷氨酸、亮氨酸)也可能会产生一定的显色干扰,因此,对于复杂生物样品来源的混合物中β-葡萄糖苷酶活性的测定,其准确性可能会有所降低。京尼平一般常作为药物中间体用于治疗肿瘤、肝硬化、神经退行性病变等疾病;同时它也是一种天然的生物交联剂,其细胞毒性极低,在药物载体领域也有着广泛的应用,因此,大多数研究人员多以京尼平苷作为酶的反应底物来筛选或改造高亲和力、高催化活性的β-葡萄糖苷酶[15-17]。除京尼平苷外,药用植物中的白藜芦醇苷和黄芩苷等也常做筛选的底物用于获得高水解活性的β-葡萄糖苷酶[18-19]。
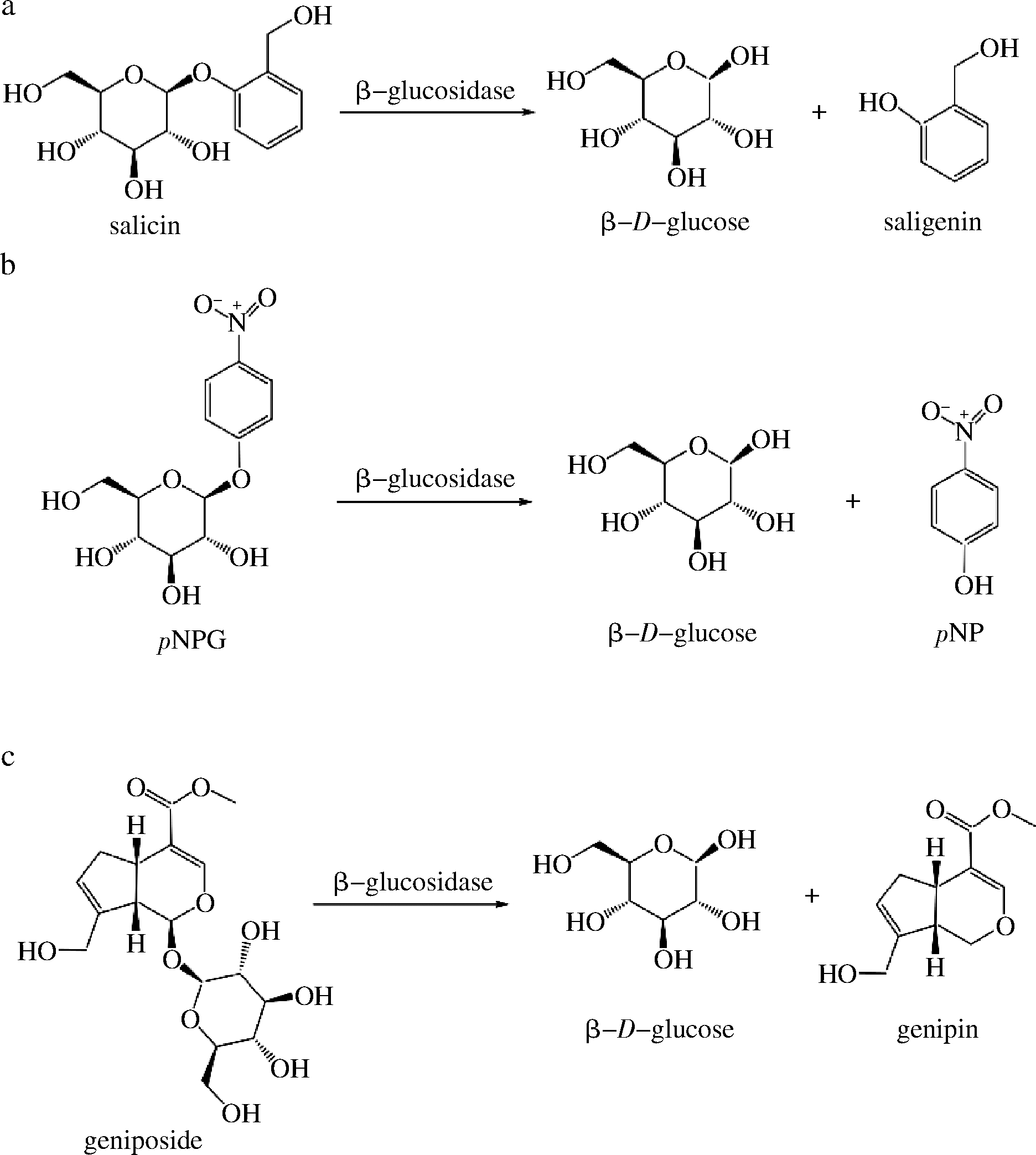
图1 分光光度法测定β-葡萄糖苷酶活性常用底物种类及反应过程
Fig.1 The substrate and reaction process of β-glucosidase activity determined by spectrophotometry
2 荧光法
荧光法是指某些化合物分子被外来辐射光照射吸收能量后由基态转变成激发态,当激发态分子跃迁回基态时常伴随发光现象,通过测定其发光强度来表征待测分子的含量,该方法在食品、卫生、环境、药物、临床生化等方面有着广泛的应用[20]。荧光法包括酶解后生成的产物直接能够产生荧光的,以及酶解产物与其它底物反应间接产生荧光2种。例如在医学上常用4-MUG来检测戈谢病病人的β-葡萄糖苷酶活性,β-葡萄糖苷酶催化4-MUG分解产生4-甲基伞形酮(4-methylumbelliferone,4-MU)和β-D-葡萄糖,通过在355 nm激发光、460 nm淬灭光波长条件下测定4-MU的荧光值强度变化来评价β-葡萄糖苷酶的活性(图2-a)[21]。但是4-MU的蓝色荧光易与某些生物样品的背景杂质信号产生重叠干扰,且反应环境的pH对其荧光强度值影响较大,尤其对于检测一些活性较低的β-葡萄糖苷酶,其应用受到了一定限制[21-22]。SERDIUK等[23]在4-MUG的基础上对荧光探针进行了改进和优化,合成了一种基于黄酮醇-β-D-葡萄糖苷分子为底物的检测新方法,通过激发态分子内质子转移(excited state intramolecular proton transfer,ESIPT)现象,酶切产生的黄酮醇(激发光350 nm,淬灭光530 nm)探针可以通过红移荧光被精确的监测,该底物较4-MUG相比,显著提高了检测β-葡萄糖苷酶活性的灵敏度(图2-b)。
程鑫等[24]建立了一种基于刃天青还原的荧光法,间接实现了对β-葡萄糖苷酶的定量分析和检测,该方法的底物是2-O-β-D-葡萄糖基-L-抗坏血酸(2-O-β-D-glucopyranosyl-L-ascorbic acid, AA-2βG),AA-2βG在β-葡萄糖苷酶的水解作用下生成具有还原性的抗坏血酸(ascorbic acid),抗坏血酸将刃天青(resazurin)还原成具有强烈荧光效应的试卤灵(resorufin),通过测定试卤灵的浓度(激发光579 nm,发射光584 nm)来表征β-葡萄糖苷酶的活性(图2-c)。该方法操作简单,现象明显,既可以通过裸眼观察显色反应过程(青蓝色逐渐变成紫红色,随后变为粉红色)实现对β-葡萄糖苷酶活性的定性评价,也可利用荧光酶标仪实现酶活性的定量分析。王龙文等[25]基于点击化学反应的原理,将β-葡萄糖苷酶水解AA-2βG产生的抗坏血酸用于还原Cu(II)成Cu(I),Cu(I)进而原位催化香豆素(coumarin)和苄基叠氮(benzyl azide)进行环加成点击化学反应产生高荧光强度的三氮唑(triazole)来定量分析β-葡萄糖苷酶的活性(图2-c),该方法的优点是与常规的pNPG 和4-MUG 法相比, 可避免400 nm 波长范围内的反应环境中可能存在的生色基团的干扰,提高测定混合样品中β-葡萄糖苷酶活性的准确度和精确度。
XING等[26]设计并合成了一种全新的荧光感应分子SY,该分子在极低浓度条件下(5.4×10-8 mol/L)就能够与β-葡萄糖苷酶水解扁桃苷(amygdalin)产生的CN-接合,进而促进SY分子内部电荷的转移引起荧光强度变化,通过多通道荧光分析仪可在双重荧光比率下(I414/I564和I803/I564)实现对CN-含量的高选择性和高精确性检测,这种双重荧光比率分析方法显著提高了β-葡萄糖苷酶活性检测的灵敏度和准确度(图2-d)。LIU等[27]建立了一种基于CN-的新型免标记荧光“turn off-on”纳米传感器用于评估土壤中β-葡萄糖苷酶活性,其原理是利用处于荧光猝灭(“turn off”)状态的半胱氨酸(Cys)包覆的CuInS2量子点(Cys-CuInS2 QDs)与经β-葡萄糖苷酶特异性水解生氰苷释放出的CN-结合,使Cys-CuInS2 QDs荧光恢复(“turn on”)。通过荧光信号的“turn off”和“turn on”能够实现对β-葡萄糖苷酶存在与否、活性大小及抑制因子进行精密的检测与分析(图2-d)。

图2 荧光法测定β-葡萄糖苷酶活性的原理
Fig.2 The principle of β-glucosidase activity detected by the fluorescence method
无论是利用β-葡萄糖苷酶水解扁桃苷生成CN-触发底物产生荧光,还是利用β-葡萄糖苷酶水解AA-2βG生成抗坏血酸引发底物产生荧光,其主要优点是都能成功实现对极低β-葡萄糖苷酶活性的准确测定,如CuInS2 QDs检测最低限为0.000 2 U/mL;三氮唑检测最低限为0.000 456 U/mL,这对于测量食品、土壤等环境中痕量的β-葡萄糖苷酶提供了极大的便利。但荧光法的缺点是反应底物不容易获得,有的需要通过专门化学合成得到,有的部分试剂(如Cys-CuInS2 QDs中的金属铟)的价格较为昂贵。荧光分析法具有快速、简单、灵敏度高,以及高选择性和高重现性等特点,且当前逐渐朝着高效、痕量、微观和全自动化的方向发展[20, 24]。
3 电化学方法
因为β-葡萄糖苷酶催化底物水解一般都能生成葡萄糖分子,CHEN等[28]基于β-葡萄糖苷酶催化级联反应,并借助个人血糖仪(personal glucose meter,PGM)建立了一种更为简便、快速的β-葡萄糖苷酶活性及抑制剂的测定方法。其反应原理和过程如图3所示,β-葡萄糖苷酶催化水杨苷水解生成葡萄糖和水杨醇(saligenin),葡萄糖在血糖检测试纸(blood glucose test strips)上的葡萄糖脱氢酶的作用下发生脱氢反应,并将电子和氢转移给氧化型辅酶I(NADP+)形成还原型辅酶I(NADPH);NADPH和水杨醇进一步触发血糖检测试纸上的铁氰化钾(K3[Fe(CN)6])还原为亚铁氰化钾(K4[Fe(CN)6]),其中转移的电子转变成PGM可检测的电信号。该检测方法将氧化还原反应电子的转移转变成血糖仪可检测的电信号,具有检测时间短,可视化强优点,就像日常测定血液中葡萄糖一样简单便捷。JIN等[29]进一步对使用血糖仪测定β-葡萄糖苷酶活性的方法做了更为详细的统计性分析和验证,测试标准曲线证明该方法具有稳定的线性关系(R2=0.999 2),且与DNS法相比,该方法具有更好的准确性、精密度、重复性、稳定性、耐用性及选择性等优点。
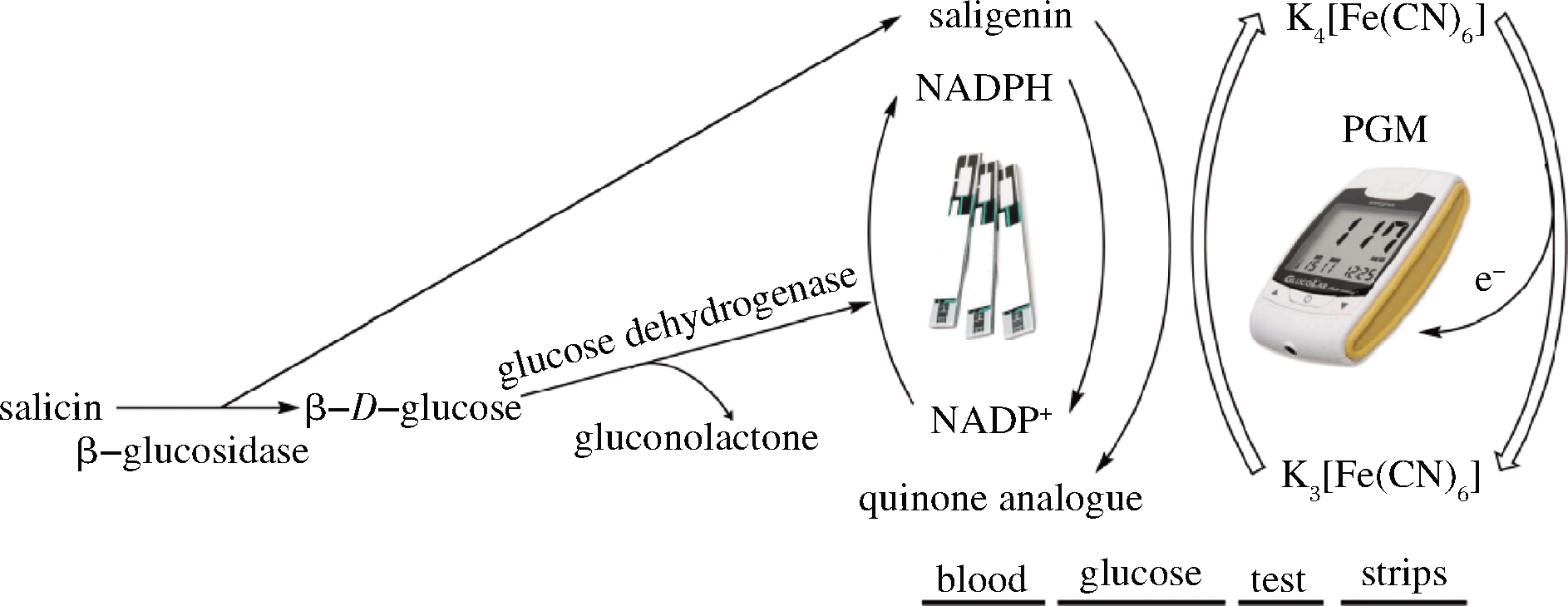
图3 血糖仪测定β-葡萄糖苷酶活性原理
Fig.3 Principle of measuring β-glucosidase activity by glucose meter
电化学方法所需检测样品量较少,只需几微升反应样品便可快速计算出酶学活力。这种简便的、快速的、小型化的β-葡萄糖苷酶检测法在医疗诊断、食品安全和环境监测等诸多领域中具有潜在的应用价值[29]。
4 试剂盒方法
β-葡萄糖苷酶催化底物水解产生的葡萄糖可以通过商品化的血糖含量测定试剂盒来进行定量,根据葡萄糖的含量来表征待测样品中β-葡萄糖苷酶的活性。市场上血糖含量测定试剂盒的工作原理有葡萄糖氧化酶法和己糖激酶法等多种。葡萄糖氧化酶能够催化葡萄糖氧化产生H2O2,过氧化物酶进一步催化H2O2氧化4-氨基安替比林偶联酚生成红色的醌类化合物,该红色化合物在505 nm处具有特征吸收峰。己糖激酶法是指葡萄糖和三磷酸腺苷在己糖激酶的作用下生成葡萄糖-6-磷酸(glucose-6-phosphate,G-6-P)与二磷酸腺苷,G-6-P在葡萄糖-6-磷酸脱氢酶(glucose-6-phosphate dehydrogenase)催化作用下脱氢,生成6-磷酸葡萄糖酸,同时使NADP+还原成NADPH,NADPH在340 nm处存在最大吸收峰,通过测定NADPH的浓度来计算葡萄糖的浓度。除了血糖含量测定试剂盒,目前市场上已经有许多针对不同物种(植物、哺乳动物及人类等)、不同样品来源而开发的专门化的β-葡萄糖苷酶活性检测试剂盒。例如,有针对血清、血浆、细胞上清液,组织匀浆等样品的“人β-葡萄糖苷酶ELISA试剂盒”,该试剂盒的工作原理主要是将含有β-葡萄糖苷酶的待测样品与试剂盒中生物素标记的抗体一起放置在96孔板中温育反应,然后加入亲和素标记的辣根过氧化物酶和显色底物共同作用产生颜色变化,根据颜色的深浅来定量测定待测样品中β-葡萄糖苷酶的浓度;“土壤 β-葡萄糖苷酶活性检测试剂盒”底物多选择pNPG,其原理属于分光光度法,通过测定水解后产生的pNP的吸光值来评价土壤样品中β-葡萄糖苷酶的活性。
试剂盒的价格虽然昂贵,但优点是实验操作过程不需要专门配置特定的试剂,且有明确的说明书,清晰的操作步骤,分析结果误差较少,灵敏度、精密度和重现性也都较好。经过对多家食品、医药和酶制剂厂家的调研发现,大部分企业公司的分析人员根据自身不同的检测需求,而选择不同的试剂盒来检测β-葡萄糖苷酶活性。
5 活体细胞中β-葡萄糖苷酶活性检测方法
β-葡萄糖苷酶在自然界中分布广泛且具有多种重要的生物学功能。β-葡萄糖苷酶能够参与微生物细胞壁中碳水化合物的降解;在植物细胞中,β-葡萄糖苷酶在色素或细胞壁的生物合成、果实成熟和病虫害防御机制中发挥重要作用;在哺乳动物细胞中,β-葡萄糖苷酶参与了神经酰胺水解等过程;在人体细胞中,β-葡萄糖苷酶活性大小可以用于诊断戈谢病等疾病[30]。但是,当前测定β-葡萄糖苷酶活性的方法,大多需要对细胞进行裂解,或者对β-葡萄糖苷酶蛋白质进行纯化回收后再准确定量总蛋白量和计算其酶活力,该操作过程比较耗时,且无法精确反应活细胞内β-葡萄糖苷酶活力的变化情况,因此,近年来,关于检测活体细胞中β-葡萄糖苷酶活性的研究方法逐渐增多。
STRAHSBURGER等[31]研究发现pNPG的酶解产物pNP一般不能被微生物细胞进一步代谢分解,因此,通过提前向培养基中添加底物pNPG,可以在405 nm波长条件下实时取样检测活细胞上清液中的β-葡萄糖苷酶的酶活力,通过试验证明该方法能够明显区分开自身不能合成β-葡萄糖苷酶的菌株Bifidobacterium longum B7254和自身能够合成β-葡萄糖苷酶的菌株Bifidobacterium pseudocatenulatum B7003;在此基础上,该团队利用96孔板进行高通量筛选,从大量的备选菌株中快速筛选出了高产β-葡萄糖苷酶活性的乳杆菌。PAN等[32]使用嵌入电化学功能的纳米毛细管实现对戈谢氏病人活体细胞的溶酶体中β-葡萄糖苷酶活性的实时监测。通过设计和制作一种纳米毛细管,一方面该纳米毛细管的尖端可用于分离活细胞内单个的亚细胞腔室(溶酶体等),形成一个微反应室便于分析溶酶体中各种蛋白质的活性;另一方面在毛细纳米管的内表面和外表面边缘涂上铂层,将涂有氯化银的银丝(Ag/AgCl)插入毛细管内作为电化学测量的参比电极,制作成一个微小电化学检测器。纳米毛细管从细胞中取出获取溶酶体后在Triton X-100作用下释放出其中的β-葡萄糖苷酶,酶水解辛基-β-D-吡喃葡萄糖苷(octyl-β-D-glucopyranoside)生成的葡萄糖分子在毛细管尖端内壁的铂电极上通过电化学氧化产生H2O2分子,在通过测量H2O2的值来表征活细胞溶酶体内β-葡萄糖苷酶的活力大小。细胞是生命活动的最基本单元,实现对活体单细胞内重要的酶学活性、特定物质转化反应等的监测,能够为探究某些疾病的起因、发展和治疗提供准确、可靠的依据。
6 β-葡萄糖苷酶抑制剂筛选方法
β-葡萄糖苷酶作为一种重要的风味酶及检测指标因子在食品、饮料,土壤质量监测等方面发挥着重要的作用。在生命机体中,β-葡萄糖苷酶参与了糖尿病、艾滋病、转移性癌症和溶酶体贮积病等多种疾病的发病过程[28]。因此,筛选高效的β-葡萄糖苷酶抑制剂不仅可以通过阻断特定的代谢过程来揭示酶在生命系统中的关键功能,也可以为相关疾病的治疗寻求具有前景的治疗方法。
β-葡萄糖苷酶抑制剂的筛选原理主要是通过抑制因子对β-葡萄糖苷酶催化底物水解反应的抑制程度来进行筛选。例如WU等[33]通过将β-葡萄糖苷酶固定在毛细管入口的内壁上,建立了一种基于毛细管电泳在线固定化β-葡萄糖苷酶筛选抑制因子的微反应器,以pNPG为模型底物,通过检测pNPG的水解程度衡量抑制因子对β-葡萄糖苷酶活性的抑制程度,利用该反应器方法成功地从12种天然的黄酮类化合物中筛选出黄芩素、染料木素、表儿茶素没食子酸酯和表没食子儿茶素没食子酸酯等4种具有β-葡萄糖苷酶抑制活性的因子;并通过分子对接对4种抑制因子的抑制作用进行模拟,表征酶-抑制因子的结合能大小依次为:表没食子儿茶素没食子酸酯>黄芩素>表没食子儿茶素没食子酸酯>染料木素,这与反应器筛选得到的抑制率顺序一致,其中表没食子儿茶素没食子酸酯与β-葡萄糖苷酶的结合能力最强,对接模拟发现能够与活性中心“口袋”中的ASP283,ARG280,SER304,LYS396和GLN276等位点结合而发挥抑制作用。CHEN等[28]利用血糖仪来筛选β-葡萄糖苷酶抑制剂,其原理是当待测反应样品中混有抑制因子如粟树精胺时,PGM的显示数值明显降低,因为β-葡萄糖苷酶的抑制作用显著降低了水杨苷分解生成葡萄糖和水杨醇的含量。通过血糖仪测试14种小分子化合物和6种茶多酚提取物对β-葡萄糖苷酶的抑制活性,发现没食子酸、原儿茶醛、隐绿原酸、表棓儿茶素(epigallocatechin)、表儿茶素和香草酸等6种化合物的抑制率均超过了40%;普洱茶和福鼎白茶的茶多酚提取物对β-葡萄糖苷酶也具有较好的抑制作用(>20%)。
7 小结
β-葡萄糖苷酶在食品工业、生物燃料及医学检测等领域具有重要的应用价值,本文介绍了近些年来测定β-葡萄糖苷酶活性的常用方法及部分典型实例,各种测定β-葡萄糖苷酶活性的方法所使用的底物分子类型、酶学活性检测范围及最低检测限等信息内容如表1所示。建议对于常规的酶学活性测定试验一般可采用经典的分光光度法,选择水杨苷或pNPG作为催化反应的底物,因为在大多数底物中,不同家族的β-葡萄糖苷酶一般对这2种底物酶解活性都较好[34-35];对于检测混合样品中低活性的β-葡萄糖苷酶可采用灵敏度和选择性较高的荧光法(三氮唑或CuInS2 QDs);如需要快速定量分析β-葡萄糖苷酶的活性时可选择电化学方法或者荧光法。虽然分光光度法在检测β-葡萄糖苷酶活性时可能会受到催化反应背景环境中吸光杂质的干扰,但其优点是操作简单,材料试剂低廉易获得,不需要昂贵的检测设备,因此,在大多高校、科研院所开展一些基础性、探究性的实验中使用最为普遍。荧光法具有快速、灵敏度和选择性较高,有些可用于活体细胞内β-葡萄糖苷酶活性的实时检测等优点,且随着当前可选择的荧光底物的种类逐渐增多(表1),检测试剂成本的逐渐降低,其在农业、环境、食品和医学领域应用的范围也将越来越广,但部分荧光法的操作流程可能会比较复杂,有的需要昂贵的仪器和训练有素的专业人员[36-37]。试剂盒和个人血糖仪的测定方法简单便捷,且准确性高,越来越受到各类生物公司的青睐,其多可用于环境、临床医学等分析现场的酶学活性的测定,期待在不久的将来能够开发出更多种类、针对更多不同来源样品、不同用途的酶学活性测定试剂盒。因为β-葡萄糖苷酶在生物体初级代谢和次级代谢活动中都发挥着重要的作用,期待将来进一步开发更多的评价活体细胞内β-葡萄糖苷酶活性的检测方法,在亚细胞水平上为进一步解析β-葡萄糖苷酶影响生命活动及各种生理机能奥秘提供可靠的工具。
表1 检测β-葡萄糖苷酶活性的方法及底物类型
Table 1 The method and substrates for determination of β -glucosidase activity

检测方法底物类型酶活性检测线性范围/(U·mL-1)酶活性最低检测限/(U·mL-1)检测时间/min参考文献分光光度法水杨苷0.5~7.00.5 20~60[28]pNPG0.005~0.250.012 320~60[30]京尼平苷0.05~1.00.0220[13]荧光法4-MUG/0.005 5[37]黄酮醇-β-D-葡萄糖苷/0.000 005>5[23]AA-2βG/刃天青1.0~301.060[24]AA-2βG/香豆素/苄基叠氮0.001~0.040.000 456120[25]SY/扁桃苷/2.05[26]CuInS2 QD/Cu2+/扁桃苷0.000 5~0.7 0.000 230[27]电化学水杨苷/血糖仪试纸1.0~9.00.45 5[28]
[1] GODSE R, BAWANE H, TRIPATHI J, et al.Unconventional β-glucosidases:A promising biocatalyst for industrial biotechnology[J].Applied Biochemistry and Biotechnology, 2021, 193(9):2 993-3 016.
[2] ZHANG P Z, ZHANG R G, SIRISENA S, et al.Beta-glucosidase activity of wine yeasts and its impacts on wine volatiles and phenolics:A mini-review[J].Food Microbiology, 2021, 100:103859.
[3] PONCE E, MOSKOVITZ J, GRABOWSKI G.Enzyme therapy in gaucher disease type 1:Effect of neutralizing antibodies to acid β-glucosidase[J].Blood, 1997, 90(1):43-48.
[4] CULLEN V, SARDI S P, NG J, et al.Acid β-glucosidase mutants linked to Gaucher disease, Parkinson disease, and Lewy body dementia alter α-synuclein processing[J].Annals of Neurology, 2011, 69(6):940-953.
[5] 徐晓, 程驰, 袁凯, 等.里氏木霉产纤维素酶研究进展[J].中国生物工程杂志, 2021, 41(1):52-61.
XU X, CHENG C, YUAN K, et al.Research progress of cellulase production in Trichoderma reesei[J].China Biotechnology, 2021, 41(1):52-61.
[6] TURNER B L, HOPKINS D W, HAYGARTH P M, et al.β-Glucosidase activity in pasture soils[J].Applied Soil Ecology, 2002, 20(2):157-162.
[7] KETUDAT CAIRNS J R, ESEN A.β-Glucosidases[J].Cellular and Molecular Life Sciences, 2010, 67(20):3 389-3 405.
[8] 金璐, 王彦, 薛芸, 等.植物源β-葡萄糖苷酶活性检测方法学研究[J].现代生物医学进展, 2016, 16(26):5 032-5 037.
JIN L, WANG Y, XUE Y, et al.Methodological research on the activity of β-glycosidase from plant origin[J].Progress in Modern Biomedicine, 2016, 16(26):5 032-5 037.
[9] SPIVAK V A, LEVJANT M I, KATRUKHA S P, et al.Quantitative ultramicroanalysis of amino acids in the form of their DNS-derivatives:IV.Some applications of the method.Quantitative evaluation of DNS-peptide maps[J].Analytical Biochemistry, 1971, 44(2):503-518.
[10] 李瑞玉, 林立庆, 刘燕希, 等.4-氨基安替比林分光光度法测定酚类化合物的方法解读[J].中国资源综合利用, 2020, 38(5):123-125.
LI R Y, LIN L Q, LIU Y X, et al.Interpretation on the determination of phenolic compounds by 4-aminoantipyrine spectrophotometry[J].China Resources Comprehensive Utilization, 2020, 38(5):123-125.
[11] 梁丽霞. 4-氨基安替比林分光法测定挥发酚不确定度[J].聚酯工业, 2021, 34(4):35-38.
LIANG L X.Uncertainty of determination of volatile phenol by 4-aminoantipyrine spectrophotometry[J].Polyester Industry, 2021, 34(4):35-38.
[12] 高院妮. β-葡葡糖苷酶基因的克隆及表达研究[D].昆明:云南大学, 2016.
GAO Y N.Studies on the cloning and expression of β-glucosidase gene[D].Kunming:Yunnan University, 2016.
[13] 梁华正, 刘富梁, 彭玲西, 等.京尼平苷为底物测定β-葡萄糖苷酶活力的方法[J].食品科学, 2006, 27(4):182-185.
LIANG H Z, LIU F L, PENG L X, et al.Method for determination of β- glucosidase activity for geniposide[J].Food Science, 2006, 27(4):182-185.
[14] PAIK Y, LEE C, CHO M, et al.Physical stability of the blue pigments formed from geniposide of Gardenia fruits:Effects of pH, temperature, and light[J].Journal of Agricultural and Food Chemistry, 2001, 49(1):430-432.
[15] 梁金凤, 汪涯, 肖依文, 等.内生真菌Eupenicillium javanicum R57水解京尼平苷β-葡萄糖苷酶的分离纯化及其酶学性质[J].菌物学报, 2017, 36(11):1 543-1 555.
LIANG J F, WANG Y, XIAO Y W, et al.Purification and characterization of geniposide-hydrolyzing β-glucosidase from endophytic Eupenicillium javanicum R57 harboring in Dongxiang wild rice[J].Mycosystema, 2017, 36(11):1 543-1 555.
[16] GONG G H, ZHENG Z M, LIU H, et al.Purification and characterization of a β-glucosidase from Aspergillus niger and its application in the hydrolysis of geniposide to genipin[J].Journal of Microbiology and Biotechnology, 2014, 24(6):788-794.
[17] YANG Y S, ZHANG T, YU S C, et al.Transformation of geniposide into genipin by immobilized β-glucosidase in a two-phase aqueous-organic system[J].Molecules (Basel, Switzerland), 2011, 16(5):4 295-4 304.
[18] ZHOU L F, LI S H, ZHANG T, et al.Properties of a novel polydatin-β-D-glucosidase from Aspergillus niger SK34.002 and its application in enzymatic preparation of resveratrol[J].Journal of the Science of Food and Agriculture, 2016, 96(7):2 588-2 595.
[19] YU H S, HAN Y T, LIU C Y, et al.Preparation of baicalein from baicalin using a baicalin-β-D-glucuronidase from Aspergillus niger b.48 strain[J].Process Biochemistry, 2020, 97:168-175.
[20] 何家洪. 分光及荧光光度法测定痕量铬(VI)的方法研究[D].重庆:重庆大学, 2008.
HE J H.Study on determination of trace chromium(VI) by spectrophotometric and fluorophotometric analysis[D].Chongqing:Chongqing University, 2008.
[21] OLIVOVA P, CULLEN E, TITLOW M, et al.An improved high-throughput dried blood spot screening method for Gaucher disease[J].Clinica Chimica Acta;International Journal of Clinical Chemistry, 2008, 398(1-2):163-164.
[22] WATANABE A, SUZUKI M, UJIIE S, et al.Purification and enzymatic characterization of a novel β-1, 6-glucosidase from Aspergillus oryzae[J].Journal of Bioscience and Bioengineering, 2016, 121(3):259-264.
[23] SERDIUK I E, RESZKA M, MYSZKA H, et al.Flavonol-based fluorescent indicator for determination of β-glucosidase activity[J].RSC Advances, 2016, 6(48):42 532-42 536.
[24] 程鑫, 张珩, 马济美.一种基于刃天青还原的荧光方法对β-葡萄糖苷酶活性的检测[J].分析测试学报, 2019, 38(3):360-363.
CHENG X, ZHANG H, MA J M.Activity determination of β-glucosidase by a turn-on fluorescent method based on reduction of resazurin[J].Journal of Instrumental Analysis, 2019, 38(3):360-363.
[25] 王龙文, 马济美, 程鑫, 等.基于酶触发的点击化学反应测定β-葡萄糖苷酶活性[J].有机化学, 2018, 38(10):2 775-2 786.
WANG L W, MA J M, CHENG X, et al.Determination of β-glucosidase activity based on enzyme-triggered click chemistry[J].Chinese Journal of Organic Chemistry, 2018, 38(10):2 775-2 786.
[26] XING P, XU Y, LI H, et al.Ratiometric and colorimetric near-infrared sensors for multi-channel detection of cyanide ion and their application to measure β-glucosidase[J].Scientific Reports, 2015, 5:16528.
[27] LIU Z P, TIAN Y, HAN Y, et al.A “turn off-on” fluorescent nanoprobe consisting of CuInS 2 quantum dots for determination of the activity of β-glucosidase and for inhibitor screening[J].Mikrochimica Acta, 2019, 186(12):806.
[28] CHEN G Y, ZHANG H, YANG F Q.A simple and portable method for β-glucosidase activity assay and its inhibitor screening based on a personal glucose meter[J].Analytica Chimica Acta, 2021, 1142:19-27.
[29] JIN M Y, ZHANG T, YANG Y S, et al.A simplified and miniaturized glucometer-based assay for the detection of β-glucosidase activity[J].Journal of Zhejiang University Science B, 2019, 20(3):264-272.
[30] KONG B, YANG T, HOU P, et al.Enzyme-triggered fluorescence turn-off/turn-on of carbon dots for monitoring β-glucosidase and its inhibitor in living cells[J].Luminescence, 2020, 35(2):222-230.
[31] STRAHSBURGER E, DE LACEY A M L, MAROTTI I, et al.In vivo assay to identify bacteria with β-glucosidase activity[J].Electronic Journal of Biotechnology, 2017, 30:83-87.
[32] PAN R R, XU M C, BURGESS J D, et al.Direct electrochemical observation of glucosidase activity in isolated single lysosomes from a living cell[J].Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(16):4 087-4 092.
[33] WU Z Y, ZHANG H, LI Q Q, et al.Capillary electrophoresis-based online immobilized enzyme reactor for beta-glucosidase kinetics assays and inhibitors screening[J].Journal of Chromatography B, 2019, 1 110-1 111:67-73.
[34] DAENEN L, SAISON D, STERCKX F, et al.Screening and evaluation of the glucoside hydrolase activity in Saccharomyces and Brettanomyces brewing yeasts[J].Journal of Applied Microbiology, 2008, 104(2):478-488.
[35] 李华, 高丽.β-葡萄糖苷酶活性测定方法的研究进展[J].食品与生物技术学报, 2007,26(2):107-114.
LI H, GAO L.Research advance on methods of determining β-glucosidase activity[J].Journal of Food Science and Biotechnology, 2007,26(2):107-114.
[36] 吕世鑫. 产β-葡萄糖苷酶的微生物的筛选鉴定及其在人参皂苷C-K转化中的应用[D].烟台:烟台大学, 2021.
LYU S X.Screening and identification of microorganisms producing β-glucosidase and its application in the transformation of ginsenoside C-K[D].Yantai:Yantai University, 2021.
[37] KWAPISZEWSKI R, SKOLIMOWSKI M, ZI
 KOWSKA K, et al.A microfluidic device with fluorimetric detection for intracellular components analysis[J].Biomedical Microdevices, 2011, 13(3):431-440.
KOWSKA K, et al.A microfluidic device with fluorimetric detection for intracellular components analysis[J].Biomedical Microdevices, 2011, 13(3):431-440.