牦牛虽然在肉牛中所占比例不大,但它却是适应青藏髙原特殊生态环境下的优势畜种,与藏文化息息相关,是当地牧民赖以生存和发展的物质基础,是西部牧区特色优势产业发展的重点,也是促进藏区稳定和发展不可忽视的部分,具有不可替代性[1]。且牦牛肉的蛋白含量高于普通黄牛、猪肉、羊肉,属于高蛋白肉品[1]。但是,由于肉类及其制品在加工贮藏过程中会不可避免受到温度、氧气和催化剂等外界因素的干扰[2],因此牦牛肉在加工贮藏过程中容易发生蛋白氧化,从而导致肉品质量下降。大蒜作为肉制品中常见的调味辅料,不仅可以起到去除肉腥味、增加肉品蒜香味的作用,而且在人和动物的饮食中,大蒜具有抗过敏和抗氧化等功能[3]。此外,虽然有研究证明了大蒜具有抑制蛋白氧化的能力,但这似乎取决于大蒜加工的方法以及肉类产品的类型[4-5]。大蒜一般以提取物、精油和粉末的形式应用于食品中。大蒜粉稳定、易贮存,保留了大蒜中原始的多种成分,具有良好的工业实用性。但是大蒜粉在食品中应用的研究极少,蒜粉的作用效果受蒜粉生产工艺及肉制品种类的影响[4,6]。近年来,对大蒜成分的研究大部分集中于药理作用和新鲜大蒜及大蒜制剂中的有机硫化物的定量研究[7]。目前尚未见大蒜粉中清除羟自由基活性成分的研究。
肌原纤维蛋白作为肌肉蛋白的主要组成部分,是影响肉嫩度和保水性的重要结构蛋白,对肉制品的质构、风味及加工特性起决定性作用。但是一些天然蛋白质由于易受加工过程中,微环境变化的影响,很少表现出能较好地满足食品工业需求的理想功能特性[8-9]。在肉类加工和贮藏过程中,能诱发蛋白氧化的物质有活性氧物质、活性氮物质以及脂肪氧化应激的二级产物等。其中羟自由基是活性氧自由基中氧化能力最强的自由基,羟自由基诱导的蛋白质氧化是肉制品加工中最普遍的一种氧化体系[10]。本文通过HPLC-DPPH法测定大蒜粉中清除DPPH自由基的活性成分,对大蒜粉中抗氧化活性成分进行研究。通过测定不同添加量大蒜粉对处于Fenton体系中牦牛肉肌原纤维蛋白理化指标的影响,探讨大蒜粉对牦牛肉肌原纤维蛋白体外氧化的保护作用,为研究大蒜粉作为食品天然抗氧化剂的作用机理,以及大蒜粉在肉制品中的应用提供参考价值。
1 材料与方法
1.1 材料与试剂
大蒜为四川温江紫皮独头蒜,四川省成都市武侯区洗面桥巷便民菜市场;牦牛肉为四川省阿坝州红原县自然放牧的3岁半健康无病公牦牛的背最长肌。
乙二醇双(2-氨基乙基醚)四乙酸[ethylenebis(oxyethylenenitrilo)tetraacetic acid,EGTA]、2,4-二硝基苯肼、8-苯胺萘磺-1-酸盐[ammonium 8-(phenylamino)naphthalene-1-sulfonate xhydrate,ANS]、乙二胺四乙酸-二钠、抗坏血酸(均为分析纯),成都科隆化学品有限公司;盐酸胍、Tris(均为分析纯),德国BioFroxx公司;5,5-二硫基-2,2-二硝基苯甲酸、甘氨酸(均为分析纯),上海源叶生物有限公司;甲醇(色谱纯),成都市科隆化学品有限公司;DPPH(色谱纯)上海思域化工科技有限公司;大蒜素(98%)、二烯丙基二硫醚(95%)、二烯丙基三硫醚标准品(98%)(均为色谱纯),上海源叶生物有限公司。
1.2 仪器与设备
5804R冷冻离心机,德国Eppendorf公司;UV1810S紫外分光光度计,上海佑科仪器仪表有限公司;T-25高速匀浆机,德国IKA公司;HH-6恒温水浴锅,国华电器有限公司;PL303分析天平,梅特勒-托利多国际股份有限公司;LD510电子天平,沈阳龙腾电子有限公司;F-4700型荧光分光光度计,日本那珂事务所;D-37520型真空冷冻干燥机,德国CHRiST公司;Agilent 1260型高效液相色谱仪,美国安捷伦科技有限公司。
1.3 实验方法
1.3.1 大蒜粉的制备
参考胡晗艳等[11]的方法,并稍作修改以制备大蒜粉。取去皮大蒜200 g,将大蒜与水按料液比1∶5打浆,浆液打至无肉眼可见颗粒。大蒜浆装盘厚度为1.5 mm,-18 ℃下预冻12 h后真空冷冻干燥,冻干参数为-56 ℃,真空度0.8~1.86 hPa,时间20 h。将制得的大蒜粉装于带盖棕色玻璃瓶中,于0~4 ℃环境贮存。
1.3.2 HPLC法测定大蒜粉的抗氧化成分
1.3.2.1 标准曲线的绘制
精密称取大蒜素标准品20 mg,用甲醇溶液稀释并定容至刻度,得到质量浓度为800 μg/mL的大蒜素对照品储备液,分别取1、2、4、6、10 mL的对照品储备液用甲醇稀释至10 mL,配制成0、80、160、320、480、800 μg/mL的标准工作液,过0.22 μm的有机滤膜,进行高效液相色谱分析。
二烯丙基二硫醚和三烯丙基二硫醚的标曲绘制方法同大蒜素。
1.3.2.2 HPLC参数设置
液相条件参考ESTEVINHO等[12],并稍作修改。色谱柱:C18柱(4.6 mm×250 mm,5 μm)。流动相为甲醇-水溶液:0~10 min,甲醇体积分数为5%~17%;10~20 min,甲醇体积分数为17%~26%;20~40 min,甲醇体积分数为26%~58%;40~50 min,甲醇体积分数为58%~95%;50~60 min,甲醇体积分数为95%~5%。流速:1.0 mL/min,柱温:40 ℃,检测波长:320 nm,进样量:20 μL。
1.3.2.3 样品溶液的制备
将大蒜粉用甲醇溶液配制成质量浓度为1 mg/mL的样品溶液。
1.3.2.4 HPLC-DPPH实验
取一定质量浓度的样品甲醇溶液500 μL,加500 μL DPPH甲醇溶液(1.8 mg/mL),作为实验组,避光反应30 min;取一定质量浓度的样品甲醇溶液500 μL,加500 μL甲醇,作为空白组。将空白组和实验组溶液过0.22 μm的有机滤膜后,在1.3.2.2中的液相参数下进行高效液相色谱分析。对主要的峰面积进行积分,根据峰面积的消减筛选出可能的抗氧化活性成分,以峰面积的消减率表示清除率,清除率按公式(1)计算:
清除率![]()
(1)
式中:S1为空白组对应的吸收峰面积;S2为实验组对应的吸收峰面积。
1.3.3 牦牛肉肌原纤维蛋白的提取
参考PARK等[13]的方法并略作修改。称取300 g已剔除筋膜、脂肪的牦牛肉,加入4倍体积提取缓冲液(0.1 mol/L NaCl,2 mmol/L MgCl2,1 mmol/L EGTA,20 mmoL/L Na2HPO4,pH 7.0),匀浆离心(4 ℃,2 500 r/min,15 min),弃上清液,取沉淀重复上述步骤3遍。向最后一次沉淀中加入4倍体积的含0.1 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 6.2)并均质处理。离心(4 ℃,2 500 r/min,15 min)移除上清液后,加入4倍体积磷酸盐缓冲液(20 mmoL/,pH 6.0)并均质。将均质液用4层纱布过滤以除去结缔组织,离心(4 ℃,2 500 r/min,15 min)后弃上清液,所得的沉淀即为肌原纤维蛋白样品。提取的肌原纤维蛋白置于4 ℃并在12 h内使用。
1.3.4 牦牛肉肌原纤维蛋白的氧化处理
参考李玲等[14]的方法并稍作修改构建Fenton体系,反应过程:抗坏血酸+Fe3+→Fe2+;Fe2++H2O2→羟自由基。将提取的肌原纤维蛋白溶于磷酸盐缓冲溶液(20 mmol/L,pH 7.0)中,以牛血清蛋白为标准,双缩脲法测定蛋白浓度。在溶解后的蛋白质溶液中依次加入FeCl3、抗坏血酸、H2O2溶液用来构建氧化体系。整个体系最终含有以下成分:40 mg/mL牦牛肉肌原纤维蛋白、0.01 mmol/L的FeCl3、0.1 mmol/L的抗坏血酸和10 mmol/L H2O2,其中大蒜粉的质量分数分别为0、0.2%、0.5%、1.0%、2.0%(以蛋白计)。在4 ℃恒温环境中氧化12 h后,用乙二胺四乙酸-二钠(1 mmol/L)终止氧化反应,并将终止反应后的肌原纤维蛋白浆4 ℃冷冻离心后备用(4 000 r/min,10 min),所得沉淀即为氧化后的牦牛肉肌原纤维蛋白,贮藏于0~4 ℃,2 d 内用完。以未加大蒜粉和氧化体系的肌原纤维蛋白组为空白对照。
1.3.5 羰基含量的测定
参考MERCIER等[15]的方法,并稍作修改进行测定。用含0.6 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 7.0)溶解氧化后的肌原纤维蛋白样品,并用双缩脲法测定蛋白浓度,调整蛋白浓度至4 mg/mL。取1 mL 的蛋白溶液,加入1 mL的2,4-二硝基苯肼(10 mmol/L),室温下避光反应40 min,每隔5 min 振荡混匀一次,反应后加入1 mL的200 g/L三氯乙酸溶液于4 ℃、12 000 r/min离心5 min。调零组加入1 mL 的2 mol/L HCl溶液,其余操作相同。移除上清液后,用1 mL乙醇-乙酸乙酯混合液(1∶1,体积比)洗涤沉淀以除去未反应的2,4-二硝基苯肼,随后4 ℃、5 000 r/min离心5 min,上述洗涤过程重复3次后,将沉淀溶于3 mL盐酸胍(6 mol/L)中,37 ℃保温15 min 后离心(4 ℃,12 000 r/min,5 min),取上清液于370 nm处测定溶液吸光度。蛋白质羰基含量根据摩尔消光系数[22 000 L/(mol·cm)]按照公式(2)计算:
羰基含量![]()
(2)
式中:A为样品吸光值;C为蛋白提取液浓度,mg/mL;D为比色光径,cm;22 000为摩尔消光系数;n为稀释倍数,n=3。
1.3.6 二聚酪氨酸荧光值测定
参考ZHANG等[16]的方法,并稍作修改进行测定。用含0.6 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 7.0)将氧化后的肌原纤维蛋白浓度调至1 mg/mL,将调好的蛋白溶液离心(4 ℃,5 000 r/min,10 min)后用荧光分光光度计测定上清液的荧光强度。激发波长为325 nm,发射波长为420 nm,狭缝宽度为10 nm,测定结果用荧光强度除以蛋白浓度,表示为相对荧光值。
1.3.7 总巯基含量的测定
参考YANG等[17]的方法测定。用含0.6 mol/L NaCl的磷酸盐缓冲液磷酸盐缓冲溶液(20 mmol/L,pH 7.0)将肌原纤维蛋白稀释为5 mg/mL,取1 mL稀释的蛋白质溶液和8 mL Tris-甘氨酸溶液(其中包括10.4 g/L Tris,0.9 g/L甘氨酸,1.2 g/L EDTA,8 mol/L尿素,pH 8.0)于离心管中。混匀后,冷冻离心15 min(10 000 r/min,4 ℃),除去不溶性蛋白。然后准确量取上清液4.5 mL,加入0.5 mL 10 mol/L的5,5-二硫代双(2-硝基苯甲酸),混匀,在室温下放置30 min后,在412 nm 处测定其吸光度。使用分子吸光系数13 600 L/(mol·cm)按照公式(3)计算蛋白中总巯基的含量:
巯基含量![]()
(3)
式中:A为样品吸光值;C为蛋白溶液质量浓度,mg/mL;13 600为摩尔吸光系数,L/(mol·cm);10为稀释倍数。
1.3.8 表面疏水性的测定
参考ZHANG等[16]的方法,并稍作修改测定肌原纤维蛋白的表面疏水性的测定。用含0.6 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 7.0)将肌原纤维蛋白调至不同浓度(0.1、0.2、0.4、0.6、0.8 mg/mL)。取4 mL 上述蛋白溶液与40 μL的ANS(8 mmol/L)在磷酸盐缓冲液(0.1 mol/L,pH 7.0)中充分混合。立即使用荧光分光光度计在374 nm的激发波长和485 nm的发射波长,狭缝宽度为5 mm下测量ANS-蛋白结合物的相对荧光强度,同时测定样品空白和试剂空白的荧光检测,并从加入ANS的蛋白结合样品中减去空白荧光。使用线性回归分析从相对荧光强度对蛋白质浓度的图的初始斜率计算肌原纤维蛋白质表面的疏水性,初始斜率表示为SoANS。
1.3.9 内源色氨酸荧光的测定
参考CAO等[18]的方法,并稍作修改。用含0.6 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 7.0)将肌原纤维蛋白质量浓度调至0.1 mg/mL,用荧光分光计测量内源色氨酸荧光。激发波长为280 nm,发射波长为290~400 nm激发和发射狭缝宽度均设为5 nm,数据采集速率为1 200 nm/min,记录荧光发射光谱。记录相同条件下的背景光谱,并从大蒜粉处理的肌原纤维蛋白样品各自的光谱中减去背景光谱。
1.3.10 蛋白质溶解性的测定
用含0.6 mol/L NaCl的磷酸盐缓冲液(20 mmol/L,pH 7.0)将肌原纤维蛋白溶液调整至5 mg/mL,离心(4 ℃,5 000 r/min,20 min)后用双缩脲法测定上清液的蛋白浓度,蛋白质的溶解度按按照公式(4)计算:
蛋白质溶解度![]()
(4)
1.4 数据统计分析
所有指标平行测定3组,结果以平均值±标准差表示。用Excel 2016软件对数据进行统计与计算,用SPSS 18.0软件对数据进行ANOVA方差分析,用Duncan多重比较对数据进行显著性分析(P<0.05表示差异显著),使用Pearson相关性分析对大蒜粉添加量与肌原纤维蛋白各指标间相关性进行分析;利用Origin 2018软件绘制图形。
2 结果与分析
2.1 大蒜粉DPPH自由基清除活性
HPLC-DPPH法测得的大蒜粉高效液相色谱结果见图1,依据空白组和实验组的峰面积的变化,计算大蒜粉中活性成分对DPPH自由基的清除率。根据标准曲线对已知的大蒜中活性成分进行定量分析,大蒜粉中DPPH自由基清除活性结果见表1。

a-空白组峰面积;b-实验组峰面积
图1 大蒜粉和DPPH反应前后色谱结果图
Fig.1 Chromatographic results before and after the
reaction between garlic powder and DPPH
由表1可知大蒜粉中含有8种可清除自由基的活性成分。根据前后峰面积的变化可知,保留时间为48.538、51.358 min的2种物质的吸收峰消失,表明1#、4# 2种成分对羟自由基有极强的清除作用。5#、6# 2种成分对羟自由基的清除作用较强,清除率分别为43.19%、67.59%。2#、7#和8# 3种成分对羟自由基的清除作用较弱,清除率在11.00%~19.89%。3#成分的峰面积极高,但对羟自由基的清除率仅为3.11%,说明此成分是大蒜粉中含量较大但抗氧化能力较弱的活性成分。此外,根据已知大蒜中活性成分标准品可以确定2#、5#、6# 3种成分分别为二烯丙基二硫醚、二烯丙基三硫醚和大蒜素,由标准曲线计算得出3种已知成分的量分别为429.5、10 687.5、93.5 μg/g。
表1 大蒜中清除DPPH自由基的活性成分结果
Table 1 Results of active ingredients in garlic
scavenging DPPH free radicals

编号保留时间/min峰面积反应前反应后清除率/%活性成分1#48.53822.40100.00未知2#50.557840.3718.414.51二烯丙基二硫醚3#51.02229 155.228 247.23.11未知4#51.35824.60100.00未知5#52.47534.519.643.19二烯丙基三硫醚6#53.174219.771.267.59大蒜素7#53.44379.170.411.00未知8#53.8221 101.3882.319.89未知
2.2 大蒜粉对牦牛肉肌原纤维蛋白羰基含量的影响
蛋白质骨架侧链上带有的氨基对羟自由基非常敏感,容易转化为羰基基团,一般来说蛋白质羰基含量越高,就说明蛋白氧化程度越高。如图2所示,氧化未添加大蒜粉组的羰基含量显著高于空白对照(P<0.05),表明经羟自由基体系氧化处理后肌原纤维蛋白氧化程度明显加深。研究表明,当肌原纤维蛋白暴露在含低浓度H2O2的高浓度FeCl3环境中时,由于蛋白质-Fe2+配合物与H2O2反应时可以还原生成活性氧,活性氧与金属结合位点上的氨基酸残疾侧链发生反应,使一些氨基酸被转化为羰基衍生物[19]。在氧化处理组中,添加大蒜粉组的羰基含量均显著低于未添加大蒜粉组(P<0.05),说明氧化环境下,大蒜粉对肌原纤维蛋白有保护作用。可能的原因如下:(1)大蒜粉中的活性成分对羟自由基的清除作用,减少了Fenton体系中的羟自由基含量;(2)大蒜粉中的酚类物质通过与蛋白质结合形成复合物来抑制蛋白质的氧化[20]。此外,大蒜粉对牦牛肉肌原纤维蛋白的保护作用与其添加量有关,当大蒜粉的质量分数在0.5%以下时,其保护作用与添加量成正比;当大蒜粉质量分数为0.5%~2.0%时,保护作用与添加量成反比。有研究表明[21-22],大蒜中富含糖类、蛋白质、氨基酸、含硫有机化合物和皂苷类等多种生物活性成分,其中果聚糖占据大蒜干重的75%以上,是脱水大蒜的主要成分。因此,当大蒜粉质量分数较大时(>0.5%),其保护作用与添加量成反比的原因可能是大蒜粉中的还原糖在高含量下与蛋白质发生非酶糖基化反应,使羰基含量上升[23]。当大蒜粉质量分数为0.5%时,羰基含量均显著低于其他各组,说明氧化条件下,大蒜粉质量分数为0.5%时,其对牦牛肉肌原纤维蛋白的保护作用较强。

图2 肌原纤维蛋白的羰基化合物含量
Fig.2 The content of carbonyl compounds in myofibrillar protein
注:肩标小写字母不同代表各处理组间差异显著(P<0.05)(下同)
2.3 大蒜粉对牦牛肉肌原纤维蛋白二聚酪氨酸荧光值的影响
二聚酪氨酸是由2个L-酪氨酸分子的C—C氧化偶联而成的一种荧光氨基酸,可用作蛋白质氧化的有用标记[24]。由图3可知,氧化未添加大蒜粉组的二聚酪氨酸荧光值显著高于空白对照(P<0.05),说明经羟自由基氧化后,蛋白质通过共价和非共价相互作用形成蛋白聚合物,氨基酸侧链受到自由基的攻击,与其他活性氨基酸残基发生共价交联,生成聚合物[14]。在氧化处理组中,添加大蒜粉组二聚酪氨酸荧光值均显著低于未添加大蒜粉组(P<0.05),表明大蒜粉具有抗氧化作用,抑制了蛋白质侧链氨基酸的聚合。当大蒜粉质量分数为0.5%、1.0%、2.0%时,二聚酪氨酸的荧光值显著低于空白对照(P<0.05)。这可能是由于大蒜粉对蛋白质侧链氨基酸的保护作用,导致氨基酸被包埋,从而使荧光强度降低[14]。

图3 肌原纤维蛋白的二聚酪氨酸荧光值
Fig.3 Dimerized tyrosine fluorescence value of myofibrillar protein
2.4 大蒜粉对牦牛肉肌原纤维蛋白总巯基含量的影响
肌原纤维蛋白中富含巯基,这些巯基易受羟自由基的攻击而转化成分子内或分子间的二硫键,导致巯基含量降低,影响蛋白质结构[25]。如图4所示,氧化未添加大蒜粉组巯基含量显著低于空白对照组(P<0.05),说明氧化处理后游离巯基被氧化成二硫键,导致巯基含量降低。在氧化处理组中,大蒜粉质量分数为0.2%和0.5%时,巯基含量显著高于未添加大蒜粉组(P<0.05),说明大蒜粉对氧化体系中肌原纤维蛋白侧链基团具有保护作用,减少了巯基损失;大蒜质量分数为1.0%和2.0%组和未添加大蒜粉组的巯基含量无显著差异(P>0.05),表明大蒜粉对氧化体系中肌原纤维蛋白的保护作用与其添加量有关,较高浓度大蒜粉对蛋白巯基损失无保护作用。有研究表明,大蒜中含有酚类物质[26],高含量酚类物质会导致碎牛肉的巯基含量进一步降低[27],可能的原因是某些酚类抗氧化物质在提供电子和氢原子后,其自身被氧化为相应的半醌或醌类物质,这些具有氧化性的物质会促进巯基转化为二硫键或者其自身作为交联剂引起蛋白分子间交联[19]。

图4 肌原纤维蛋白的总巯基含量
Fig.4 The total sulfhydryl content of myofibrillar protein
2.5 大蒜粉对牦牛肉肌原纤维蛋白表面疏水性的影响
蛋白质是复杂的两性物质,其表面分布着亲水性和疏水性氨基酸残基,其中疏水性氨基酸残基通过疏水键结合在蛋白质分子中心,在蛋白质内部形成疏水区[28]。因此蛋白质的表面疏水性能反映出疏水基团在蛋白质内部的暴露程度,表明蛋白质结构的变化,疏水基团的暴露程度越大,蛋白质的表面疏水性越大。由图5可知,氧化未加大蒜粉组的表面疏水性显著高于空白对照组(P<0.05),说明氧化处理后表面疏水性增加,有更多的疏水性氨基酸暴露在分子表面,导致蛋白构象发生变化[29]。在氧化处理组中,添加大蒜粉组的表面疏水性显著低于未添加大蒜粉组(P<0.05),说明大蒜粉对氧化条件下牦牛肉肌原纤维蛋白的构象有保护作用。当大蒜粉的质量分数为0.5%时,牦牛肉肌原纤维蛋白表面疏水性较低(P<0.05),说明此添加量下大蒜粉对氧化条件下牦牛肉肌原纤维蛋白构象的保护作用最强。

图5 肌原纤维蛋白的表面疏水性
Fig.5 Surface hydrophobicity of myofibrillar protein
2.6 大蒜粉对牦牛肉肌原纤维蛋白内源色氨酸荧光的影响
由于蛋白质内源色氨酸荧光对色氨酸残基周边的微环境特别敏感,因此色氨酸荧光是表征蛋白质三级构象的一种有效方法。如图6所示,氧化未添加大蒜粉组的内源色氨酸荧光值与空白对照组相比明显降低。说明氧化诱导了蛋白质空间结构部分展开,色氨酸暴露在极性环境中,使肌原纤维蛋白的荧光强度显著降低[14]。在氧化处理组中,大蒜粉质量分数为0.2%时,牦牛肉肌原纤维蛋白内源色氨酸荧光显著低于其他4组(P<0.05)。由于2.5中表面疏水性结果显示,添加0.2%质量分数的大蒜粉对牦牛肉肌原纤维蛋白的构象具有保护作用。另有研究表明,多酚类物质能增强极性环境并对色氨酸产生屏障作用,从而使色氨酸荧光强度进一步降低[30]。因此,大蒜粉质量分数为0.2%时,牦牛肉肌原纤维蛋白内源色氨酸荧光显著降低的原因可能是:当大蒜粉质量分数为0.2%时,其中的多酚物质占据主导作用,对色氨酸产生了屏障作用。大蒜粉质量分数为0.5%时,牦牛肉肌原纤维蛋白内源色氨酸荧光与未添加大蒜粉组无显著差异(P>0.05);大蒜粉质量分数为1%和2%时,色氨酸荧光显著高于未添加大蒜粉组(P<0.05)。色氨酸荧光强度随大蒜粉添加量的增加而显著增强的原因可能是:(1)大蒜粉对牦牛肉肌原纤维蛋白的构象具有保护作用;(2)随大蒜粉添加量增加,大蒜素等其他抗氧化活性成分发挥主导作用,清除了体系中的羟自由基,减弱了极性环境,从而使色氨酸的荧光强度增强。

图6 肌原纤维蛋白的内源色氨酸荧光
Fig.6 Endogenous tryptophan fluorescence of
myofibrillar protein
2.7 大蒜粉对牦牛肉肌原纤维蛋白溶解性的影响
蛋白质的溶解性是蛋白质最重要的功能性质之一,蛋白质的许多功能性质都与其溶解性密切相关,如蛋白质的乳化性、起泡性及凝胶性等[31]。由图7可知,氧化未添加大蒜粉组的蛋白质溶解性显著低于空白对照(P<0.05),说明羟自由基加速了牦牛肉肌原纤维蛋白的氧化,诱导蛋白质结构发生改变,引起蛋白质溶解度降低、交联聚集情况加剧。有研究表明,牦牛肉肌原纤维蛋白对羟自由基较为敏感,在该氧化体系下蛋白质的氧化性质发生了明显的变化[32],与本文研究结果一致。在氧化处理组中,添加0.2%大蒜粉时,蛋白质溶解性与未加大蒜粉组差异不显著(P>0.05);添加0.5%大蒜粉时,蛋白质的溶解性与未加大蒜粉及添加0.2%大蒜粉组相比显著增加(P<0.05);而当大蒜粉质量分数为1.0%和2.0%时,蛋白质的溶解性显著低于空白对照(P<0.05)。有研究表明,蛋白质的溶解性与氨基酸组成、pH值、温度、离子强度、蛋白质浓度、表面疏水性等有关,其中pH值对蛋白质溶解度的影响较为明显[33]。且由表面疏水性结果可知,添加1.0%和2.0%大蒜粉组牦牛肉肌原纤维蛋白的表面疏水性与添加0.2%大蒜粉组无显著差异,可排除表面疏水性引起的蛋白质溶解度的改变。因此添加1.0%和2.0%的大蒜粉后蛋白质的溶解性显著低于空白对照的原因可能是因为高浓度大蒜粉的加入使蛋白溶液的pH值达到了等电点附近,此时蛋白质分子所带净电荷很少,分子间相互聚集使蛋白质沉淀,导致蛋白质溶解度降低。

图7 肌原纤维蛋白的蛋白质溶解性
Fig.7 Protein solubility of myofibrillar protein
2.8 相关性分析
由表2中相关性分析结果可知,大蒜粉质量浓度与牦牛肉肌原纤维蛋白的二聚酪氨酸含量呈极显著负相关(r=-0.868)。牦牛肉肌原纤维蛋白的羰基含量与巯基含量(r=-0.610)和表面疏水性(r=-0.800)呈极显著负相关;巯基含量与表面疏水性呈极显著负相关(r=-0.683)。本研究中,添加大蒜粉能够显著降低Fenton体系中牦牛肉肌原纤维蛋白的二聚酪氨酸荧光值,说明大蒜粉对牦牛肉肌原纤维蛋白的侧链氨基酸有保护作用,能抑制Fenton体系中蛋白质侧链氨基酸的聚合。但是由于大蒜粉对蛋白质侧链氨基酸的保护作用,导致氨基酸被包埋[14],从而使大蒜粉的质量浓度与二聚酪氨酸荧光值呈极显著负相关(r=-0.868)。
表2 相关性分析结果
Table 2 Correlation analysis results

项目大蒜粉质量浓度羰基含量二聚酪氨酸荧光值巯基含量表面疏水性蛋白质溶解性大蒜粉质量浓度10.021-0.868∗∗0.1360.000-0.332羰基含量10.020-0.610∗∗0.800∗∗-0.177二聚酪氨酸荧光值1-0.1650.0770.271巯基含量1-0.683∗∗0.355表面疏水性1-0.279蛋白质溶解性1
注:*表示显著相关(P<0.05);**表示极显著相关(P<0.01)
3 结论
大蒜粉具有较强的DPPH自由基清除作用,其共含有8种能清除DPPH自由基的活性成分,其中已知的3种成分及含量分别为大蒜素93.5 μg/g、二烯丙基二硫醚429.5 μg/g、二烯丙基三硫醚10 687.5 μg/g,另外5种成分需要进一步的研究确定。
大蒜粉能够降低Fenton体系中牦牛肉肌原纤维蛋白的羰基含量、二聚酪氨酸荧光值和表面疏水性,增加总巯基含量及内源色氨酸荧光值;且在大蒜粉质量分数为0.5%时,牦牛肉肌原纤维蛋白的羰基含量、二聚酪氨酸荧光值和表面疏水性较低,巯基含量和蛋白质的溶解性较高。综上,大蒜粉对Fenton体系中的牦牛肉肌原纤维蛋白具有保护作用,且当大蒜粉质量分数为0.5%时,保护作用较强。
[1] 孙鹏飞, 刘书杰, 崔占鸿.牦牛肉产量及其品质特性研究进展[J].食品研究与开发, 2015, 36(17):169-175.
SUN P F, LIU S J, CUI Z H.Research progress on meat production and quality characteristics of yak[J].Food Research and Development, 2015, 36(17):169-175.
[2] 崔文斌, 宋艳艳, 李明华, 等.高铁肌红蛋白氧化对牦牛肉肌原纤维蛋白生化特性的影响[J].食品科学, 2020, 41(12):77-83.
CUI W B, SONG Y Y, LI M H, et al.Effect of metmyoglobin oxidation on biochemical characteristics of myo?brillar protein in yak meat[J].Food Science, 2020, 41(12):77-83.
[3] KIM J H, NAM S H,RICO C W, et al.A comparative study on the antioxidative and anti-allergic activities of fresh and aged black garlic extracts[J].International Journal of Food Science and Technology, 2012, 47(6):1 176-1 182.
[4] MANCINI S,MATTIOLI S,NUVOLONI R, et al.Effects of garlic powder and salt additions on fatty acids profile, oxidative status, antioxidant potential and sensory properties of raw and cooked rabbit meat Burgers[J].Meat Science, 2020, 169:108226.
[5] AYD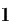 NS, TAHMAS
NS, TAHMAS ![]() D.Antioxidant effect potential of garlic in vitro and real food system:Effects of garlic supplementation on oxidation stability and sensory properties of butter[J].European Journal of Lipid Science and Technology, 2020, 122(3):1900261.
D.Antioxidant effect potential of garlic in vitro and real food system:Effects of garlic supplementation on oxidation stability and sensory properties of butter[J].European Journal of Lipid Science and Technology, 2020, 122(3):1900261.
[6] KIM J H, JANG H J, LEE C H.Effect of aged garlic powder on physicochemical characteristics, texture profiles, and oxidative stability of ready-to-eat pork patties[J].Asian-Australasian Journal of Animal Sciences, 2019, 32(7):1 027-1 035.
[7] RAMIREZ D A, LOCATELLI D A, TORRES-PALAZZOLO C A, et al.Development of garlic bioactive compounds analytical methodology based on liquid phase microextraction using response surface design.Implications for dual analysis:Cooked and biological fluids samples[J].Food Chemistry, 2017, 215:493-500.
[8] ZHUANG X B, JIANG X P, ZHOU H T, et al.Insight into the mechanism of physicochemical influence by three polysaccharides on myofibrillar protein gelation[J].Carbohydrate Polymers, 2020, 229:115449.
[9] XU L L, ZHAO Y, XU M S, et al.Changes in physico-chemical properties, microstructure, protein structures and intermolecular force of egg yolk, plasma and granule gels during salting[J].Food Chemistry, 2019, 275:600-609.
[10] 马文慧, 邝吉卫, 李保玲, 等.氧化条件下精氨酸对肌原纤维蛋白结构及凝胶性能的调控[J].食品科学, 2021,42(24):24-31.
MA W H, KUANG J W, LI B L, et al.Effects of different concentrations of L-Arg onstructures and gelling properties ofmyofibrillar proteinunder oxidative conditions [J].Food Science, 2021,42(24):24-31.
[11] 胡晗艳, 胡云峰, 王娜,等.真空冷冻干燥黑大蒜粉的加工工艺[J].中国调味品, 2016, 41(12):74-76.
HU H Y, HU Y F, WANG N, et al.The processing technique of black garlic powder with vacuum freeze drying[J].China Condiment, 2016, 41(12):74-76.
[12] ESTEVINHO L, PEREIRA A P, MOREIRA L, et al.Antioxidant and antimicrobial effects of phenolic compounds extracts of Northeast Portugal honey[J].Food and Chemical Toxicology, 2008, 46(12):3 774-3 779.
[13] PARK D, XIONG Y L, ALDERTOM A L.Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J].Food Chemistry, 2007, 101(3):1 239-1 246.
[14] 李玲, 季慧, 康大成,等.氧化条件下茶多酚对猪肉肌原纤维蛋白理化和凝胶特性的影响[J].食品科学, 2019, 40(2):12-17.
LI L, JI H, KANG D C, et al.Effect of tea polyphenols on physicochemical and gel properties of pork myofibrillar protein under oxidative conditions[J].Food Science, 2019, 40(2):12-17.
[15] MERCIER Y, GATELLIER P, VIAU M, et al.Effect of dietary fat and vitamin E on colour stability and on lipid and protein oxidation in Turkey meat during storage[J].Meat Science, 1998, 48(3-4):301-318.
[16] ZHANG B, FANG C D, HAO G J, et al.Effect of kappa-carrageenan oligosaccharides on myofibrillar protein oxidation in peeled shrimp (Litopenaeus vannamei) during long-term frozen storage[J].Food Chemistry, 2018, 245:254-261.
[17] YANG H, MENG P P, XIONG Y L, et al.Oxidation in HiOx-packaged pork longissimus muscle predisposes myofibrillar and sarcoplasmic proteins to N-nitrosamine formation in nitrite-curing solution[J].Meat Science, 2013, 95(3):465-471.
[18] CAO Y G, AI N S, TRUE A D, et al.Effects of (-)-epigallocatechin-3-gallate incorporation on the physicochemical and oxidative stability of myofibrillar protein-soybean oil emulsions[J].Food Chemistry, 2018, 245:439-445.
[19] PARK D, XIONG Y L, ALDERTON A L.Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J].Food Chemistry, 2007, 101(3):1 239-1 246.
[20] MAJUMDER R K, SAHA A, DHAR B, et al.Effect of garlic extract on physical, oxidative and microbial changes during refrigerated storage of restructured product from Thai pangas (Pangasianodon hypophthalmus) surimi[J].Journal of Food Science and Technology, 2015, 52(12):7 994-8 003.
[21] 宋百灵, 张唯, 史荣梅, 等.大蒜化学成分不同测定方法比较及相关性探讨[J].药物分析杂志, 2016, 36(4):727-732.
SONG B L, ZHANG W, SHI R M, et al.Study on the comparison and correlation of chemical constituents of garlic[J].Chinese Journal of Pharmaceutical Analysis, 2016, 36(4):727-732.
[22] 史守纪, 章海风.大蒜的化学成分及生物活性影响因素研究进展[J].中国调味品, 2019, 44(11):194-197.
SHI S J, ZHANG H F.Research progress on influencing factors of garlic chemical components and biological activity[J].China Condiment, 2019, 44(11):194-197.
[23] 张建友, 赵瑜亮, 丁玉庭, 等.脂质和蛋白质氧化与肉制品风味特征相关性研究进展[J].核农学报, 2018, 32(7):1 417-1 424.
ZHANG J Y, ZHAO Y L, DING Y T, et al.Relationships of lipid oxidation and protein oxidation with flavor characteristics of meat products [J].Journal of Nuclear Agricultural Sciences, 2018, 32(7):1 417-1 424.
[24] KIM C J, LEE D I, LEE C H, et al.A dityrosine-based substrate for a protease assay:Application for the selective assessment of papain and chymopapain activity[J].Analytica Chimica Acta, 2012, 723:101-107.
[25] JIA N, WANG L T, SHAO J H, et al.Changes in the structural and gel properties of pork myofibrillar protein induced by catechin modification[J].Meat Science, 2017, 127:45-50.
[26] SHIN J H, KANG M J, KIM R J, et al.The quality characteristics of sausage with added black garlic extracts[J].Korean Journal of Food and Cookery Science, 2011, 27(6):701-711.
[27] JONGBERG S, GISLASON N E, LUND M N, et al.Thiol-quinone adduct formation in myofibrillar proteins detected by LC-MS[J].Journal of Agricultural and Food Chemistry, 2011, 59(13):6 900-6 904.
[28] KANGII J, MATSUMURA Y, MORI T.Characterization of texture and mechanical properties of heat-induced soy protein gels[J].Journal of the American Oil Chemists′ Society, 1991, 68(5):339-345.
[29] SUN W Z, ZHOU F B, SUN D W, et al.Effect of oxidation on the emulsifying properties of myofibrillar proteins[J].Food and Bioprocess Technology, 2013, 6(7):1 703-1 712.
[30] 李亚丽, 许玉娟, 徐幸莲. 多酚对肌原纤维蛋白结构与功能特性的影响研究进展[J]. 食品与发酵工业, 2021, 47(19): 296-306.
LI Y L, XU Y J, XU X L. Research progress on the effect of polyphenols on the structural and functional properties of myofibrillar protein[J]. Food and Fermentation Industries, 2021, 47(19): 296-306.
[31] 白登荣. γ-聚谷氨酸复合TGase对鸡肉肌原纤维蛋白功能特性的影响及机理研究[D].重庆:西南大学, 2018.
BAI D R.Effects and mechanism of γ-polyglutamic acid combined with transglutaminase on the functional properties of chicken myofibrillar protein [D].Chongqing:Southwest University, 2018.
[32] 崔文斌, 王惠惠, 刘小波, 等. 羟自由基氧化对牦牛肉肌原纤维蛋白生化特性的影响[J]. 核农学报, 2019, 33(6): 1 165-1 172.
CUI W B, WANG H H, LIU X B, et al. Effect of hydroxyl radical oxidation on the biochemical characteristics of myofibrillar protein of yak meat[J]. Journal of Nuclear Agricultural Sciences, 2019, 33(6): 1 165-1 172.
[33] 尚永彪, 李洪军, 夏杨毅, 等.溶液环境对PSE猪肉肌原纤维蛋白溶解度及热诱导凝胶强度的影响[J].食品科学, 2010, 31(5):35-39.
SHANG Y B, LI H J, XIA Y Y, et al.Effect of solution conditions on solubility and heat-induced gel strength of PSE porcine myofibrillar proteins[J].Food Science, 2010, 31(5):35-39.